抗生物膜肽研究进展
2021-04-26张阳程鹏李晓芬陈红伟
张阳 程鹏 李晓芬 陈红伟,2
(1. 西南大学动物医学院,重庆 402460;2. 西南大学医学研究院免疫学研究中心,重庆 402460)
细菌生物膜是细菌黏附在生物或者非生物表面并被分泌的蛋白质、多糖、eDNA(Extracellular DNA)等水合基质(胞外多糖复合物,Extracellular polymeric substances,EPS)包裹的特殊聚集体[1]。如果将生物膜看做一个细菌城市,生物膜细菌就是生活在城市里的市民,而EPS 就是城市的基础设施,为生物膜细菌提供必要的保护。研究表明,生物膜细菌可以产生比浮游细菌高达10-1 000 倍的抗生素耐药[2]。抗微生物肽因其丰富的种类、抗微生物特性和强大的免疫调节特点受到学者的广泛关注。2008 年,Hancock 等[3]首次报道了人源抗微生物肽LL-37 具有抑制细菌生物膜形成的能力以来,一些具有抗生物膜活性的抗微生物肽被研究者相继发现,也将这一部分抗微生物肽称之为抗生物膜肽(Antibiofilm peptides)。本文就抗生物膜肽的相关研究进展进行了综述,并汇总整理了部分目前已报道的抗生物膜肽(表1)。
1 抗生物膜肽与生物膜各组分间的相互作用
1.1 抗生物膜肽与蛋白质相互作用
生物膜的胞外基质中包含大量蛋白质,包括菌毛、IV 型菌毛以及多种由细菌分泌的酶(如蛋白酶)等。以铜绿假单胞菌为例,其菌毛和IV 型菌毛具有多种生物学功能,并且通过多种动物研究证明了以鞭毛为靶抗原能够预防铜绿假单胞菌导致的感染。除此之外,IV 型菌毛还能与生物膜中其他成分相互结合使得生物膜更加稳定[4]。Gowrishankar等[5]发现环二肽CLP 能够使表皮葡萄球菌的生物膜多糖、蛋白质、eDNA 显著降低,但具体机制尚不明确。Duperthuy 等[6]发现霍乱弧菌能增强OMVs蛋白表达来增强胞外基质中的Bap1 蛋白。Bap1 蛋白可以连接LL-37 和OMVs 表面的OmpT 蛋白,使得生物膜内游离的LL-37 浓度降低到有效浓度以下,使得生物膜细菌免受LL-37 的作用。多种细胞外酶既是生物膜的组成成分,也是细菌的毒力因子组成成分之一。Akeel 等[7]发现富含丙氨酸的抗生物膜肽PT13 能够减少金黄色葡萄球菌毒力因子的产生。而其他具有杀灭生物膜细菌作用的抗生物膜肽也能通过杀灭细菌的方式减少毒力因子的产生。
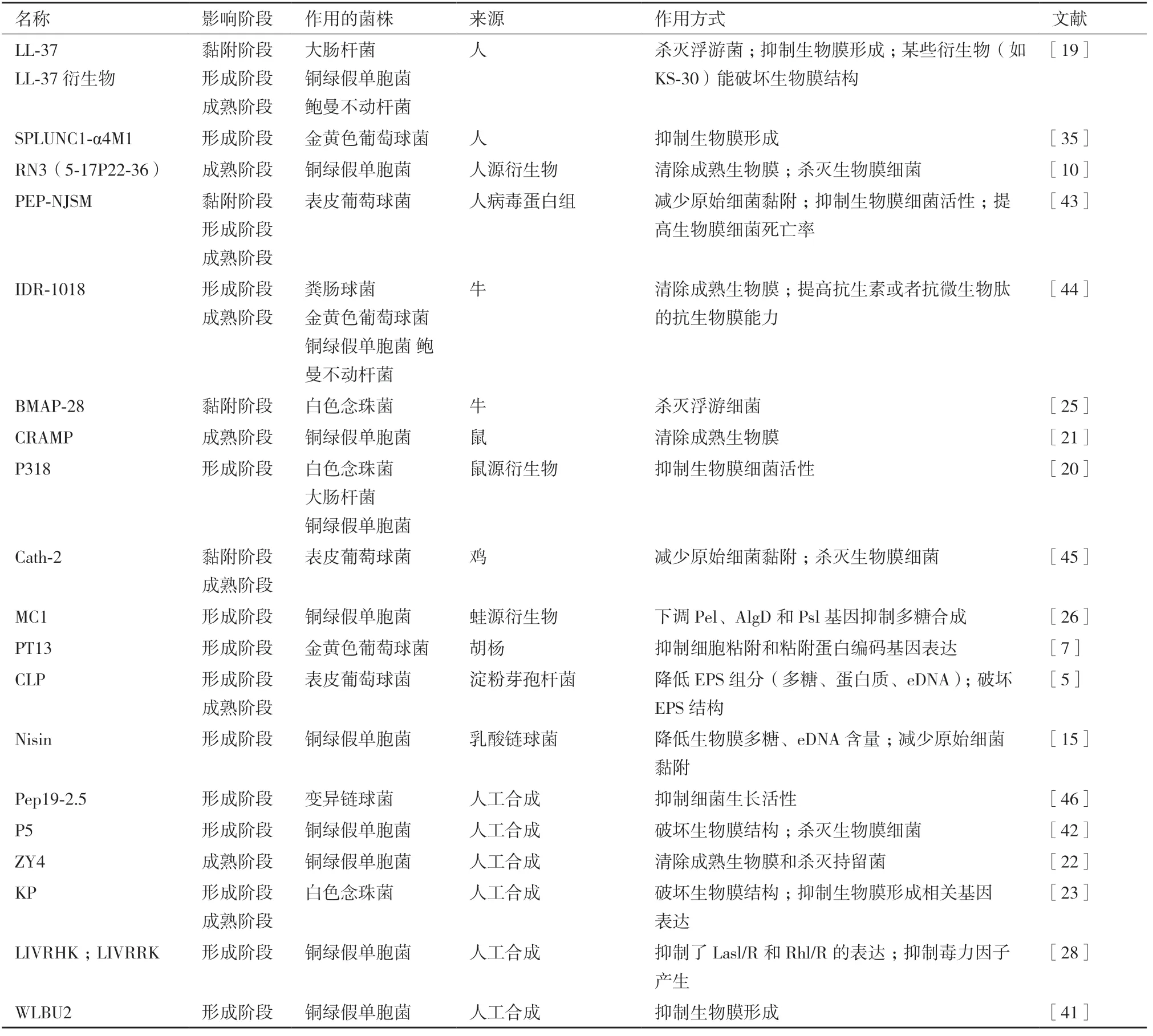
表1 已报道的抗生物膜肽对细菌生物膜的影响
1.2 抗生物膜肽与胞外多糖相互作用
生物膜中的多糖结构可以是单糖或者是大分子聚合物,主要用于维持生物膜的骨架结构。多糖还可以通过物理或化学截留抗生素穿透、抑制中性粒细胞的趋化作用、抑制抗微生物肽活性、以及清除活性氧,有助于细菌在严苛的环境中生存[8]。
不同的致病菌产生的胞外多糖也有差异。大多数的致病菌产生阴离子胞外多糖,如铜绿假单胞菌的藻多糖(Alg),少数致病菌也会产生阳离子胞外多糖,如表皮葡萄球菌的细胞间多糖黏附素(PIA)。此外,同种细菌产生的胞外多糖也可能有差异。例如,肺炎克雷伯菌KpTs101 产生中性胞外多糖,而KpTs113 产生阴离子胞外多糖[9]。一些抗生物膜肽能够直接渗透进入生物膜内或导致胞外多糖断裂。如Pulido 等[10]合成设计了RNase3 氮端衍生肽,并通过研究证实了活性位点缺陷突变体具有与亲本蛋白相同的抗生物膜活性,并且具有比亲本蛋白更加优越的EPS 穿透性。另外,破坏胞外多糖结构也是抗生物膜肽作用的另一方面,在EPS 与环二肽CLP相互作用后发现,CLP 能使表皮葡萄球菌EPS 脱水,并使糖基乙酰化阻止α 糖苷键连接[5]。值得注意的是,胞外多糖与抗生物膜肽间的静电相互作用会导致生物膜内细菌对于抗生物膜肽的抵抗性增强。如阳离子抗微生物肽LL-37 和hBD3 与PIA 的静电排斥作用能够减少其与细菌接触[11]。而KpTs113 带负电荷的胞外多糖能促使阳离子抗生物膜肽BMAP-27由线型螺旋化,并且KpTs101 中性胞外多糖表现出更强的诱导抗生物膜肽螺旋化的能力[9]。
1.3 抗生物膜肽与eDNA相互作用
细胞外DNA(eDNA)是细菌主动释放、分泌或是在细菌溶解后释放在胞外基质中的DNA,在细菌活动中起着十分重要的作用。(1)构成生物膜:是维持生物膜细菌黏附、聚积和生物膜稳定性的重要组成成分[12];(2)营养作用:可以作为大肠杆菌唯一的磷、氮和碳的营养来源[13];(3)螯合作用:可以螯合金属离子(如Mg2+)及抗生素(如氨基糖苷类药物)[14];(4)降低pH;eDNA 在生物膜中的累积会使生物膜局部环境酸化,酸性pH 值会促进铜绿假单胞菌的耐药表型产生[12]。一些抗微生物肽能够导致生物膜中eDNA 含量下降或者直接与之结合,使得eDNA 无法发挥其功能。Wang 等[15]发现乳酸链球菌肽(nisin)在高浓度条件下能够减少生物膜中eDNA 的含量,且呈浓度依赖性变化。Jones 等[14]发现人源抗微生物肽(hBD-3)能够直接与eDNA 结合,但同时破坏了抗微生物肽hBD-3 的生物活性。不能忽视的是,Lewenza 等[16]报道了eDNA 结合金属阳离子(如Mg2+)后,能够激活PhoPQ 和PmrAB双组分系统。导致细菌表面结构发生变化、负电荷被掩盖(表型结构特化细菌),使得阳离子抗生物膜肽正电荷无法作用于细胞膜。
1.4 抗生物膜肽与生物膜细菌相互作用
生物膜是一个具有“蘑菇样”或“飘带样”的3D 结构实体,里面的生物膜细菌也各司其职[4]。部分是负责生物膜的累积并不断分泌EPS 的生物膜建设者,其与浮游态细菌并无两样。另一部分是如前文所述经历了细胞表面表型变化的表型结构特化细菌,能够产生高度的抗生素耐药。最后是一些底层生物膜细菌,由于其不断的受到低营养、低氧、低pH 的极端环境挑战[17],因此一些细菌为了生存由此转入了一种“低代谢活动状态”甚至是“休眠状态”。使其对一些作用于基因复制位点、mRNA、核糖体等代谢活动相关抗生素高度耐药,并且该生物膜细菌是在不经历基因遗传变化的情况下产生对抗生素的耐药[18]。
随着生物膜试验研究不断深入,一些能够针对不同阶段生物膜细菌的抗生物膜肽相继被发现。LL-37 是研究最广泛的人源抗生物膜肽,LL-37 自身及其片段、衍生物都被证实具有抗生物膜活性(包括抑制生物膜形成和破坏成熟生物膜)并能杀灭生物膜细菌[19]。De Brucker 等[20]发现了鼠源抗生物膜肽CRAMP 在亚抑菌浓度下,能够抑制白色念珠菌生物膜的形成。Chen 等[21]发现鸡源抗生物膜肽Cath-2 能够穿透铜绿假单胞菌成熟生物膜并杀灭生物膜细菌,而CRAMP 对整个生物膜有明显的清除作用。Mwangi 等[22]发现抗生物膜肽ZY4 能够杀灭鲍曼不动杆菌生物膜中的持留菌。Paulone 等[23]发现了一种合成抗生物膜肽KP,能够通过抑制生物膜细菌生物膜形成相关基因的表达来破坏白色念珠菌成熟生物膜。
2 抗生物膜肽对生物膜形成的干预作用及其调控
生物膜的形成是一个连续、动态的过程,主要分为黏附阶段、形成阶段、成熟阶段和释放阶段[24]。其形成的具体过程常常受到基因调控与环境的共同作用。
2.1 抑制细菌黏附
致病菌形成生物膜的一个很重要环节就是细菌必须黏附于一个生物或者非生物表面。当细菌未黏附时甚至黏附不牢固时生物膜形成时间和质量都会受到影响。因此,利用抗微生物肽改变细菌的黏附能力或黏附的材料表面就能够减少生物膜的形成。Scarsini 等[25]利用抗生物膜肽LL-37 减少了念珠菌对聚苯乙烯和硅酮表面的黏附从而阻止了念珠菌生物膜的形成。还有一些抗生物膜肽涂层研究将在本文应用及展望中描述。
2.2 干预生物膜组分的形成
通过直接调控生物膜组分基因的表达也能影响生物膜的形成过程。Yu 等[26]发现抗生物膜肽MC1可以通过下调铜绿假单胞菌pelA、AlgD和PslA基因的相对表达量减少胞外多糖合成来抑制生物膜的形成。Akeel 等[7]发现富含丙氨酸的抗生物膜肽PT13能够抑制细菌黏附和细菌黏附蛋白编码基因、减少EPS 的产生,抑制生物膜的形成。
2.3 作用于密度感应系统
密度感应(Quorum sensing,QS)系统存在于多种细菌之中,调控着细菌多种毒力因子及生物膜的形成相关基因[27]。铜绿假单胞菌的QS 系统主要由2 组高丝氨酸(AHL)驱动LasI/R 和RhlI/R 系统、2组非AHL 驱动的PQS 和IQS 系统组成,与生物膜相关的多为前者[27]。Taha 等[28]合成了2 种抗生物膜肽,结果显示,其能减少铜绿假单胞菌PAO1 生物膜的形成和毒力因子产生,并通过荧光定量PCR测定QS 相关基因变化,并发现lasI、lasR、rhlI和rhlR的基因表达水平显著降低。Ciulla 等[29]报道了金黄色葡萄球菌的生物膜QS 系统是由RNAIII 活性肽(RAP)及其靶蛋白(TRAP)介导的,RNAIII 抑制肽(RIP)能够与RAP 竞争从而抑制TRAP 的磷酸化,来减少细菌黏附和生物膜形成。但此类抗生物膜肽并不具有杀菌活性,因此可作为药物的增效剂。优势是直接作用于生物膜的形成,可以恢复抗生素和免疫系统对生物膜细菌的杀伤活性。
2.4 作用于c-di-GMP
3,5-环二聚鸟苷单磷酸(c-di-GMP)是广泛存在于细菌内的第二信使,与多种生物学过程相关,同时也与生物膜的形成直接相关。c-di-GMP 含量增加可以促进细菌表面黏附、聚集和EPS 的分泌来诱导生物膜形成,降低则导致生物膜分散,因此可以通过减少细胞内的c-di-GMP 水平来促进已经形成的生物膜分解扩散[30]。这一现象的机制可能与藻多糖的形成过程相关,Whitney 等[31]证实了Alg44 具有一个具有二聚模式的PilZ 折叠区域,能够与c-di-GMP 结合,控制藻酸盐的分泌。随后Foletti 等[32]发现富含脯氨酸的四肽Gup-Gup-Nap-Arg 在水中结合c-di-GMP 比其他核苷酸拥有更高的选择性,并且能抑制铜绿假单胞菌生物膜的生长。这一现象为抗生物膜肽的结构优化提供了参考。
3 抗生物膜肽目前存在的问题及解决思路
由于抗生物膜肽具有抑制生物膜形成或清除已经成熟的生物膜的特点,越来越多的研究者认为,它是是防治细菌生物膜感染的潜在新型药物,但目前其自身还存在诸多缺陷使其很难应用于临床。
3.1 体内稳定性差
天然多肽在体内很容易被蛋白酶水解以及血浆半衰期短。因此,如何提高抗生物膜肽在体内的稳定性至关重要。抗微生物肽结构修饰是重要的一步,目前可以通过将直链肽环化、将L-型氨基酸更换为D-型氨基酸、改变多肽链中单个或者多个氨基酸、改变多肽链的亲/疏水性、利用药剂学方法将多肽进行包被等手段可提高抗生物膜肽的稳定性和延长血浆半衰期[33]。
3.2 细胞毒性较大
抗生物膜肽往往容易对真核细胞表现出一定的溶血性或细胞毒性。为此,如何对抗生物膜肽进行修饰显得至关重要。一方面是降低原有肽的细胞毒性,如Kang 等[34]通过对Pseudin-2 进行一系列修饰,通过取代色氨酸和丝氨酸来增加疏水性,获得的Pse-Anal6 和Pse-Anal7 可以显著减少细胞毒性和溶血性。此外,其被赖氨酸取代类似物的截断物Pse-T3 和Pse-T4 也能减少细胞毒性和溶血性。另一方面是在较低细胞毒性的基础上,增加抗生物膜肽的抗生物膜性能,如Yu 等[35]对SPLUNC1-α4螺旋结构域增加阳离子数量和色氨酸的含量合成SPLUNC1-α4M1,这一改变显著增加了肽的抗生物膜能力,但并没有增加肽的溶血性和细胞毒性。除此之外,Kłodzińska 等[36]利用改性透明质酸组成的纳米凝胶包被抗生物膜肽DJK-5 后,纳米凝胶中的DJK-5 比未包被的肽的毒性降低了4 倍,而不影响肽的抗菌性能。说明通过新型药剂学的手段也可以降低抗生物膜肽的毒副作用。
3.3 合成费用昂贵
抗微生物肽虽然种类繁多,但是来源却十分有限。研究表明外源性添加活性成分可以上调机体内源性抗生物膜肽的表达[37],但是分离纯化难度大、产率低,难以直接满足使用需要。虽然化学合成的方法可以解决抗生物膜肽产量低的问题,但生产成本高。利用基因工程的方法来表达抗生物膜肽似乎是个不错的选择。目前,抗微生物肽主要的表达系统包括原核表达系统(大肠杆菌表达系统、病毒表达系统、枯草芽孢杆菌表达系统)、真核表达系统和动植物表达系统等,但仍然存在在表达过程中对蛋白酶较为敏感,回收率低导致成本高等问题。可以通过修饰增强酶稳定性,提高基因转导准确性,采取适当工艺提高产品回收率等办法,最终提高抗生物膜肽的生产效率、降低成本,真正实现规模化和产业化[38]。
3.4 联合用药
由于抗生物膜肽自身的不足、生产成本昂贵以及专门针对生物膜的药物开发周期较长等缺陷。因此,在现有抗生素的基础上开展与抗生物膜肽的联合用药具有重大意义。Dosler 等[39]通过研究3 种抗生物膜肽和5 种抗生素联合用药,提出抗生物膜肽与抗生素联合使用有助于预防或者延缓耐药性的出现。随后Dosler 等[40]又发现抗生物膜肽即使在1/10MIC 浓度条件下,也能显著增强抗生素的杀菌活性,甚至某些抗生素的最小生物膜根除浓度(MBEC)降低了8 倍。Lashua 等[41]报道了WLBU2 阳离子抗菌肽,与妥布霉素、环丙沙星、头孢他啶、美罗培南联用时显著增强了抗生素对生物膜细菌的杀伤活性。但其具体机制尚不明确,推测如下:(1)抗生物膜肽增加了EPS 的通透性。如Martinez 等[42]利用共聚焦激光扫描显微镜发现,P5 抗生物膜肽可以破坏铜绿假单胞菌生物膜原有结构。若此时联合本身具有抑杀该类细菌活性的抗生素,可使其在生物膜内局部浓度升高而起到协同作用;(2)抗生物膜肽恢复生物膜细菌代谢活性。生物膜细菌常常处于活性较低甚至是可逆的休眠状态,而通常抗生素对低代谢活性的细菌作用较弱,从而导致高度的抗生素耐药[18],抗生物膜肽可能促使生物膜细菌由休眠态重新复苏,联合用药之后可使生物膜细菌对抗生素更加敏感;(3)抗生物膜肽影响生物膜成熟程度,有利于抗生素发挥杀菌作用。如前文所述,某些抗生物膜肽直接参与生物膜形成的调控过程,虽本身并不具有杀菌活性,但可降低生物膜的高度结构化,联合使用抗生素后更有利于后者发挥杀菌作用。
4 应用及展望
随着由生物膜引起的致病菌耐药性不断加剧,抗生物膜肽由于其种类丰富、作用机制独特及不易产生耐药性的特点而受到广泛的关注。近年来已有一些抗微生物肽被应用于临床实践。例如,由Xoma公司合成的Neuprex 被应用于脑膜炎双球菌血症患儿。EntoMed SA 公司合成的Thanatin 衍生肽被应用于免疫低下患者全身性真菌感染和多重耐药菌感染。Micrologix 生物技术公司合成的MBI-肽被应用于尿道相关的血流感染、鼻腔感染。Demgen 和Dow 制药公司合成的Histatin 衍生肽被应用于牙跟炎、口腔感染和口腔念珠菌感染[37]。
但随着研究的不断深入,抗生物膜肽的应用不仅在医学临床治疗细菌感染方面发挥作用,其应用领域也在不断拓宽。(1)医学材料:钛合金因具有较好的生物相容性被广泛应用于口腔医学,但常因生物膜的形成导致这些种植体受到微生物的感染而使种植失败。Geng 等[47]利用将抗微生物肽嵌合在钛表面来预防钛表面生物膜的形成。研究发现,其能很好地抑制钛表面不同链球菌生物膜的产生,且能在唾液和血清中保持稳定。De Brucker 等[20]提出用鼠源抗生物肽CRAMP 衍生肽AS10 覆盖骨种植体预防表面生物膜产生,并证明了AS10 不会影响细胞在种植体中的生存能力和功能。由于医疗中医疗器械的植入很容易形成生物膜导致植入感染,因此未来会有更多的抗生物膜肽会以肽镀层的方式应用于抗生物膜感染中;(2)新药开发:受抗微生物肽的启发,人们能根据抗微生物肽的性质,人工合成出更加安全、有效、低毒性的针对生物膜及生物膜细菌的药物。Basak 等[48]合成设计了30 多个NH125类似物并研究其生物活性发现了多个NH125 类似物具有强大的抗细菌和抗真菌活性,能同时清除细菌和真菌生物膜,并且能在静止期快速清除耐甲氧西林金黄色葡萄球菌的持留菌;(3)食品领域:食品中的致病菌一直是研究者们关注的重点,除防腐剂外,合理的食品包装保证了食品的质量、安全性和保质期。Agrillo 等[49]利用抗生物膜肽1018K6 与聚对苯二甲酸乙二醇酯(PET)偶联获得了具有抗菌和抗生物膜特性的包装。研究表明其能够显著降低食品中的细菌总量,并且即使在不同环境下肽的固化率比较高,也不容易释放至食品中。提示抗生物膜肽也可用于保障食品新鲜和储存领域中;(4)工业领域:在广袤的海洋环境中拥有着大量的环境微生物,其形成的海洋生物膜也具有诸多危害,常常造成金属材料锈蚀老化。Doiron 等[50]利用雪蟹中提取的抗微生物肽(SCAMPs)能够延缓海水中钢材表面形成生物膜导致的金属锈蚀,且不会向海洋中释放合成的化学物质污染环境;(5)畜牧兽医领域:抗生素滥用导致的细菌耐药性增长日益严重,2020年中国已全面禁止抗生素在饲料中添加,临床迫切需求针对生物膜细菌感染的抗生素替代品。近年来,兽医临床也相继出现了关于细菌生物膜感染的研究报道,Shah 等[51]研究发现急性和亚急性乳腺炎金黄色葡萄球菌分离株的体外生物膜形成与耐甲氧西林基因间存在显著的相关性。乳房炎的持续存在会严重导致产奶量和牛奶安全性下降,造成重大经济损失,而耐药基因和生物膜的存在使得抗生素的使用收效甚微。而抗生物膜肽的广泛生物学活性、独特的抗菌机制和抗生素增效机制以及不易产生耐药性的优势有望解决上述问题。
未来将不断探索和拓展抗生物膜肽的种类和功能。抗生物膜肽将会以多种形式应用于生活中的各个领域,由细菌生物膜引起的感染和困扰将被逐一解决。