阿戈美拉汀治疗抑郁症伴睡眠障碍的疗效和安全性的系统评价Δ
2021-04-23黄云慧杜爱玲牛慧芳黄宇靖赵奕帆董锦锦岳恺晨赵喆堃王领军杨世昌
郭 飞,黄云慧,杜爱玲,牛慧芳,黄宇靖,卫 博,赵奕帆,董锦锦,岳恺晨,赵喆堃,王领军,杨世昌#
(1.新乡医学院第二附属医院药学部,河南 新乡 453002; 2.新乡市第一人民医院风湿免疫科,河南 新乡453000; 3.新乡医学院第二附属医院神经内科,河南 新乡 453002; 4.新乡医学院药学院,河南 新乡453003; 5.新乡医学院第二附属医院精神科,河南 新乡 453002)
抑郁症为一种发病率高、自残率高的精神疾病,患者不仅表现出心境低落,而且约有40%~90%的患者伴有失眠症状[1]。一项研究结果显示,睡眠障碍可能是影响抑郁症发生和发展的重要因素[2]。另一项研究结果显示,治疗抑郁症患者的失眠症状可有效降低抑郁症的复发率[3]。目前,临床对于抑郁症患者的失眠症状多采用5-羟色胺(5-HT)再摄取抑制剂进行治疗,但5-HT对睡眠结构、性功能影响较大,且效果不佳[4-5]。近年来的研究结果发现,褪黑素受体激动剂阿戈美拉汀可改善抑郁症伴睡眠障碍患者日间兴趣、快感缺失等症状,且可有效恢复昼夜节律[6]。因此,国外多推荐使用阿戈美拉汀用于抑郁症伴睡眠障碍患者的治疗。但国内尚缺乏多中心、大样本的临床研究,所得结论尚有局限性。因此,本研究收集国内该类研究进行荟萃分析(Meta分析),旨在评价阿戈美拉汀对抑郁症伴睡眠障碍患者的睡眠改善效果,进而评价其有效性和安全性,为临床用药提供循证证据。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型:有关阿戈美拉汀改善抑郁症伴睡眠障碍患者睡眠情况的随机对照研究;无论是否采用双盲;语言限定为中文和英文。
1.1.2 研究对象:研究对象须符合《国际疾病分类手册(第10版)》中抑郁症的诊断标准;汉密尔顿抑郁量表(hamilton depression scale,HAMD)(HAMD-17)总分≥17分;匹茨堡睡眠质量指数(Pittsburgh sleep quality index,PSQI)总分>5分且失眠持续时间>3个月;年龄18~75岁;中国人。
1.1.3 干预措施:研究组患者单独使用阿戈美拉汀口服治疗;对照组患者采用5-HT再摄取抑制类抗抑郁药(米氮平、帕罗西汀或艾司西酞普兰等)或安慰剂治疗,或阿戈美拉汀联合其他药物治疗;两组患者治疗时间≥6周。
1.1.4 结局指标:包括HAMD评分、蒙哥马利抑郁量表(Montgomery-Asberg depression rating scale,MADRS)评分、PSQI总分和有效率。根据HAMD减分率评定临床疗效,HAMD减分率=(治疗前HAMD总分-治疗后HAMD总分)/治疗前HAMD总分×100%;痊愈,HAMD减分率≥75%;显著进步,HAMD减分率为50%~<75%;有效率=痊愈率+显著进步率。
1.1.5 排除标准:(1)仅有摘要而无全文的文献;(2)重复发表的文献;(3)研究数据缺失而无法提取数据的文献;(4)内容表述不清楚或数据明显存在问题的文献;(5)动物实验;(6)其他明显不符合纳入标准的文献。
1.2 文献检索策略
计算机检索PubMed、the Cochrane Library、EMBase、中国知网、万方数据库和维普数据库。中文以“阿戈美拉汀”“抑郁症”“失眠”和“睡眠障碍”为检索词,英文以“agomelatine”“depression”“insomnia”和“sleep disorder”为检索词。检索时限为各数据库建库至2020年4月8日。
1.3 文献筛选、数据提取及质量评价
由2名研究者根据文献纳入和排除标准各自独立完成筛查,并对提取的资料交叉核对;如遇分歧,则咨询第3名研究者协助判断。数据提取内容包括:第一作者姓名、研究发表年份、入组病例数、干预措施、HAMD评分、PSQI总分和不良反应发生情况[7]。由2名研究者独自根据Cochrane风险偏倚评估工具中所列内容对文献进行质量评估,其中包括随机方法、分组方案隐藏、双盲设定、研究结果完整性及选择性报告结果等方面,如评价结果意见不同,则由所有研究者讨论决定[8]。
1.4 统计学方法
采用RevMan 5.3软件进行Meta分析,连续性变量采用标准化均数差(SMD)为统计量,并计算其95%置信区间(CI)。使用Q检验进行异质性检验,当检验结果无异质性或异质性较小时(I2≤50%),采用固定效应模型进行Meta分析;当检验结果存在较大统计学异质性(I2>50%)而临床异质性不明时,采用随机效应模型进行Meta分析;当存在明显异质性时,分析异质性来源[9]。
2 结果
2.1 文献筛选流程与结果
初检得到相关文献490篇,剔除重复文献、动物实验、会议论文及综述等得到文献84篇,进一步阅读全文,最终纳入8篇文献。文献筛选流程与结果见图1。
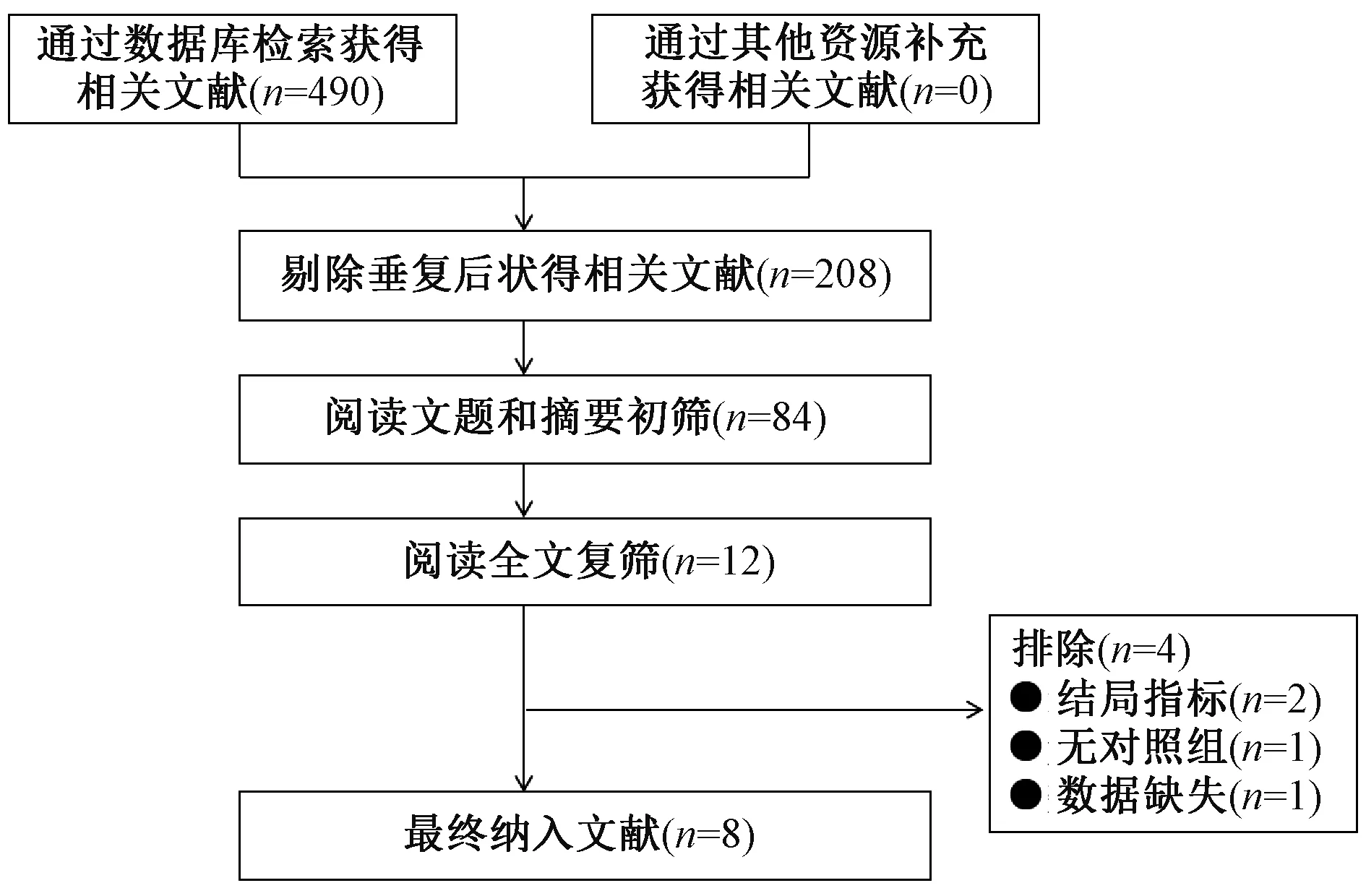
图1 文献筛选流程与结果Fig 1 Literature screening process and results
2.2 纳入文献的基本特征
纳入的8篇文献[10-17]共涉及332例患者,除1篇文献[10]的研究周期为6周外,其余文献的研究周期均为8周。纳入文献的基本信息见表1。

表1 纳入文献的基本特征Tab 1 General information of included literature
2.3 文献质量评估及发表偏倚评估
根据RevMan 5.3软件提供的质量评分方法,分别从随机序列的产生、分配隐藏、盲法、选择性结果报告及不完整的结果数据等方面对纳入的8项研究的质量进行评估,结果见图2。

图2 8项研究的风险偏倚评估Fig 2 Risk bias assessment of 8 literature
2.3.1 随机序列的产生:纳入的8篇文献中,除2篇文献[10,12]没有明确提出随机分组方法外,其余6篇文献[10-11,13-17]对纳入的研究对象均采用随机数字表法进行分组,选择性偏倚风险较低。
2.3.2 分配隐藏:纳入的8篇文献均未明确说明采用的分配隐藏方式和方法,因此不能很好地通过该项判断选择性偏倚风险高低。
2.3.3 盲法:纳入的8篇文献均未对盲法进行详细描述,分析原因可能是阿戈美拉汀与其他抗抑郁药在服药时间和片型上有较大差异,容易让受试者和执行者察觉疾病治疗方案,因此盲法在该研究中较难实施,造成实施偏倚和测量偏倚的风险可能较高。
2.3.4 选择性结果报告及不完整的结果数据:纳入的8篇文献中,有332例患者采用阿戈美拉汀单独治疗,仅3例患者在研究中失访[13,17],因此具有较低的损耗性偏倚。对患者抑郁症状严重程度的评价,有1篇文献采用MADRS进行评定[10],其余文献采用HAMD进行评定;对睡眠质量的评价,8篇文献均采用PSQI进行评定;8篇文献均有较完整的数据报告。
2.4 Meta分析结果
2.4.1 HAMD评分:7篇文献[11-17]采用HAMD评定抑郁症状的严重程度,但各研究间异质性较高(I2=88%,P<0.000 01),故对HAMD结局采用随机效应模型进行分析。Meta分析结果显示,抑郁症伴睡眠障碍患者单独使用阿戈美拉汀治疗后,其HAMD评分较治疗前明显降低,差异有统计学意义(SMD=-5.31,95%CI=-6.28~-4.33,P<0.000 01),见图3。

图3 单独使用阿戈美拉汀治疗前后患者HAMD评分比较的Meta分析森林图Fig 3 Meta-analysis of comparison of HAMD scores before and after treatment with agomelatine alone
2.4.2 PSQI总分:8篇文献[10-17]均采用PSQI评定睡眠质量,各研究间异质性较高(I2=74%,P=0.000 4),故对PSQI结局采用随机效应模型进行分析。Meta分析结果显示,抑郁症伴睡眠障碍患者单独使用阿戈美拉汀治疗后,其PSQI总分较治疗前明显降低(SMD=-3.66,95%CI=-4.16~-3.17,P<0.000 01),见图4。
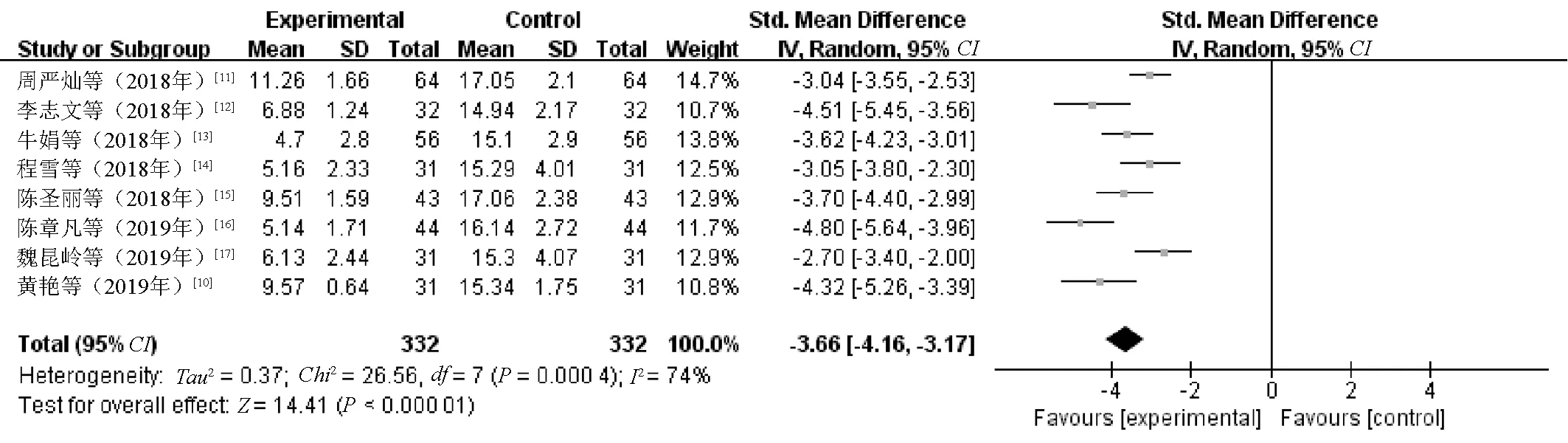
图4 单独使用阿戈美拉汀治疗前后患者PSQI总分比较的Meta分析森林图Fig 4 Meta-analysis of comparison of PSQI scores before and after treatment with agomelatine alone
2.4.3 有效率:6篇文献[10-12,14,16-17]报告了有效率,各研究间无异质性(I2=0%,P=0.99),故对有效率结局采用固定效应模型进行分析。Meta分析结果显示,抑郁症伴睡眠障碍患者单独使用阿戈美拉汀治疗后的有效率为87%(RD=0.87,95%CI=0.61~1.13,P<0.000 01),见图5。
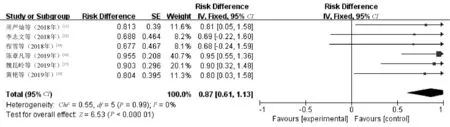
图5 单独使用阿戈美拉汀治疗后患者有效率的Meta分析森林图Fig 5 Meta-analysis of comparison of clinical efficacy between two groups
2.4.4 偏倚分析:针对PSQI总分绘制漏斗图,所纳入研究呈不对称分布,可能存在发表偏倚,见图6。
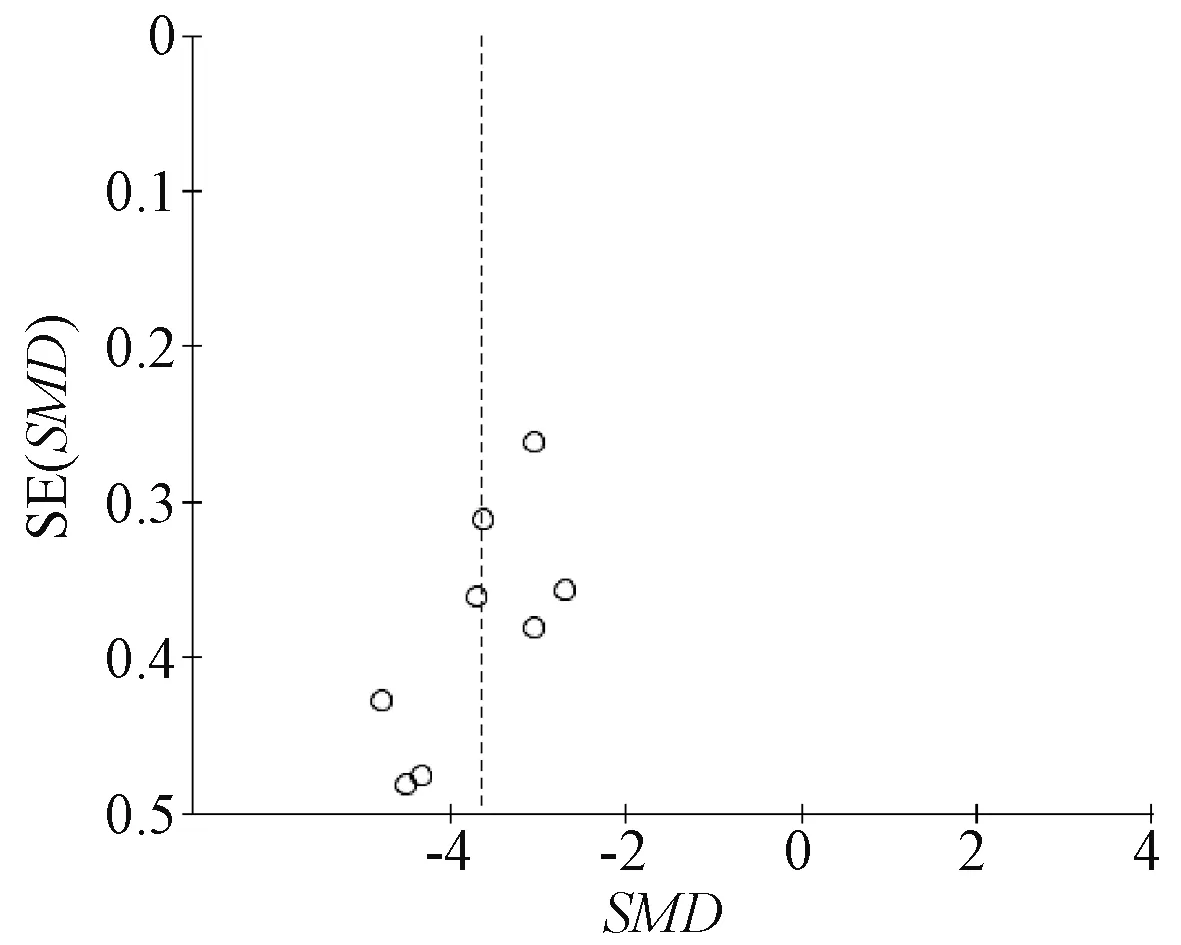
图6 PSQI总分的漏斗图Fig 6 Inverted funnel plot of PSQI scores
2.5 安全性评价
2.5.1 消化道系统反应:6篇文献[11-15,17]提及阿戈美拉汀可引起恶心症状,合计13例,其中1篇文献[13]未说明发生恶心的病例数;4篇文献[11-12,14-15]报告服用阿戈美拉汀可引起口干,合计7例;3篇文献[11,13,15]报告患者出现腹泻症状,合计4例,其中1篇文献[13]未说明发生腹泻的病例数。
2.5.2 头晕头痛:6篇文献[11-12,14-17]报告服用阿戈美拉汀可引起头晕头痛症状,其中4篇文献[12,14,16-17]报告患者出现头晕症状,合计15例;3篇文献[11,15,17]报告患者出现头痛症状,合计10例。
2.5.3 其他不良反应:纳入的8篇文献中, 7篇文献描述了不良反应类型,1篇文献[10]未说明,但提及阿戈美拉汀的不良反应发生情况与其他抗抑郁药无显著差异。服用阿戈美拉汀后尚有其他不良反应,如嗜睡(3例)、视物模糊(1例)、焦虑(1例)、多汗(4例)、肝功能异常(1例)及其他(2例)。研究中可能存在同一患者出现2种及以上不良反应的现象,故无法换算出总体不良反应发生率,仅能对单个不良反应类型进行阐述。
2.6 敏感性分析
针对本次Meta分析结果的异质性,每次去除其中任何一个研究后,重新分析阿戈美拉汀对抑郁症状和睡眠症状的疗效,但Meta分析结果均不受影响,采用固定效应模型或随机效应模型的分析结果一致,表明该Meta分析结果稳定。
3 讨论
阿戈美拉汀为褪黑素受体激动剂和5-HT受体拮抗剂,除具有较好的抗抑郁作用外[18-19],还可调节生物节律,改善睡眠质量,降低觉醒概率等[20]。因此,从理论上而言,阿戈美拉汀可能对抑郁症伴睡眠障碍患者有较好的治疗效果。
本研究共纳入8篇文献,合计332例患者。Meta分析结果发现,抑郁症伴睡眠障碍患者单独使用阿戈美拉汀治疗后,其HAMD评分显著低于治疗前,提示阿戈美拉汀对抑郁症状有较好的疗效;其PSQI总分显著低于治疗前,提示阿戈美拉汀可改善该类患者的睡眠状况。
在阿戈美拉汀的安全性方面,纳入的研究中仅比较了阿戈美拉汀与对照药物可能产生的头痛、口干和恶心等不良反应或各自的不良反应发生率,但未对阿戈美拉汀可能产生的肝损伤进行研究[21-22]。临床研究结果显示,阿戈美拉汀会引起血清转氨酶(丙氨酸转氨酶、天冬氨酸转氨酶)水平升高[22];但与安慰剂相比,其转氨酶升高的患者所占比例并无显著差异[18,23]。另有研究报道,阿戈美拉汀可引起便秘,但发生率较低[24-25]。牛娟等[13]对60~75岁的老年抑郁症患者采用阿戈美拉汀治疗时,发现其对抑郁症状和睡眠症状具有较好的改善作用,且不良反应少,但因纳入的样本量有限,其安全性尚无充足证据支持。国外对阿戈美拉汀的管理中,明确规定其禁用于>75岁的老年患者,以减少对该类人群的肝损伤[26]。因此,临床使用阿戈美拉汀时,应密切关注患者的肝功能,防止出现肝损伤或肝衰竭,如转氨酶高于3倍正常值上限时,应停止使用[26]。
本研究的局限性:符合纳入标准的文献仅8篇,且未说明研究是否为双盲试验,因此可能存在较大偏倚;受到各研究间纳入样本量、地域分布等因素的限制,所得结论是否适用于我国各民族人群有待进一步验证。虽然现有证据显示,在我国,阿戈美拉汀对抑郁症伴睡眠障碍患者的睡眠情况有一定的改善效果。然而,证据质量评价结果显示,证据级别较低,缺乏高质量的随机对照试验研究佐证结论,因此,未来仍需大样本、多中心和长时间的随访结果进行验证。
综上所述,阿戈美拉汀对抑郁症伴睡眠障碍患者的抑郁症状、失眠症状均有较好的改善效果。本研究可为临床相关治疗提供更多参考,并为阿戈美拉汀适应证的扩大提供循证证据。
