基于液相色谱 -质谱联用技术同时测定乌灵胶囊多组分含量Δ
2021-04-23高宏杰
李 君,高宏杰,张 艳,李 涛
(1.中国中医科学院西苑医院检验科,北京 100091; 2.中国中医科学院中医药信息研究所党委办公室,北京 100700; 3.南方医科大学中医药学院,广东 广州 510515; 4.中国中医科学院广安门医院心理科,北京 100053)
乌灵胶囊是以我国珍稀药用真菌——乌灵菌经现代技术精制而成的纯中药制剂,在临床被用于治疗失眠、抑郁和焦虑等[1-2]。既往对乌灵胶囊的研究主要集中在药理方面[3-5],而关于成分鉴别和含量测定等方面的研究有限。研究结果显示,乌灵菌粉富含多种氨基酸、蛋白质、微量元素、粗多糖及核苷等[6-7]。《中华人民共和国药典》记载乌灵菌的质量标准中目前只有腺苷及甘露醇类物质的含量测定。而菌类植物内源性成分众多且复杂,乌灵菌的药理功效来自于各种成分的协同作用。过往单纯将乌灵菌中腺苷、染料木素及甲基蜂蜜曲霉素等有限成分作为质量控制监测指标[8-9],无法反映乌灵菌整体成分信息,不能有效监控乌灵菌不同批次间成分含量差异,难以保证药效的重复性。本研究采用液相色谱-质谱联用技术(liquid chromatography-mass spectrometry,LC-MS)对乌灵胶囊中不同类型的主要组分进行含量测定,为乌灵胶囊内源性成分的整体质量控制和药效成分研究提供参考依据。
1 材料
1.1 仪器
Agilent 1200系列快速高分辨液相色谱仪(美国安捷伦科技有限公司);四极杆串联飞行时间质谱仪(Triple-TOF 5600 PLUS,美国AB SCIEX公司)。Adventurer AR1140型十万分之一电子分析天平(美国OHAUS公司);Milli-Q Plus纯化水仪器 (Millipore公司);SB-5200 DTD型超声波清洗仪(宁波新芝生物科技股份有限公司);MS3型旋涡混合器(德国IKA公司);Captiva 96孔板过滤装置(美国安捷伦科技有限公司);SpeedVac SPD121P型离心浓缩仪(美国Thermo公司)。
1.2 药品与试剂
乌灵胶囊(批号:190558-191009;浙江佐力药用有限责任公司);腺苷对照品(批号:110867-201809)、染料木素对照品(批号:111853-201607)及5-甲基蜂蜜曲霉素对照品(批号:11872-201532)均购自中国食品药品检定研究院,纯度均>98%;鸟苷(批号:SLBR2025V)、尿苷(批号:SLBR2327V)、尿酸(批号:SLBR4791V)、胆碱(批号:SLBR5231V)、左旋肉碱(批号:SLBR7143V)、多巴胺(批号:SLBR3951V)、甘氨酸(批号:SLBL4867V)、蛋氨酸(批号:SLBK1781V)、酪氨酸(批号:BCBQ3889V)、组氨酸(批号:SLBR4399V)、苏氨酸(批号:SLBK2266V)、丙氨酸(批号:BCBQ3887V)、亮氨酸(批号:BCBQ9997V)、异亮氨酸(批号:SLBN6787V)、色氨酸(批号:WXBC0573V)、赖氨酸(批号:BCBR4758V)、天冬氨酸(批号:BCBQ7264V)、天冬酰胺(批号:SLBM5873V)、缬氨酸(批号:SLBK4255V)、苯丙氨酸(批号:STBF1734V)、脯氨酸(批号:SLBQ5622V)、丝氨酸(批号:SLBN3834V)、谷氨酸(批号:SLBL3592V)、谷氨酰胺(批号:SLBP5086V)、精氨酸(批号:SLBK3324V)、牛磺酸(批号:BLBN1549V)及γ-氨基丁酸(批号:BCBN3020V)均购自Sigma公司。同位素腺苷(批号:PR-28063)、同位素尿苷(批号:1-23265)、氘代胆碱(批号:PR-28063)、氘代肉碱(批号:PR-15366)、氘代丙氨酸(批号:PR-17582)、氘代精氨酸(批号:PR-18725)、氘代缬氨酸(批号:I-19231)、氘代异亮氨酸(批号:PR-26535)、氘代苯丙氨酸(批号:PR-23811)及氘代色氨酸(批号:PR-14798)均购自剑桥同位素公司。甲酸、甲醇及乙腈均为色谱纯,购自Fisher公司;Milli-Q纯化水。
2 方法与结果
2.1 标准品溶液的制备
分别精密称取30种标准品和10种同位素标准品,用50%甲醇水(体积分数)溶液配制成质量浓度为1 000 μg/ml的单标储备液。移取适量单标储备液混合于同一容量瓶中,获得混合对照品储备液。检测时用纯水逐级稀释配制0.01~10 μg/ml系列混合标准品溶液,每份混标液中均含有0.2 μg/ml的10种同位素标准品(内标)。
2.2 供试品溶液的制备
精确称取乌灵菌粉20 mg, 加入80%甲醇溶液1 ml,超声(功率为300 W,频率为40 kHz) 提取30 min, 4 ℃、12 000 r/min离心10 min,上清液转移至离心管,离心浓缩至干。复溶溶剂选用2%乙腈(含0.2 μg/ml的10种同位素标准品),每份干燥样品以200 μl复溶,涡旋混匀,96孔板过滤于收集盘,待上机检测。
2.3 色谱-质谱条件
2.3.1 色谱条件:色谱柱为UPLC HSS T3柱(1.8 μm,2.1 mm×100 mm,美国Waters公司);流动相为乙腈-0.1%甲酸溶液,A相为水(含有0.1%甲酸),B相为乙腈(梯度洗脱过程中A相比例变化如下:0 min,98%;6 min,50%;8 min,30%;10 min,0%;13 min,0%;13.1 min,98%;16 min,98%);进样量为5 μl;流速为0.35 ml/min;柱温为40 ℃。
2.3.2 质谱条件:正离子电离模式,电喷雾电压5 500 V,雾化气温度500 ℃,解簇电压80 V,气帘气35 psi,雾化气50 psi,辅助气60 psi,高分辨全扫描模式,扫描范围m/z70~600,平行设定信息依赖采集(information dependent acquisition,IDA)功能,二级质谱扫描范围m/z40~600,每个扫描周期选定10个最强母离子触发二级质谱,碰撞能量(CE)设为(30±15) eV。
2.4 数据处理
原始数据提取与定量结果输出采用AB SCIEX公司的Analyst 1.7.1、PeakView 2.2和MultiQuant 3.0.2软件。
2.5 方法专属性考察
以本研究建立的LC-MS方法,分析白溶剂、加入混标的乌灵菌粉提取液,结果显示,所有目标成分均的分离不受背景与基质的干扰,见图1。
2.6 线性范围与定量限
取来自于10个不同批次的混合乌灵菌粉作为混合基质,以“2.2”项下制备方法提取并挥干,用“2.1”项制备的系列混标液各200 μl复溶混合基质,同时平行制备空白基质(含0.2 μg/ml的10种同位素标准品内标)。依照“2.3”项下参数条件进行分析。用加标的混合基质中各标准品峰面积扣除空白基质中对应的内源性成分峰面积后,与对应内标峰面积的比值作为纵坐标(Y),以检测目标成分浓度为横坐标(X),采用加权最小二乘法拟合(权重1/X2),得出各检测成分的回归方程、相关系数、检出限(信噪比S/N≥3)和定量限(信噪比S/N≥10),结果表明,所有目标成分线性关系良好,见表1。
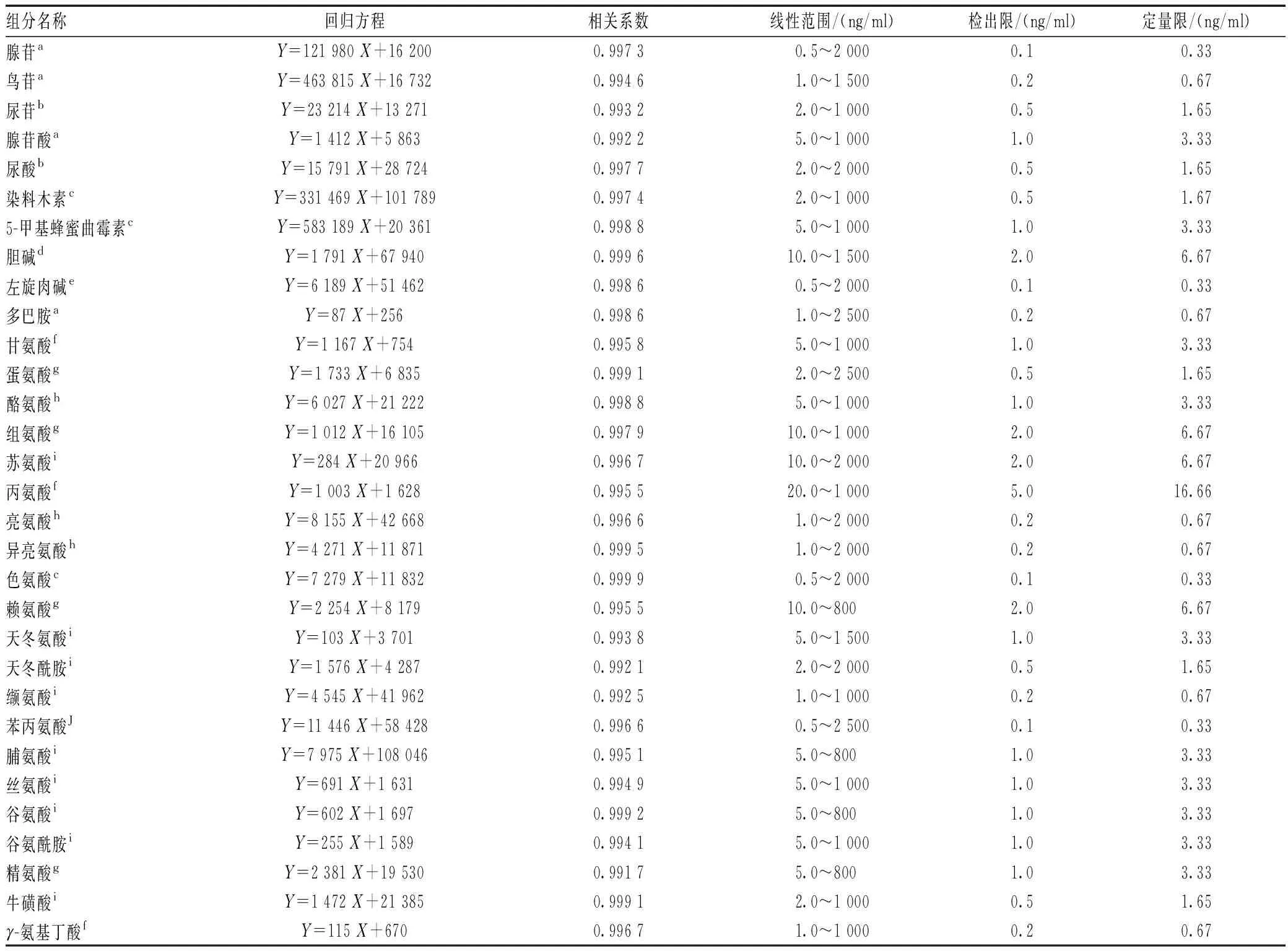
表1 乌灵混合基质中各标准品组分的线性回归方程、定量限、检出限及定量限Tab 1 Linear regression equation, limit of quantification, limit of detection and limit of quantification of each standard components in Wuling mixed matrix
2.7 精密度试验
乌灵菌粉提取基质中分别加入低、中及高3个质量浓度的混合标准品溶液200 μl,所含内标溶液质量浓度均为0.2 μg/ml,每个浓度平行6份,按“2.3”项下仪器条件分析,连续进样5 d,计算日内、日间精密度。结果表明,所有组分日内及日间精密度的RSD均<10%,见表2。
2.8 提取回收率
精密称取10个批次的混合乌灵菌粉,分别加入低、中及高3个质量浓度的混合标准品与内标液,每个浓度平行6份,按照“2.2”项下方法处理样品,作为处理前加标样品。同时平行处理相同份数的未加标乌灵菌粉,在复溶样品时,加入低、中及高3个质量浓度的混合标准品与内标液,每个浓度平行6份,作为后加标样品。所有样品均按照“2.3”项下仪器条件检测,提取回收率=(后加标浓度-前加标浓度)/已知浓度×100%,结果见表2。
2.9 稳定性试验
精密称取10个批次的混合乌灵菌粉,分别加入低、中及高3个质量浓度的混合标准品与内标液,每个浓度6份平行,按照“2.2”项下方法处理样品,分别考察室温(25 ℃)放置24 h,经过3次冻融后各成分的稳定性。按照“2.3”项下仪器条件检测不同阶段所有成分与0时刻浓度的比值变化,结果显示,所有变化率均<10%,表明上述样品处理与存放条件下,样品比较稳定,测定准确。
2.10 样品测定
取10批乌灵菌粉,按照“2. 2”项下供试品制备方法制备成供试品,按照“2.3”项下仪器条件测定,结果见表2。

表2 精密度、提取回收率结果及10个批次乌灵菌粉中多组分含量检测结果Tab 2 Precision, recovery tests,and multi-component contents of 10 batches of samples
3 讨论
乌灵菌是我国珍稀药用真菌。乌灵菌粉富含染料木素、5-甲基蜂蜜曲霉素、氨基酸、蛋白质、微量元素及粗多糖等多种营养成分[10]。其中许多组分具有很好的药理活性和潜在的药用价值。例如,多巴胺是一种神经传导物质,其体内水平过低与抑郁症发病密切相关[11]。但是对于乌灵菌(乌灵胶囊)的分析,未见有关这类成分的研究报道。因此,有必要建立乌灵菌胶囊多组分监测的质量控制方法,以确保不同批次间药效的重复性。
单纯依赖色谱、光谱手段检测药品中指标成分的含量,易受异构体等杂质干扰,且无法实现多组分的同时确检测。质谱技术具有灵敏度高、特异性强等优势,结合液相色谱(liquid chromatography, LC)或气相色谱(gas chromatography, GC)联用手段,已成为当前药物质量控制的首选方法[12-15]。三重四极杆质谱仪(triple quadrupole, QqQ)被认为是药物定量检测的最佳技术[16-17]。但是QqQ对标准品依赖性较强,易受杂质干扰[18]。当需要对中药的化学成分进行整体质量控制时,LC-QqQ则无法监控标准品以外的成分。本研究采用的四极杆串联飞行时间质谱仪(高分辨质谱)恰好能够弥补这一不足,可以更好地区分这些干扰组分,通过获得中药整体内源性成分的精确分子量、一级、二级质谱,与数据库比对,即可同时获得定性、定量信息,无需使用标准品。本研究在采用高分辨全扫描方法获得组分定量信息的同时,结合信息依赖采集技术进一步减少假阳性发生的概率[18-19]。与已报道高效液相-荧光检测相比,本方法不仅可以增加氨基酸谱的覆盖度[8],包括色氨酸、赖氨酸、天冬酰胺、谷氨酰胺及牛磺酸,还可以分离前者无法区分的组氨酸与甘氨酸等。
中药质量控制分析,需要同时获得整体内源性组分的定性、定量信息[20]。因此,本研究采用液相色谱-质谱联用技术,开展了乌灵胶囊多组分含量研究。结果表明,肉碱、多巴胺、黄酮、核苷酸及氨基酸等组分含量较高,提示需要同时监控乌灵胶囊多组分含量,以确保不同批次的药效可重复性。本研究为乌灵胶囊更加严格的质量控制提供了技术方法支撑,并为更深入地研究其功效成分提供了依据。
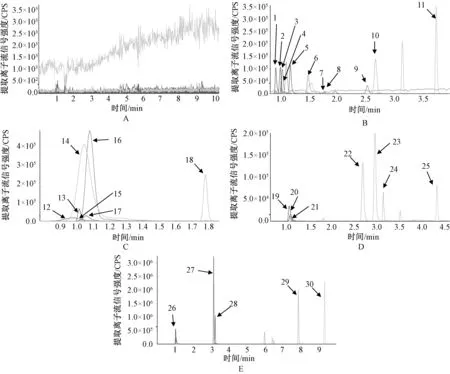
A. 空白溶剂;B—E. 混合标准品加入乌灵菌粉提取液;1—30号分别为赖氨酸、精氨酸、天冬酰胺、天冬氨酸、脯氨酸、缬氨酸、腺苷酸、尿酸、尿苷、酪氨酸、苯丙氨酸、组氨酸、丝氨酸、牛磺酸、甘氨酸、谷氨酸、苏氨酸、蛋氨酸、丙氨酸、γ-氨基丁酸、左旋肉碱、异亮氨酸、亮氨酸、多巴胺、色氨酸、胆碱、腺苷、尿苷、染料木素及5-甲基蜂蜜曲霉素A.blank solvents; B to E.mix standards were spiked into extracted solvents of Wuling powder; No.1 to No.30 indicates lysine, arginine, asparagine, aspartic acid, proline, valine, adenylate, uric acid, uridine, tyrosine, phenylalanine, histidine, serine, bovine Sulfonic acid, glycine, glutamic acid, threonine, methionine, alanine, γ-aminobutyric acid, L-carnitine, isoleucine, leucine, dopamine, tryptophan, choline, adenosine, guanosine, genistein and 5-methylellein图1 混合标准品的提取离子流色谱图Fig 1 Extracted ion chromatograms of standard references
