COPD急性加重期血清Ferr、CEA和D-二聚体水平变化及意义
2021-04-21金旭包先丽张春芳樊启光李博
金旭,包先丽,张春芳,樊启光,李博
(北京市和平里医院急诊科,北京 100013)
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)为一种以不完全可逆性气流受限为主要特征的慢性气道炎症性病变,尤其急性加重者频繁急性发作,严重损伤患者肺功能与健康状态,导致其住院率及病死率上升。若能对COPD急性发作作出早期预测,可有效进行及时干预与治疗,减轻急性炎症对肺功能的损害,减少患者致残和病死风险[1]。铁蛋白(Ferr)为机体中储存铁的可溶性组织蛋白,其水平升高与COPD有一定关系[2-3];癌胚抗原(CEA)为参与细胞黏附的癌胚糖蛋白,血清CEA既是恶性肿瘤的标记物,也在良性呼吸系统性疾病中升高[4];D-二聚体(D-D)为体内发生凝血活化与纤溶活性增强后的降解产物,其水平升高提示体内存在继发性纤溶功能亢进,也能间接反映炎症反应程度[5]。本研究通过分析COPD急性加重期患者血清Ferr、CEA、D-D水平变化,借以了解其临床意义。
1 资料与方法
1.1 一般资料
选取2016年5月至2019年6月北京市和平里医院收治的COPD患者210例为研究对象,根据病情分为观察组(急性加重期,n=100例)和对照组(稳定期,n=110例)。本研究获得医院伦理委员会批准同意,患者均对本研究内容知情,且签署知情同意书。观察组和对照组年龄和性别比较,差异无统计学意义(P>0.05),观察组病程长于对照病(P<0.05)。见表1。
纳入标准:(1)符合COPD诊断标准[6]。(2)急性加重期(AECOPD)为慢性咳嗽、咳痰加重,气喘、痰量增多,肺功能分级Ⅱ~Ⅲ级;稳定期为慢性咳嗽、咳痰等症状相对稳定,且无明显变化。(3)慢性阻塞性肺疾病全球倡议(GOLD)分级为1~2级的患者病情相对于3~4级者风险较低,故纳入3~4级患者进行分析。GOLD分级标准:1级为轻度,FEV1>80%预计值;2级为中度,50%≤FEV1<80%预计值; 3级为重度,30%≤FEV1<50%预计值; 4级为极重度,FEV1<30%预计值。(4)患者临床资料完整。排除标准:(1)合并肝脏疾病等影响血清Ferr、CEA、D-D测定者;(2)合并其他部位细菌性感染者;(3)合并恶性肿瘤、冠心病、糖尿病、炎性肠病等影响凝血功能的疾病;(4)近1周内有使用阿司匹林、低分子肝素、激素等影响凝血功能与炎症反应者。
1.2 方法
1.2.1 标本采集 患者入院后第1天、第3天、第7天、第14天(观察组在出院时28 d采集1次标本)采用普通真空采血管抽取空腹肘静脉血3 mL,3 000 rpm离心10 min,分离血浆,置于-20 ℃下低温保存待测,标本均无溶血、脂血等。
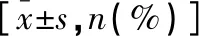
表1 两组一般资料比较
1.2.2 血清Ferr、CEA、D-D水平的测定 Ferr、CEA采用Beckman coulter Dxl800全自动免疫分析系统进行测定,试剂均为厂家配套的Ferr、CEA试剂盒;D-D采用日本Sysmex CA7000全自动凝血分析仪以免疫比浊法进行测定,试剂与质控品均为CK2651公司配套产品。所有操作均严格依据SOP文件执行。参考范围:Ferr:男性23.90~336.20 ng/mL,女性11.00~306.80 ng/mL;CEA:0~5.00 ng/mL;D-D:0~0.65 mg/L。
1.3 观察指标
(1)入院14 d内血清Ferr、CEA、D-D水平变化;(2)不同病情(入院7 d内)和不同预后(出院时)COPD急性加重期患者血清Ferr、CEA、D-D水平;(3)出院时Ferr、CEA、D-D水平对COPD急性加重期患者预后的预测价值。
1.4 统计学分析
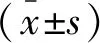
2 结果
2.1 两组患者入院14 d内血清Ferr、CEA、D-D水平变化
两组患者入院14 d内的血清Ferr、CEA、D-D水平比较,差异有统计学意义(P<0.05);观察组患者入院第1天、第3天、第7天血清Ferr、CEA、D-D水平高于对照组(P<0.05),两组患者第14 d血清Ferr、CEA、D-D水平比较,差异无统计学意义(P>0.05)。见表2。
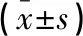
表2 两组患者入院14 d内血清Ferr、CEA、D-D水平变化
2.2 不同病情COPD急性加重期患者血清Ferr、CEA、D-D水平比较
100例COPD急性期患者中,GOLD分级3级54例,4级46例。GOLD分级4级的COPD急性加重期患者入院7 d内平均Ferr、CEA、D-D水平高于GOLD分级3级者(P<0.05)。见表3。
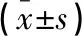
表3 不同病情COPD急性加重期患者血清Ferr、CEA、D-D水平比较
2.3 不同预后COPD急性加重期患者血清Ferr、CEA、D-D水平比较
28 d内有10例COPD急性加重期患者死亡,90例存活,死亡者血清Ferr、CEA、D-D水平高于存活者(P<0.05)。见表4。
表4 不同预后COPD急性加重期患者血清Ferr、CEA、D-D水平比较
2.4 血清Ferr、CEA、D-D对COPD急性加重期预后的预测价值
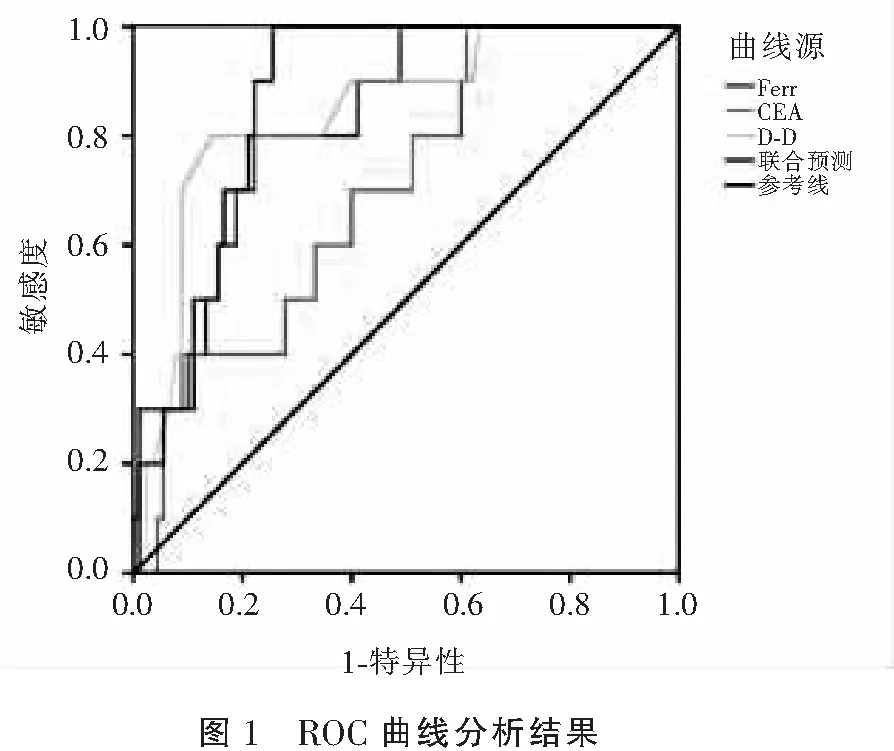
ROC曲线分析发现,出院时血清Ferr、CEA、D-D水平联合预测COPD急性加重期患者28 d内死亡的曲线下面积为0.869,均高于血清Ferr、CEA、D-D单项预测值(0.828、0.702、0.845)。见图1。
3 讨论
COPD是以呼吸道气流受限为主要特征的肺部疾病, 急性加重期是其反复发作导致机体缺氧,并进展至呼吸衰竭,有较高病死率,且呈逐年上升趋势[7-8],尽早诊治并判断预后有重要意义。CEA为一种非器官特异性肿瘤标志物,在胃肠癌、胰腺癌、乳腺癌等恶性肿瘤中升高。研究[9]发现,CEA在肺癌患者中呈高表达,而其在COPD中的研究较少;D-D水平作为体内高凝状态与纤溶亢进的分子标志物标准[10]。张俊等[11]研究发现,缺氧时COPD患者的凝血功能与气道炎症反应有一定关系;Fer是反映人体储存铁量的可溶性组织蛋白。研究[12]发现,Fer联合CEA对肝癌有一定检测价值。关于Fer、CEA和D-D联合检测在COPD急性加重期患者的变化情况及临床意义研究甚少。
本研究发现,观察组入院第1天、第3天、第7天血清Ferr、CEA、D-D水平高于对照组(P<0.05),表明COPD急性加重期患者入院7 d内血清Ferr、CEA、D-D水平发生变化。D-D为纤维蛋白经纤溶酶水解后得到的产物,是人体重要的抗凝系统,生理状态时,凝血与纤溶处于动态平衡[13]。D-D含量高低可反映机体内部纤溶过程,当D-D含量上升时常提示纤溶系统存在异常,血液处于高凝状态。因而D-D对体内高凝状态与血栓性疾病的诊断、疗效观察、预后判断有广泛的应用价值,在COPD急性加重期的病理状态下,机体平衡受破坏,纤维蛋白降解产物增多,D-D释放含量上升,与肖桂贤等[14]的研究结论一致。CEA为参与细胞黏附的癌胚糖蛋白,主要在胎儿发育过程中分泌,但在出生不久后停止,近年来研究发现CEA水平升高可能与肺部炎症反应相关联,能预示局部炎症的存在[15]。本研究中,观察组入院后CEA有一定变化,且入院7 d内CEA水平均高于对照组(P<0.05),表明COPD急性加重期患者的肺泡、间质与远端气道损伤或局部缺氧可能有助于CEA的释放。COPD急性加重期患者的血清Ferr也较COPD稳定期患者高(P<0.05),可能是因为COPD患者肺动脉收缩压舒适度升高及弥散能力受限,需要更多的Ferr以满足机体的需要[16], Kim等[17]研究证实,COPD患者血清铁、血红蛋白与FEV1有一定关系。本研究也发现COPD急性加重期患者中,GOLD分级4级者入院7 d内平均Ferr、CEA、D-D水平较GOLD分级3级者高(P<0.05),表明血清Ferr、CEA、D-D水平对COPD急性加重期患者病情也有较好评估作用。COPD急性加重期患者疾病发展过程中,体内凝血-纤溶系统发生改变,出现高凝状态,肺部出现微小血栓,D-D水平升高[18-19],同时机体免疫功能也受损,炎症反应加重,使血清Ferr、CEA释放也增多[20]。
本研究COPD急性加重期患者中28 d死亡者出院时血清Ferr、CEA、D-D水平高于存活者,而ROC曲线分析发现出院时血清Ferr、CEA、D-D水平联合预测COPD急性加重期患者28 d死亡的曲线下面积为0.869,均较血清Ferr、CEA、D-D单项预测时(0.828、0.702、0.845)高,证实血清Ferr、CEA、D-D水平在评估COPD急性加重期患者预后方面也有一定价值,在临床实践中可将其作为COPD急性加重期诊断与预后评估的重要指标。
综上所述,血清Ferr、CEA和D-D水平随COPD病情加重而升高,出院时Ferr、CEA和D-D水平对COPD预后有一定预测价值,值得在临床推广实践。
