快速康复外科在胰十二指肠切除术围术期管理中的应用价值
2021-04-14曹昕彤宁彩虹李嘉荣林嘉晏阳建怡朱帅黄耿文
曹昕彤,宁彩虹,李嘉荣,林嘉晏,阳建怡,朱帅,黄耿文
(中南大学湘雅医院 普通外科/胰腺外科,湖南 长沙 410008)
快速康复外科(enhanced recovery after surgery,ERAS)是指在术前、术中及术后采取各种已证实有效的措施以减少手术应激及并发症,从而加快患者康复。自1997年Kehlet教授[1]提出该理念以来,越来越多的临床循证医学资料提示,ERAS理念的应用在普通外科各领域的围术期处理中发挥了积极的作用[2-3],可有效减少患者术后并发症、缩短住院时长和降低住院费用,并促进了日间手术的成功开展。然而,胰十二指肠切除术(pancreaticoduodenectomy,PD)作为腹部外科规模最大的手术之一,具有手术难度大、并发症多、住院时间长、病死率高等特点。出于对医疗风险的顾虑,ERAS在PD围术期的应用目前十分有限。中南大学湘雅医院胰腺外科自2017年引入ERAS理念以来,已前瞻性收集32例应用ERAS管理模式的PD患者资料,并与同期采用传统围术期管理模式的患者进行对比,以期探讨ERAS理念在PD围术期管理中的应用价值。
1 资料与方法
1.1 一般资料
前瞻性收集2017年12月—2019年9月间中南大学湘雅医院胰腺外科连续收治的101 例行开腹 PD术的患者,其中男55例(54.5%),女 46例(45.5%);年龄27~81岁,中位年龄56岁。所有患者的手术过程及围术期管理均由同一外科团队完成。根据患者是否接受ERAS措施分为ERAS组(共32例)与传统组(共69例)。两组的入组标准为:(1) 择期行标准PD术的患者[包括经典PD(Whipple术)和保留幽门的PD(pyloruspreserving PD,PPPD)];(2) 术前、术中均未发现原发病灶明显局部侵犯和远处转移,恶性肿瘤可达到R0切除者;(3) 无严重心、肺、肝、肾等重要脏器功能不全者。本研究所有过程遵从赫尔辛基宣言[4],并经过中南大学湘雅医院伦理委员会审批者(项目编号:201707777)。
1.2 围手术期处理
1.2.1 ERAS 组术前:(1) 主刀医师主导与患者及家属沟通(必要时高风险谈话),主管护士协助医师指导患者学习术后快速康复贴士(包括戒烟、口香糖假饲、围术期饮食和药物管理、术后活动计划、助步器使用);(2) 手术高风险患者的特殊准备:严重梗阻性黄疸患者(总胆红素≥250 μmol/L)行术前减黄,严重贫血患者(Hb ≤70 g/L)予输注浓缩红细胞,严重营养不良患者(NRS2002 营养风险评分≤3 分)予以术前营养支持治疗(首选口服肠内营养);(3) 术前常规留置胃管,非常规行术前肠道准备(合并肠道梗阻、肿瘤侵犯肠管者除外);(4) 术前6 h 禁固体进食,术前2 h 禁液体饮食; (5) 术前预防性使用抗生素。术中:(1) 采用术中加温毯,温盐水腹腔灌洗,维持患者体温于37 ℃左右;(2) 在无明显术中失血的情况下(失血量≤800 mL),采用限制性输液策略[5~6 mL/(kg·h)];(3) 术中进行胰瘘风险评分(fistula risk score,FRS),判断患者的胰瘘风险程度(0~2 分为低危,3~10 分为高危);(4) 术毕手术切口予以罗哌卡因皮下注射。术后:(1) 限制性补液策略(手术日及术后第1、2 天分别给予液体量2000、1500、1000 mL(或20 mL/kg),术后第3 天给予液体量500 mL(或10 mL/kg),从术后第4 天始停止所有静脉给药,改为口服给药);(2) 常规使用β 受体阻滞剂(美托洛尔,有哮喘等禁忌者禁用);(3) 预防性使用NSAIDS(帕瑞昔布,有胃黏膜病变或出血者禁用)、止吐药(甲氧氯普胺)和糖皮质激素(氢化可的松,用于高危患者),非预防性使用生长抑素及其类似物;(4) 胃管拔除:术后第1、2 天以20 mL NS冲洗胃管并抽吸胃液,若术后第2 天胃液引流量<300 mL 且无胃出血,则予以拔除胃管;(5) 饮食计划:低危患者于术后第1、2 天可分别少量饮水和进清流质(<30 mL/h),术后第3 天可正常饮水并进半流质,术后第4 天及以后可恢复普通饮食;高危患者于术后第1~3 天禁食,术后第4 天酌情开始进清流质,并根据临床情况适当调整饮食计划;(6) 活动计划:术后当天患者可在床上活动下肢,家属按摩小腿;术后第1 天可在床上活动下肢、半坐位或坐位,术后第2 天在病房内坐椅子;术后第3 天可在病房内少量活动;术后第4 天及以后基本恢复下床活动;⑺ 引流管拔除:常规于术后第1、3、7 天动态监测患者的腹腔引流液淀粉酶(drainage fluid amylase,DFA)情况。若术后第7日或以后的DFA 处于正常范围,且引流管引流量<10 mL/d的患者,可拔除腹腔引流管。具体的ERAS 流程图见表1。

表1 PD 术的标准化ERAS 路径Table 1 Standardized ERAS pathway for PD
1.2.2 传统组术前常规与患者进行谈话,告知手术方案及风险。术前12 h 禁食,8 h 禁饮,并常规进行肠道准备(磷酸钠盐90 mL,术前1 天晚上口服)。术中无保温措施以及输液量限制,无胰瘘风险相关性评估,术毕不予以手术切口局部镇痛,而采用阿片类药物(布托啡诺、舒芬太尼)持续静脉泵入止痛。术后充分补液(液体量为3000~4000 mL 左右),并预防性使用生长抑素(生长抑素泵,30 mg,术后连续5 d 缓慢泵入)。术后从患者肛门排气排便时开始饮食,从流质 10 mL/h 开始,以后每日增加10 mL/h,直至恢复正常饮食。无明确活动内容规划,具体根据患者的耐受情况决定。当患者胃管及腹腔引流管内无明显液体引流出时,均予以拔除。
1.3 临床指标观察
包括患者的术中相关资料、术后恢复情况和术后并发症及预后情况。术中相关资料包括胰腺质地、胰管直径、FRS评分、术中失血量和手术时长。术后恢复情况包括肛门排气时间、下床活动时间、术后血清白蛋白水平、术后第1、3、7天的DFA值、术后住院时长和住院费用。术后并发症情况包括POPF、PPH、DGE、PBL、肺部并发症、并发症严重程度分级、术后90 d内死病率和再入院率。其中,POPF、PPH和DGE均参考国际胰腺外科研究小组(International Study Group of Pancreatic Surgery,ISGPS)发布的诊断标准[5-7];而PBL参考国际肝脏外科研究小组(International Study Group of Liver Surgery)发布的诊断标准[8];肺部并发症定义为术后经血常规、痰培养、血气分析、胸部X线或者肺部CT等检查所诊断的肺部感染、胸腔积液、肺不张或急性呼吸窘迫综合征等;并发症严重程度参照 2004年Dindo等[9]发布的诊断标准,可从轻至重分为I、II、III、IV和V等5个等级。
1.4 统计学处理
计数资料以例数(百分比)[n(%)]表示,其比较采用χ2检验;计量资料中符合正态分布的数据以均数±标准差(±s)表示,其比较采用t检验;符合偏态分布的数据以中位数(范围)表示,其比较采用Mann-WhitneyU检验。以上均通过SPSS 22.0统计软件分析,当P<0.05时认为差异有统计学意义。
2 结 果
2.1 一般资料比较
ERAS组与传统组的一般资料比较差异无统计学意义(均P>0.05),具有可比性(表2)。
2.2 手术相关资料比较
与传统组相比,ERAS组具有更低的术中失血量[(381.3±225.7)mLvs.(528.6±286.6)mL,P=0.012]。余胰腺质地、胰管直径、FRS评分及手术时长等因素组间差异均无统计学意义(均P>0.05)(表3)。
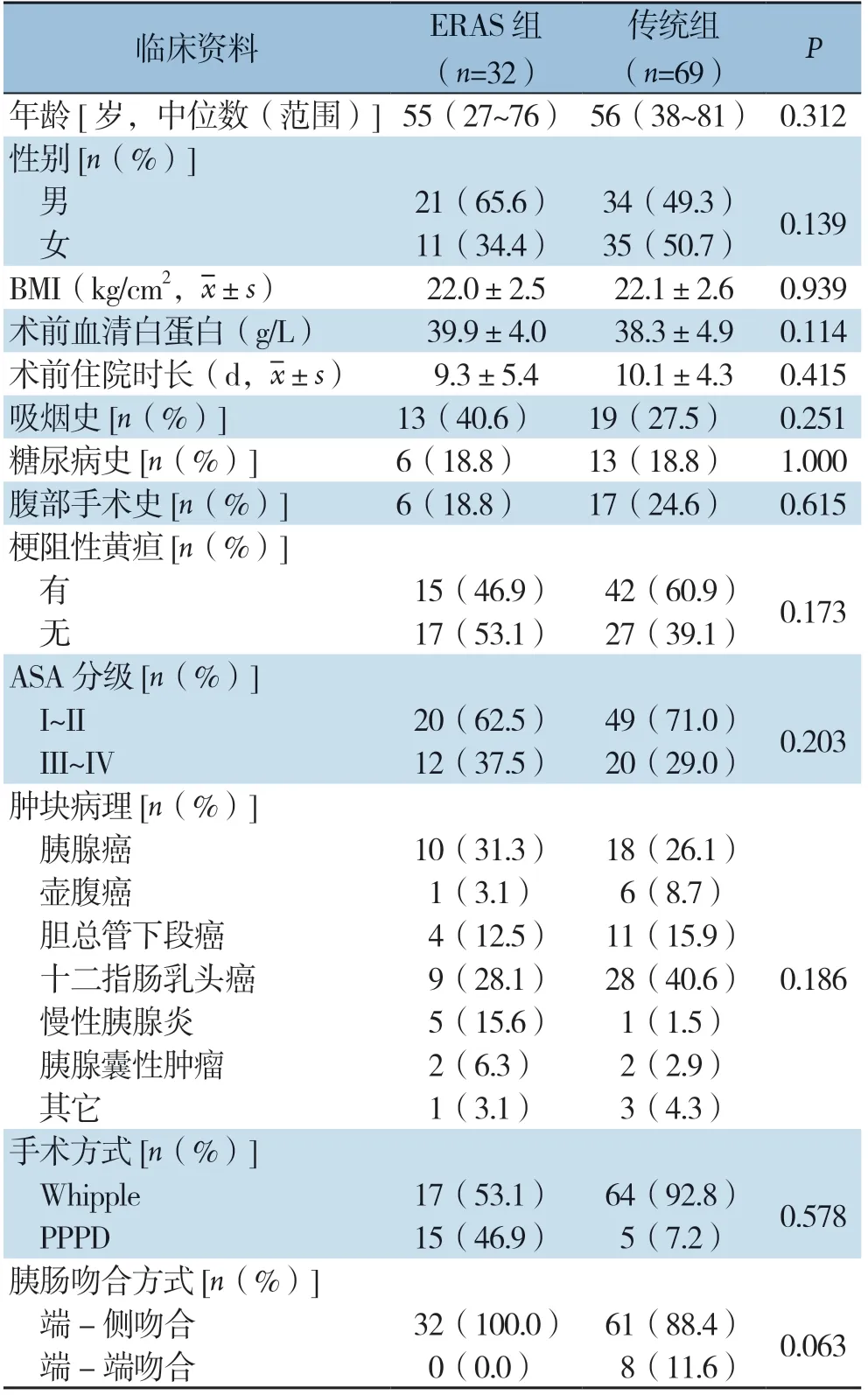
表2 ERAS 组与传统组PD 患者临床基线资料比较Table 2 Comparison of the baseline characteristics of patients undergoing PD between ERAS group and conventional group

表3 ERAS 组与传统组PD 患者术中相关资料比较Table 3 Comparison of intraoperative variables of patients undergoing PD between ERAS group and conventional group
2.3 术后恢复情况比较
ERAS组的术后血清白蛋白水平[(35.4± 5.1)g/Lvs.(31.8±4.4)g/L,P=0.001]明显高于传统组,但术后第1、3、7天的DFA值组间差异无统计学意义(均P>0.05)。此外,ERAS组较传统组的术后肛门排气时间[(2.7±0.9)dvs.(3.1±1.0)d,P=0.003]、下床活动时间[(3.8±0.6)dvs.(5.5±1.7)d,P=0.024]和术后住院时长[(14.1±3.2)dvs.(18.9±9.5)d,P=0.005]明显短于传统组,住院费用明显少于传统组[(9.0± 2.4)万元vs.(11.8±3.9)万元,P <0.001] (表4)。
2.4 术后并发症情况及预后情况比较
在术后并发症方面,ERAS组的术后胰瘘(postoperative pancreatic fistula,POPF)发生率(25.0%vs.47.8%,P=0.049)和肺部并发症发生率(28.1%vs.53.6%,P=0.019)明显低于传统组,并具有更高的无并发症患者比例(59.4%vs.26.1%,P=0.002)。然而,两组在PPH率、DGE率、PBL率等并发症方面差异无统计学意义(均P>0.05)。根据Clavien-Dindo术后并发症分级,ERAS组术后总体并发症率为40.6%(13/32),其中包括I级2例(6.3%),II级7例(21.9%),III级3例(9.4%),IV级0例(0.0%)和V级1例(3.1%),均明显低于传统组(P<0.001)。就预后情况比较而言,ERAS组的术后90 d内病死率和再入院率均略低于传统组,但差异无统计学意义(均P>0.05)(表5)。

表4 ERAS 组与传统组PD 患者术后恢复情况比较Table 4 Comparison of postoperative recovery status of patients undergoing PD between ERAS group and conventional group

表5 ERAS 组与传统组PD 患者术后并发症情况及预后情况比较Table 5 Comparison of postoperative complications and outcomes of patients undergoing PD between ERAS group and conventional group
3 讨 论
近年来,随着ERAS的理念不断在临床推广,如何促进患者快速康复、提高患者的生活质量,已成为业内共同追求的目标。然而,由于PD 常伴有更高的病死率和并发症率,外科医生常倾向于选择保守的围术期管理模式,故患者术后住院时间长达12~27 d不等[10-11],使得ERAS在胰腺外科中的应用相对滞后[12]。2012年,由加速康复协会(ERAS Society)、欧洲临床营养与代谢协会(ESPEN)和国际手术代谢与营养协会共同发布的《PD围术期管理指南》问世[13](后文称指南),其目的旨在为制定PD围手术期统一的ERAS流程提供必要的参考标准。此后,国内外的各中心相继进行了相关的临床实验[14-15],取得了一定的成果。然而,就ERAS是否能降低术后并发症的发生方面仍尚存争议[16-17]。基于以上情况,自2017年12月起,笔者所在的中心对指南中的推荐意见进行合理改良,制定了针对于PD的、以降低术后并发症为核心的标准化的ERAS方案。前瞻性研究结果显示,ERAS模式下的患者,在明显减少了以POPF为首的多种术后并发症发生率的基础上,进一步显著缩短了术后住院时长,降低了住院费用,从而证明ERAS是一种行之有效、值得推广的管理模式。
POPF作为PD术后最常见、最严重的并发症,可继发引起PPH、DGE等多种并发症,同时也是导致患者住院时间延长,经济负担增加,甚至死亡的主要原因[18-19]。尽管对于高流量胰腺中心而言,PD术后病死率已经降低至5%以下,但POPF的比率仍然高达20%~40%[20-21]。因此,对POPF进行精准预测以及风险分层,是ERAS在胰腺外科中广泛应用的必要前提。目前国外研究证实,FRS是目前第一个基于结果的、风险调整的胰瘘评分系统,用于测量PD后的POPF潜在风险[22]。自于2013年由Callery等[23]所创建以来,FRS已通过了多项内部和外部实验的验证,表明其对POPF具有较强的预测能力[24-25]。此外,甚至有研究将FRS应用于PD术后患者POPF风险分层以及术后管理,如腹腔引流管的早期拔除[26-27]。本研究采纳FRS作为POPF危险度分层的评估指标,对低、高危的患者分别实现个体化的ERAS管理途径。结果显示,ERAS组的POPF率与术后并发症率分别为25.0%和40.6%,术后中位住院时间和住院费用分别为13.5 d 和 8.5万元,明显促进了患者的快速康复,并带来了良好的经济效益。
除预测POPF 发生风险外,ERAS流程的关键还在于降低术后并发症率的发生。传统标准围术期管理认为,术后早期维持大量补液(3000~ 4000 mL)可维持外周循环稳定,减少血容量不足、器官功能不全等情况的发生。然而有研究表明,过量补液会导致水钠潴留、组织水肿,进一步引起DGE、肠梗阻以及胰肠吻合口破裂等并发症[28-29]。本研究中ERAS组严格采取限制性补液策略,术后第4天基本停止静脉给药,明显降低患者的容量负荷。此外,特殊药物的使用在降低并发症方面也具有一定的作用。Ahl等[30]认为围术期应用β受体阻滞剂可明显降低患者循环、呼吸系统并发症及脓毒症的发生,并可明显延长患者的生存期(HR=0.43,P<0.001)。Laaninen等[31]认为术中胰腺切面的创伤可激活残余胰腺的一系列炎症反应,成为PD术后并发症的根源,故提倡对于胰瘘高危患者(腺泡>40%,与胰腺质地相关)术后预防性使用糖皮质激素。 另外,术后疼痛管理是患者早期下床的必要前提,且可减少下肢深静脉血栓、坠积性肺炎等情况的发生,成为ERAS成功实施的另一关键。既往的研究认为,硬膜外镇痛或阿片类药物是术后镇痛的最佳选择[32]。但近年来试验证明,帕瑞昔布除具有更佳的镇痛效果外,还可明显降低术后炎症反应[33-34]。本研究联合采用上述药物,结果显示ERAS组的POPF、肺部并发症以及总体并发症率均显著低于传统组,从而印证了上述措施的有效性。
既往的观点认为,在胰腺切除术后常规应用生长抑素(somatostatin,SS)可抑制胰液的分泌,降低胰液中胰酶以及碳酸酐酶活性,减少胰液对胰肠吻合口的侵蚀,从而能预防POPF发生[35-36]。 此外,也有SS的类似物(如奥曲肽、帕瑞肽等)被应用于术后预防POPF发生的报道[21,37]。然而,近年来的研究发现,该类药物不但无法减少POPF发生率,相反可能导致POPF发生率增加[38]。Ecker等[20]的Meta 分析显示非预防性使用生长抑素是降低POPF 发生率的独立危险因素(OR=0.49, 95%CI=0.30~0.78)。Matthew等[39]的多中心研究则发现,预防性使用奥曲肽可显著引起患者POPF率升高(21%vs.7%,P<0.001)和住院时间延长(13 dvs.11 d,P<0.001)。在本研究中,ERAS组患者均采用非预防性使用SS及其类似物的策略,结果证实改组术后POPF 率显著低于传统组,与近年来的研究结果一致。就其相关的发生机制而言,有学者[39]提出了如下假说:(1) SS及其类似物可明显降低胰腺及肠道黏膜的血流灌注,引起吻合口缺血;(2) 该类药物多有抑制各种激素以及细胞因子的作用(如生长激素、IGF-1、EGF等),可导致吻合口愈合缓慢或不愈合;(3) 该类药物可导致胰酶浓度长时处于波动状态,不利于吻合口的愈合。然而,目前这些猜想仍有待后期大样本前瞻性研究以进一步证实。
总之,通过上述标准化的ERAS路径,患者的术后并发症发生率显著降低,住院时长和住院费用明显减少,达到了促进患者快速康复的目的。因此,将ERAS理念应用于胰十二指肠切除术围术期管理是一项安全、有效的举措,值得在临床进一步推广和应用。
