国际近视研究院《近视控制的行业指南和伦理考量》解读
2021-04-12徐琼赵明威
徐琼 赵明威
北京大学人民医院眼科 眼病与视光医学研究所 视网膜脉络膜疾病诊治研究北京市重点试验室 北京大学医学部眼视光学院 100044
近视目前影响了全球约30%的人口,预计2050年将增至50%[1]。近视度数快速增长,可能会合并一系列并发症,如近视性黄斑变性(myopic macular degeneration,MMD)、青光眼、白内障和视网膜脱离,潜在致盲风险更高[2-9]。目前,近视已经成为全世界范围内视力受损以及盲的主要原因[1,9-10],近视防控也成为全社会关注的重点领域。近年来,已有大量旨在延缓近视发病和进展的研究,所涉及的治疗方法包括户外活动、药物治疗、角膜塑形镜(orthokeratology,简称OK镜)、周边离焦软性角膜接触镜、渐变焦和双焦眼镜等[11-16]。国际近视研究院(International Myopia Institute,IMI)的《控制近视发生和进展的干预方法报告》中详细介绍了各种近视防控方法的相关内容[17]。这些方法给参与治疗决策的研究人员和临床医生带来了许多伦理争议问题,比如在决策过程中需要考虑哪些潜在利益冲突?对开处方的临床医生有什么监管上的考量?企业参与的近视控制研究涉及哪些伦理问题?学术组织应该如何适当传播近视控制研究的成果信息?开处方者的资质如何认证?近视防控医疗产品应该如何销售给开处方的医生以及患者?IMI 2019年发表的《近视控制的行业指南和伦理考量》[18]参考最新的临床研究和相关循证指南,汇总了以上问题的国际认识和解决方案,本文结合中国国情,对国际近视防控治疗的现状和相关问题及解决建议进行解读。
1 监管部门
1.1 近视防控手段的审批现状
OK镜和周边离焦软性角膜接触镜均属于角膜接触镜,目前美国食品和药物管理局(food and drug administration,FDA)仅批准角膜接触镜应用于成人,以往儿童应用角膜接触镜的临床研究非常少,研究者主要担心的问题是角膜接触镜会对儿童发育中的眼造成长期不良影响,儿童使用接触镜发生眼部感染的概率可能会比成人更高。但是,最新研究显示,不论是OK镜,还是软性角膜接触镜,儿童并没有比成人表现出更多的并发症[19-21]。相关临床研究证实了角膜接触镜的有效性和安全性[12,14,16,19-23],配戴OK镜和多焦点软性角膜接触镜目前也成为儿童近视防控的可行方案。
目前临床研究证实,质量分数0.5%和1%的阿托品滴眼液可以显著延缓近视进展[15,24-26],但是由于其具有扩大瞳孔的作用和停药后的反跳现象,阿托品滴眼液的长期临床应用受到限制,而更低浓度的阿托品滴眼液被证明也有很好的控制近视效果,瞳孔扩大作用和停药反跳现象轻微[27-30],成为儿童近视防控潜在可行的方案[16,25,30]。然而,目前大部分国家并未批准低浓度阿托品滴眼液应用于儿童近视防控,目前也没有便捷的渠道能够获取药物。究其原因,可能是因为新药审批难度较大,开展长期、大规模儿童临床试验的财政支出较大,所以低浓度阿托品滴眼液的临床应用遇到重重阻力。
其实对于近视防控方法,目前已经积累了很多临床数据能够证明其疗效,包括相关的病例报告,回顾性、前瞻性临床研究和Meta分析,证明相关方法是安全、有效的[11-12,14-16,23,32]。监管部门也在通过减免税收、授予独家代理权、增加市场保护时间和减少收费来激励公司开发现有产品的新适应证,或者通过立法发布临时的超说明书(off-label)使用权限,例如法国和匈牙利现在就在使用这种临时法案。美国眼科协会最新的报道认为,有明确证据证明低浓度阿托品可以预防近视进展,也为该药物的使用提供了更有利的依据[15]。
1.2 制定相关法规
目前近视防控方法的监管存在很大的地域差异,监管相对复杂,全球统一标准很难,美国FDA和日本医疗器械管理部门管理严格,为该领域的监管树立了一个良好的示范。他们要求相关医疗产品通过审批的前提是有良好的实验室研究规范和企业生产规范,光学、药物和眼科企业都要依据全球标准进行相关的生产和使用,同时还要遵循良好的临床试验标准,依据《药物临床试验质量管理规范》要求进行临床试验的设计、规划、监测、记录、分析和报告。
2 医保:超说明书使用的报销问题
目前off-label使用的药物和设备没有办法通过国家医疗保险报销,患者因此要承担更高的经济成本,这可能会影响到部分近视防控方法的实施。现在国际上有国家建议,在确保安全、有效的前提下,列出off-label使用的药物和设备清单,进行医保备案,法国和意大利允许在没有其他更好的选择时,国家医保可以对以上备选清单中的选项进行报销[33]。
3 企业:近视防控方法的宣传规定
目前低浓度阿托品药物并未获得FDA授权批准,按照规定企业不能直接进行营销宣传。但美国FDA的报告显示,在实际应用中,宣传off-label使用的药物也是有意义的,off-label使用药物的审批流程耗时耗力又错综复杂,对这类方法的宣传能够让医疗人员和患者在没有其他选择时有机会了解到更优的治疗方法。但FDA也规定,相关的宣传必须是准确、可信的,在传播给大众之前必须先提交给FDA审核[34]。2010年,美国颁布的《真实处方药物营销方案》中指出,医生和患者可以将非法的off-label药物营销直接报告给FDA。与美国不同,英国主要通过自我监管体系来披露“非法”off-label行为,依赖大众批判的声音,其立法也更重视和保护这类“吹哨人”[35]。
为了获得off-label类医疗手段全面、真实的研究数据,FDA也批准了off-label药物相关资料的获取渠道,例如药品使用方法,相关的研究数据、论著等。这些资料中近视控制有效性指标主要通过眼轴和屈光度指标来判定,因此IMI也对相关有效性说明有具体的要求,其必须是随机对照研究结果,并且,屈光度必须是扩瞳验光结果,眼轴测量必须是高分辨率的,结果需精确到最小分度10 μm。而且,动物实验的结果并不能作为临床决策的有力证据,必须依据监管部门认证或授权的实验室开展的人类临床对照研究[29-36]。
4 学术组织
学术组织在近视防控方法安全性和有效性科学数据的传播方面具有重要的作用,他们承担了以下4种主要职责。
4.1 公众卫生倡议
学术组织应通过国家层面的公共卫生举措唤起大众的眼健康意识,增强公众对近视现状的认识,并注重通过学校和教育机构科普高度近视的风险,以及近视防控的科学手段。然而目前一些公众平台发布的相关信息不是基于循证的,可靠性不高,学术组织有义务为临床医生和大众提供准确的信息[37-39]。
4.2 收集并建立信息源
要让大众获取有效、可靠的信息,必须建立一个可更新的知识平台,及时更新相关研究的最新进展。
4.3 建立学术研究和临床应用的桥梁
为了让临床医疗人员更便捷地获得最新学术研究结果,目前很多学术机构和专业组织承诺提供终身学习的机会,例如继续教育项目或课程研讨会。临床医生可以利用这些资源获取高质量的循证知识更新,并应用到临床操作中。除此以外,医生还可以阅读一些专业的已发表文献、国内和国际会议报告,获得更有针对性的知识。
4.4 眼科专业领域之外的科普
防控近视不能只靠眼科专业人士,大众同样需要获取相关知识,目前,中国已经在学校进行相关干预,如强化户外锻炼、减轻学生学业负担等[44]。国家要求小学老师都必须了解近视控制的新方法,并且能够将相关信息传达给家长和学生。儿科医生和其他科室医疗相关人员也应该对近视防控措施有所了解。当地学术组织应该积极推动科学知识的普及和及时更新。
5 医疗相关人员
5.1 行为指南
医疗人员在进行近视防控决策时,尤其是使用off-label药物时,需要提高警惕,明确了解治疗方案的专业原理,并且密切监控治疗效果和安全性,预防不良事件的发生。
从伦理角度看,患者有权了解药物、设备的授权状态,off-label治疗可能存在的未知风险,以及有效性依据,在充分知情的情况下,由父母或监护人决定是否接受治疗,如果可以,尽量使用通过批准的治疗方法。此外,医疗人员有义务告知患者父母或监护人,医保可能无法涵盖off-label的治疗方法,费用需要由患者自理。
FDA推荐医务人员对于近视防控策略选择的流程见图1
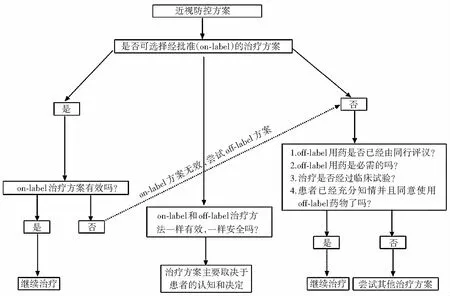
图1 近视防控策略选择流程图 注:on-label:说明书内;off-label:超说明书
5.2 资质许可
各国之间能够进行近视防控决策的从业者资质范围和培训水平有很大差别,在一些发达国家,如英国、美国、澳大利亚和加拿大,视光学专业已经成熟到成为一门独立的医学专业,视光师有资格开具近视防控的处方,但在许多其他国家,视光师只被允许开具框架眼镜和角膜接触镜处方,没有药品处方权。另一些国家,只有眼科医师有未成年人角膜接触镜的处方权,视光师没有权限。中国的现状是经过FDA批准的角膜接触镜可以由有执业资格的眼科医生在医院或眼科诊所开具处方,而眼镜零售店可以开具软性角膜接触镜处方,但不能验配OK镜。
因为产品注册和从业者资质在不同国家之间差异明显,所以“治疗许可资质”的标准化非常复杂,目前尚缺少定论。
6 近视防控医疗产品应该如何销售
销售需要建立在宣传的基础上,近视防控产品的销售需要先将相关的知识技能传递给服务在近视防控一线的医疗工作者,可以通过科研会议、论著或者讲座的形式,但这些活动举办周期通常比较长,一般为每年1次或每2年1次;职业继续教育项目也能为临床工作者和科研人员传授知识和技能。
除此以外,利益相关者还需要给更广泛的群体提供相关的产品知识或技能,包括临床相关人员,视光产业、眼科产业或医药企业、产品监管部门、从业者立法部门、医疗保健机构、学术机构、视觉与眼健康协会、执业协会从业人员,以及患者群体。
当然,企业也可以寻求其他渠道的跨领域合作来促进近视防控医疗产品的销售和宣传,包括非政府组织、非光学企业、个人或公司。合作伙伴可以为近视防控项目提供资金来源,直接或间接地增加相关产品的销售量,开发新的市场,从而使行业受益。在合作的过程中应注意,这类项目的赞助需要进行伦理监管以避免任何潜在的利益冲突,并保证最终获益者是患者。
7 总结
对目标人群进行近视防控治疗会带来各种利益相关者的道德挑战。监管机构、制造商、研究者和医疗人员都有共同的道德责任,负责确保公司使用的产品是安全且有效的,并且配戴者对治疗的作用效果及潜在风险充分知情。医疗人员有义务为有近视发展风险的患者提供准确的治疗相关信息。IMI的报告强调了这些伦理问题的现状,并为利益相关者提供了产品发展、获取经济支持、处方、宣传、销售等方面的可行建议方案。
利益冲突所有作者均声明不存在利益冲突
