煤化学链燃烧载氧体研究进展
2021-04-08白歆慰刘金昌
白歆慰,刘金昌,白 磊
(1.美国西弗吉尼亚大学 化学与生物工程系,摩根敦 26505;2.中国矿业大学(北京) 化学与环境工程学院,北京 100083)
0 引 言


本文将综述近年来固体金属载氧体的研究进展,讨论载氧体和燃料的反应路径、机理和潜在的问题,并对未来研究方向进行展望。
1 煤的化学链燃烧反应途径
1.1 煤的原位气化化学链燃烧的反应途径
煤的化学链燃烧由3个主要部分构成:燃料反应器、氧化反应器、载氧体,3者关系如图1所示。在原位气化化学链燃烧(Gasification chemical looping combustion,iG-CLC)过程中,高温下,煤首先被热解生成煤焦(C)和气体挥发物(CO、H2、CH4等)。气体挥发物在燃料反应器中被载氧体(MexOy)氧化,生成CO2和水。与此同时,煤焦与气化剂(如水蒸气)在高温下发生煤气化反应生成CO和H2,一部分焦炭与CO2发生Boudouard反应生成CO。焦炭理论上也可以与载氧体发生氧化还原反应释放热量,但反应速率比气体挥发物和载氧体的反应速率慢得多。被还原的载氧体(MexOy-1)被传送至氧化反应器中被空气氧化再生。气体挥发物被载氧体氧化的过程比较复杂。Cheng等[13]通过DFT模拟CH4在铁基载氧体的氧化,发现吸附在载氧体表面的Fe位点的CH4首先裂解成CHx自由基,释放出氢离子。这些氢离子与表面的晶格氧结合生成水分子,脱离载氧体表面形成载氧体表面的氧空位。下层的晶格氧可以通过扩散填充表面的氧空位,然后吸附在Fe位点的C再次结合附近的表面晶格氧,生成CO2并脱附。由此可见,载氧体在此体系中起到了举足轻重的作用。
1.2 煤的氧解耦化学链燃烧的反应途径
除了原位气化燃烧的反应途径,氧解耦化学链燃烧(Chemical looping with oxygen uncoupling,CLOU)也是煤的化学链燃烧途径。这个反应系统最早由Mattisson等[14]提出。该反应装置与原位气化化学链燃烧(图1)基本相同,主要区别在于燃料燃烧的反应机理。在燃料反应器中,高温下除了煤的热解,载氧体也发生脱氧反应释放出气态氧后与焦炭和煤的气态挥发物发生燃烧反应。这个反应过程中没有煤气化反应,因此不需要水蒸气的参与。该反应系统对载氧体的性能有较高要求:燃料反应器中载氧体需有良好的氧解耦性能,且被还原的载氧体在氧化反应器中需易被氧化。因此,2种反应系统中载氧体的成分有较大差异。值得注意的是,同一种载氧体在煤的化学链燃烧中可以同时存在这2种反应途径,部分研究称之为氧解耦辅助化学链燃烧(Chemical looping assisted by oxygen uncoupling,CLaOU)[15]。这类载氧体的研究还处在起步阶段,因此本综述将不做单独讨论。

图1 煤的iG-CLC和CLOU化学链燃烧反应装置示意
2 铁基载氧体的发展
铁基载氧体价格低廉、环境友好。由于铁矿资源储量丰富,铁基载氧体的生产成本低于其他金属基载氧体,如铜、镍等。值得注意的是,部分研究发现天然铁矿石可被直接作为化学链燃烧的载氧体使用[16-17],且铁作为日常生活使用的材料,无毒无害,因此,铁基载氧体受到了国内外学者广泛关注[18-19]。在煤的化学链燃烧中,铁被普遍认为有4种存在形式:单质Fe、FeO、Fe3O4以及 Fe2O3。Chen 等[20]研究了铁氧化物的CO还原反应动力学,发现Fe2O3还原至Fe3O4的反应活化能明显低于Fe3O4→FeO 以及FeO→Fe。一般来说,化学链燃烧中使用燃料的还原性低于CO。所以,使用单一铁氧化物作为载氧体的反应速率及载氧能力较低。近年来,学者主要使用碱金属掺杂和复合组分法来解决这个问题。由于铁基载氧体的化学特性,单一的铁基载氧体一般适用于iG-CLC反应途径。

综上,单一铁基载氧体虽然价格低廉,但反应速率有限且机械强度不佳。目前研究通过使用惰性载体和黏合剂可以提升载氧体机械强度从而延长使用寿命。适量掺杂碱金属或碱土金属可以合成具有特殊铁酸盐结构的载氧体,从而提升载氧体的反应活性与稳定性。
3 锰基载氧体的发展
与铁基载氧体相似,锰基载氧体同样具有价格低廉以及环保的优点。相对于铁基载氧体,锰基载氧体有着较高的载氧能力和熔点。自然界中锰有+4、+3 等多种氧化态,其中氧含量最高的二氧化锰在500 ℃分解成三氧化二锰和氧气,而三氧化二锰虽然热力学稳定,但一旦还原成低价锰氧化物后在高温下非常难再生,而再生产物仅为四氧化三锰[43]。因此,在煤气化化学链燃烧中,锰的氧化还原循环被认为是Mn3O4/MnO,且在900 ℃下,被还原的载氧体中单质锰并未被发现[44]。
在煤的化学链燃烧中,单一锰氧化物载氧体的反应性能并不理想。以甲烷化学链燃烧为例,在950 ℃反应条件下,甲烷转化率最高仅为40%左右,而使用铁基载氧体在第1个循环达到接近100%的甲烷转化率[45]。此外,单一锰氧化物载氧体的颗粒强度不够,从而导致载氧体快速损耗。因此,近年来学者使用惰性载体负载或混合氧化锰载氧体来加强氧传递能力以及载氧体机械强度。Galinsky等[46]通过半经验法和DFT计算氧空位生成能,选择了锶作为添加剂,合成了A位Sr修饰的钙钛矿型Ca0.75Sr0.25MnO3载氧体,发现锶的添加可以阻止高温下钙钛矿结构的分解,且这种新型载氧体在较低温度(~650 ℃)下可进行氧解耦反应,释放出气态氧,从而提升载氧体的稳定性和反应能力。热重试验结果表明焦炭的转化率可以达到100%,且载氧体的氧解耦能力可以维持100个循环不退化。Hanning等[47]通过烧结Mn3O4和SiO2、TiO2的混合物制得载氧体,并分别使用甲烷、合成气以及木焦炭测试载氧体的反应活性。通过表征发现氧化锰与氧化硅烧结时可以形成褐锰矿型(Mn7SiO12)和蔷薇辉石型(MnSiO3)晶体结构,在高温(约1 050 ℃) 缺氧条件下这些晶体可相变成二价的尖晶石型(Mn3O4)和锰橄榄石型(Mn2SiO4)晶体从而释放出气态氧。通过这种方式可以较大改进锰基载氧体的氧传递能力。添加二氧化钛虽然降低了载氧体的孔隙率,从而一定程度上抑制了氧解耦能力和反应活性,但极大提升了载氧体的机械强度,从而将载氧体的使用寿命从7 h延长至至少24 h(连续运行)。结果还表明可燃气体主要通过与锰基载氧体的晶格氧发生氧化还原反应,而固态焦炭则是与这种载氧体高温下释放的气态氧发生反应。Schmitz等[48]在中试化学链燃烧器(10 kW,流化床) 测试Mn3O4-SiO2-TiO2载氧体性能,发现煤的转化率可以达到94.5%,且载氧体寿命预计可达几百至几千小时。Kun等[49]使用修正Stöber法合成核壳结构的Mn@meso-SiO2作为化学链煤气化的载氧体制取合成气,煤的转化率可达80%且合成气的选择性可达78%。该研究指出这种锰载氧体能实现比较好的煤与载氧体之间的固固反应。Nascimento等[50]使用浸渍法将锰(20%)负载到使用微波辅助燃烧法制备的铝酸镁载体上,通过热重分析发现使用这种载氧体可以实现100%的煤燃烧,被还原的载氧体可完全被空气氧化再生。通过XRD分析,Nascimento等[50]确认了MgMn1.75Al0.25O4复杂晶体结构以及Mg6MnO8和MgMn2O4固溶体的存在。该课题组[51]早期发现Mg6MnO8具有非常高的理论传氧量(R0) 。Chung等[52]通过热重分析发现Mg6MnO8存在松散附着和紧密附着2种不同类型的晶格氧,松散附着的晶格氧可在高温(840 ℃) 惰性气氛中以气态氧形式释放,而紧密附着的晶格氧可在高温下和还原性物质(如煤焦)发生反应。该研究还确认了紧密型晶格氧的含量约是松散型的1.5倍(质量比)。因此,这种锰载氧体对iG-CLC和CLOU反应系统均适用。

表1 含碱金属(如K、Na等)铁基载氧体的制备

表2 含碱土金属(如Ca、Ba等)铁基载氧体的制备
除人工合成锰基载氧体外,也有研究直接使用锰矿石作为价格低廉的载氧体进行煤的化学链燃烧反应。Mei等[53]研究了4种不同组分的锰矿石在煤的化学链燃烧反应的表现,结果显示锰矿石比铁矿石更能促进焦炭的气化速率。认为除了矿石中的Mn3O4可以氧化气态挥发物外,锰矿石中的钾、钠和钙在高温下被气化释放后可与焦炭颗粒结合,对焦炭气化有催化作用,提高了焦炭的转化速率。这几种锰矿石和焦炭不会发生固固反应。Velasco-Sarria等[54]使用产于西南哥伦比亚的锰矿石(主要成分为85.6%的蔷薇辉石和6.1%的方铁矿)作为载氧体测试次烟煤的化学链燃烧。结果发现固体燃料可以被完全燃烧,反应机理被认为是焦炭气化的产物和锰矿石中的结晶氧发生氧化还原反应,反应过程中载氧体并不会释放出气态氧。Linderholm等[55]在全尺寸化学链燃烧器(100 kW,流化床) 测试哥伦比亚煤和木焦炭的煤气化化学链燃烧,煤的转化率可达80%以上且气化后的气体转化率达到88%。在这种大型反应装置中,锰矿石载氧体的寿命长达100~400 h。锰基载氧体的制备方法和条件见表3。

表3 锰基载氧体的制备
综上,由于反应活性和颗粒强度的限制,单一锰基载氧体的反应活性并不理想。通过使用惰性成分(如TiO2)以及合成特殊的晶体结构,锰基载氧体的机械性能以及反应性能得到较大提升。与一般铁基载氧体不同的是,部分锰基载氧体在一定条件下可以释放气态氧,而气态氧的存在可以有效提升煤气化后固态成分(如焦炭)的转化。因此,这种反应机理方面的差异可以提升煤的总转化率。
4 复合组分载氧体的发展
除了传统的铁基、锰基等单一组分载氧体外,近年来,越来越多研究者开发含有2种或更多种金属的复合载氧体。通过添加或混合其他金属,如铜、镍等,载氧体的强度、寿命以及反应活性均显著提高。本文将主要讨论含铜、硫酸钙(CaSO4)以及其他组分复合载氧体的研究进展。
4.1 含铜载氧体的发展
研究表明,与铁基载氧体比较,铜基载氧体拥有更高的载氧能力与氧传递能力,理论上拥有更高的反应活性[56-58]。并在一定条件下,CuO可以发生氧解耦反应,释放出气态氧从而被还原成Cu2O。然而,铜价格较为昂贵且熔点较低易烧结,因此,铜常被作为次要组分或活性添加剂与传统的载氧体混合,不但可以在燃料反应器中释放气态氧,也可以增加载氧体的机械强度,提升煤燃烧的反应活性和载氧体寿命。
早期研究发现铜与合成气的氧化还原反应是吸热反应,而铁与合成气的氧化还原反应是放热反应,因此,铜-铁双金属载氧体在燃料反应器中理论上可以实现自热平衡[59]。由于这种特性,铜-铁双金属载氧体近年来被广泛研究。Siriwardane等[60-61]使用喷雾干燥法制备30% CuO-30% Fe2O3/40% Al2O3载氧体(流化床),发现850 ℃下载氧体可以释放出气态氧,因此未添加水蒸气气化剂时也可与煤(烟煤与次烟煤)发生燃烧反应,但在燃料反应器中添加水蒸气后氧解耦过程会被抑制。添加水蒸气后可以达到100%的煤气化转化率。这种制备方法可以大批量商业化生产载氧体,从而大大降低载氧体的制备成本。Jiang等[62]通过混合赤铁矿载氧体和CuO制得Fe-Cu载氧体(CuFe2O4)。与Siriwandane等[60-61]制备的载氧体相比,铁矿石中含有的碱金属与碱土金属可以提高反应速率,添加CuO后载氧体的寿命也有了一定提高,然而,Jiang等[62]通过SEM表征发现,过度添加CuO(Cu/Fe>2.7)会导致金属烧结从而降低载氧体的反应速率。Yang等[63]混合铁矿石(赤铁矿)和铜矿石(主要成分CuFe2O4和CuO),通过比较添加单位质量铜矿石对传氧系数、反应速率和释氧系数的影响,发现添加铜矿石的最佳比例为10%~20%。Tian等[64]使用水泥作为黏合剂结合废弃的赤铁矿和铜矿石粉末制得不同Cu-Fe比的载氧体,发现Cu/Fe质量比为20%时可实现理论上的自热平衡;产物中二氧化碳浓度从18%(未添加铜)提升至21%(20%铜)。通过XRD确认,水泥中Ca2Al2SiO7相在高温下非常稳定,且可以有效减缓载氧体中的金属聚集现象。Wang等[65]通过混合废弃的铜矿石粉末、赤泥(含Fe2O3)和水泥黏合剂制备低成本的载氧体并实现了较高的反应活性:载氧体/燃料比为2.5时褐煤的燃烧效率从92%提升至最高97%。相对于氧化铁,氧化铜具有更高的氧传递能力,但高温下易产生聚集导致失活;铁矿石的加入可以减缓这种聚集从而改进铜矿石的氧传递能力。铁矿石中的Fe2O3可与铜矿石表面的CuO反应生成CuFe2O4,而CuFe2O4拥有很高的氧传递能力,从而提高了这种载氧体的反应活性。这些研究都通过XRD等表征发现了载氧体中CuFe2O4的存在。CuFe2O4并不能等同于CuO和Fe2O3的混合物。Liu等[66]使用热重分析CuFe2O4的还原,发现CuFe2O4的还原反应速率高于CuO、Fe2O3混合物的还原反应速率;CuFe2O4拥有尖晶石结构(Fe3+[Fe3+Cu2+]O4),当CuFe2O4被还原生成Cu单质后从尖晶石结构中分离,产生晶格缺陷。Siriwardane等[67]提出这种晶格缺陷可以加速气体扩散,从而使得Fe2O3更易被还原。还发现CuFe2O4中Cu—O键比氧化铜中的Cu—O键更长,CuFe2O4具有更高的还原反应速率。除了铜-铁双金属载氧体外,近年来还有其他含铜双金属载氧体的研究,如西班牙碳化学研究所(Instituto de Carboquimica)[68-70]开发的Cu-Mn载氧体在880~930 ℃时有较高的气态氧生成速率,每千克载氧体的气态氧生成速率可以达到0.31×10-3~0.62×10-3kg/s(880~930 ℃),且载氧体寿命预计可达20 000 h;O′Malley等[71]使用选择性吸附浸渍法制备了CuO/NiO@SiO2复合载氧体,发现少量添加NiO促进剂(摩尔分数1%)可以加速Cu2O→CuO的氧化过程,而多孔的SiO2载体可以分散负载的金属并避免高温下的金属聚集,使得该载氧体可在975 ℃高温条件运行不失活,从而提高了载氧体的反应活性和寿命。Yan等[72]合成了多种铜基双金属载氧体,虽然载氧体和焦炭的反应速率较高:铜-钴载氧体在950 ℃下碳转化率10 min内达到100%,且二氧化碳选择性接近100%;煤燃烧过程中,由于载氧体烧结和煤灰的堆积等原因,载氧体易失活;以铜-钴载氧体为例,载氧体的传氧系数从第1个循环的8.25%退化至第20个循环的不足5%。Dai等[73]研究发现煤气化产生的煤灰对含铜载氧体的氧解耦性能有抑制作用,从而降低反应活性。因此,煤灰分离造成的载氧体失活也应当被重视。表4总结了部分重要文献的载氧体的制备方法和条件。
综上,由于优秀的氧解耦性能,含铜的载氧体被广泛研究。铜-铁复合载氧体可以通过iG-CLC和CLOU两种路径实现煤燃烧。铜-锰复合载氧体相比单一组分载氧体拥有更高的氧解耦效率。然而,铜及其氧化物的低熔点使得含铜载氧体易失活。因此,如何攻克这一难题是下一步研究重点。

表4 含铜复合载氧体的制备
4.2 含CaSO4载氧体的发展

Zhang等[76]通过向CaSO4载氧体上添加锂、钠、钾的三元共晶盐制得新型CaSO4载氧体,将煤焦的转化率从77.46%提升到86%,加快了反应速率。XRD证明了烧结过后的载氧体上碱金属以多元碳酸盐(LiKCO3、LiNaCO3等)形式存在,而这种多元碳酸盐在反应温度(920 ℃)下分解成金属氧化物、氢氧化物或单质,并呈现熔融状态。这种熔融盐可使CaSO4表面出现熔化从而加强还原气体在CaSO4载氧体上的扩散效果。 Ding等[77]通过向CaSO4中添加少量赤铁矿(Fe2O3∶CaSO4≤ 0.28)制备新型Fe2O3/CaSO4载氧体,发现载氧体的寿命、碳转化率以及CO2产率显著提高(925~975 ℃)。该研究还指出,添加的铁氧化物对CaSO4和还原性气体的反应有催化作用。但随着循环次数增加,CaSO4和Fe2O3的交界处会产生CaS层,导致反应气体扩散速率降低,从而降低Fe2O3的催化效果和载氧体的反应活性。Sunphorka等[78]通过湿法混合Fe2O3和CaSO4粉末后烧结制得不同比例的Fe2O3/CaSO4载氧体,发现了20% Fe2O3/CaSO4载氧体可以提高煤化学链燃烧的反应速率以及CO2产率(950 ℃)。Zhang等[79]将CaCO3和CaSO4作为促进剂加入Fe2O3/Al2O3载氧体中,通过研究CO的化学链燃烧,发现添加5%的CaSO4可以将CO转化率从85.8% 提升至100%。从反应动力学角度来说,添加CaSO4可以降低CO化学链燃烧反应的活化能。高温下CaSO4发生的分解反应虽然对燃烧反应有促进作用,但该研究通过XRD发现这种载氧体中Ca可与Al2O3载体结合生成CaAl2O4和CaAl4O7,使CO转化率降低[79]。这种载氧体在煤的化学链燃烧中的作用还需进一步研究。除铁-CaSO4载氧体外,Wang等[80-83]还开发了CaSO4-CuO、CaSO4-Mn3O4、CaSO4-CoO和CaSO4-Ca2CuO3煤燃烧载氧体,均具有较好的性能和寿命。表5总结了这些载氧体的制备方法。综上,复合CaSO4载氧体是今后煤燃烧载氧体的一个重要研究方向。

表5 含CaSO4复合载氧体的制备
4.3 其他复合载氧体的发展
一些其他复合金属载氧体近年来也被广泛研究。Shafiefarhood等[84]发现铁-锰和铁-钴复合氧化物载氧体在860~950 ℃可以释放出气态氧;使用钙钛矿作为载体可进一步提高载氧体的反应活性和使用寿命。该研究认为在高温下,钙钛矿载体也有解耦合晶格氧的能力,且氧解耦的能力随着Mn或Co负载量的增加而增强。Pérez-Vega等[85]发现铁-锰混合氧化物载氧体在空气中高温烧结后具有方铁锰矿型((MnxFe1-x)2O3)结构,该结构在惰性气氛中高温下可分解成尖晶石型((MnxFe1-x)3O4)结构并释放出气态氧,而且尖晶石型结构还可以进一步分解成含锰的方铁矿型(MnxFe1-xO)结构,释放气态氧。因此,这种载氧体在气态(CO、H2)和固态(煤)燃料化学链燃烧中具有良好的反应活性,反应后的载氧体具有磁性,使得载氧体和煤灰分离更加容易。该研究组近期发现添加二氧化钛后,在高温惰性气氛中,方铁锰矿型和尖晶石型结构中的锰可以与二氧化钛结合生成红钛锰矿型(MnTiO3)结构并释放出气态氧,进一步增强载氧体在高温下的脱氧能力,从而更有利于煤的化学链燃烧[86-87]。Galinsky等[88]发现使用铁修饰B位的CaMnO3钙钛矿型载载体(CaMn1-xFexO3,x≤0.5)在较低温度(600 ℃)下即有良好的氧解耦能力,850 ℃下可以达到90%以上的煤焦转化率。钙钛矿结构非常稳定,850 ℃反应条件下可以维持100个循环。Miccio等[89-91]开发了一系列使用多孔的聚硅酸钾作为载体负载铁和铁-锰的载氧体,这种载体可以提高载氧体的机械强度,且负载的锰和载氧体结合成的硅酸锰可以加强载氧体在高温下氧解耦的能力,从而提高煤焦的转化率。Chung等[8]创造了高机械强度的铝基骨架包裹的铁-钛载氧体,在中试反应器下测得寿命高达3 000个循环,但未详细介绍铝基骨架的合成手段。早期研究发现镍基载氧体具有良好的反应性能[92],但也具有易硫毒化、成本较高、环保性能不佳等缺点[93]。因此,近年镍基载氧体研究较少,更多作为促进剂或次要组分进行研究。Frick等[94]测试了一系列不同金属比例的Mn-Ni载氧体,发现Mn-Ni(质量比2∶1,烧结温度1 200 ℃)载氧体对于合成气和甲烷化学链燃烧有良好的反应活性,二氧化碳产率接近100%;然而高温下(1 050 ℃)的金属聚集问题亟需解决。通过相图,Frick等[94]认为高转化率是由于高温下Mn-Ni尖晶石结构((NixMn1-x)3O4)被转化为NixMn1-xO从而释放出气态氧。Lin等[95]合成了MgO-NiO促进的红泥载氧体,通过研究甲烷的化学链燃烧,发现甲烷转化率从未添加促进剂的53%提升至最高75%,且二氧化碳选择性为99%(MgO、NiO与红泥的质量比为10∶15∶75)。通过XRD表征发现添加NiO后烧结可生成NiFe2O4结构,这种结构对甲烷的氧化有促进作用;而且镍的存在可能促进甲烷热解,生成无定型碳和氢气;相比于甲烷,无定形碳更易被晶格氧氧化[95]。表6总结了这些载氧体的制备方法。
综上,通过添加新的组分或改变载氧体结构可改变载氧体与燃料反应的路径以及载氧体的机械强度,有效延长载氧体寿命以及改善载氧体性能。含镍的复合载氧体也有一定进展,但高温金属聚集以及硫毒化问题还需进一步研究。目前新型复杂组分载氧体的研究相对较少,亟需更多的研究成果。
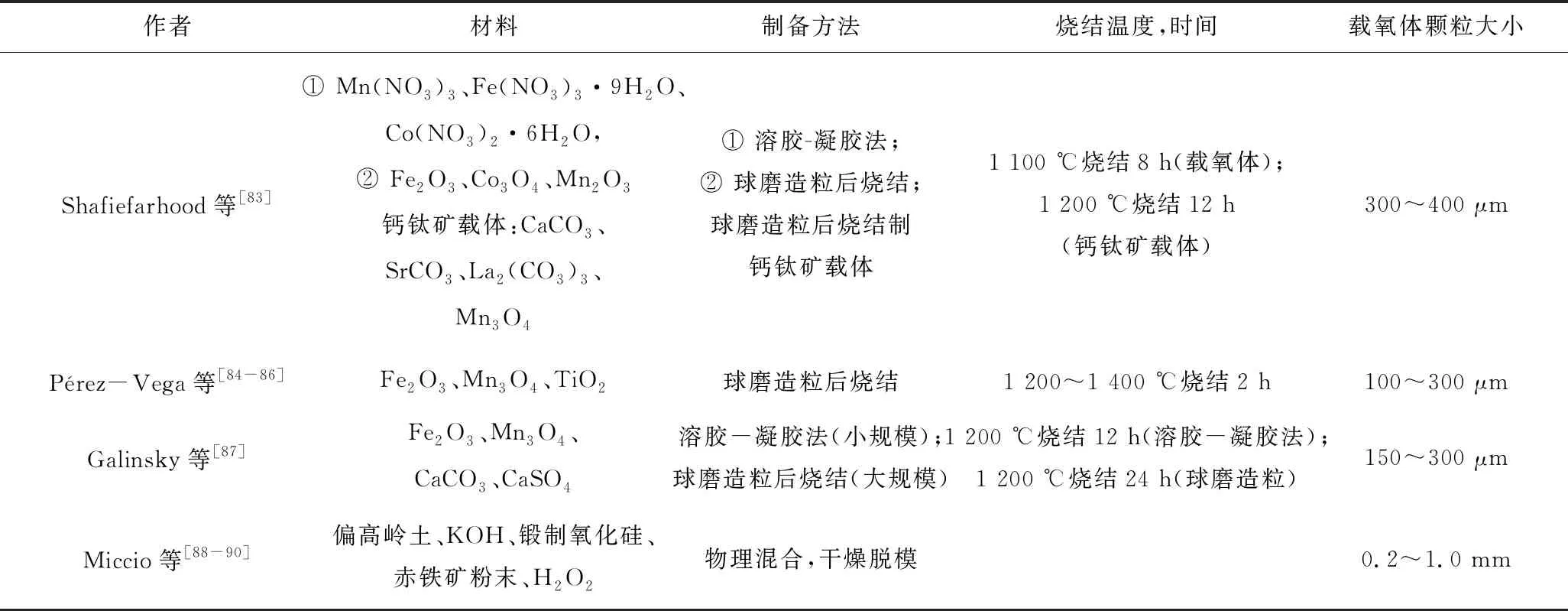
表6 其他复合载氧体的制备
5 结语与展望
近年来,化学链燃烧技术吸引了国内外学者广泛关注,载氧体作为燃料反应器和氧化反应器中氧的传递媒介,在化学链燃烧技术中起到了举足轻重的作用。近年来,大量研究成果有效改善了载氧体的性能和使用寿命,通过试验、表征和分子模拟等手段对载氧体与燃料之间的反应机理以及载氧体失活原理有了进一步的认知。
1)铁基载氧体具有环保、价格低廉等优点,但载氧能力偏低。铁基载氧体一般不与煤焦进行固-固反应。添加碱金属可以增强铁基载氧体的氧传输能力,且对煤气化燃烧过程中的Boudouard 反应有催化作用,从而提高煤焦转化率。但过量添加有可能造成载氧体颗粒聚集,从而导致载氧体失活。适量添加碱土金属可以通过形成铁酸化合物而增强载氧体的反应活性,但过量添加可能导致载氧体载氧能力的降低。
2)锰基载氧体同样具有环保、价格低廉等优点,在高温惰性气氛下可进行晶型转换从而释放出气态氧,加速燃烧反应。但单一锰基载氧体的反应活性和颗粒强度不足,通过使用惰性载体或添加碱土金属形成特殊的晶体结构,一方面改善锰基载氧体的氧解耦能力,另一方面加速还原气体和晶格氧的反应速率,从而有效提高锰基载氧体的表现。此外,直接使用含碱金属或碱土金属的锰矿石也可以有效提升载氧体的表现。
3)通过合成新型双金属或多金属氧化物载氧体可以避免单一金属载氧体的缺陷,从而提升载氧体的性能。含铜载氧体具有较好的氧解耦性能,但由于铜及其氧化物的熔点较低,易产生金属聚集,且煤灰堆积会影响含铜载氧体的氧解耦能力。这些问题在载氧体设计中应被关注。
对于目前载氧体研究的发展成果以及所遇到的挑战,从以下4方面提出发展建议:
1)通过结合煤燃烧iG-CLC和CLOU两种反应机理设计新型的CLaOU载氧体。通过同时存在晶格氧和气态氧,提高载氧体的传氧效率,从而提升燃料的转化率和燃烧效率。
2)现有新型材料载氧体的研究较少,如聚合物负载金属氧化物载氧体等。这些新型组分载氧体将是未来载氧体的创新方向之一。
3)使用工业废料并添加其他促进剂合成的载氧体也具有较为广阔的发展前景。通过这种方式进行废物利用,有利于环境保护以及降低载氧体的生产成本。
4)通过合成包括核壳结构和特殊骨架结构在内的新型特殊结构载氧体可以解决载氧体金属聚集、机械强度、气体扩散速率等问题。因此,特殊结构载氧体将会成为未来载氧体的重要发展方向之一。
