从高考题看辩证思维的运用——以“外界条件对可逆反应的影响”相关问题为例
2021-04-08湖北
湖北
催化剂、温度、压强、浓度等外界条件对可逆反应的影响是化学反应速率和化学平衡章节的重要内容,可结合实际的生产、生活和科学研究情境,讨论外界条件对可逆反应的影响问题,可以考查考生进行四个层次的能力,是新高考的热点问题。
此类问题的难点主要有两个方面:一是可逆反应可受多种外界条件影响,其中温度、浓度、压强和催化剂是主要的影响因素,而催化剂的影响又与温度有关;二是外界条件可以从多个角度影响可逆反应,如反应速率、反应限度、反应能耗以及反应设备要求等。笔者发现,运用辩证思维能有效解决与外界条件对可逆反应的影响有关的问题。
一、辩证思维的运用基础
辩证思维是认识事物的科学思维方式,其特点是从影响事物的各个相互联系的方面进行分析,以便从整体上、本质上全面地认识事物。温度、压强、浓度和催化剂是影响可逆反应的关键因素,从这些方面进行综合分析能更加完整地认识外界条件对可逆反应的影响。对立统一规律是辩证思维的基本规律之一,揭示了事物发展变化的根本原因是具有矛盾性。例如对于合成氨反应来说,高温有利于加快反应速率,却不利于提高反应限度,那么合成氨的条件是选择低温还是高温就需要在对立中把握反应速率与反应限度的平衡,即根据催化剂活性选择反应温度。分析综合是辩证思维的体现,分析是把可逆反应分解为反应速率、反应限度、生产能耗等不同的方面,分别研究外界条件对这些方面的影响,而综合是按照实际生产条件的要求、结合化学反应速率和化学平衡移动原理进行综合调控,以形成更加深刻的认识。
二、辩证思维的运用模型
在高考题中,外界条件对可逆反应的影响涉及多个方面,如温度、催化剂、浓度、压强等,所以在分析题目时首先要确定研究对象,再分析对象的各个影响因素,研究单个因素对其产生的影响,最后按照实际生产的需要在对立中把握统一,辨别主要因素和次要因素,综合分析结果,进而得出结论。运用辩证思维解答此类问题的思维模型如图1所示:
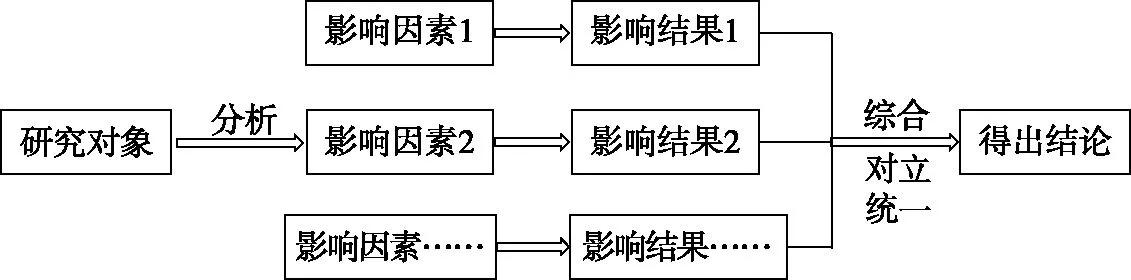
图1
三、辩证思维的运用实例
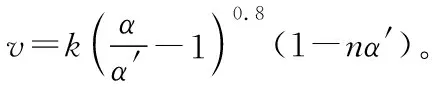
式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α′为某时刻SO2转化率,n为常数。在α′=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v-t曲线,如图2所示。

图2
曲线上v最大值所对应温度称为该α′下反应的最适宜温度tm。t
【答案】温度升高,k增大使v逐渐提高,但α降低使v逐渐下降。当t
【解析】该图为速率—温度曲线,研究对象是速率,根据速率方程,在α′一定的情况下,影响速率大小的因素有两个:k和α。运用辩证思维的分析模型如图3:
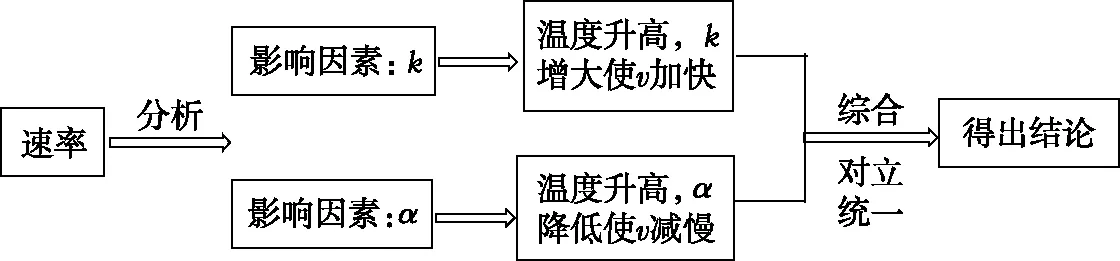
图3
【点拨】在本题中,分析对象是速率,图像信息只涉及了温度对反应速率的影响,但是结合速率方程可知温度是通过影响k和α两个方面最终影响反应速率,再分析温度变化对这两个因素的影响,最后进行综合分析得出结论。分析过程体现了辩证思维的特点,从对象在各个方面的相互联系中进行考查,以便从整体和本质上认识对象。



图4
②在恒容的密闭容器中充入一定量的NO和O2气体,保持其他条件不变,控制反应温度分别为T3和T4(T4>T3),测得c(NO)随t(时间)的变化曲线如图5。转化相同量的NO,在温度________(填“T3”或“T4”)下消耗的时间较长,试结合反应过程能量图(图4)分析其原因:。

图5
【答案】T4温度升高,反应Ⅱ的速率加快;ΔH1<0,温度升高,反应Ⅰ平衡逆向移动,c(N2O2)减小,反应速率减慢。浓度降低的影响大于温度对反应Ⅱ速率的影响
【解析】分析曲线可知,转化相同量的NO在温度为T4时消耗的时间较长,说明温度为T4时反应速率较慢,为什么温度越高反应速率越慢呢?当影响反应速率的变量只有温度时,则温度升高,反应速率加快。故一旦出现温度升高反应速率却减慢的情况,则可判断影响反应速率的因素除了温度外,还可能有反应物浓度或催化剂的活性等其他因素。
结合图4所示反应历程可知Ea1 图6 【点拨】本题综合性较强,问题层次较深,分析影响反应速率的因素难度较大。其一是考查了化学反应历程的相关知识,即活化能越小反应速率越快,总反应速率由慢反应过程的速率决定;其二是影响反应Ⅱ速率的因素有温度和反应物的浓度,反应Ⅰ快速平衡后在温度的影响下平衡发生移动,导致N2O2浓度减小,间接造成了对反应Ⅱ速率的影响。慢反应即反应Ⅱ是决定总反应速率的步骤,但在温度变化时反应Ⅰ也通过平衡移动所产生的影响证明了自己的重要性,所以反应历程中的两步反应过程彼此联系、相互影响,体现了认识事物就要认识事物的各个方面,认识事物本质的辩证思维。 【例3】(2019·江苏卷·20节选)CO2的资源化利用能有效减少CO2排放,充分利用碳资源。 (3)CO2催化加氢合成二甲醚是一种CO2转化方法,其过程中主要发生下列反应: ΔH=-122.5 kJ·mol-1 在恒压、CO2和H2的起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图7。其中: 图7 ①温度高于300℃,CO2平衡转化率随温度升高而上升的原因是。 【答案】反应Ⅰ为吸热反应,升高温度,平衡向正反应方向移动,CO2的平衡转化率增大,反应Ⅱ为放热反应,升高温度,平衡向逆反应方向移动,CO2的平衡转化率降低。根据图像可知上升幅度超过下降幅度 【解析】题目分析的对象是CO2的平衡转化率,由反应Ⅰ和反应Ⅱ共同决定,运用辩证思维的分析模型如图8: 图8 【点拨】本题的分析对象是CO2的平衡转化率,反应对象涉及相互关联且相互竞争的两个反应,而两个反应中一个是吸热反应,一个是放热反应,反应特点不同,升高温度对两个可逆反应的影响结果相互矛盾,最终的结论表现了矛盾双方的对立统一。 解答此类题时一定要辨析清楚题目所给出的转化率、产率、体积分数或含量是否为平衡状态的量,若不是平衡量,问题的分析角度就会发生变化。 以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的热化学方程式如下: (2)图9为丙烯腈产率与反应温度的关系曲线,最高产率对应的温度为460℃。低于460℃时,丙烯腈的产率________(填“是”或者“不是”)对应温度下的平衡产率,判断理由是 ; 高于460℃时,丙烯腈产率降低的可能原因是________(双选,填标号)。 A.催化剂活性降低 B.平衡常数变大 C.副反应增多 D.反应活化能增大 图9 【答案】不是 该反应为放热反应,平衡产率应随温度升高而降低 AC 【解析】本题曲线中的产率未指明是否为平衡产率。当温度低于460℃时,产率随温度的升高而增大,变化结果与平衡产率的变化趋势不一致,所以此时为非平衡产率。温度高于460℃时的产率是否一定为平衡产率呢?通过分析题干信息可知,反应除了生成丙烯腈外还有副产物丙烯醛生成,所以影响产率的因素可能还存在副反应;反应条件有催化剂,而催化剂的活性会受到温度的影响;当然,如果反应达到平衡状态,则升高温度平衡逆向移动也可能导致产率降低。运用辩证思维的分析模型如图10: 图10 【点拨】温度低于460℃时,产率随温度的变化结果与平衡产率随温度的变化趋势不一致,所以此时为非平衡产率,这个结论相对容易得出。但温度高于460℃时的产率是否一定为平衡产率呢?图10是产率—温度曲线,随温度的变化曲线出现了拐点,按照学生的习惯性思维,容易误判为最高点和最高点之后是平衡状态,最高点之前是非平衡状态,所以培养学生的辩证思维能有效解决思维定式的问题。从辩证思维的角度全面分析影响产率的因素,并且认识到这些因素之间是彼此联系的,如加入催化剂能加快反应的速率,升高温度也能加快反应的速率,但两个因素同时作用时,对速率的影响结果就不能确定了,因为催化剂的催化活性受到温度的影响。 本题影响产率的因素除平衡移动因素外,还有速率因素和副反应因素,所以温度高于460℃时的产率不一定是平衡产率。但如果影响因素只有平衡移动,则该产率为平衡产率。故在遇到此类问题时,若判断影响因素有多个时,则应先分析单一因素的影响,再进行综合分析。 “外界条件对可逆反应的影响”的相关问题包含外界条件对浓度、速率、转化率、含量等多个方面的影响,这些因素之间又相互联系,试题中所讨论的可逆反应状态一般涉及非平衡和平衡两种状态,非平衡状态下的影响主要是从速率的角度讨论,平衡状态下的影响主要从平衡移动的角度讨论。纵观此类高考题的设问,大都情况复杂、综合性较强、难度较大,辩证思维是解决此类高考题的有效方法,运用辩证思维模型,先确定研究对象,判断可逆反应所处状态,依据事物之间的普遍联系找出影响对象的不同因素,再依据反应速率理论和化学平衡原理分析影响对象的结果,最后按照对立统一的规律从整体上、本质上进行综合以得出结论。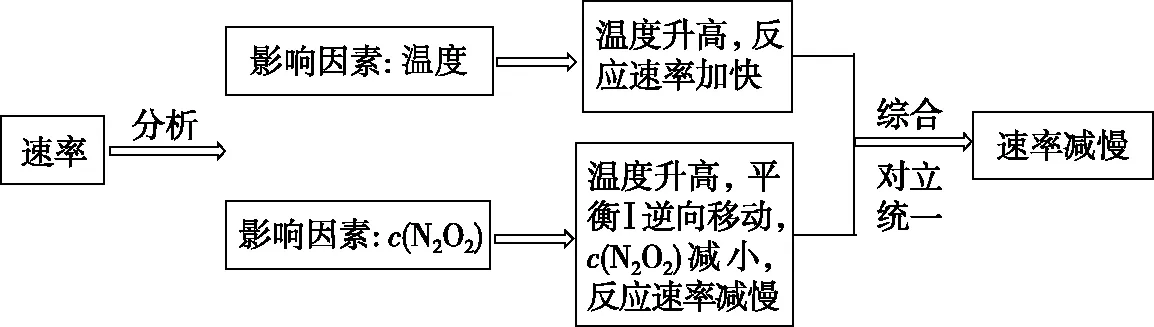








四、启发

