探究常见锂“x”电池的分析方法与解答策略
2021-04-08黑龙江
黑龙江
从近几年全国各地的高考真题和模拟试题来看,电化学中新型电池种类繁多,尤其各种锂电池考查的频率极高,多以选择题的形式呈现,且出现在高考选择题中较靠后的位置,试题难度较大,具有较高的区分度。
这类试题情境素材非常新颖,结合电池装置示意图和电池总反应式等题干信息考查电化学基本知识,笔者总结了近几年的高考试题的规律,锂电池一般从以下几个角度进行选项设置:①结合图示装置判断电池的电极,②分析电子流向或离子移动方向,③结合总反应式或题干信息书写电极反应式,④电化学计算,判断反应一段时间后,某电极的质量变化或溶液pH变化,⑤结合图示装置分析电解质的选择等。
这类电池材料相对比较复杂,在电极反应式或总反应式中经常出现LinOm-x、LixC6和Li1-xMOn(M代表一种或几种金属元素,m、n、x表示数字)等物质,出现陌生物质和物质中的字母数字等导致试题难度增大,使很多同学无从下手。结合教学实际和学生的答题情况,以高考真题为例,笔者重点从电极名称判断和电极反应式书写等角度探讨此类锂“x”电池的分析方法与解答策略。
【例题】(2018·全国卷Ⅲ·11)一种可充电锂-空气电池如图1所示。当电池放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法正确的是
( )

图1
A.放电时,多孔碳材料电极为负极
B.放电时,外电路电子由多孔碳材料电极流向锂电极
C.充电时,电解质溶液中Li+向多孔碳材料区迁移
【答案】D
【解析】结合图示装置可知该锂-空气电池在放电时,O2发生还原反应与Li+生成Li2O2-x,而锂发生氧化反应生成Li+。结合题中信息和图示装置可写出放电和充电时的电极反应式。

电极电极反应式放电负极(锂电极)2Li-2e-2Li+正极(多孔碳材料电极)2Li++1-x2 O2+2e-Li2O2-x充电阴极(锂电极)2Li++2e-2Li阳极(多孔碳材料电极)Li2O2-x-2e-2Li++1-x2 O2总反应2Li+1-x2 O2放电充电Li2O2-x
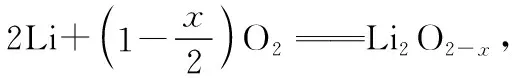

放电时的工作原理为原电池,电池工作时,电子的流动方向为负极→导线→正极,而电流方向与电子流向恰好相反,即电流方向为正极流向负极;为了保持溶液呈电中性,阳离子向正极移动,阴离子向负极移动。而充电时,装置相当于电解池,工作时阴离子向阳极移动,阳离子向阴极移动。
同时,由于锂为活泼金属,能与水和电解质溶液等反应,因此锂金属电池中通常选用非水电解质或某些固态电解质等。这也是命题时常设置选项的一个角度。
通过对以上例题的分析与解答拓展等,这类形形色色的锂“x”电池均属于新型二次电池,解答该类试题大体可以按照以下三个步骤进行综合分析。
第一步:判断电极。
结合图示装置或题中总反应式等信息能正确判断充、放电时的电极材料与电极名称,如例题中放电时负极材料是金属锂或锂合金(如LixC6等),则另一电极为正极;同样根据放电时电子流向或离子移动方向等也可以判断电极名称,如图2所示装置中Li+向左侧移动,即电极a为正极,电极b为负极。
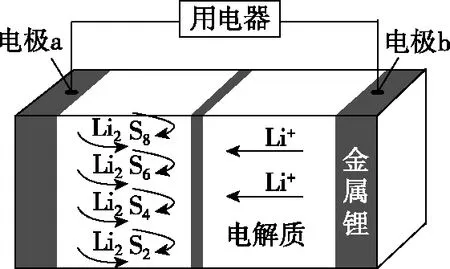
图2
第二步:书写电极反应式。

第三步:分析选项与计算。
在写出电极反应式的基础上,可结合选项进行分析,如判断放电时电子流向(负极→导线或负载→正极)、离子移动方向(阳离子→正极,阴离子→负极)等;根据电路中转移电子数目相等,可结合电极反应式进行简单计算,如根据转移电子的物质的量,可计算正极或阴极增重质量等。
锂“x”电池在2017和2018年全国卷等高考试题中多次考查过,在近2年全国各地的高考模拟试题中也频繁出现,备受命题教师青睐,很有可能在2021年高考中继续呈现,试题可能相对更加新颖,但考查知识点不会有较大改变。本文精选2020年3道模拟试题仍以书写电极反应式为突破口,对其进行综合分析,并对分析方法进行总结,便于在高考或模拟考试中顺利解答。

( )

图3
A.放电时,a极为负极,发生氧化反应
B.LiLaZrTaO固态电解质起到传导Li+的作用

D.充电时,每转移xmol电子,a极增重7 g
【答案】D
【解析】结合图示装置,根据电子移动方向或电池中Li+迁移方向,均可判断放电时a极为负极,b极为正极,相反充电时,a极为阴极,b极为阳极。参考总反应式可写出如下电极反应式。
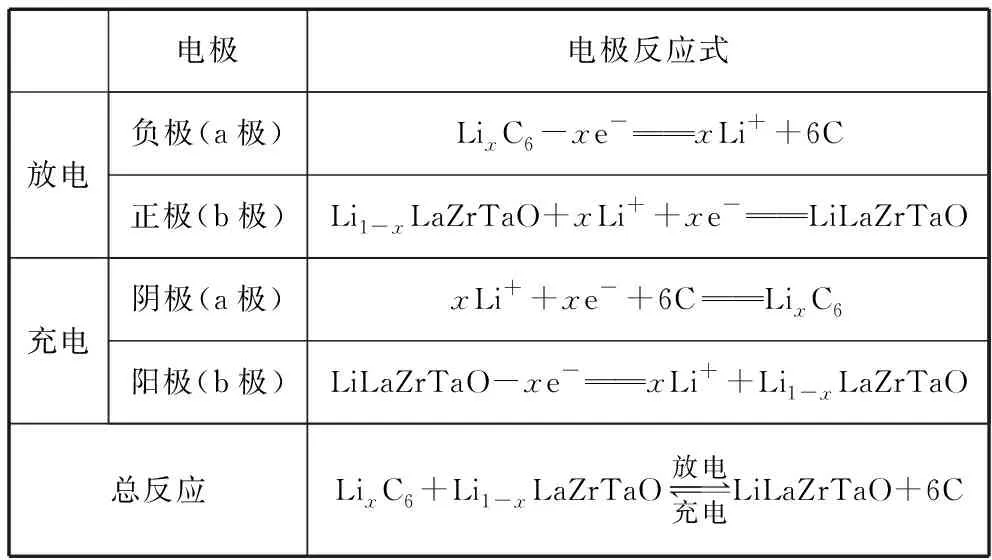
电极电极反应式放电负极(a极)LixC6-xe-xLi++6C正极(b极)Li1-xLaZrTaO+xLi++xe-LiLaZrTaO充电阴极(a极)xLi++xe-+6CLixC6阳极(b极)LiLaZrTaO-xe-xLi++Li1-xLaZrTaO总反应LixC6+Li1-xLaZrTaO放电充电LiLaZrTaO+6C

解答锂“x”电池相关问题时,需根据图示及其信息准确地判断电极名称,并能根据总反应等写出充、放电时的电极反应式,这也是解题的关键。题中LixC6可认为是xmol Li被C6吸附,反应过程中碳元素保持化合价不变,在LixC6、Li1-xLaZrTaO的转化中仅Li元素的化合价变化,其他元素化合价均不发生变化。通过电极反应式和转移电子数目可进行相关计算。

( )
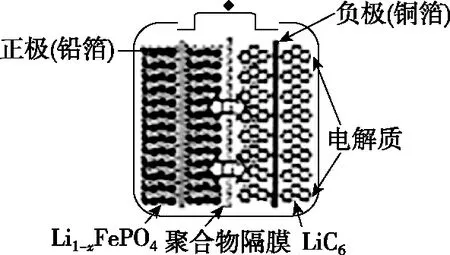
图4
A.“刀片电池”和三元锂电池(镣钻锭酸锂电池)相比几乎没有污染

C.充电时,锂离子在阴极脱嵌;放电时,锂离子在正极脱嵌
D.该电池维持电流强度4.825 A,工作10分钟,理论上正极增加重量0.21 g(已知F=96 500 C/mol)
【答案】C
【解析】放电时为原电池,充电时为电解池;充电时阳极接正极,阴极接负极;结合正极反应和图示可写出“刀片电池”各电极反应式。
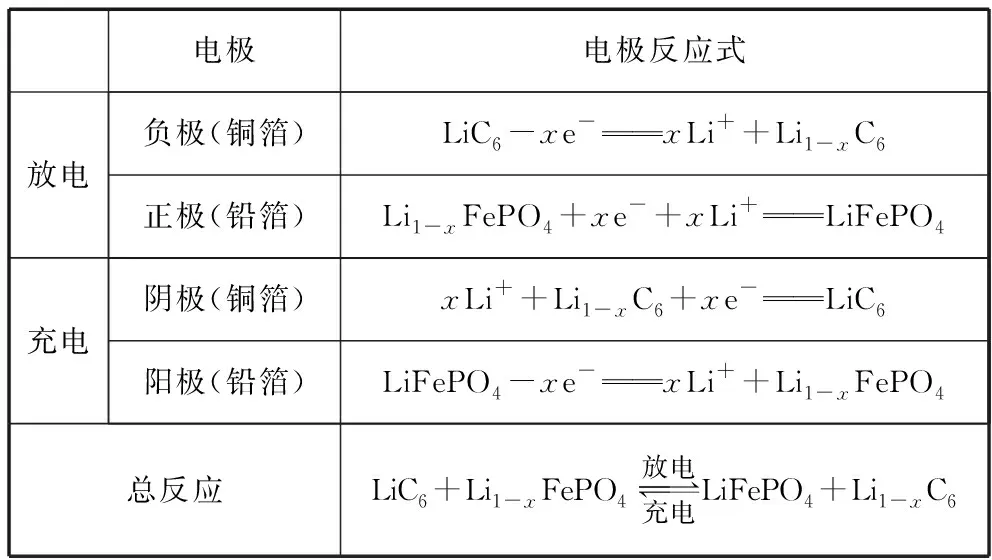
电极电极反应式放电负极(铜箔)LiC6-xe-xLi++Li1-xC6正极(铅箔)Li1-xFePO4+xe-+xLi+LiFePO4充电阴极(铜箔)xLi++Li1-xC6+xe-LiC6阳极(铅箔)LiFePO4-xe-xLi++Li1-xFePO4总反应LiC6+Li1-xFePO4放电充电LiFePO4+Li1-xC6



( )
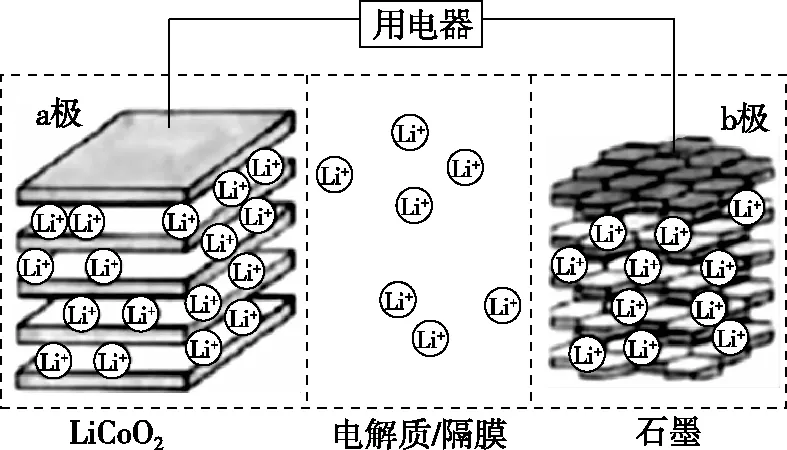
图5
A.充电时a极接外电源的负极
B.放电时Li+在电解质中由a极向b极迁移
C.充电时若转移0.02 mol电子,石墨电极将减重0.14 g
D.该废旧电池进行“放电处理”有利于锂在LiCoO2极回收
【答案】D
【解析】结合图示和电池反应式可知,电池放电时,a极由Li1-xCoO2生成LiCoO2,即a极为正极;b极为负极,发生Li+脱嵌的反应;充电时a极为阳极,b极为阴极。结合电池反应式可写出各电极的反应式。

电极电极反应式放电负极(b极、石墨)LixC6-xe-xLi++C6正极(a极、LiCoO2)Li1-xCoO2+xe-+xLi+LiCoO2充电阴极(b极、石墨)xLi++C6+xe-LixC6阳极(a极、LiCoO2)LiCoO2-xe-Li1-xCoO2+xLi+总反应LixC6+Li1-xCoO2放电充电C6+LiCoO2

二次电池放电时看作原电池,充电时看作电解池;充电过程中,外电源正极接二次电池的正极,简单记做“正接正,负接负”。结合上述各电极反应还可以看出,放电时负极和充电时阴极反应恰好相反,同理,放电时正极和充电时阳极反应恰好相反,无论充放电,电子都应出现在电极反应式的左侧,根据负极、正极反应书写阴极、阳极反应时需进行电子的移项处理。

