油气管线钢土壤环境硫酸盐还原菌腐蚀研究进展
2021-04-07韦博鑫许进高立群覃清钰付琦于长坤孙成王振尧
韦博鑫,许进,高立群,覃清钰,付琦,于长坤,孙成,王振尧
(1.中国科学院金属研究所 辽宁沈阳土壤大气环境材料腐蚀国家野外科学观测研究站,沈阳 110016;2.中国科学技术大学 材料科学与工程学院,沈阳 110016)
随着国民经济的发展和生态文明建设,油气在我国一次能源中的比例持续攀升,埋地管线的建设得到蓬勃发展。我国长输油气管道总里程以每年超过5000 km 的速度逐年增长,预计到2025 年将超过24万km[1]。我国油气输送管道沿线人口密集,生态环境脆弱,一旦发生事故,会造成泄露甚至爆炸,不仅影响能源供给,更会对环境、公共安全造成重大影响,并产生巨大的经济损失。研究表明土壤环境中微生物的存在不仅对土壤生态环境起到重要作用,还会影响埋地管道的腐蚀[2-3]。腐蚀调查结果表明[4-6],2014 年全国总腐蚀成本为21 278.2 亿元人民币,约占当年国内生产总值的3.34%,相当于我国每人承担1555 多元的腐蚀成本,而其中微生物腐蚀造成的损失约占20%。微生物腐蚀(Microbial influenced corrosion,MIC)是指微生物在新陈代谢过程中直接或间接对金属产生作用,进而影响金属腐蚀过程和机理,也是威胁埋地油气管道安全运行的最主要的一种腐蚀形式。油气管道MIC 是“3M”综合作用的结果(图1),即微生物(Microorganisms)、介质(Media)和金属(Metals)。MIC 研究是集土壤学、材料学、腐蚀科学和微生物学等多学科交叉的课题,这也进一步增加了MIC 研究的难度。同时,由于MIC 和非生物腐蚀经常同时发生,这也进一步增大了MIC 机理研究的复杂性。本文从土壤腐蚀微生物的种类和特征、环境因素对微生物腐蚀的影响、微生物腐蚀研究方法以及微生物腐蚀机理4 个方面的最新研究进展进行了综述,并在此基础上提出对微生物腐蚀研究工作的建议。
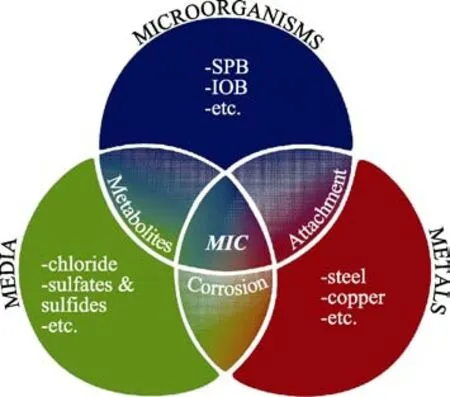
图1 “3M”协同作用下MIC[7]Fig.1 MIC under the coupling effects of microorganisms, media and metals[7]
1 土壤微生物腐蚀
1.1 土壤腐蚀微生物
土壤微生物种类繁多,它们与土壤中的碳、氮、铁、硫等元素循环息息相关,而与腐蚀相关的微生物多是土壤中铁硫循环的参与者[8]。根据微生物对氧气的需求不同可以将腐蚀微生物分为厌氧型和好氧型。目前研究较多的腐蚀微生物主要有以下几类(表1):厌氧型细菌包括硫酸盐还原菌(Sulfate reducing bacteria,SRB)、硝酸盐还原菌(Nitrate reducing bacteria,NRB)、铁还原细菌(Iron reducing bacteria,IRB)和产酸菌(Acid-producing bacteria,APB)等;好氧型细菌包括硫氧化菌(Sulfur oxidizing bacteria,SOB)和铁氧化细菌(Iron oxidizing bacteria,IOB)等。以上并非是微生物分类学上的概念,而是一类具有特征代谢能力细菌的统称。SRB 是可以通过氧化有机化合物,将硫酸盐、亚硫酸盐、硫代硫酸盐甚至单质硫(作为其电子传递链的最终电子受体)还原为H2S 的一类细菌,从而获得其生理活动所需的能量[8]。在众多引起微生物腐蚀的土壤细菌中,SRB 引起的腐蚀最严重,也是研究最广泛的一种细菌[9-11]。据统计,油井腐蚀中75%以上的腐蚀是由SRB 引起的,而地下管线和线缆腐蚀中50%是SRB 腐蚀[12]。SOB 与SRB 作用刚好相反,是将还原态的硫化物(如H2S,硫代硫酸盐等)或单质硫氧化成H2SO4的一类细菌。NRB 是指可以将硝酸盐还原为亚硝酸盐,并通过脱硝作用将亚硝酸盐还原为气态氮化合物或异化转化为NH4+的一类细菌。近年来的研究表明[13-14],土壤中NRB 同样会造成较严重的微生物腐蚀。IRB 是一类利用有机物或H2作为电子供体,Fe3+(或者Mn4+)等作为电子受体,从而获得能量的细菌。IOB 则是在厌氧条件下能有效利用Fe2+进行能量代谢的一类细菌。而与上述细菌作用机理不同的是APB。APB 对金属的腐蚀主要是使金属局部发生酸性溶解,这是因为其代谢产物包括多种有机酸和无机酸,可以造成局部酸化,从而使金属发生严重的点蚀。目前,上述类型的细菌仅为一小部分与金属腐蚀相关的已知细菌,而土壤环境中仍有大量其他种类的细菌未被发现和分离。因此,管线钢MIC 的研究仍存在具大挑战。

表1 与金属腐蚀相关的微生物Tab.1 Bacteria related to MIC of metal
1.2 埋地管线钢微生物腐蚀
人们对于微生物腐蚀已有百年以上的研究历史。早在19 世纪90 年代初,Garrett[21]就报道了有关微生物腐蚀的研究。1934 年,Von Wolzogen Kuhr 等[22]首次报道了微生物腐蚀导致的服役管线失效案例。他们认为SRB 是硫酸盐富集土壤环境中管道腐蚀的主要原因,并且提出了“阴极去极化”理论以解释MIC机理。大量现场分析和实验室研究结果表明,SRB 是诱发和加速管线钢腐蚀的典型细菌,也是对埋地管线钢腐蚀影响最大、被研究最多的一种腐蚀性细菌[23]。Sarioǧlu 等[24]的研究结果表明,在SRB 作用下,管线钢的腐蚀速率增大了6 倍左右。近年来,我国也报道了大量由SRB 导致管线腐蚀失效的案例。2013 年,新疆地区一条X52 输油管道发生爆管泄露,事故的最终调查认为微量游离水或积水聚积在管道起伏低洼处,为SRB 大量繁殖提供了有利环境,最终导致管线发生MIC 腐蚀而失效[25]。随后,牛涛等[26]报道了1 条X60 级埋地输气管线钢管在使用13 个月后发生了腐蚀穿孔。取样分析表明,腐蚀孔附近的腐蚀产物表面含有大量S。最终认定SRB 腐蚀是引起管线腐蚀穿孔事故的主要原因。金属尤其是钢铁材料的MIC已经成为腐蚀领域中的一个研究热点。根据“3M 理论”,MIC 发生需要介质(土壤环境)、材料(埋地金属)和微生物3 个基本条件。因此,针对这3 种基本因素,研究人员对埋地管线钢SRB 腐蚀开展了大量研究。
1.2.1 土壤类型
我国土壤类型众多,不同土壤对微生物的生理活性和腐蚀影响各不相同。吴堂清等[27-28]研究了酸性土壤环境中SRB 对管线钢腐蚀行为的影响。他们发现接菌初期(24 h),由于土壤的强酸性导致SRB 细菌数量下降1 个数量级,随着SRB 对新环境的逐渐适应,SRB 开始繁殖,并呈现指数级增长。他们还指出,实验前期SRB 活性生物膜对管线钢腐蚀起抑制作用,而后期SRB 则加速了钢的腐蚀。孙福洋等[29]对西北典型盐渍性土壤中X100 管线钢SRB 腐蚀行为进行了研究。他们发现SRB 新陈代谢改变了基体表面的微环境,使得表面腐蚀产物产生明显裂纹,从而加剧了管线钢的腐蚀。Liu 等[30]在实验室模拟加拿大粘土覆盖下SRB 对X52 管线钢的腐蚀影响。结果表明,SRB显著加速了裸钢的腐蚀,平均腐蚀速率可达0.68 mm/a。随着土层厚度的增加,钢表面固着SRB 细胞的数量逐渐减少,腐蚀速率也随之降低。他们最终认为土壤层阻碍了SRB 与钢基体的接触。虽然一些学者对具体类型土壤中管线钢的MIC 进行了一些研究,但是由于土壤本身组成的复杂性,相应的腐蚀规律也很难进行归纳。
1.2.2 交流电流
随着交流电腐蚀问题日益突出,交流电引起的管线钢的腐蚀逐渐受到各国研究人员的关注。当土壤中存在交流电时,会对土壤中管线钢的腐蚀造成直接影响[31]。与此同时,管线实际服役环境中,交流电腐蚀和微生物腐蚀有可能同时发生。交流电还会对SRB的新陈代谢及金属表面微生物膜的吸附状态产生影响,进而影响金属的腐蚀。Seok Hong 等[32]认为,交流电对微生物膜的影响分为两方面,当交流电处于负半周期时,由于电排斥力会促进微生物膜中细菌(通常细菌带负电)的脱附,而正半周期通过电吸引力加强金属表面微生物膜中细菌的粘附,但过大的阳极电流具有杀菌作用。卿永长等[33-34]研究了交流电和SRB对Q235 钢的腐蚀影响。结果表明,交变电场降低了微生物膜的吸附性,促进了微生物膜的脱附。实验前期,活性生物膜对钢腐蚀起抑制作用,而实验后期,由于微生物膜活性降低,导致部分膜层脱落,最终促进了钢腐蚀。他们认为交流电整流效应、交变电场作用以及点蚀自催化效应等共同加速了金属腐蚀。钟方丽等[35]则从微生物角度出发,研究了交流电对生物膜胞外聚合物(EPS)提取过程的影响。他们发现,小于10 A/m2的电流对生物膜内微生物细胞的影响较小,多糖和蛋白质的提取量较少;而大于10 A/m2的电流对微生物细胞活性的影响较大,可提取的蛋白质和多糖量明显增多,特别是蛋白质的量。虽然对于交流电作用下金属微生物腐蚀进行了一些研究,但多集中于对金属腐蚀影响的研究,而对于交流电对金属表面生物膜形成和发展,以及与金属基体间相互作用机理等研究相对较少,这些方面还需要更加深入的研究。
1.2.3 阴极保护
阴极保护(CP)是埋地管线防护最有效的方法之一。通过施加阴极电流引起埋地管线钢发生极化,使得受保护管线管地电位整体发生负移并进入免蚀区,从而阻止和减缓埋地管线钢腐蚀[36]。在微生物存在下,生物膜的形成会使得极化电阻增大,达到相同的电位所需的极化电流也增大。因此,阴极保护对金属MIC 行为的影响一直是研究的重点[36]。Li 等[15]的实验结果表明,即使在管线处于CP 下,SRB 也会加速腐蚀。孙成等[37]的研究发现,钢在接种SRB 的土壤中的腐蚀速率远高于无菌土壤中的腐蚀速率。在相同的阴极电位下,接菌土壤中钢的阴极电流密度大于无菌土壤中的阴极电流。李国华等[38]研究了阴极极化对埋地Q235 钢SRB 腐蚀行为的影响。在相同的外加电位下,Q235 钢在接菌土壤中所需要的阴极极化电流密度更大。随着阴极极化电位不断负移,Q235 钢周围土壤中的SRB 数量逐渐减少,但即使阴极电位为–1.05 V(vs. CSE)时,Q235 钢试件周围土壤中SRB 仍能够存活。在相同的阴极极化电位下SRB 增大了Q235 钢的腐蚀。SRB 和微生物膜的电负性,以及导电性代谢产物硫化物(如FeS)的存在都对钢阴极保护过程产生影响,从而改变了钢的腐蚀机理和阴极保护效率,然而对于此方面机理研究相对较少。可见,微生物作用下埋地管线阴极保护的可靠性,以及微生物和阴极极化相互作用关系等研究仍然值得关注。
1.2.4 应力

图2 SRB 在裂纹尖端腐蚀电化学过程示意图[41]Fig.2 Electrochemical modes of the corrosion process of a cracking tip in the presence of SRB[41]
近年来国内外相继报道了多起管线腐蚀开裂事故,现场失效分析证实了微生物直接或间接参与了SCC 裂纹萌生和扩展过程。因此,微生物作为SCC研究的主要影响因素引起各国学者的关注。Abedi 等[9]对伊朗一条X52 管线进行失效分析时发现,SRB 是管线腐蚀开裂的主要原因。他们还发现SRB 作用下的宏观裂纹尖端呈圆形,与大家知道的纯粹SCC 诱发的尖锐条状裂纹明显不同。根据Slobodian 等[39]和Serednyts'kyi 等[40]的研究,图2 给出了SRB 在裂纹尖端腐蚀电化学过程各阶段示意图[41]。第一阶段,氧的阴极去极化反应和尖端铁的阳极溶解反应;第二阶段,水在金属活性表面的催化分解,氢离子的释放和氢的去极化,以及铁的阳极溶解;第三阶段,腐蚀产物的沉淀、FeS-Fe 微电偶形成,以及点蚀形成。吴堂清等[42-49]系统地研究了外加应力作用下管线钢的MIC 腐蚀行为,并提出了“微生物致裂(MAC)”的概念。他们基于Gutman 的力学-化学交互作用理论、微生物能量学和腐蚀电化学理论,给出了土壤环境中2 种典型细菌SRB 和NRB 致裂的热力学和动力学解释。从热力学和动力学上来看,外加应力和微生物共同作用导致Fe 基金属具有更高的腐蚀趋势和裂纹扩展速率。他们还发现SRB 及其代谢产物硫化物加速了管线钢表面点蚀的萌生,SRB 和外应力共同作用诱发了蚀坑底部的“二次点蚀”和裂纹壁上的“二次开裂”,进而对管线钢SCC 产生协同加速作用。赵健等[50]研究了应变速率对SRB 作用下X70 应力腐蚀开裂行为的影响。研究结果表明,当应变速率为5×10–7s–1时,接菌土壤溶液中试样的应力腐蚀敏感性远大于无菌条件下试样的应力腐蚀敏感性,SRB 的存在对管线钢SCC 起到很大程度的促进作用。当应变速率为1×10–6s–1时,SRB 对于管线钢SCC 的影响较小,而力学因素起主导作用。
1.2.5 剥离涂层
目前,大量关于管线钢微生物腐蚀的研究都集中于裸钢的研究。实际上,在服役过程中埋地管线通常采用防腐涂层与阴极保护联合防护的方式。但是涂层在施工和服役过程中,不可避免地发生多种形式的破坏和失效,如剥离、针孔或大的缺陷、起始于针孔的剥离等。一旦这些缺陷涂层发生剥离,腐蚀性介质就会渗透进入涂层内部,同时剥离涂层会对阴极保护电流产生屏蔽效应,最终使得剥离涂层下的管线钢发生腐蚀[2]。因此,研究管线钢在剥离涂层下的微生物腐蚀行为并揭示其腐蚀机理,对于埋地管线的腐蚀与防护更具有实际意义。Xu 等[51-54]研究表明,SRB 的存在增大了阴极保护电流密度,同时加速了剥离涂层下管线钢的腐蚀。Wu 等[55]也通过电化学测试证明了剥离涂层下缝隙内的SRB 对X80 钢的腐蚀加速作用。Liu 等[56]通过土壤薄液膜模拟实验研究了剥离涂层下管线钢的腐蚀。结果表明,SRB 加速了薄液膜下X52管线钢的腐蚀。同时,还发现CO2气体可以促进SRB的生长和生物膜的形成,SRB 和CO2对钢的腐蚀具有协同加速作用。目前,剥离涂层下管线钢微生物腐蚀的研究相对较少,多集中于单因素影响(如应力等),而多因素耦合作用下剥离涂层下的管线钢微生物腐蚀行为和机理研究将成为今后研究的重点。
1.2.6 其他微生物
近年研究表明,硝酸盐还原菌(NRB)也会加速埋地钢的腐蚀[57-58]。Etique 等[59]实验结果发现,NRB可以通过耦合硝酸盐的还原将Fe2+氧化成Fe3+。他们还从热力学角度探讨了硝酸盐还原导致金属氧化的可行性。Wan 等[57]采用电化学方法研究了X80 钢的NRB 腐蚀行为。结果表明,NRB 加速了X80 钢的腐蚀,腐蚀形貌以点蚀为主。Li 等[60]的研究结果也表明NRB 加速了X80 钢表面点蚀的形成。他们认为点蚀的形成可能是由于NRB 加速了铁的阳极溶解。同时NRB 可以将生物膜或损坏的腐蚀产物膜中的硝酸盐还原并获得电子,最终加速钢的腐蚀。Xu 等[58]对比研究了碳钢NRB 和SRB 腐蚀。结果表明,在严格的厌氧条件下,NRB 比SRB 更具有腐蚀性。接菌NRB体系中的钢试样在第 7 天时的腐蚀速率达到 0.89 mg/cm2,最大蚀坑深度为14.5 μm。
目前大量的研究多集中于单一菌种的影响,而实际土壤环境中微生物种类繁多,对于埋地管线钢腐蚀产生影响的也并非单一菌群。埋地管线钢表面微生物膜内寄居多种微生物,各种微生物之间可能会发生共生、竞争、拮抗等不同的作用,从而对钢腐蚀产生影响[61]。因此,土壤环境中混合菌对MIC 耦合作用的研究也将成为MIC 行为和机理研究的挑战和机遇。
2 微生物腐蚀研究方法
2.1 电化学测试技术
微生物吸附在电极表面会形成生物膜,对金属电极表面的电化学行为产生影响。因此,线性极化测试(LPR)、交流阻抗谱法(EIS)和电化学噪声(EN)等电化学测试技术,常用于实验室和现场评价微生物腐蚀[51]。

线性极化测量只需施加小的极化电位,通常|ΔE|小于10 mV。该方法对腐蚀体系中金属试样的影响较小,且可以快速得到相应的腐蚀参数。该方法常用于管线实时腐蚀信息监测和服役寿命评估。在大多数情况下,对于给定腐蚀体系,βa和βc的值在60~120 mV之间。因此,在一些研究中,通常选取βa和βc的值都等于120 mV,即B=26 mV。但采用LPR 评价管线腐蚀速率时,应该注意,对于微生物存在条件下的B值并非一个固定值。Sun 等[62]采用LPR 和失重法研究了X80 管线钢在铜绿假单胞菌、醋酸杆菌和普通脱硫弧菌存在下的B 值。结果表明,在3 种不同细菌存在的条件下,B 值分别为(35.60±0.55)、(33.00±1.00)、(58.60±0.55) mV。因此,采用线性极化对管线钢微生物腐蚀进行测量和评价时,通常采用的B 值(26 mV)并不适用,需要根据具体的试验条件,重新测量和计算极化曲线的βa和βc值,以获得更准确的B 值。
电化学阻抗谱(EIS)是施加一个频率不同的小振幅的正弦交流电,测量阻抗值随正弦波频率ω 的变化,或者是阻抗的相位角Φ 随ω 的变化,进而获得电极界面相关电化学过程的信息,如电极过程动力学、双电层和扩散等。EIS 是获取电极过程动力学信息和电极界面结构信息,从而判断金属腐蚀变化的一种常用方法[63]。虽然可以通过观察阻抗值的变化趋势,获得双电层电容、扩散等相关腐蚀动力学信息,但是该种方法需要具备一些专业知识的人员对EIS数据进行拟合处理。因此,该方法更适用于实验室微生物腐蚀机理研究。
电化学噪声(EN)是指电化学动力系统演化过程中系统状态参量(如电极电位和外测电流密度)随机非平衡波动现象[64]。EN 技术能够原位、连续、无损地监测局部腐蚀萌生与发展,将其应用于腐蚀监测领域的关键是通过合适的信号处理方法提取有效的特征参数,然后关联其与特定腐蚀机制或腐蚀发展过程[65]。Zhao 等[66]认为线性极化电阻和电化学阻抗谱抑制样品表面生物膜的附着和生长,并影响内部电场,而电化学噪声作为一种被动的电化学测量技术对生物膜没有负面影响。同时EN 测试所得的腐蚀速率与失重数据最为接近。与LPR 和EIS 相比,EN 更适合用于MIC 研究,但由于数据处理需要丰富的相关经验和复杂的处理过程,从而限制了其应用。
2.2 先进表面分析技术
土壤微生物腐蚀研究涉及土壤学、材料学、腐蚀科学和微生物学等多种学科,是一个多学科交叉的研究课题,而化学和电化学分析技术、微生物分析技术以及材料表征技术等的联用也将为土壤微生物腐蚀行为和机制的研究提供更多的研究方法,这也有助于更好地理解微生物/材料之间的相互作用机制。
2.2.1 荧光标记显微技术
近些年来,生物技术与光学显微技术也广泛应用于MIC 研究。采用不同荧光染料可标记细胞活死状态或生物膜中的不同成分(如核酸、蛋白质、多糖等),并利用激光共聚焦显微镜(Confocal laser scanning microscope,CLSM)可以显像微生物和微生物膜的三维结构,从而使得微生物膜立体化和易视化[67]。图3 和图4 为接菌土壤中X80 钢表面活死细胞平面和断层空间荧光成像图,其中绿色代表活细胞,红色为死细胞。从图3 和图4 中可以看出,试样表面可以观察到大量固着的活细胞和死细胞,且固着的活细胞数量远远多于死细胞数量。利用CLSM 测试软件还可以测量样品表面微生物膜的厚度。

图3 接菌土壤中X80 钢试样表面SRB 活死细胞的CLSM 图Fig.3 2D-CLSM images of SRB biofilms on X80 coupon surfaces in SRB containing soil: a) live cells of SRB, b) dead cells of SRB
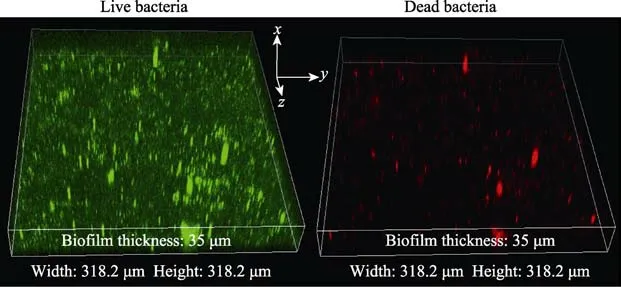
图4 接菌土壤中X80 钢试样表面SRB 生物膜的三维CLSM 图像Fig.4 3D-CLSM images of SRB biofilms on X80 coupon surfaces in SRB containing soil
虽然荧光显微技术可以对样品表面微生物膜的形成过程进行可视化研究,但是在MIC 研究过程中,该技术仍存在着挑战。例如,当金属材料表面形成多种细菌混合生物膜时,该技术无法分辨单一细菌微生物膜的形成过程以及单一细菌在微生物膜成膜过程中的贡献。此外,由于腐蚀产物膜与生物膜都同时存在于腐蚀金属表面,腐蚀产物膜具有很差的透光性,这也对样品表面微生物膜的荧光观察造成困难[63]。
2.2.2 聚焦离子束(FIB)技术
众所周知,MIC 与微生物膜的结构和性质关系密切。微生物首先附着在金属表面,并分泌代谢产物从而形成微生物膜,最终诱发MIC。因此,微生物膜的结构、组成及成膜过程都会对金属腐蚀反应热力学与动力学产生影响。同时,细菌在生物膜中的分布和界面处的物质信息也是了解MIC 过程的关键。长期以来,由于微生物活动的复杂性以及缺乏微生物膜与金属界面之间交互作用的深刻认识,因此限制了微生物腐蚀机理的认知和理解[68]。随着纳米技术的发展,纳米尺度制造业发展迅速,通过FIB 技术对样品进行纳米尺度加工已实现暴露后亚表面特征的无损成像,为深入研究MIC 机制提供了更精确的微观分析方法,并有助于更好地理解细菌/金属界面的相互作用。在传统的截面样品制备中,通常采用金相砂纸打磨截面,该方法很容易对细菌细胞造成破坏。而FIB 可以在保持样品完整形态的同时,利用高强度聚焦离子束对材料进行纳米加工,配合扫描/透射电镜(SEM/TEM)等高倍数电子显微镜观察微生物膜的结构和分布情况,这也为科研人员从纳米尺度理解MIC 机理提供了有效的工具。李迎超等[69]利用FIB-SEM 研究了细菌细胞和腐蚀产物层的形态,以及生物膜和腐蚀产物中细菌的分布和材料特性(图5)。他们发现腐蚀产物和生物膜下的样品表面覆盖着完整的FeS 层。他们还分析了细菌在生物膜中的分布和MIC 点蚀的纵向元素分布,并提出了细菌分布、生物膜和产物离子选择性的点蚀机理,同时认为SRB 生理活动产生的 H+在生物膜下的累积是导致点蚀发生的主要原因。FIB 技术为深入理解微生物引起的点蚀机理研究提供了强有力的证据。Li 等[70]也结合FIB 铣削技术和SEM/TEM 对地衣芽孢杆菌细胞/X80 钢的界面情况进行了分析,并且通过FIB-TEM 表征揭示了细胞的超微结构。FIB 结合其他微观分析技术必将成为今后MIC 研究中不可或缺的一种表征技术。

图5 聚焦离子束结合扫描电镜研究MIC 结果[69]Fig.5 MIC results of carbon steel studied using FIB-SEM[69]: a) element mapping at the interface between iron sample and biofilm, b) linear element mapping of a single SRB cell
3 硫酸盐还原菌腐蚀机理研究
腐蚀是金属与周围环境发生化学或电化学反应,遭受破坏而引起性能劣化的现象。微生物可通过多种方式影响金属的腐蚀过程[71]:(1)影响腐蚀过程的阴/阳极反应,如分泌能够促进阴极还原的酶;(2)微生物生理活动过程产生促进(或抑制)金属腐蚀的化合物;(3)改变金属表面状态,微生物吸附在金属表面并形成微生物膜改变了金属表面腐蚀微环境;(4)改变腐蚀反应类型,如微生物引起局部腐蚀。
在土壤环境中,SRB 是引起微生物腐蚀最主要也是最严重的一种厌氧菌[72]。研究人员对SRB 腐蚀机制进行了大量的研究,并提出多种腐蚀机理。但是,由于SRB 与金属之间的相互作用复杂,涉及多种生物和物理化学过程。所以,单一的机制并不能完全解释SRB 引起的MIC,有时需要多种机理共同进行解释说明。下面主要对一些得出普遍承认的SRB 腐蚀机理进行阐述。
3.1 阴极去极化理论
1934 年Von Wolzogen Kuhr 和Van der Vlugt[73]首次提出“阴极去极化理论”(CDT),对SRB 腐蚀机理进行了解释。CDT 理论认为SRB 通过消耗“氢化酶”来消耗阴极氢,同时把SO42–还原成HS–,通过这种阴极去极化作用使得金属持续发生阳极溶解,从而加速金属腐蚀。在腐蚀过程中,阳极溶解转变成Fe2+进入溶液,Fe2+分别与S2–和OH–反应生成腐蚀产物FeS 和Fe(OH)2并堆积在金属表面,致使其内外形成浓差电池。以上过程的反应式为:

图6 总结了基于CDT 理论的SRB 腐蚀过程。细菌通过氢化酶从铁表面的阴极区域除去氢,同时还原SO42–。这个过程产生的腐蚀产物是FeS 和Fe(OH)2。SRB 通过还原SO42–,催化吸附的氢原子H(ads)复合成氢气(H2),提高阴极反应速率。因此,SRB作用下阴极反应的去极化会间接加速腐蚀反应的进行。CDT 理论从电化学角度解释了SRB 引起的MIC腐蚀过程,但仍然存在难以解决的问题。例如,基于CDT 理论,4 mol Fe2+发生反应生成1 mol FeS,理论比值应为4。然而,Javaherdashti 等[74]的研究指出这个比率在0.9~1 之间变化,远远偏离理论值。由于MIC 过程的复杂性,金属界面的物理和化学参数随微生物的代谢发生不断变化。因此,很难用单一的电化学理论来解释MIC 机制。

图6 SRB 阴极去极化理论示意图Fig.6 Schematic of the cathodic depolarization theory of SRB
3.2 代谢产物腐蚀理论
H2S 和FeS 是SRB 的典型代谢产物,也是导致金属腐蚀加速的原因之一[75]。Romero 等[76]报道生物膜具有扩散阻挡作用,减缓了H2S 的溢出,SRB 生物膜中的细菌可以达到108cfu/cm2,可以产生大量的腐蚀性H2S,从而造成严重的局部腐蚀。Jia 等[77]通过厌氧瓶顶空容积试验,验证了H2S 变化对固着细胞数、培养基pH 值、腐蚀失重和点蚀的影响。研究发现,较大的顶部空间会导致更多的H2S 逸出,增大了游离和固着的细胞数量,从而导致更严重的MIC。

图7 SRB 生物膜结构示意图[78]Fig.7 Schematic of SRB-biofilm[78]
FeS 是SRB 腐蚀的典型产物。研究表明[78],如图7 所示,SRB 生物膜由SRB 细胞、胞外聚合物、铁硫化物等组成,且存在大量的孔隙和微小的裂缝,这些缺陷的存在会降低微生物膜的稳定性,从而导致膜发生破裂。同时,由于FeS 的嵌入,微生物膜的导电性升高,在电解质与铁基体之间形成连续的电子传递路径,而代谢产物硫化物(阴极)和裸露的钢基体(阳极)之间形成了一个电偶对,进而加速了钢基体的腐蚀。
3.3 胞外电子传递理论
一些研究表明[79-82],微生物能直接从金属表面获取电子,从而加速金属的腐蚀。Sherar 等[83]发现,当培养基中缺乏有机碳源时,“饥饿”的SRB 会利用菌毛将它们与钢表面连接,并通过菌毛从铁基体中直接获取电子。Venzlaff 等[79]通过电化学技术证实了SRB 的直接电子传递过程。Xu 和Gu[80]研究也进一步证实,当培养基中缺少碳源时,SRB 可以将铁作为电子供体,并利用菌毛从碳钢表面转移电子进行硫酸盐还原并获取自身所需的能量,从而氧化铁基体。在SRB 引起的MIC 中,有机碳源(如乳酸)需要扩散到SRB 细胞的细胞质中并被氧化,给SO42–还原过程提供电子。当缺乏碳源时,电子供体Fe 的氧化反应发生在细胞外,而SO42–还原则发生在细胞内。这也意味着Fe 首先在细胞外发生氧化并释放的电子,随后电子穿过细胞壁进入细胞质以完成硫酸盐的还原过程。一般认为,腐蚀过程中的微生物通过两种方式(图8)获取电子:(1)利用细胞膜结合的氧化还原蛋白(如c 型细胞色素、导电纳米线(pili))进行的直接电子转移[81-82];(2)利用电子载体(如氢)或电子转移介质(如核黄素和黄素腺嘌呤二核苷酸(FAD))的电子转移[84-85]。

图8 微生物腐蚀金属的电子传递方式[3]Fig.8 Electronic transfer pathway of MIC[3]
3.4 生物阴极还原理论
根据CDT 理论,SRB 加速MIC 过程必须需要氢化酶。而有很多的SRB 并不能产生氢化酶,也同样加速了金属的腐蚀[58]。因此,传统的CDT 理论并不能用于解释所有的SRB 引起的MIC。随着表面分析测试技术的发展,人们对MIC 的相界面反应过程有了更加深入的了解,并逐渐意识到生物膜在MIC 过程中扮演着重要的作用。顾停月和徐大可[80,86]提出了生物催化硫酸盐还原机理(BCSR)理论,首次从生物能量学角度对MIC 进行解释。BCSR 理论认为,当周围环境中有充足的碳源(如乳酸)时,SRB 优先利用有机物质乳酸作为电子供体,阳极发生乳酸氧化反应(反应(10))。当介质中缺少碳源时,SRB 不能通过氧化碳源来获取自身所需的能量,使其处于生长停滞阶段。但是,此时SRB 的能量代谢过程仍然在继续,SRB 可以将Fe 作为电子供体并从中“捕食”电子,同时将SO42–还原(反应(11)和反应(12)),以获取自身新陈代谢所需的能量。主要发生的腐蚀反应如下。
阳极反应:

从反应热力学角度来看,在25 °C、pH=7、溶质浓度为1 mol/L、气体分压为0.1 MPa 的条件下,反应(10)的电极电位为E0′ = −0.430 V(vs. SHE),反应(11)的电极电位为E0′ = −0.447 V(vs. SHE),反应(12)的电极电位为E0′ = −0.217 V(vs. SHE)。可以看出,Fe2+/Fe 的电极电位值(−0.447 V)比CO2+CH3COO−/CH3CHOHCOO−的值(−0.430 V)更负。因此,Fe 氧化释放的能量略高于乳酸。BCSR 理论从微生物自身的能量交换着手,分析金属的腐蚀过程,从生物电化学和生物能量学角度来解释微生物为什么以及如何造成金属腐蚀,为探索MIC 防治的新方法、杀菌剂的研发以及新型抗菌材料的研发提供了理论指导。
4 管线钢微生物腐蚀防护与监检测技术
MIC 是材料、环境和微生物共同作用的结果,因此抑制MIC 就应该从这3 个方面来着手。目前,对于金属MIC 防治提出了多种方法[87]:(1)物理方法,即采用紫外线、磁场等物理措施进行杀菌处理,如在管道输送系统中安装紫外线杀菌装置等;(2)化学方法,即使用杀菌剂等化学试剂直接杀死环境介质中的微生物,如戊二醛和四羟甲基硫酸磷等杀菌剂对MIC 均有抑制作用;(3)防护性涂层,即采用喷涂等方法在金属表面形成一层特殊的防护层,从而降低微生物在金属表面吸附;(4)电化学方法,即利用电化学原理对金属进行防护,如对管线施加阴极电流以抑制金属微生物腐蚀,通常在SRB 存在的环境中,阴极保护电位需要达到−0.95 V(vs. CSE)或更负才能达到抑制作用;(5)生物防治法,即通过微生物之间的竞争和拮抗等关系来防止微生物腐蚀,如NRB对SRB 的抑制作用。实际服役环境中,埋地管线土壤环境MIC 防护面临较大的挑战。由于土壤服役环境的限制,物理法和化学法难以用于环境杀菌。杀菌剂的使用会改变土壤微环境,既增加环境的负荷,又会引发破坏生态环境的风险。此外,对于微生物来说,长期使用杀菌剂易诱导微生物变异,产生耐药菌。因此,抗菌涂层开发和耐微生物腐蚀管线钢研发为MIC防治提供了一个新的研究路径。
合金的抗SRB 腐蚀性能与合金中抗菌元素密切相关,而重金属元素和大部分稀土元素(如铜、铈、钨、镧、钼、镍等)都具有抗菌作用[88-89]。因此,在合金成分中添加适量的抗菌元素,一旦细菌与材料接触或者材料受到侵蚀,其抗菌元素就会释放重金属离子穿透细胞膜,干扰细胞代谢过程或各种酶的活力,从而抑制微生物的生长繁殖。同时,上述抗菌元素也具有良好的耐腐蚀性能。史显波等[90-92]设计了一种含铜管线钢。由于钢表面富Cu 相的析出赋予此类钢优异的抗菌功能,使其具备一定的耐微生物腐蚀性能。他们发现在接菌土壤溶液中浸泡20 d 后,含铜抗菌X80 管线钢表面点蚀数量和最大点蚀深度均远小于X80 管线钢。同时,抗菌涂层也是一种重要的控制和抑制金属微生物腐蚀的主要手段。Xu 等[93]研发了一种新型抗菌MoO3-SiO2纳米复合镀层。该涂层在厌氧条件下,通过在表面形成Mo(V)-S 配合物,可以有效地抑制SRB 的生长。Zhang 等[94]采用热喷涂方法制备出了一种低孔隙率(0.76%)的新型铁基非晶涂层。该涂层具有优良的抗腐蚀、抗菌性能。他们发现喷涂涂层试样表面生物膜厚度和表面活细胞数量急剧降低(图9)。虽然新型抗菌管线钢和抗菌涂层都表现出优异的抗微生物腐蚀性能,但是其发展和应用还存在巨大的挑战。一方面,从科学研究的角度来看,抗菌元素在微生物腐蚀过程中的作用机理,以及对细菌生物膜形成和发展过程的影响机理等尚无明确结论;另一方面,抗菌元素的含量通常受其在合金基体中固溶性的限制,过量添加会削弱合金的机械性能,而材料性能的均衡性也是该方法面临的主要问题。我国管线钢正朝着高压、高强和大口径方向发展,这也对管线钢材料的力学性能、焊接性能和耐蚀性能提出了更高的要求。因此,如何在不影响其他性能的前提下,通过增加抗菌、耐蚀元素的含量来提高这些合金的抗菌和耐蚀性能是关键问题。添加一种或几种抗菌元素并同时获得综合性能优异的管线钢材料,开发复合型耐微生物腐蚀管线钢将是未来耐微生物腐蚀管线钢研发的重要方向。
由于管线服役环境的特殊性和复杂性,微生物腐蚀的防治要综合应用多种手段才能达到较好的控制效果。目前对MIC 防护的研究主要集中在机理与抗菌材料开发,土壤微生物监检测技术的研究是整个腐蚀研究领域中最薄弱的环节之一,仍具有巨大的挑战。一方面,土壤腐蚀监测的智能化较低,急需研发长效的土壤环境MIC 原位监测设备,如何通过“移动端+大数据+云计算”的体系框架,实现管道MIC监测的数字化、网格化与智能化是今后研究需重点解决的难题;另一方面,土壤环境生物多样性的变化规律与土壤MIC 的关系未被考虑。20 世纪50 年代末,国家科学技术委员会组织并建立了“全国大气、海水、土壤腐蚀试验站网”,开始了我国土壤环境腐蚀试验研究工作。经过系统建设,我国的土壤腐蚀野外站在长期连续基础数据获取、自然现象和规律认知、推动领域方向发展等方面发挥了重要作用。但是,目前的主要问题是缺少生物多样性动态变化的实时监测方法和技术、研究方法不统一、数据整合困难等。国家腐蚀野外观测站应布设生物多样性监测网络观测点,利用生物信息学技术,围绕土壤微生物群落和功能基因组的组成与多样性,开展长期定点的动态监测。通过土壤微生物多样性监测,将有助于阐明土壤微生物组成、多样性、功能基因的时空变化特征和驱动机制,建立土壤微生物多样性变化与管线材料腐蚀速率的关系及相关的模型,预测环境条件变化下土壤微生物的演变规律,为土壤微生物腐蚀监检测技术开发与相关机理研究提供科学依据。土壤环境MIC 是一个复杂的生物/化学过程,随着表面分析技术和生物信息学方法的快速应用及发展,将会进一步促进微生物监检测技术向更深和更广的方向发展[95]。

图9 SRB 菌液中浸泡21 d 后试样表面的CLSM 活/死细胞图像[94]Fig.9 CLSM live/dead cell images of coupon surface after 21 days immersion in SRB-inoculated media[94]:a) Fe-based amorphous coating, b) 304SS stainless steel, c) X80 steel
5 展望
随着我国基础设施建设和能源消费的日益增长,埋地管线钢的MIC 逐渐受到人们的重视。尽管对MIC现象进行了大量的研究,但对于各影响因素(生物的还是非生物的)与MIC 过程的相关性,以及主导MIC过程的腐蚀机理等仍然存在争议。随着材料科学、微生物学、电化学和表面分析技术的进步和发展,更先进和精确的研究手段为科研人员更好地理解MIC 的动态过程,以及这些过程如何影响腐蚀电化学反应的机理提供了可能性。由于土壤环境的复杂性,土壤微生物腐蚀研究仍存在巨大的挑战,涉及以下几个主要问题:
1)埋地管线钢腐蚀受到土壤类型、含水量、应力、杂散电流和材料性能等多因素的影响。目前大量的研究仍主要集中于单因素的研究,多因素耦合作用下埋地管线钢微生物腐蚀规律研究的报道较少。而多种因素相互作用机理的研究对深入揭示土壤服役环境中管线钢使用性能更具有实际的指导意义。
2)土壤微生物腐蚀研究方法仍面临巨大的挑战,需要新的研究方法和测试手段以配合土壤微生物腐蚀的深入研究。在未来,结合基因技术、分子生物学、光谱电化学及微区腐蚀观察等原位技术手段,从多角度研究微生物的呼吸代谢、电子传递途径和金属界面反应机制等。
3)自然界中,单一的微生物菌落群很难存在,往往是多种微生物通过生理相互作用共同存在于生物膜内。微生物群落通过释放多种信号分子得以相互“沟通”,形成合作或竞争群体,共同对金属材料腐蚀产生影响。因此,实际情况下通常是多种机制以不同的方式在腐蚀过程中共同发生作用。揭示混合菌种间的相互作用机理、生物多样性的变化规律和如何影响腐蚀过程,以及与单一菌种腐蚀间的区别,将是今后深入研究微生物腐蚀机理的方向。对于多种微生物对金属腐蚀耦合作用的研究,更有助于揭示实际环境中的MIC 机理,将为MIC 的防治方法和策略提供理论支持。
