超声和钼靶X线摄影与MRI对乳腺导管内原位癌的临床诊断价值
2021-04-05李巍周丹叶国麟
李巍 周丹 叶国麟
佛山市第一人民医院 528000
乳腺癌目前是女性最常见恶性肿瘤之一。2018年美国癌症统计报告中,乳腺癌占女性新发癌症病例的30%,远超其他癌症所占的比例[1-2]。乳腺癌的诊断方式包括血液检查、乳腺X 线摄影、超声等,对乳腺癌患者进行早期筛查并尽早明确诊断是非常必要的[3]。乳腺癌中最早期病变是乳腺原位癌,包括导管内原位癌(癌细胞未突破导管壁基底层)与小叶原位癌(癌细胞未突破末梢乳管或腺泡基底膜),其中以乳腺导管内原位癌(ductal carcinoma in situ,DCIS)多见,被看成是一种癌前病变,从而快速向恶性进展[4]。病理检查为临床诊断DCIS 的金标准,但是无法对广大人群进行普查。随着科技的进步和诊断技术的提高,乳腺早期的病变检出率得到了较大提高,并且乳腺X 线能发现B 超发现不了的微钙化,有助于早期诊断[5-7]。据报道,九成以上的DCIS 可因钼靶片发现的钙化而得到早期诊断,相对生存率在20年仍可达97%[8]。但是,部分原位癌早期却发病隐蔽,患者无典型的症状和体征,单纯钼靶检查可能会漏诊,往往错过最佳的治疗时间。本研究的主要目的是分析超声、钼靶X线摄影与MRI对DCIS的临床诊断价值。
1 资料与方法
1.1 一般资料 收集2015 年6 月至2018 年6 月本院手术并经病理确诊的DCIS患者40例,全部患者均采用超声检查,必要时行乳腺钼靶及MRI检查。均为女性,年龄范围为29~78 岁,中位年龄为47 岁,其中体检触及肿块的患者有23 例(肿块直径为1~2 cm 和>2 cm 患者分别为11、12 例),而未触及肿块的患者有17 例,乳头溢液10 例(6 例暗红,2 例淡红,2 例淡黄)。排除标准:穿刺为导管内原位癌但术后病理含浸润性癌即不是纯原位癌的病例。
1.2 方法 患者术前常规行乳腺超声检查,必要时行钼靶及MRI检查。超声检查:患者检查时仰卧,用彩超对患者乳房以及腋窝进行全方位扫描,使用BI-RADS 分级;主要查看是否有肿块,包括肿块的形状、纵横比、边界、回声;是否有钙化,包括钙化的大小、分布、形态;若B 超显示边界不规则的结节影或者结节内部见钙化灶为阳性。钼靶检查:对患者MLO 位和CC 位进行摄影,主要查看是否有结构扭曲;是否有肿块,包括肿块的边缘、形态、密度;是否有钙化,包括钙化的类型、分布;若钼靶显示不对称密度影、结构紊乱、肿块或者簇状密集的钙化为阳性。MRI扫描:患者检查时俯卧,对患者乳房及腋窝进行全方位扫描,记录结果;主要查看是否有肿块,包括肿块的形态、边缘、内部强化情况;是否含有非肿块强化;若MRI显示边界呈蟹足状或毛刺样的强化结节为阳性。
1.3 观察指标 主要检查患者有无导管扩张、肿物及钙化。如患者的导管扩张应记录大小、是否有肿物;对于肿物,记录大小、形状、边缘等;如有钙化,记录其钙化分布、形状和数量。
1.4 统计学方法 本研究均采用SPSS20.0 软件进行分析,计数资料以n(%)表示,组间比较采用χ2检验,P<0.05表示差异有统计学意义。
2 结果
2.1 超声结果 40 例患者全部行术前超声检查,根据超声检查结果,29 例诊断为低回声结节,4 例为肿块伴钙化,3 例为导管扩张,2 例为增生结节,1 例为囊实性结节,1例未见异常。其中,阳性结果为低回声结节(BIRADS分级3~5级),肿块伴钙化,导管扩张伴其内异常回声,囊实性结节;阴性结果为单纯导管扩张,增生结节,未见异常;超声诊断的阳性率为90.00%,具体见表1。
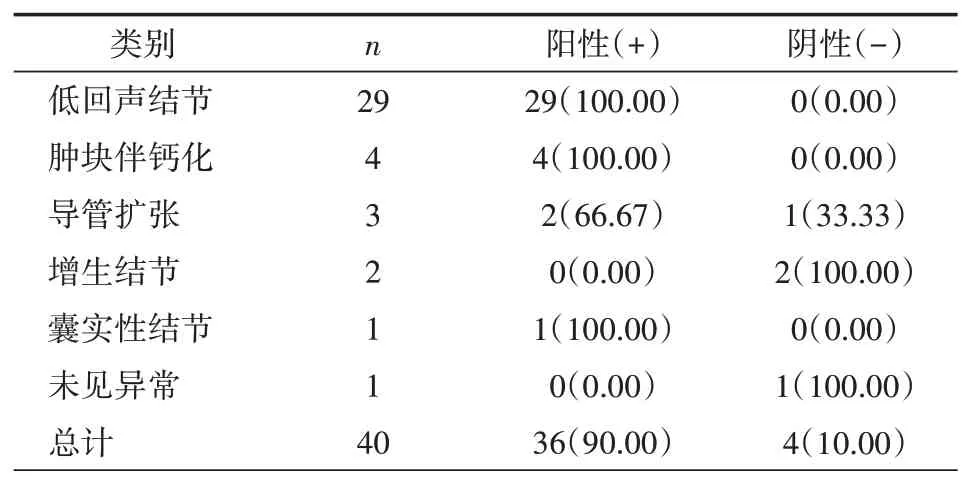
表1 超声诊断情况分析[n(%)]
2.2 钼靶诊断结果 共21例患者行术前钼靶检查,根据钼靶检查结果,10 例诊断为密度增高实质伴钙化,6 例未见异常,3 例为等密度结节,1 例为单纯密度增高影,1 例为单纯钙化;其中,阳性结果为密度增高实质伴钙化,等密度结节(BIRADS 分级3~5 级);阴性结果为单纯密度增高影,单纯钙化,未见异常;钼靶诊断的阳性率为61.90%,见表2。
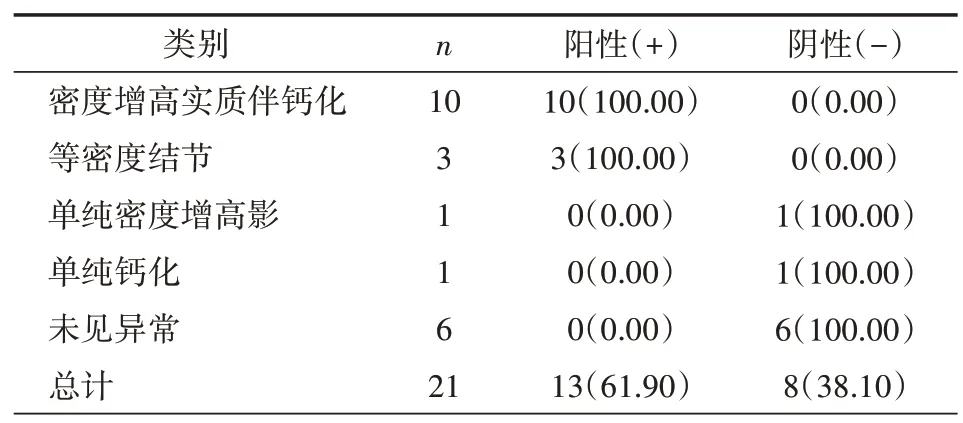
表2 钼靶诊断情况分析[n(%)]
2.3 MRI 诊断结果 共15 例患者行术前MRI 检查,根据MRI 检查结果,12 例诊断为强化结节,2 例为非强化结节,1例为单纯导管扩张。其中,阳性结果为强化结节,非强化结节(BIRADS 分级3~5 级);阴性结果为单纯导管扩张;MRI诊断的阳性率为93.33%,见表3。
2.4 超声、钼靶与MRI 对乳腺导管内癌的联合诊断价值 从以上结果我们发现,超声、钼靶与MRI对乳腺导管内癌的诊断阳性率分别为90.00%、61.90% 和93.33%(χ2=9.102,P=0.011)。超声和钼靶联合的诊断阳性率为95.00%(38/40),其中这两例患者超声和钼靶均未发现阳性征象,但是MRI 检查发现有强化结节;因此,当超声、钼靶与MRI三者联合使用时,对DCIS 的诊断阳性率可达到100.00%(40/40)。
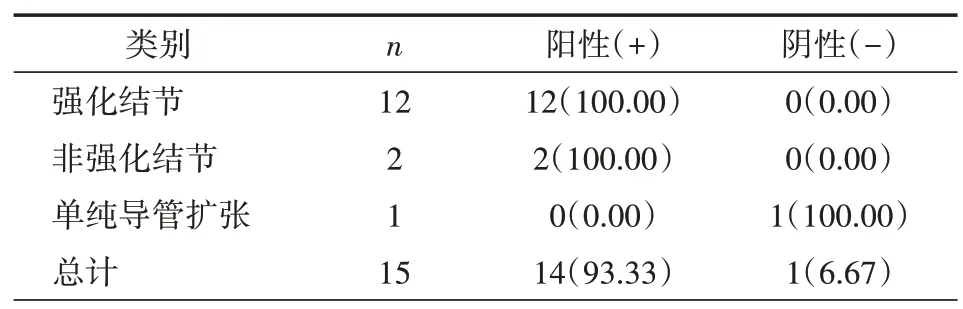
表3 MRI诊断情况分析[n(%)]
3 讨论
自乳腺早期筛查的提高以来,DCIS 的检出率出现急剧上升。数据显示美国每年有超过60 000 名患者被诊断为DCIS[9]。有学者认为,高等级DCIS 可能隐藏有高等级浸润性癌症[10-11]。Ozanne 等[12]建立了一个可以预测癌症进展率的模型,发现高级别DCIS在10年内进展成侵袭性癌的发生率是60%,低级别DCIS 是16%。另有研究表明,低、中、高评分的DCIS 病例的10 年的复发率分别是12.7%、33.0%与27.8%[13]。
DCIS 的一个重要特征是有钙化,钼靶对钙化往往比较敏感。因为中国女性乳腺多见致密型的腺体,密度较脂肪大,射线穿透困难,所以钼靶不太容易检出其病变。本组资料中钼靶检出率为52.4%,相对超声来说,钼靶对钙化的检出率较高[14-16]。
超声对软组织的分辨率良好,可显示高密度腺体内的异常改变。超声漏诊DCIS 的主要因素是未见肿物及大的钙化[17-18]。本组资料钙化检出率超声为10.00%,而多数为低回声结节,达到72.50%。导管原位癌在病灶较小的时候,超声和钼靶检查可能检测不出。但MRI 检查的分辨率较高,可能在超声和钼靶检查都未检测出病灶的时候发现异常[19]。本组资料中超声和钼靶联合的诊断阳性率为95.00%(38/40),其中有2 例患者超声和钼靶均未发现阳性征象,但是MRI 检查发现有强化结节,最终三者联合将DCIS的诊断率提升到100.00%。
综上所述,钼靶近年来大大提高了乳腺病的早期诊断率,而早期诊断的提高将最终提高乳腺癌患者的长期生存率及治愈率。但是,中国女性由于致密型乳腺较多,单纯依靠钼靶检查导致DCIS 的漏诊率会比较高,而联合使用超声及MRI 可以大大提高DCIS 的检出率。筛选出早期低风险的DCIS,从而通过最适合的治疗手段达到治愈疾病的目的,对患者具有极其重要的意义。
