碳掺杂六方氮化硼氧化脱硫性能的理论研究
2021-04-05吕乃霞
吕乃霞
碳掺杂六方氮化硼氧化脱硫性能的理论研究
吕乃霞
(兴义民族师范学院, 贵州 兴义 562400)
采用密度泛函方法计算了包括苯并噻吩(BT),二苯并噻吩(DBT),二甲基二苯并噻吩(DMDBT)在内的芳香性硫化合物在掺杂碳的六方氮化硼表面的吸附及氧化机理。结果表明,O2在掺杂碳的氮化硼首先被活化为O2-, O2-作为活性氧物种进一步将硫化物氧化为亚砜或砜。三种芳香性硫化物在碳掺杂氮化硼表面的脱硫性能按照DMDBT,DBT,BT的顺序降低。
密度泛函;氧化脱硫;碳掺杂;六方氮化硼
随着燃料中硫含量标准日趋严格,传统的加氢脱硫工艺(HDS)对苯并噻吩(BT)、二苯并噻吩 (DBT) 及其衍生物 4,6-二甲基二苯并噻吩 (DMDBT)的脱除效率较低,因此必须寻找新的方法及工艺以更有效的脱除芳香性硫化物[1-4]。吸附脱硫 (ADS)[5-6]和氧化脱硫技术 (ODS)[7-9]应运而生。其中,ODS 因其温和的操作条件和高效的脱硫性能引起了人们的关注。通过ODS工艺,苯并噻吩类硫化物最终转化为高极性的亚砜或砜,这些亚砜或砜很容易通过萃取或吸附去除。因此寻找合适的催化剂,实现温和条件下硫化物的氧化是 ODS 反应的关键。
近年来,作为一种新型二维材料,六方氮化硼 (h-BN) 具有高的化学稳定性,优良的热稳定性和大的比表面积,已在吸附、催化及功能材料等领域应用[10-12 ]。有趣的是在 h-BN 的制备过程中 B- 或者 N- 点缺陷位极易获得,而这些缺陷位点又赋予了 h-BN 极大的化学活性,并为在缺陷位点引入非金属或者金属原子形成掺杂类型的氮化硼提供了可能[13]。目前已有文献报道了掺杂类型的 h-BN 在催化领域的应用[14-19]。例如,Zhao[16]及Gao[18]的理论计算预测了碳原子掺杂的 h-BN 可以有效活化 O2并成为氧还原反应 (ORR) 的催化剂。Maji 也报道了石墨烯岛掺杂的 h-BN 可以成为高效的 ORR 催化剂[19]。实验上已经合成了碳掺杂的氮化硼,并理论预测了BCN(=10~50)可以成为有效的吸附脱硫材料[20]。因此本文主要通过计算的方法探讨三种硫化物 BT、DBT 及 DMDBT 在碳掺杂 h-BN 表面的氧化脱硫机理,为寻找高效的ODS催化剂提供理论依据。
1 计算模型与计算方法
选用 B21N21簇模型模拟 h-BN 单层,边缘的原子全部用 H 原子饱和,如图1所示。在此模型的基础上,分别用碳原子替换一个中心 B 或 N 原子,可得到 CB及 CN的碳掺杂的模型,分别为图1(a)、(b)。
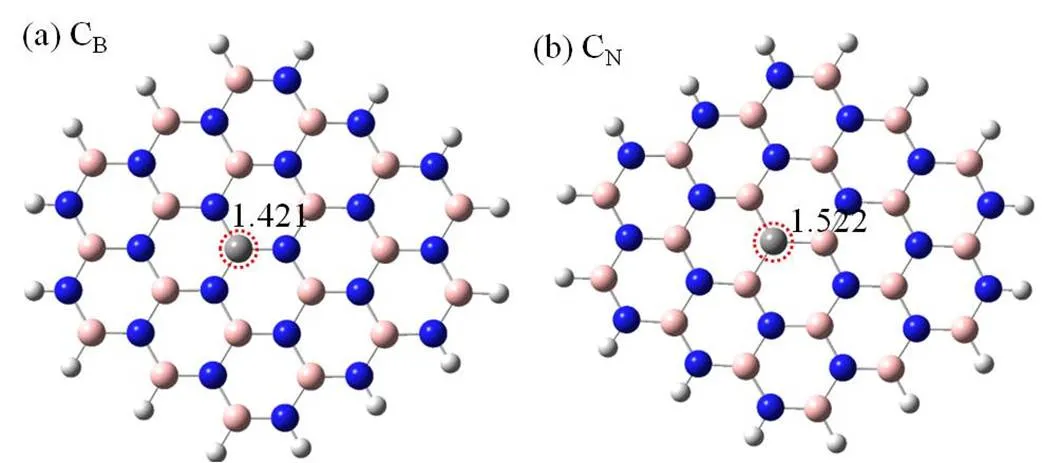
图1 计算模型的选取
(a) 碳掺杂在B位, CB; (b) 碳掺杂在N位,CN
选用色散矫正的密度泛函方法(M06-2X+D3)[21],采用6-311G(d,p) 基组进行计算。对所有的原子坐标进行全优化,并结合频率确认稳态结构没有虚频,而过渡态结构仅有一个虚频。计算采用 Gaussian16 程序包完成[22]。
吸附能用如下公式计算:
ΔG = Gads/C−BN− GC−BN− Gads(1)
公式(1)中,Gads/C−BN代表吸附物种在碳掺杂氮化硼的吉布斯自由能,GC−BN代表碳掺杂氮化硼的吉布斯自由能,Gads代表吸附物种的吉布斯自由能。由此公式定义的吸附能负值表示热力学稳定的体系。
2 计算结果与讨论
2.1 计算模型的优化结构
如图1所示,(a) 为C掺杂在B位置,形成CB缺陷位,三个 C ̶N 键长均为1.420 Å;(b) 为C掺杂在N位置,形成CN缺陷位,三个C ̶B键长分别为1.522 Å,1.523 Å,1.523 Å。两种类型的碳掺杂结构都保持六方氮化硼的平面构型。根据公式:
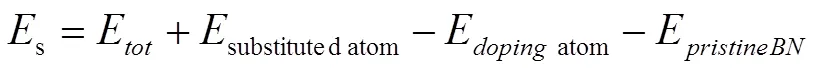
其中,Etot是碳掺杂的构型的总能量, Esubstituted atom是指被取代原子的总能量,Edoping atom是指掺杂碳原子的总能量,Epristine BN是未掺氮化硼的总能量。由公式(2) 可得到缺陷位CB和CN位的取代能分别为77.6、40.2 kcal·mol-1,因此,碳原子掺杂在氮化硼表面N位所需能量更低,是实验上更易获得的缺陷位。本文将探讨三种硫化物BT、DBT、DMDBT在碳掺杂六方氮化硼的吸附及氧化转化过程。
2.2 DMDBT 在CN位的吸附及转化
图2 给出了 DMDBT 在 CN缺陷位氧化转化过程的优化构型。(a) 为 O2和 DMDBT 的共吸附构型。O2吸附在掺杂的 C 原子上,吸附高度为 1.491 Å,吸附后 O2键长增加到 1.299 Å,说明 O2在 CN位被明显活化,NBO电荷分析表明吸附后O2上的电荷为-0.31 e。DMDBT 以近乎平行于表面的方式吸附在 O2附近,S、O 之间的最短距离为 3.130 Å。构型 (b) 是 DMDBT 氧化过程的第一个过渡态(TS1)。O2的键长拉伸到 1.639 Å,S、O 之间的距离进一步缩短到 1.749 Å,以实现 O2解离得到的 O 原子转移到 DMDBT,形成中间体(c)。在构型 (c) 中,S-O 键形成,键长为 1.507 Å。至此,O2中的一个氧原子转移至 DMDBT,完成了由硫化物向亚砜的转化,而剩余的 O 原子由垂直吸附模式转变为倾斜地吸附在C、B 之间,形成桥式的 C-O*-B 表面物种,其中 C-O 及 B-O 键长分别为 1.376,1.403 Å。接下来,C-O*-B 作为活性氧物种继续氧化亚砜,(d) 为亚砜氧化的过渡态(TS2)。在过渡态TS2中,桥式的 C-O*-B 转化为端式的 C-O*,进而将表面 O*转移至 S 原子上,完成氧化过程。(e) 为最终的氧化产物砜。
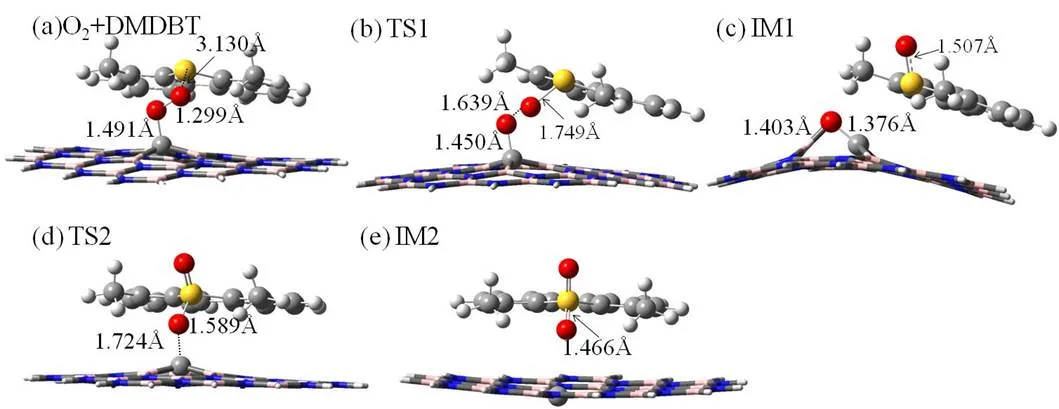
图2 DMDBT在CN位氧化过程的结构
(a) O2与DBT共吸附构型; (b) TS1; (c) IM1; (d) TS2; (e) IM2
表1给出了两步氧转移过程的反应能垒及反应热。在CN位,对于硫化物BT及DBT,从两步的反应能垒(ΔG1≠、ΔG2≠)可以看出,第一步的反应能垒远高于第二步的反应能垒,说明第一步氧转移过程为速决步,反应能垒分别为43.3、40.1 kcal·mol-1,反映了DBT比BT更容易氧化。对于DMDBT,由于中间产物IM1中B-O*-C物种特别稳定,导致两步的反应能垒差别不大,分别为41.9、43.9 kcal·mol-1。图3给出了三种硫化物(BT,DBT,DMDBT)在CN缺陷位的反应势能面。从势能曲线可以看出,第一步氧转移过程是反应的决速步骤,即由硫化物转化为亚砜的过程,BT、DBT、 DMDBT三种硫化物的表观活化能分别为38.8、33.3、32.1 kcal·mol-1,表观活化能依次降低,说明硫化物的反应活性与烃基数目有关,烃基数目越多,给电子的效应越明显,硫化物S原子的电子密度越大,越容易被氧化,与实验结论基本一致[23]。
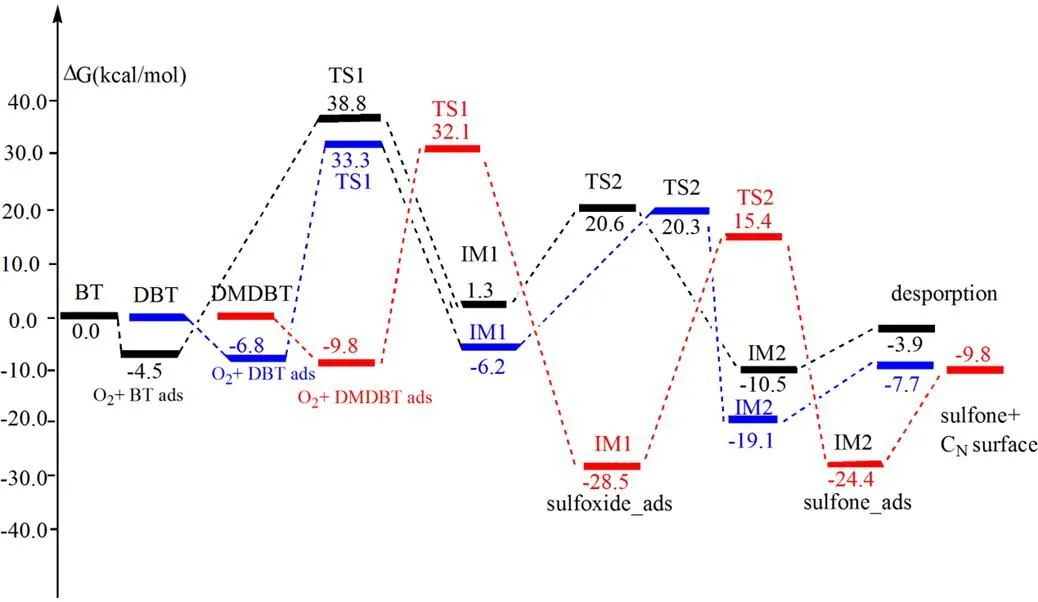
图3 BT、DBT及DMDBT 在h-BN CN位氧化过程的势能图
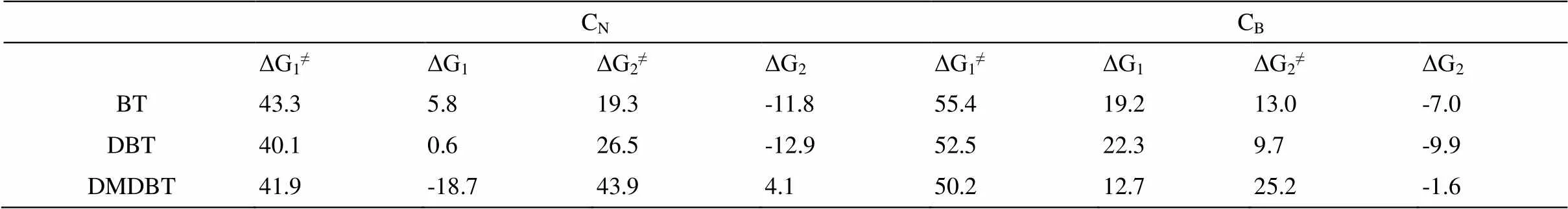
表1 BT, DBT, DMDBT在CN及CB缺陷位的反应能垒(ΔG≠) 及反应热(ΔG), kcal/mol
2.3 DMDBT 在CB位的吸附及转化
图4给出了DMDBT 在CB位氧化过程的优化构型。(a)为O2+DMDBT的共吸附构型。值得注意的是,在共吸附构型中,O2吸附在C附近的B原子上,吸附高度为1.542 Å,O2的键长拉伸到1.309 Å,NBO电荷分析表明吸附后O2上的电荷为分别为-0.55 e。因此在碳掺杂的h-BN,吸附后O2的键长接近超氧离子O2-的键长1.33 Å,可以认为O2首先被活化为O2-,是下一步硫化物发生氧化反应的关键。(b)为DMDBT氧化过程中的第一个过渡态TS1,在此过渡态中,O-O键长为1.650 Å,说明O2已完全解离。解离后的氧原子与DMDBT上的S结合,O-S之间的距离缩短到1.766 Å,说明S-O键正在形成。经历TS1后,DMDBT被氧化为亚砜,并形成了表面B-O*物种,见结构 (c)。构型 (d) 是过渡态TS2,B-O*作为活性氧物种,进一步将亚砜氧化为砜。构型(e)为最终氧化产物砜。
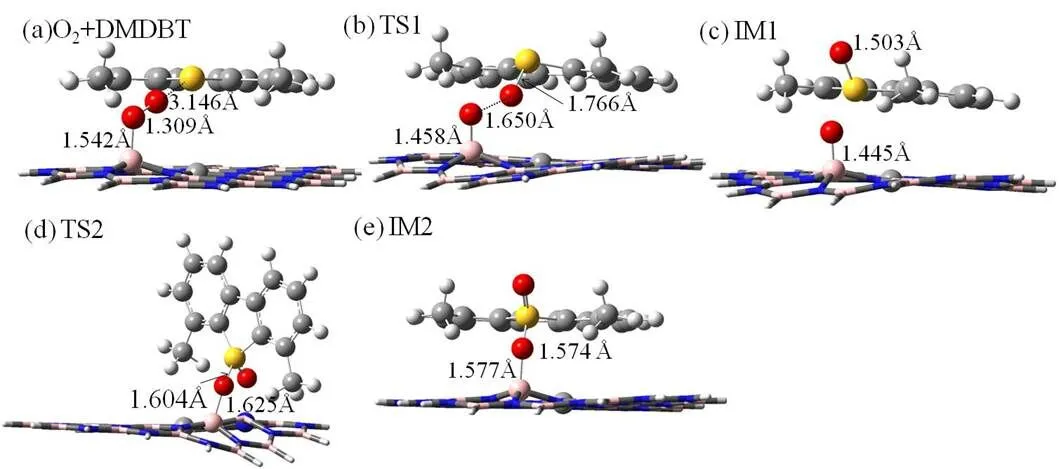
图4 DMDBT在CB位氧化过程的结构
(a) O2与DBT共吸附构型 (b) TS1 (c) IM1 (d) TS2 (e) IM2
表1列出了三种硫化物在CB位的反应能垒, BT、DBT、DMDBT第一步氧转移过程的反应能垒(ΔG1≠)分别为55.4、52.5、50.2 kcal·mol-1;而第二步氧转移过程的反应能垒(ΔG2≠)较低,分别为13.0、9.7、25.2 kcal·mol-1。图5给出了三种硫化物在CB位氧化的势能曲线,BT、DBT、DMDBT的表观活化能分别为21.5、15.3、11.0 kcal·mol-1。因此,第一步氧转移过程即硫化物氧化为亚砜的过程是反应的速决步,并且反应活性随着烷基数目增加而增加,DMDBT最容易被氧化,与CN位反应活性表现一致。
与CN位相比,三种硫化物在CB位的表观活化能降低,但速决步的反应能垒(ΔG1≠)增加。比较图3和图5,可以看出,O2与三种硫化物BT、DBT、DMDBT在CN位的共吸附构型的吸附能分别为-4.5、-6.8、-9.8 kcal·mol-1,而在CB位的吸附能分别为-33.9,-37.2,-39.2 kcal·mol-1,因此共吸附结构在CB位更稳定导致了反应的势阱加深,硫化物在CB的反应活性略低于CN位。在CN或CB位的共吸附构型中,O2的键长分别为1.299、1.309Å,吸附能分别为-2.4、-27.0 kcal·mol-1,而O2在未掺杂的六方氮化硼的吸附能为 3.3 kcal·mol-1,O-O键长与气相相比基本不变(1.198 Å),因此与未掺杂的六方氮化硼相比,碳掺杂的氮化硼有能力活化O2,O2的活化是后续氧化反应的关键。
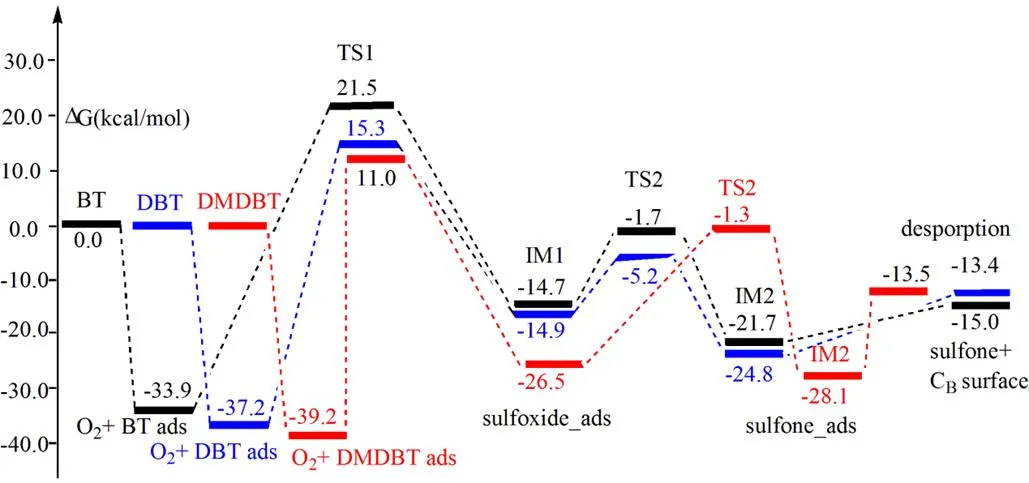
图5 BT、DBT及DMDBT 在h-BN CB位氧化过程的势能图
3 结 论
本文利用密度泛函M06-2X方法计算了三种硫化物BT、DBT、 DMDBT在碳掺杂六方氮化硼的吸附及氧化机理。计算表明,碳掺杂的氮化硼可以形成两种掺杂结构,即CN和CB掺杂结构。CN掺杂构型在能量上更稳定。O2在CN位或CB位,均可以被有效活化,成为活性氧物种(O2-)。硫化物在碳掺杂的氮化硼表面通过两步反应完成氧化过程。第一步,硫化物被表面活化的O2-氧化为亚砜,这是反应的速决步;第二步,亚砜被表面的氧物种继续氧化为砜。三种硫化物按照BT、DBT、DMDBT的顺序反应活性依次升高,这可能与DMDBT上的烷基数目有关。CN位与CB位相比,速决步的反应能垒略低。
[1]张海燕,代跃利,蔡蕾.杂多酸催化剂催化氧化脱硫研究进展[J].化工进展,2013,32(4):809-815.
[2]刘淑芝,孙兰兰,张晓丽,等.柴油氧化脱硫技术研究进展[J].化工进展,2007,26( 2):212-220.
[3]何爱珍,刘红光,王坤,等.轻质燃料油脱硫技术研究进展[J].工业催化,2010,18(7):8-12.
[4]BREYSSE M G,DJEGA-MARIADASSOU S,PESSAYRE C,et al. Deep desulfurization:reactions, catalysts and technological challenges[J].,2003, 84 (3):129-138.
[5]IRAVANI A A, GUNDA K, NG F T T,et al. Adsorptive removal of refractory sulfur compounds by tantalum oxide modified activated carbons[J].,2017, 63: 5044-5053.
[6]LUO J, CHAO Y, TANG Z, et al. Design of Lewis Acid Centers in Bundlelike Boron Nitride for Boosting Adsorptive Desulfurization Performance[J].,2019, 58:13303-13312.
[7]ZHANG W, ZHANG H, XIAO J, et al. Carbon nanotube catalysts for oxidative desulfurization of a model diesel fuel using molecular oxygen[J].,2014, 16: 211-220.
[8]MJALLI F S, AHMED O U, AL-WAHAIBI T, et al. Deep oxidative desulfurization of liquid fuels[J].,2014, 30: 337-378.
[9]ZHU W, WANG C, LI H, et al. One-pot extraction combined with metal-free photochemical aerobic oxidative desulfurization in deep eutectic solvent[J].,2015, 17: 2464-2472.
[10] ABDUL A H M,WASEY, CHAKRABARTY S, et al. h-BN Monolayer on the Ni(111) Surface: A Potential Catalyst for Oxidation[J]., 2013, 5:10404-10408.
[11] WU J, WANG B, WEI Y, et al. Mechanics and Mechanically Tunable Band Gap in Single-Layer Hexagonal Boron-Nitride[J].. Lett. 2013,1:200-206.
[12] OBRAZTSOVA E A, SHTANSKY D V, SHEVEYKO A N, et al. Metal Ion Implantation of Multiwalled Boron Nitride Nanotubes[J]., 2012, 67: 507-510.
[13] PETER R, BOZANIC A, PETRAVIC M, et al. Formation of defects in boron nitride by low energy ion bombardment[J].,2009, 106: 083523.
[14] HUANG C, CHEN C, ZHANG M, et al. Carbon-doped BN nanosheets for metal-free photoredox catalysis[J].,2015, 6: 7698.
[15] GAO X, WANG S, LIN S. Defective hexagonal boron nitride nanosheet on Ni(111) and Cu(111): stability, electronic structures, and potential applications[J]., 2016, 8: 24238-24247.
[16] ZHAO J, CHEN Z. Carbon-Doped Boron Nitride Nanosheet: An Efficient Metal-Free Electrocatalyst for the Oxygen Reduction Reaction[J].,2015, 119: 26348-26354.
[17] SINTHIKA S, MATHAN K E, RANJIT T. Doped h-BN monolayer as efficient noble metal-free catalysts for CO oxidation: role of dopant and water in activity and catalytic de-poisoning[J].,2014, 2: 12812-12820.
[18] GAO M, ADACHI M, LYALIN A, et al. Long Range Functionalization of h-BN Monolayer by Carbon Doping[J]..,2016, 120: 15993-16001.
[19] MAJI R,BHATTACHARJEE J. A Synergistic View of Magnetism, Chemical Activation, and ORR as Well as OER Catalysis of Carbon Doped Hexagonal Boron Nitride from First-Principles[J].,2019, 123:16731-16740.
[20] LI H, ZHU S, ZHANG M, et al. Tuning the Chemical Hardness of Boron Nitride Nanosheets by Doping Carbon for Enhanced Adsorption Capacity[J]., 2017, 2:5385-5394.
[21] ZHAO Y,TRUHLAR D G. Exploring the Limit of Accuracy of the Global Hybrid Meta Density Functional for Main-Group Thermochemistry, Kinetics, and Noncovalent Interactions[J].,2008, 4:1849-1868.
[22] FRISCH M J, TRUCKS G W, SCHLEGEL H B, et al. Gaussian 16 ed., Gaussian, Inc, Wallingford, CT, 2016.
[23] OTSUKI S, NONAKA T, TAKASHIMA N, et al. Oxidative Desulfurization of Light Gas Oil and Vacuum Gas Oil by Oxidation and Solvent Extraction[J].2000, 14: 1232-1239.
Theoretical Study on the Oxidative Desulfurization Performance of Carbon Doped Hexagonal Boron Nitride
(Xingyi Normal University for Nationalities, Xingyi Guizhou 562400, China)
The adsorptions of aromatic sulfur compounds involving the benzothiophene(BT), dibenzothiophene (DBT), and 4,6-dimethyl-dibenzothiophene (DMDBT) on the carbon doped hexagonal boron nitride and the subsequent conversion were calculated by density functional theory. The calculation results indicated that the adsorption of O2was firstly activated to superoxide (O2-) on the CNor CBdoped surface, and then the sulfur compounds were oxidized to sulfoxide or sulfones. The reaction activity of three aromatic sulfides on carbon doped boron nitride surface decreased in the order of DMDBT, DBT and BT..
DFT; ODS; Carbon-doped; Hexagonal boron nitride
黔西南州科技项目(项目编号:2019-2-51)。
2020-01-21
吕乃霞(1979-),女,贵州省兴义市人,副教授,博士学位,2008年毕业于厦门大学物理化学专业,研究方向:从事理论计算工作。
TQ013
A
1004-0935(2021)03-0285-04
