独脚金内酯D环中间体3-甲基-5-羟基呋喃-2(5H)-酮的一步法合成*
2021-04-02周国华欧思敏
周国华,欧思敏
(岭南师范学院化学化工学院,清洁能源材料化学广东普通高校重点实验室,广东 湛江 524048)
自2008 年Gomez-Roldan等和Umehara等两个研究小组分别于《Nature》发表文章[1-2],认为独脚金内酯是一种控制植物分枝的新激素以来,独脚金内酯引起了广大科研工作者的兴趣。而对独脚金内酯及其类似物的合成是众多研究工作开展的重要的前提。独脚金内酯及其类似物(图1)具有相似的结构,包括A、B、C、D四个环结构,及连接C、D环的b不饱和酮。在人工合成过程中先制备ABC环及D环中间体,再将两个中间体连接成完整的活性分子[3-6]。D环中间体最主要为3-甲基二氢呋喃-2(5H)-酮(1)和3-甲基-5-羟基呋喃-2(5H)-酮(2)。对化合物1的合成最初由Johnson等[4]和Zwanenburg等[3]提出,但他们的方法都存在不足,如原料较为昂贵,成本高,合成路线较长,操作复杂,且需要用较危险的溴水等。
此外,对于中间体2的合成,Johnson等[7]提出以丙酮酸乙酯和醋酸乙烯酯为原料,经过两步合成获得,收率48%。Morris和McErlean则提出以甲基丙二酸二甲酯为起始原料,先经碱水解成甲基丙二酸,再与乙二醛(3)反应合成出目标产物2[8]。该方法操作相对简单,但同样经两步获得最终产物,且综合收率只有37%。因此,发展D环中间体新的合成方法,对于独脚金内酯的分析测定及其植物生理功能研究具有重要意义。
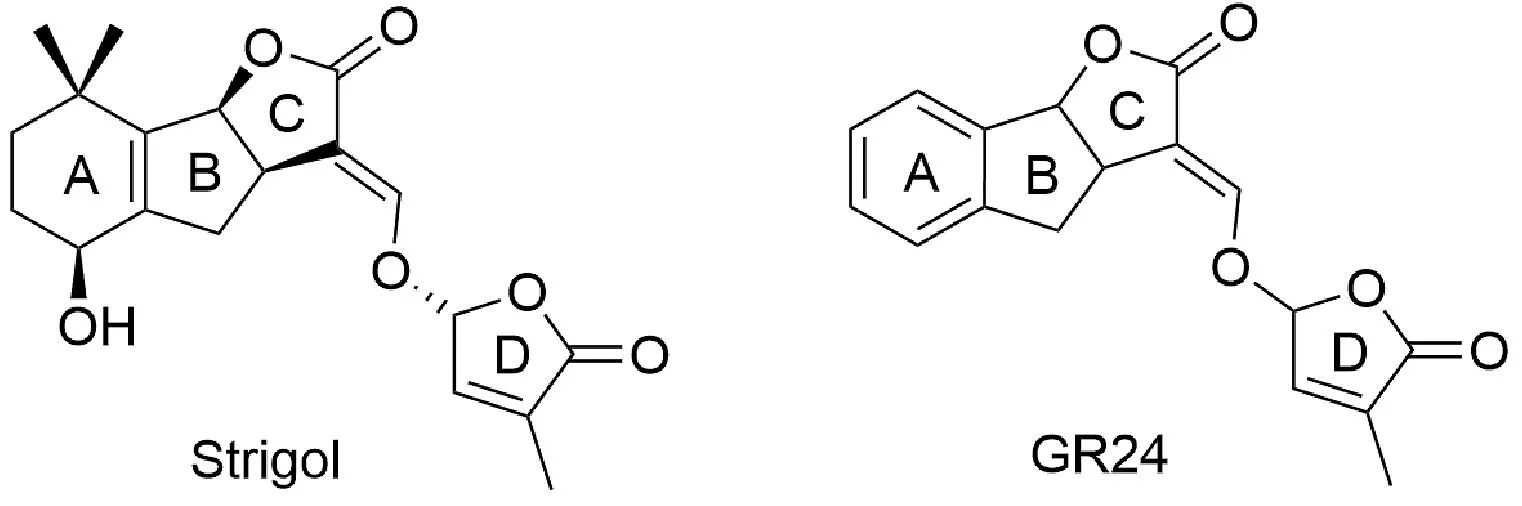
图1 独脚金内酯Strigol及其类似物GR24的结构Fig.1 Structures of strigol and its analog GR24

图2 化合物2的一步法合成路线Fig.2 Synthesis route of compound 2 proposed
本文在文献调研及前期研究工作的基础上,对文献方法进行改进,以化合物3和甲基丙二酸二乙酯(4)为起始原料,在水体系中经H+的催化,酯的水解和羟醛缩合同时进行,实现一步法合成目标化合物2,综合收率提高至54%,其结构经1HNMR和13CNMR确证。该方法不仅大大简化了化合物2的合成,而且提高了其收率,对于独脚金内酯及其类似物GR24的规模化生产,促进独脚金内酯及其植物生理研究,以及其它具有多取代2(5H)-呋喃-2-酮类药物的合成研究具有重要意义。
1 实 验
1.1 仪器与试剂
核磁共振波谱仪(AVANCE III HD 400 MHz型),Bruker 公司;液相色谱仪(L600型;色谱柱:pGrandsil C18柱,250×4.6 mm;流动相:50%甲醇,流速1 mL/min;检测器:紫外可见光检测器L600UV,l=254 nm),普析公司。
甲基丙二酸二乙酯(分析纯),郑州希派克科技有限公司;40%乙二醛水溶液和732型氢型强酸型阳离子交换树脂,上海麦克林生化科技有限公司;其余所用试剂均为分析纯试剂。
1.2 合成方法
在100 mL单口烧瓶中加入7.89 g(54 mmol)40%的乙二醛水溶液、5.6 g(32 mmol)甲基丙二酸二乙酯、45 mL水,搅拌均匀,再向其中加入10滴浓硫酸,加热回流约16小时。反应结束后,向混合溶液中加入氯化钠固体至溶液饱和,用乙酸乙酯(3×25 mL)萃取,合并有机层,无水硫酸镁干燥,过滤,旋转蒸发浓缩,真空干燥得到粘稠状液体。经快速柱层析(乙酸乙酯:石油醚=2:3)纯化,最终得到2 g淡黄色粘稠状液体化合物1,收率54%。1HNMR (CDCl3, 400 MHz) δ: 6.89 (s, 1H, =CH-), 6.10 (s, 1H, -CHOH-), 4.12 (q, 1H, J=7.2 Hz, -OH), 1.96 (s, 3H, -CH3);13CNMR (CDCl3, 101 MHz) δ: 172.16 (C=O), 144.15 (=CH-), 133.95 (=CCH3-), 96.58 (-CHOH-), 10.56 (CH3)。表征数据与文献报道一致。
2 结果与讨论
2.1 反应条件优化
为了获得最优的反应条件,对反应中催化剂、溶剂和原料配比等因素进行了考察。
(1)催化剂
本研究为了在一步反应中偶合酯的水解、羟醛缩合反应以及内酯的环合,选择酸性催化条件,为此分别考察了常用无机酸硫酸、盐酸,以及便于分离、回收的固体酸性催化剂氢型强酸型阳离子树脂和人造沸石对反应的影响,结果见表1。
由表1可见,该反应中催化剂的加入是必需的,这与酯的水解和羟醛缩合的反应条件一致。而不同催化剂的添加对反应的效果不同,酸性较强的H2SO4和强酸型阳离子树脂的效果较好,经硅胶柱纯化后的收率达54%,而HCl的催化效果相对较差,最终收率仅为19%。另外,从结果可知,该反应有赖于H+使基团质子化,形成活泼中间体,从而催化反应的进行。因为同为常用酸性催化剂的人造沸石为Lewis酸,无法提供质子而不能催化反应的进行。因此,从反应效率和收率考虑,硫酸和阳离子树脂都是可选的催化剂。但从产业化角度考虑,虽然阳离子树脂的成本相对较高,但使用过程中比硫酸更安全和环保,且产物分离更方便,可实现催化剂的循环使用。因此,若该方法发展为产业化生产,阳离子树脂是首选催化剂。

表1 不同催化剂对一步法反应的影响Table 1 Effect of different catalysts on the one-step method for compound 1a
(2)溶剂
由于反应原料为40%的乙二醛水溶液,因此在溶剂考察中主要选择水,以及与水互溶的强极性溶剂甲醇、乙醇和四氢呋喃。结果如表2所示。

表2 不同溶剂对化合物1的合成影响Table 2 Effect of different solvent on the synthesis of compound 1a
结果表明,该反应只有以水为溶剂时才能获得产物,可能原因有二:(1)以甲醇和乙醇为溶剂时,由于大量醇的存在,使得酯的水解反应平衡左移;(2)丙二酸经羟醛缩合后的脱羧反应需要在较高温度下进行[9-10],而甲醇、乙醇和四氢呋喃的回流温度不够高。除此之外,以水为溶剂相比其它有机溶剂对环境更友好,因此该反应以水为溶剂最佳。
(3)物料比

表3 物料比对化合物1的合成影响aTable 3 Influence of mass ratio of reactant on the synthesis of compound
合成中的羟醛缩合反应效率受到物料比的影响。理论上,为了避免1个化合物3分子与2个化合物4分子发生缩合,应该控制原料3在反应体系过量,因此对反应物3和4的比例进行了考察,结果如表3所示。
从结果可见,化合物2的收率的确随着化合物3用量的增加而增加。当化合物3:化合物4从1.1:1增加至1.5:1时,收率由18%迅速增加至54%,但继续增加3的用量,即使比例大于20:1,对收率已经不再产生影响,由此可知,此时总体反应平衡已经不是由羟醛缩合步骤决定,而受到了酯水解、内酯形成的动态平衡决定。因此,从反应原子经济性、成本和环保角度考虑,物料比以1.5:1为宜。
3 结 论
本文以廉价的乙二醛和甲基丙二酸二乙酯为原料,在H+的催化下,一步合成独脚金内酯的中间体3-甲基-5-羟基呋喃-2(5H)-酮。通过反应中各种条件的考察,确定了反应的最佳条件为:以水为溶剂,低成本的硫酸或者相对高成本但可回收利用的氢型强酸型阳离子树脂为催化剂,乙二醛与甲基丙二酸二乙酯的比例为1.5:1,110 ℃回流。在该最优条件下,反应的产率为80%,纯化的收率为54%。相比文献报道的合成方法,“一步法”合成简单、绿色环保、成本低,整体收率较分步法提高17%,具有较好的工业前景,为独脚金内酯类似物GR24的产业化及独脚金内酯的深入研究提供基础,同时也为其它多取代2(5H)-呋喃-2-酮类药物的合成研究提供参考。
