酸浸法回收废锂电池中有价金属钴的研究进展
2021-03-29蒋梦迪张继予谢宏泽何俊沂杜大兴吴文荣唐庆杰
蒋梦迪,张继予,谢宏泽,何俊沂,杜大兴,吴文荣,唐庆杰
(河南理工大学化学化工学院,河南 焦作 454000)
锂离子电池因具有质量轻、能量密度大、自放电率低、循环寿命长、无记忆效应等诸多优点,已在移动电子设备、医疗、航天航空等诸多领域广泛应用,随之而来的则是锂电池的废弃量逐年增加。绝大多数废锂电池并未得到有效处理,造成电池中的有价金属元素大量浪费,同时也带来不可避免的环境污染。对废锂电池进行回收再利用,既可节约成本,避免资源浪费,又能减轻环境污染问题。钴是一种重要的国家战备金属,在锂电池中具有最高的回收价值,品位远高于一般矿石,回收价值比例约占整个电池回收比例的82.4%[1](表1、表2)。本文对国内外废锂电池中的有价金属元素钴的回收现状及回收工艺进行了详尽的综述,比较分析后得出结论,酸浸法更具市场推广前景,应用价值更高,并归纳总结出了浸出钴的最佳工艺条件。

表1 锂电池中所含金属的市场价格 /元·t-1

表2 锂电池正极材料成分 /%
1 废锂电池中金属钴的回收工艺
目前,国内外从废锂电池中回收有价金属的工艺主要为火法冶金、湿法冶金或者两种工艺的结合。典型的火法冶金能耗大,操作复杂,对环境的污染严重。湿法冶金工艺具有效率高、毒性气体排放较少、得到的产物纯度高、反应条件温和等优点,因此成为工业中回收和再循环利用锂电池中有价金属的常用工艺。
作为湿法冶金的关键步骤,浸出受到人们的广泛关注。目前常采用氨浸出、生物浸出、酸浸出等工艺来回收电池中的有价金属。浸出后,锂离子电池中的有价金属以溶解性络合物或溶解态在浸出液中存在,此时还需通过分离纯化、原位再生等分离手段,从浸出液中分离出有价金属离子。其中分离纯化通过萃取、沉淀、吸附、电化学等一系列技术手段,将各种金属逐一分离,以便更好地回收目标金属[2]。原位再生是对浸出液进行萃取除杂,并外加一定比例的金属盐,再采用共沉淀或溶胶凝胶法制备前驱体,最后在适宜的温度下焙烧再生废锂电池正极材料,从而实现有价金属的回收再利用[3]。图1是废锂电池的火法与湿法回收工艺流程图。
1.1 氨浸出
氨浸出工艺目前已应用于提取废锂电池中的有价金属,对金属Ni、Co、Cu和Zn等具有较好的选择性,并能与这些金属形成稳定的配合物,尤其是电池中的钴金属元素,具有与氨的高络合能力。反应方程式如下:
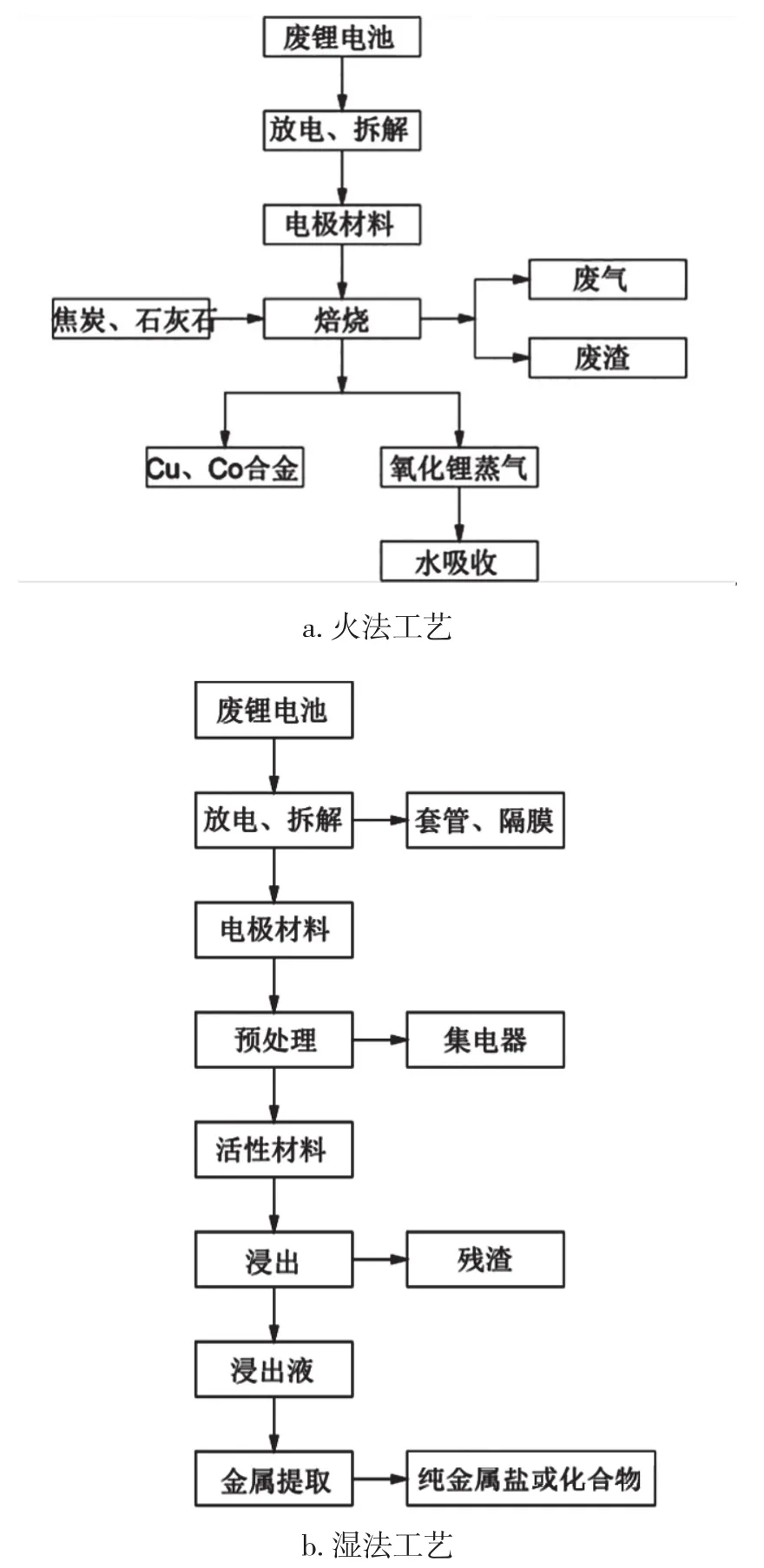
图1 废旧锂离子电池的火法工艺和湿法工艺流程

锂电池中的电极材料发生反应时,高价态的Co首先被还原为Co2+,随后Co2+进入溶液,与溶液中的游离氨(NH3)及氨根(NH4+)反应,生成Co(NH3)m2+,从而达到浸出的目的。
已有许多学者对氨浸出工艺进行了研究。Zheng等[4]提出了使用“氨+铵盐”体系从废锂离子电池中选择性提取Li等有价金属的新工艺。该法以 NH3•H2O和(NH4)2SO4为浸出剂,Na2SO3为还原剂,浸出废LiNi1/3Co1/3Mn1/3O2正极废料中的有价金属。Ku等[5]研究了以碳酸铵为pH缓冲剂,碳酸铵+氨水+亚硫酸铵三元浸出体系下的浸出工艺,确定了氨+亚硫酸铵+碳酸铵为最佳组合,且在最优条件下,电池中的Co和Cu可完全浸出。Wang等[6]以H2O2为还原剂,采用NH3H2O+NH4HCO3体系浸出废旧锂离子电池中的有价金属,其中电池中Co的浸出率达到94.57%。
氨作为选择性浸出剂,具有降低生产成本、可回收再利用的优点,可作为锂电池浸出回收工业化的潜在浸出剂。但氨浸出工艺仍存在氨易挥发、仪器密闭性要求高、对环境及人体有一定的潜在危害等缺点。
1.2 生物浸出
生物浸出常采用无机嗜酸菌,以单质硫和亚铁离子作为其自身的能量来源,在浸出液中生成硫酸和铁离子代谢物,促进电池中的金属溶解,从而实现对Co等有价金属元素的选择性浸出。
Mishra等人[7]通过引入铁硫杆菌,探究从废锂电池中浸出Co和Li的工艺,结果表明电池中Co和Li的浸出率较低。为提高生物浸出工艺的效率,Zeng等人[8]尝试以铜为催化剂,回收废锂电池中的有价金属。研究发现,加入少量的铜离子作为催化剂,在提高钴浸出速率的同时,也提高了钴的回收率。
与酸浸出和氨浸出相比,生物浸出具有在低浓度下的选择性高、运行成本低、操作方便、浸出条件温和、环境友好等优点,但生物浸出工艺仍存在浸出时间长、浸出效率低、细菌难以培养等缺点。
1.3 酸浸出
酸浸出通常是用酸将废锂电池中的金属转化成对应的金属离子,并转入到浸出液中。目前酸浸出工艺主要分为有机酸浸出与无机酸浸出两类,优缺点各不相同,有学者对其进入了深入的研究。
1.3.1 无机酸浸出
无机酸具有来源广、成本低等优点,被广泛应用于废锂电池的有价金属浸出。常用的HCl、HNO3、H2SO4等无机酸可较好地浸出正极材料,盐酸和硫酸的浸出机理如下:

以HCl作为酸浸出试剂时,钴的浸出率接近100%。但盐酸与硝酸的挥发性较大,在以二者作为浸出试剂时,会有NO2和Cl2产生,需采用尾气治理装置,成本加大,操作环境较恶劣,且对环境不友好[9],所以一般常采用硫酸作为主要的酸浸出试剂。图2是以硫酸作酸浸出试剂回收废锂电池中的有价金属的流程图。
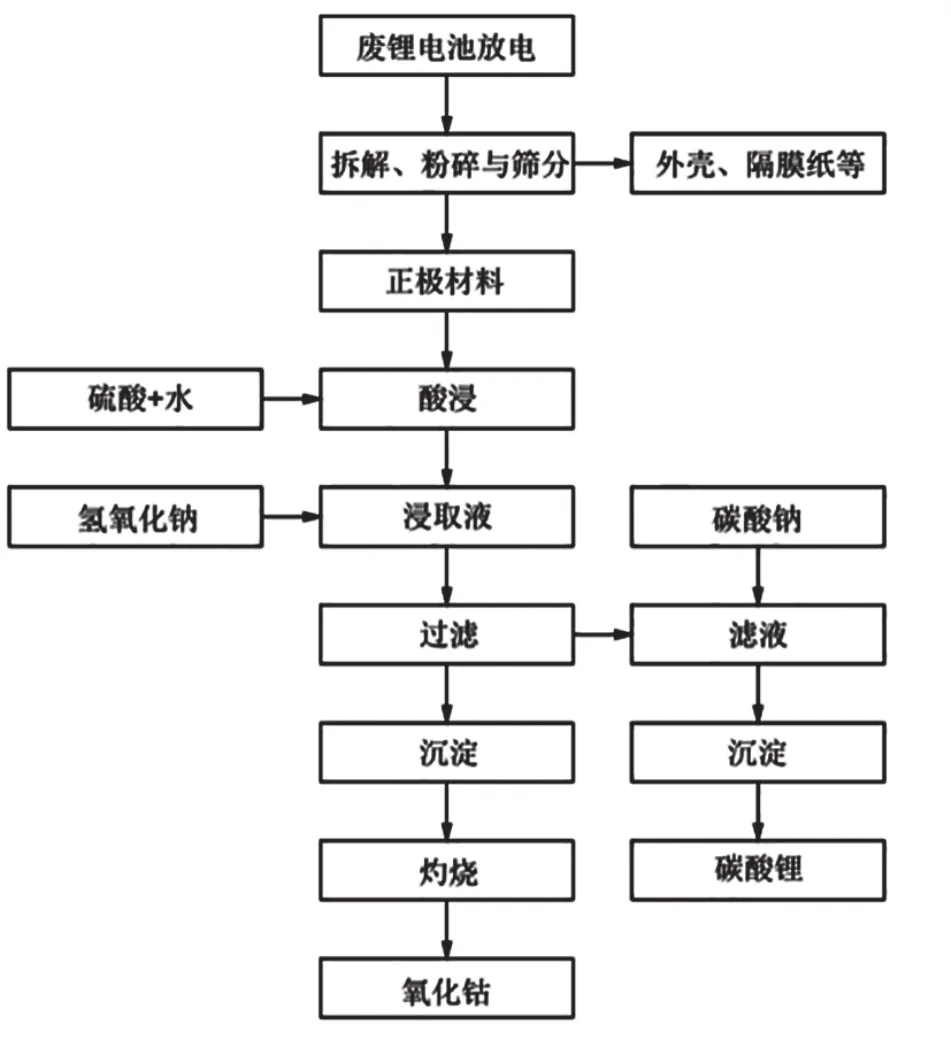
图2 硫酸浸出废锂电池中的有价金属的流程图
陆修远等[10]通过正交实验得出结论,在H2SO4浓度为 2mol•L-1、浸出剂与原料比为 0.01g•L-1、搅拌速度500r•min-1、浸出温度40℃的条件下,浸出2h后,Co的浸出率为96.79%。He等[11]以1mol•L-1H2SO4+1% H2O2体系为浸出剂,适宜条件下Li、Ni、Co和Mn的浸出率达到 99.7%以上。张阳等[9]采用正交实验,探究在有无双氧水条件下Co的浸出效率,结果表明在单一硫酸体系中,Co的浸出率低于60%;在H2O2+H2SO4体系下,钴的浸出率可达90%以上。
综合诸多学者的研究结果可知,在适宜条件下,不管是单元锂电池还是多元锂电池,无机酸均能有效地将电池中的Li、Ni、Co等有价金属浸出。但浸出液中会含有多种金属离子,这增加了各金属的分离纯化难度,同时浸出过程会产生一定的废水和废气,不利于操作人员的身体健康和环境保护。
1.3.2 有机酸浸出
有机酸具有浸出效率高、温度低、对环境友好等优点,近年来在工业与学术领域备受关注。常见的可用作废锂电池浸出剂的有机酸有柠檬酸、苹果酸、天冬氨酸、抗坏血酸、酒石酸、亚氨基二乙酸等[12-15]。但这些有机酸并不能完全浸出金属,为提高有价金属的浸出效率,常使用1vol%~6vol%的H2O2作还原剂[16]。Chen等[17]探究了“柠檬酸+H2O2” 浸出体系,发现在温度 70℃、固液比 50g•L-1、还原剂量0.6g•L-1的条件下,浸出80min后,Co的浸出率约为98%。Li等[14]探究了乳酸对阴极材料中有价金属浸出效果的影响,在温度70℃、乳酸浓度 1.5 mol•L-1、固液比 20g•L-1、H2O2浓度为 0.5%的条件下,浸出20min后,Li、Ni、Co、Mn的浸出效率分别达到97.7%、98.2%、98.9%、98.4%。
对于单元锂电池,还原剂的存在对各种有机酸浸出目标金属的效果均无影响。但是对于多元锂电池,有机酸不能实现对目标金属的选择性浸出,会将非目标金属(Al、Fe、Mn)浸出,带来了分离纯化的难题,生产成本高,工业化应用困难。
1.4 3种浸出工艺的比较
表3是氨浸出、生物浸出、酸浸出3种工艺的对比。氨浸出对设备的要求高,生物浸出的菌种不易培养且周期较长,因此这2种工艺仍处于研究阶段,尚未应用于大规模工业化生产。酸浸出因浸出率高、酸易获得等优势,在市场中处于绝对的地位。现阶段,废锂电池正极材料回收利用的相关工艺,以湿法浸出为研究重点,“酸+还原剂”为典型的浸出模型[18]。

表3 3种浸出工艺的比较
2 酸浸出最佳条件的探索
2.1 酸浸出的研究成果
乔 秀 丽 等[19]将 HCl、H2SO4、HNO3分 别 与30%H2O2混合作浸取液,通过正交实验,探究出HCl+30% H2O2为最适宜的浸取液,且最佳工艺条件为:HCl浓度 4.0mol•L-1,30% H2O2与 HCl的体积比为1∶5,反应时间61min,反应温度73℃,固液比为1∶30.3。在此条件下,Co2+浸出率达到99.8%。郭雅峰等[20]以H2SO4+H2O2体系作浸出液,采用正交实验,从废锂电池正极材料中分离出黑色混合粉末,以此为原料探究浸出钴的最佳条件,得到钴的浸出率约为99.6%。此外,pant等[21]探究用富含柠檬酸、抗坏血酸和苹果酸的柑橘类果汁浸出废锂电池中的有价金属Co。结果表明,Co的浸出率达到94%以上。Joulié等[22]研究了HCl、HNO3和H2SO4等常用无机酸浸出废锂电池中有价金属的效果,结果表明HCl溶液的浸出效果明显,几乎所有的Li、Ni、Co和Al金属被浸出。李荣念等[23]采用柠檬酸+过氧化氢体系,研究了浸出过程中的各种因素对有价金属Co浸出率的影响。结果表明,在柠檬酸浓度为1.25mol•L-1、H2O2分数为6%、反应温度50℃的条件下,反应50min,钴浸出率为91.37%。
但这些工艺都有着共同的缺点:工业应用效果欠佳,难以大规模推广,不具备经济可行性。所以探寻一种更为经济可行的钴回收酸浸法,成为后续研究的方向。
2.2 最佳酸浸条件的探索
2.2.1 无机酸最佳浸出条件
常用的盐酸、硝酸、硫酸等无机酸可较好地浸出废锂电池中的有价金属,但硝酸与盐酸具有较大的挥发性,应用于酸浸出时会产生有害气体,实际生产中常采用硫酸作为主要的酸浸出试剂。在酸浸锂离子的电极材料钴的过程中,有诸多因素会对浸出效率造成影响。
张阳与郭雅峰等均采用“硫酸+过氧化氢”混合体系,深入探究了酸浸出工艺的最佳条件。研究发现,在其他条件相同时,加入双氧水可大幅度提高钴的浸出率。在张阳的研究中,最佳反应条件为:温度85℃,硫酸浓度4 mol•L-1,双氧水浓度2.0 mL•g-1,液固比 10∶1,浸出 120 min后,钴的浸出率达93.2%。在郭雅峰的研究中,最佳反应条件为:硫酸浓度 3mol•L-1,双氧水浓度 2.4mol•L-1,黑色粉末密度60g•L-1。反应30min,此时Co浸出率达99.6%。“硫酸+双氧水”体系中常采用连续高液固比来浸出正极材料,但此法耗费大量的酸,生产成本及环保费用较高。为优化酸浸出工艺,张阳等[24]探索了在低耗酸碱的前提下浸出钴的方法,即先用低液固比浸出,再用高液固比二次浸出,此法可高效率地浸出Co,减少酸中和的用碱量,实际工业生产中可减少设备投资、能耗及劳动力消耗等。高桂兰[25]以少量硫酸+维生素C为浸出体系,通过正交实验,在硫酸浓度3mol•L-1、维生素C浓度0.28mo1•L-1、浸出温度70℃、固液比15g•L-1条件下,浸出75min后,钴的浸出率可达到95.46%。除采用过氧化氢作为浸出阶段的还原剂外,也有研究采用更为稳定的硫代硫酸钠[26-27]和亚硫酸氢钠[28-33]等作为还原剂,还有研究者以生物质的还原剂如燕麦秸秆[34-35]和葡萄糖[36-37]等,来替代双氧水用于锂电池正极材料的浸出。
2.2.2 有机酸最佳酸浸条件
有机酸因不产生废气污染的特点,受到了业界的青睐,目前可作为酸浸出试剂的有机酸有柠檬酸、苹果酸等。在众多有机酸中,柠檬酸能在水溶液中离解,有利于废旧锂电池中有价金属的浸取。在废锂电池的酸浸过程中,学者对柠檬酸+还原剂体系的研究较多。
邱江华等[39]以柠檬酸+葡萄糖为浸出体系,在100℃、柠檬酸浓度1.5mol•L-1、葡萄糖与正极片质量比1∶1、固液比20g•L-1条件下,浸出3h后,钴的浸出率达到98.0%。Li Li等[40]以柠檬酸+双氧水为浸出体系,研究发现,在此体系下Co的最佳浸出条件为:90℃、30min、固液比 20g•L-1,柠檬酸浓度为 1.25mol•L-1、H2O2体积分数为 1%,此时有90%以上的金属钴被浸出。李荣念等采用柠檬酸+双氧水体系,在适宜条件下,Co浸出率可达92.97%。郑莹等[41]以柠檬酸+抗坏血酸为浸出体系,研究发现,在此体系下Co的最佳浸出条件为:抗坏血酸与钴酸锂的摩尔比为1∶1,柠檬酸与钴酸锂的摩尔比为1∶3.5,固液比15g•L-1,反应温度80℃,反应5h,此时Co的浸出效率达91%。除此之外,还有学者研究了其他有机酸+还原剂体系。Zhang等[42]基于“废物+废物 资源”的理念,采用DL-苹果酸+葡萄籽体系为浸出体系,此法是废锂电池中有价金属回收的一种新型绿色工艺。周涛等[43]以苹果酸+双氧水为浸出体系,研究了废旧锂电池中有价金属的浸出。
3 结论与展望
本文对废旧锂离子电池中有价元素钴的回收现状及工艺进行了综述,得到的结论与建议如下:
1)酸浸法更具应用推广价值;2)无机酸浸提法的研究较广泛,进展也较好,但环境不友好,会带来二次污染;3)有机酸浸提法虽然环境友好,但研究较少且不完善;4)从浸提推广的价值及环境角度看,有机酸浸提的发展前景更乐观。
