牛角膜浑浊和渗透性试验方法结合组织病理学对化妆品眼刺激性的预测价值
2021-03-28陈舒怀何立成朱社敏匡荣
谢 珍 陈舒怀 刘 璐 何立成 朱社敏 匡荣
浙江省食品药品检验研究院,浙江杭州 310052
日常生活中,人们的眼睛偶尔会暴露于化妆品,如沐浴露及染发类产品等。因此,化妆品引起的潜在眼刺激性的评估对于确保产品安全是至关重要的[1-2]。近年来,许多发达国家已经立法,以禁止动物试验并推广替代技术。全球目前有近40 个国家/地区已经正式实施了化妆品动物试验禁令,还有数十个国家正在立法的过程中,这些法规的变化对全球化妆品的产品研发、安全风险评估、立法监督和国际贸易均产生深远的影响[3-5]。而国内的化妆品安全性评价法规还是依据动物实验为主,依据2015 版《化妆品安全技术规范》[6]中“急性眼刺激性/腐蚀性”项下规定,结合本实验室多年的化妆品检测经验,沐浴露、染发类化妆品的眼刺激反应等级多为无刺激性、微刺激性至轻刺激性,加之传统的Draize 试验存在较多缺陷[7],有必要寻找合适的体外测试方法。
牛角膜浑浊和渗透性(bovine corneal opacity and permeability,BCOP)试验是经济合作与发展组织(OECD)认可的眼刺激试验的替代方法之一,可对无刺激性(不分类)和严重刺激性(1 类)的物质进行准确分类[8],但对弱到中等刺激程度(2B 和2A 类)的样品不能完全准确判断[9]。到目前为止,没有单一的体外替代方法能够完全代替Draize 试验[10]。角膜的组织病理学评估可作为BCOP 测试的附加参数,提供病变类型和损伤深度这些重要的补充信息[11]。尽管OECD TG 437[12]中尚未将角膜的组织病理学评估纳入其中,但OECD 已发布了相关指导文件以促进这一评估的应用[13]。已有学者[14]将其与牛角膜的组织学观察相结合建立预测模型,包括上皮、基质和内皮3 层结构,来对化学品的眼刺激性进行评估。本研究将BCOP 测得的结果与每种受试物对应的角膜上皮的相应组织病理学检查结果进行比较,包括市售的沐浴露及染发剂,将角膜上皮的病变损伤分级与体外刺激评分值(IVIS)及Draize试验的体内数据相结合,建立化妆品眼刺激性的预测模型,为化妆品的安全评估提供实验依据。
1 材料与方法
1.1 材料
1.1.1 牛眼球 牛眼球来源于浙江省富阳市九鲜肉牛定点屠宰场。试验前日晚由屠宰场受训人员于牛死亡后立即摘除眼球放入HBSS 溶液中,置运输冷藏箱中运至实验室。
1.1.2 实验动物 普通级新西兰家兔,购于浙江省桐乡市银海牧业专业合作社,生产许可证号:SCXK(浙)2018-0002,动物质量合格证号:No.1907170115,体重:1.9~2.6 kg,雌雄皆用。动物饲养于浙江省食品药品检验研究院实验动物中心,实验动物房使用许可证号:SYXK(浙)2016-0009。动物饲料由江苏协同医药生物工程有限公司提供,生产许可证号:苏饲证(2019)01008。饲养环境:温度20~25℃,相对湿度40%~70%。实验动物试验前在动物房适应环境至少3 d。动物实验方法经浙江省食品药品检验研究院动物福利和伦理委员会审核批准。
1.1.3 试剂与仪器 MEM 培养液(2053121)、MEM 培养液(含酚红,2048092)、HBSS 缓冲液(1897082)购于美国gibco 公司;荧光素钠(20170426)、无水乙醇(20190618)购于国药集团化学试剂有限公司。
CTHI-150B 型恒温恒湿箱[施都凯仪器设备(上海)有限公司];OPACITOMETER 混浊度仪(德国DURATEC Analysentechnik GmbH);MAX190 型紫外可见连续光谱酶标仪(美国Molecular Devices Corporation)。ST5010 自动载玻片染色机、EG1150 包埋机、HI1220 烘片机、RM2235 切片机、DM4000BLED 显微镜(德国徕卡公司)。
1.2 方法
1.2.1 Draize 试验法 参照2015 版《化妆品安全技术规范》[6]“急性眼刺激性/腐蚀性”项下所示方法。每个样品取没有眼病的健康家兔3 只,染发剂类(#1、#2、#3、#4、#5)样品按说明书进行配制,沐浴露类(#1、#2、#3、#4)样品使用原液,将0.1 mL 的样品加入一侧结膜囊中,眼闭合1 s,至第4 秒(染发剂类)/第30 秒(沐浴露类)时用足量、流速较快但又不会引起动物眼损伤的水流冲洗30 s,另侧眼睛不处理作自身对照,按要求对动物眼睛进行检查并判定受试物对眼的刺激强度。
1.2.2 BCOP 试验法 试验方法按照OECD TG 437[12],将分离的角膜安装在角膜固定器中,平衡后测量初始浊度值,每个样品平行3 个角膜,阴性对照为纯化水,阳性对照为无水乙醇。分组后将角膜暴露于受试物中,染发类产品依据样品说明书现配现用,其余受试物使用原液。孵育结束后读取终末浊度值。加入荧光素钠溶液孵育后在490 nm 波长处读取后室液体的吸光度值并计算IVIS。IVIS≤3,无刺激性(GSH 不分类);3<IVIS≤55,轻微到中等刺激(GSH 为2A 或2B 类);IVIS>55,严重刺激(GSH 为1 类)。
1.2.3 组织制片及分析方法 测试结束后取下角膜,置于10%的中性福尔马林溶液中固定,取材部位为角膜中间区域,常规乙醇脱水、二甲苯透明、石蜡包埋,角膜横切面进行切片,厚度4 μm,使用苏木精-伊红(HE)染色法染色,用光学显微镜观察角膜上皮细胞,基质和内皮细胞的组织病理学变化并拍照。角膜上皮的病变分级评分(H)标准如下:0 表示不值得注意;1 表示轻微;2 表示轻度;3 表示中度;4 表示严重。刺激分级根据角膜的病变部位:鳞状细胞(轻微),鳞状细胞至上翼状细胞(轻度),鳞状细胞至翼状细胞下层(中度),基底细胞(严重)。
2 结果
2.1 受试物眼刺激性试验结果
依据现标准,眼刺激性检验结果均合格,BCOP结合H 分类结果与Draize 试验结果一致。见表1。
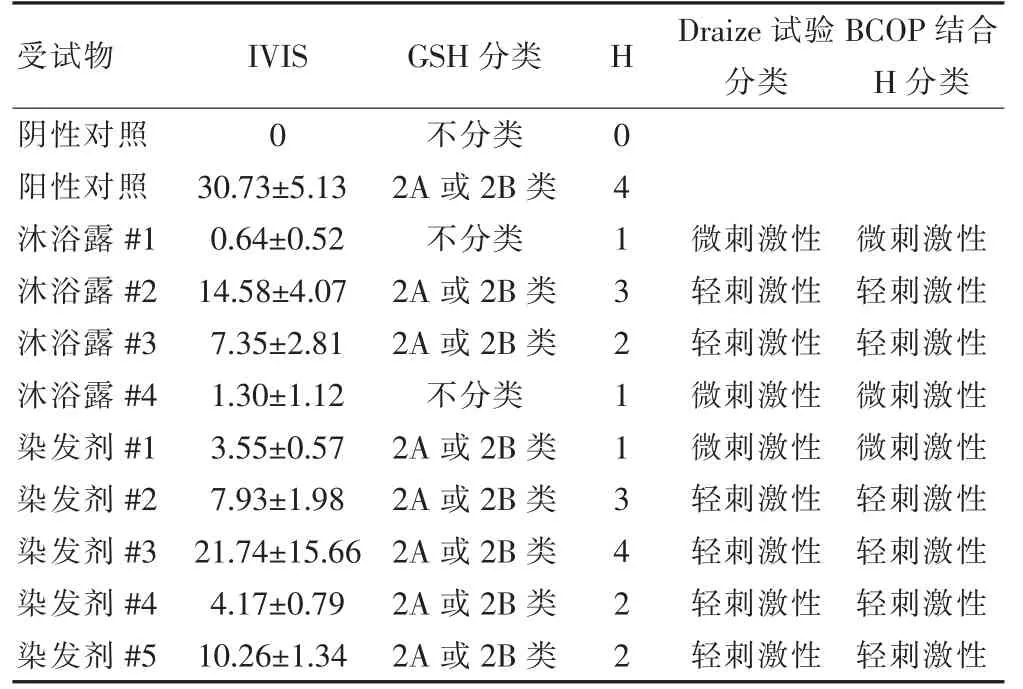
表1 受试物眼刺激性结果(n=3)
2.2 角膜组织病理学变化
暴露于不同受试物的角膜的具体组织学变化情况见图1。(1)阴性对照:角膜3 层结构完整,最外层细胞由于生命周期的原因可见轻微脱落,H 值为0,见图1A。(2)阳性对照:上皮表层鳞状细胞凝固,翼状细胞和基底细胞显示出明显的细胞质和细胞核空泡化,在基质的上半部分观察到松散的胶原束和角膜细胞的肿胀,内皮完整,H 为4 分,见图1B。(3)组织病理学评分较低(轻微),病变仅限于鳞状细胞层,H 值为1:①沐浴露#1:最外层的鳞状细胞可见轻微肿胀和脱落。其余未见明显病理变化。内皮完整,见图1C。②沐浴露#4:鳞状细胞表现出连续的水肿及肿胀,可观察到细胞核融合及肿胀。内部鳞状细胞层未显示出明显的病理变化,维持了角膜上皮的分层结构。角膜基质无变化。内皮完整,见图1D。③染发剂#1:最外层的鳞状细胞可见轻微脱落。其余未见明显病理变化。内皮完整,见图1E。(4)组织病理学评分仍较低(轻度),且病变局限于鳞状细胞和上翼状细胞层,H值为2:①沐浴露#3:鳞状细胞层部分缺失,细胞质的空泡化延伸至翼状细胞层表层细胞。角膜基质无变化。内皮完整,见图1F。②染发剂#4:鳞状细胞呈圆形或椭圆形。在上翼状细胞层中可观察到细胞质的空泡化。与病变部位直接接触的翼状细胞表现出核凝结。其余未观察到明显变化。内皮完整,见图1G。③染发剂#5:鳞状细胞层完全缺失,在上翼状细胞层中可观察到细胞肿胀。其余未观察到明显变化。内皮完整,见图1H。(5)组织病理学评分为中度,病变位于鳞状细胞层至上、下翼状细胞层,或严重至延伸到基底细胞,H 值为3 或4:①染发剂#2:整个鳞状细胞层及表层翼状细胞缺失,其余翼状细胞可见显著的细胞质空泡化。基底细胞保持完整。角膜基质无变化。内皮完整,见图1I。②沐浴露#2:鳞状和上翼状细胞层缺失,深层翼状细胞层和基底细胞仍存在,在向基底细胞过渡区域的翼状细胞周围存在小空泡。角膜基质无变化。内皮完整,见图1J。③染发剂#3:整个鳞状细胞层缺失及剩余细胞之间的粘附丧失,连接断裂。上翼状细胞层肿胀明显,呈圆形或椭圆形,深层翼状细胞层和基底细胞仍存在,均显示出更广泛的细胞质空泡化和肿胀(细胞之间空隙清晰)。角膜基质无变化。内皮完整,见图1K。
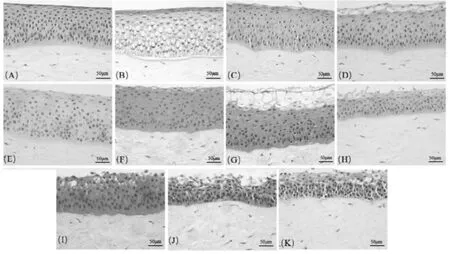
图1 角膜组织病理学变化(HE 染色)
2.3 BCOP 结合角膜上皮组织学变化预测化妆品眼刺激性的分级标准
依据表1 和图1,建立IVIS 结合角膜上皮病变评分的眼刺激性等级的预测模型,见表2。如果IVIS≤3,且H=0,则判定为无刺激性;如果IVIS≤6,且H≤1,则判定为微刺激性;如果6<IVIS<25,且角膜基质及内皮无异常,则判定为轻刺激性。

表2 BCOP 结合角膜上皮组织学变化预测化妆品眼刺激性的分级标准
3 讨论
BCOP 测试由浑浊度和荧光素钠通透性这两个主要终点组成,来间接量化由测试物质引起的对角膜的损伤。浑浊度受角膜上皮蛋白质的沉淀或变性的影响。角膜上皮由从前到后由3 层组成:鳞状细胞层、翼状细胞层和基底细胞层,上皮细胞起源于基底细胞并分化成为翼细胞,然后分化成鳞状细胞。角膜上皮在成人中大约每7 天会更新换代1 次。眼部创伤后上皮细胞有丝分裂活跃[15-17]。此外,上皮细胞具有细胞间连接,例如紧密连接和黏附连接,其中紧密连接是角膜最顶端的结构,可消除细胞间隙以提供渗透性屏障。细胞间连接的破坏,如上皮层细胞变性、坏死或缺失,会增加上皮的通透性,进而显著影响物质的眼刺激性潜力[18]。同时,物质对角膜上皮的细胞毒性是其作用的重要方式[19],加之BCOP 方法对弱到中等刺激程度的样品不能准确判断。作为BCOP 测定的补充参数,病理组织学分析可确定角膜病变的深度及程度[20]。因此,角膜上皮的组织病理学评估可为眼刺激性分类提供更可靠的依据。
文中展示了9 种市售沐浴露和染发剂在BCOP测定中所观察到的组织病理学特征,结果显示组织,病理学结果与测试物质的IVIS 相当。IVIS 越大,物质损伤角膜的深度越深,组织学评分的分值越大[21],提示角膜上皮的组织病理学特征为化妆品体外眼刺激性分类为无刺激性至轻刺激性提供更好的佐证。依据受试物的IVIS、角膜上皮组织学特征及Draize 试验结果,本文建立了IVIS 结合角膜上皮组织学的预测模型来评估化妆品的眼刺激性,本研究将微刺激性和轻刺激性的IVIS 临界值定为6,这与已有的文献报道[22]一致,认为IVIS≤6 的物质引起的组织病理学变化仅限于鳞状细胞层,且可迅速恢复。此外,即如果IVIS≤3,且H=0,则判定为无刺激性;如果IVIS≤6,且H=1,则判定为微刺激性;如果6<IVIS<25,且角膜基质及内皮无异常,则判定为轻刺激性。结合实验室多年的化妆品检测经验,沐浴露、染发类化妆品的眼刺激反应等级多为无刺激性、微刺激性至轻刺激性,极少为中刺激性,未见腐蚀性[23],依据文中9 种受试物的有限数据,该预测模型目前未把中刺激性和腐蚀性纳入其中,虽尚未覆盖全部刺激谱,但可将微刺激性和轻刺激性进行区分,满足日常化妆品眼刺激性的评估工作。总之,结合角膜上皮组织病理学评分的BCOP 法可作为微刺激性或轻刺激性分类的依据,适用于化妆品眼刺激性的检测。
