红参中总皂苷及人参皂苷Rg1、Re、Rb1含量的测定
2021-03-26刘春霖谢强胜李启艳高天阳刘慧香蒋慧
刘春霖,谢强胜,李启艳,高天阳,刘慧香,蒋慧
(山东省食品药品检验研究院,山东省食品药品安全检测工程技术研究中心,山东 济南 250101)
红参为五加科植物人参(PanaxginsengC.A.Mey. )的栽培品经蒸制后的干燥根和根茎。具有大补元气,复脉固脱,益气摄血的功能[1]。现代科学研究表明,红参可以提高人体免疫力、抗疲劳、抗衰老、抑制肿瘤、调节神经、心血管及人体内分泌系统等功效[2-7]。红参中含有的成分很多,人参皂苷类成分是其主要药理活性成分。红参是将鲜参或生晒参经高温蒸制干燥而得,鲜参中的皂苷类成分会发生糖苷键和酯键的断裂,生成某些特有皂苷[8],主要体现在较大极性人参皂苷的脱糖基转化以及人参皂苷C-17位侧链的变化[9-11]。红参中特有的皂苷组分所含糖链更少,极性更低,更有利于人体肠道吸收。因此,人参皂苷是衡量红参质量优劣的重要指标。
人参皂苷的主要分析方法有高效液相色谱法(HPLC)、比色法(UV)、薄层色谱法(TLC)、气相色谱-质谱联用法(GC-MS)、液相色谱-质谱联用法(LC-MS)等[12]。其中高效液相色谱法和比色法为常用的人参皂苷测定方法,高效液相色谱法适合单体人参皂苷含量的测定,比色法适合人参总皂苷含量的测定[13]。因此,本文以皂苷类成分为测定指标,采用紫外可见分光光度法、高效液相色谱法,分别对红参中总皂苷及人参皂苷Rg1、Re、Rb1的含量进行测定。
1 仪器与试药
1.1 仪器 Mettler Toledo Ms十万分之一电子天平(德国梅特勒公司);TU-1901紫外分光光度计(北京普析通用公司);岛津LC-20A高效液相色谱仪(日本岛津公司);KQ-500DE数控超声波清洗器(昆山市超声仪器有限公司);恒温水浴锅(上海树立仪器仪表有限公司)。
1.2 试剂试药 甲醇、乙腈,色谱纯;磷酸、正丁醇、三氯甲烷、乙醇、高氯酸、冰乙酸,分析纯;水为超纯水;5%香草醛溶液:称取5 g香草醛,加冰乙酸溶解并定容至100 mL。
对照品:人参皂苷Re(含量测定用,中国食品药品检定研究院,批号110754-201626,纯度97.4%);人参皂苷Rg1(含量测定用,中国食品药品检定研究院,批号:110703-201832,纯度92.4%);人参皂苷Rb1(含量测定用,中国食品药品检定研究院,批号:110704-201424,纯度93.7%)。
红参药材:吉林省20批,辽宁省4批,黑龙江省2批,均经山东中医药大学田景振教授鉴定为五加科植物人参(PanaxginsengC.A.Mey.)的栽培品经蒸制后的干燥根和根茎。
2 方法与结果
2.1 红参中总皂苷含量的测定方法 精密称取红参样品粉末适量(过四号筛,称样量根据总皂苷含量定),置100 mL容量瓶中,加少量水,超声15 min,再用水定容至100 mL,摇匀,放置,吸取上清液1.0 mL进行柱层析。取层析柱,内装3 cm D-101大孔吸附树脂,上加1 cm中性氧化铝。先用25 mL 70%乙醇洗柱,弃去洗脱液,再用25 mL水洗柱,弃去洗脱液,精确加入1.0 mL上述已处理好的样品溶液,用25 mL水洗柱,弃去洗脱液,再用25 mL 70%乙醇洗脱总皂苷,收集洗脱液于蒸发皿中,置于60 ℃水浴挥干,以此作显色用。在上述已挥干的蒸发皿中准确加入0.2 mL 5%香草醛冰乙酸溶液,转动蒸发皿,使残渣溶解,再加入0.8 mL高氯酸,混匀后移入10 mL带塞刻度离心管中,60 ℃水浴上加热10 min,取出,冰浴冷却后,准确加入冰乙酸5.0 mL,摇匀后,以1 cm比色皿于560 nm波长处与标准管一起进行比色。
2.1.1 对照品溶液制备及线性关系考察 精确称取人参皂苷Re对照品17.92 mg,用甲醇溶解并定容至10 mL,即每1 mL含人参皂苷Re 1.745 mg。吸取上述人参皂苷Re标准溶液25、50、75、100、125 μL置蒸发皿中,于60 ℃水浴挥干,加水适量溶解残渣,以下操作从“柱层析”起,与样品相同,测定吸光度值。以浓度(μg)为横坐标,吸光度值为纵坐标,绘制标准曲线,回归方程为:Y=0.00428X-0.01892,相关系数r=0.999 7。结果表明,人参皂苷Re在43.62~218.1 μg范围内线性关系良好。
2.1.2 精密度试验 取标准曲线第3点显色后的溶液,连续测定6次吸光度,计算平均吸光度为0.553,RSD为0.093%。结果表明,精密度良好。
2.1.3 加样回收率试验 精密称取6份样品(编号:1),每份约0.125 g,分别精密加入人参皂苷Re标准溶液(1.745 mg·mL-1)1.5 mL,按上述试验方法进行处理,测定吸光度,计算平均回收率为92.5%,RSD为2.6%。结果表明,回收率良好。
2.1.4 重复性试验 精密称取6份样品(编号:1),每份约0.25 g。按上述试验方法进行处理,测定吸光度,计算总皂苷平均含量为2.20%,RSD为2.0%。结果表明,重复性良好。
2.1.5 检出限 参照GB/T 5009.1-2003《食品卫生检验方法 理化部分 总则》中附录A.2.2规定,检出限为3倍空白值的标准偏差(测定次数n≥20)相对应的质量,吸光法按国际理论与应用化学家联合(IUPAC)规定。检出限按下式进行计算:检出限=Ks/b;b—标准曲线回归方程中的斜率;s—20次空白值的标准偏差;K—一般为3。计算检出限为2.4 μg。
2.1.6 样品测定 按上述试验方法,对26批不同产地的红参样品中总皂苷含量进行测定。结果显示,总皂苷含量为1.2%~3.0%,说明不同产地红参的总皂苷含量存在差异,这与文献报道结果基本一致。具体结果见表1。

表1 红参药材总皂苷测定结果
方法学验证试验表明,紫外可见分光光度法测定红参中总皂苷的方法精密度好,重现性高,方法专属性强。
2.2 红参中人参皂苷Rg1、Re、Rb1含量的测定 方法:取红参样品粉末(过四号筛)约l g,精密称定,置索氏提取器中,加三氯甲烷加热回流3 h,弃去三氯甲烷液,药渣挥干溶剂,连同滤纸筒移入100 mL锥形瓶中,精密加水饱和正丁醇50 mL,密塞,放置过夜,超声处理(功率250 W,频率50 kHz)30 min,滤过,弃去初滤液,精密量取续滤液25 mL,置蒸发皿中蒸干,残渣加甲醇溶解并转移至5 mL量瓶中,加甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
2.2.1 色谱条件 色谱柱:Thermo Hypersil C18柱(4.6 mm×250 mm,5 μm);检测波长:203 nm;柱温:40 ℃;流速:1.0 mL·min-1;进样体积:10 μL;乙腈为流动相A,水为流动相B,按下表进行梯度洗脱。
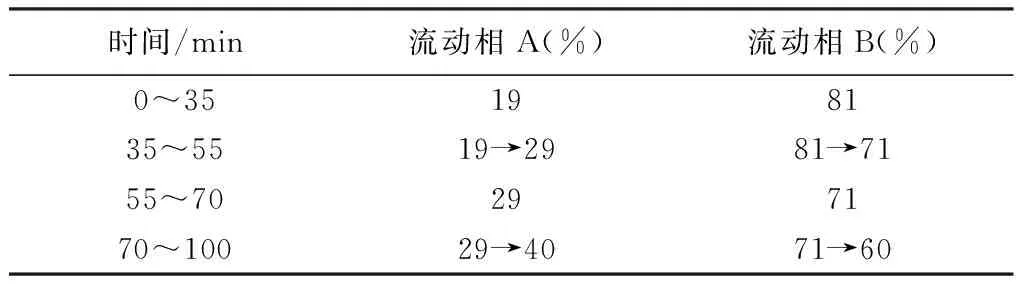
表2 梯度洗脱程序
2.2.2 对照品溶液制备及线性关系考察 取人参皂苷Rg1、Re、Rb1对照品适量,精密称定,加甲醇制成每1 mL含人参皂苷Rg1、Re、Rb1各1 000 μg的混合标准溶液。分别精密量取混合标准溶液0.1、0.4、1、2、5、10 mL加甲醇定容到10 mL,制备标准曲线,即得。按上述色谱条件,注入液相色谱仪,测得峰面积。以峰面积为纵坐标,对照品浓度(μg·mL-1)为横坐标,绘制标准曲线,回归方程分别是:人参皂苷Rg1为Y=3 945.08X+1 099.92,相关系数r=0.999 9;人参皂苷Re为Y=3 312.86X-1 659.22,相关系数r=0.999 9;人参皂苷Rb1为Y=2 753.65X+3 564.87,相关系数r=0.999 9。结果表明,人参皂苷Rg1在8.574 7~857.47 μg·mL-1,人参皂苷Re在10.393~1 039.3 μg·mL-1,人参皂苷Rb1在9.754 2~975.42 μg·mL-1范围内线性关系良好。
2.2.3 精密度试验 取每1 mL含人参皂苷Rg1、Re、Rb1各0.2 mg的混合标准溶液,按上述色谱条件重复进样6次,计算平均峰面积,分别是人参皂苷Rg1为645 177,RSD为0.53%;人参皂苷Re为652 791,RSD为0.61%;人参皂苷Rb1为516 661,RSD为0.60%。结果表明,精密度良好。
2.2.4 稳定性试验 取混合标准溶液,按上述色谱条件分别于0、2、4、8、12、24 h进样,计算平均峰面积,分别是人参皂苷Rg1为685 611,RSD为0.24%;人参皂苷Re为693 030,RSD为0.31%;人参皂苷Rb1为546 901,RSD为0.18%。结果表明,各组分在24 h内稳定。
2.2.5 加样回收率试验 精密称取同一编号红参样品9份,每份约0.5 g,低、中、高浓度水平各3份。分别精密加入人参皂苷Rg1、Re、Rb1对照品适量,按上述试验方法和色谱条件测定峰面积,计算平均回收率,分别是人参皂苷Rg1为101.3%,RSD为0.46%;人参皂苷Re为102.0%,RSD为1.3%;人参皂苷Rb1为98.9%,RSD为1.4%。结果表明,各组分回收率良好。
2.2.6 重复性试验 精密称取同一编号红参样品6份,每份约1 g。按上述试验方法和色谱条件测定峰面积,计算平均含量,分别是人参皂苷Rg1为0.314%,RSD为0.57%;人参皂苷Re为0.155%,RSD为0.48%;人参皂苷Rb1为0.501%,RSD为0.53%。结果表明,重复性良好。
2.2.7 样品测定 按上述试验方法,对26批不同产地的红参样品中人参皂苷Rg1、Re、Rb1的含量进行测定。结果显示,人参皂苷Rg1、Re总量在0.17%~0.61%,人参皂苷Rb1含量在0.21%~0.81%,说明不同产地红参的3种人参皂苷含量存在差异,这与文献报道结果基本一致。具体结果见表3。

表3 红参药材3种人参皂苷测定结果
方法学验证试验表明,高效液相色谱法测定红参中人参皂苷Rg1、Re、Rb1方法精密度好,重现性高,方法专属性强。
3 讨论
3.1 《中国药典》2015年版(一部)红参规定,本品按干燥品计算,含人参皂苷Rg1和人参皂苷Re的总和不得少于0.25%,人参皂苷Rb1不得少于0.20%。本文26批红参药材中有1批含量低于限值规定,合格率为96.2%。所测结果最大比值为3.9倍,显示含量差异较大,这可能与红参的产地、参龄、加工炮制等有关,需要进一步加以研究。
3.2 GB/T 22538-2018《红参分等质量》规定,本品按干燥品计算,人参总皂苷≥2.00%。本文26批红参药材中有11批含量低于限值规定,合格率为57.7%。合格率较低的原因可能是不同产地的红参药材本身质量存在差异;另外总皂苷没有统一的国标检测方法,不同检测方法也可能导致结果的差异。GB/T 22538-2018《红参分等质量》非强制性国家标准,而《中国药典》2015年版(一部)红参未规定总皂苷指标。建议对红参中总皂苷指标加以控制,能更加全面客观地反应红参的内在质量。
3.3 本文26批红参药材中人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1含量之和与总皂苷含量的比值为0.32~0.57,平均比值为0.45,结果显示,这3种单体人参皂苷在红参皂苷类成分中只占一部分。红参中除了与鲜参、生晒参共有的皂苷成分(如人参皂苷Ro、Rc、Rd、Rf等)外,还含有一些特有皂苷成分(如人参皂苷Rh1、Rh2、Rg3、Rg5、Rg6等),需要进一步的研究。
