伊维菌素制备工艺研究
2021-03-25马志珺胡晓敏李晓露高月麒任风芝张雪霞
马志珺,胡晓敏,李晓露,高月麒, 任风芝*,张雪霞*
(1.华北制药集团新药研究开发有限责任公司 微生物药物国家工程研究中心 河北省工业微生物代谢 工程技术研究中心,河北 石家庄 050015;2.华北制药集团爱诺有限公司,河北 石家庄 052165)
伊维菌素为阿维菌素的衍生物,属半合成的广谱抗寄生虫药,对体内外寄生虫特别是线虫和节肢动物均有良好驱杀作用。伊维菌素因其高效、用量少、副作用小等优点,广泛用于牛、羊、马、猪的胃肠道线虫、肺线虫和寄生节肢动物,犬的肠道线虫、耳螨、疥螨、心丝 虫和微丝蚴,家禽胃肠线虫和体外寄生虫等的防治[1-4]。伊维菌素现被视为非常重要的动物健康药,在国内外市场上具有很强的竞争力。
目前,制药行业主要采用阿维菌素在威尔森催化剂作用下加氢的工艺制备伊维菌素,存在副产物双氢阿维菌素和少量四氢阿维菌素。伊维菌素提纯的主要目的是去除催化加氢的副产物,其结构与主产物H2B1a结构极其相近(图 1)。

图1 伊维菌素主产物与副产物的结构式Fig.1 Structural formulas of main product and by-product of Ivermectin
伊维菌素的纯化技术主要是采用冷却降温结晶的方法,降温过程采用人工控制冷却水的方式,该方法结晶次数多、产品纯度低。作者以阿维菌素为原料、甲苯为溶剂,通过催化加氢反应得到伊维菌素粗粉,再通过重结晶纯化得到伊维菌素精粉,并优化阿维菌素加氢反应条件及伊维菌素粗粉纯化工艺,拟开发一种简洁高效、质量稳定的伊维菌素制备工艺。
1 实验
1.1 试剂与仪器
阿维菌素原粉(纯度≥98.5%),华北制药集团爱诺有限公司;乙腈、甲醇,色谱纯,Merck公司;其它试剂均为分析纯;实验用水为纯化水,自制。
高效液相色谱仪(SPD-M20A型紫外检测器,LC-20AT泵,SIL-20A型自动进样器,CTO-10AS型柱温箱),日本Shimadzu公司;Optimax 1001型反应釜,梅特勒-托利多公司;DSB-10/20型低温冷却液循环泵,郑州长城科工贸有限公司;Loborata 4000型旋转蒸发器,Heidolph公司;T-1000型电子天平,常熟双杰测试仪器厂;DZF-6050型真空干燥箱,上海精宏实验设备有限公司;Mastersizer 2000型粒度分析仪,Malvern公司。
1.2 伊维菌素粗粉的制备
称取阿维菌素原粉150 g加入到反应釜中,再加入500 mL甲苯,在氮气搅拌下加入1.5 g催化剂三苯基膦氯化铑[RhCl(Ph3P)3],加热升温至70 ℃,打开氢气阀至反应釜压升至 0.5 MPa 进行加氢反应,每隔1 h取样,检测至反应终点后,停止反应;将反应液脱除催化剂后,降温至30 ℃过滤、干燥,即得伊维菌素粗粉。
1.3 伊维菌素粗粉的纯化
晶种制备[5-6]:称取伊维菌素精粉10 g,加入50 mL乙醇溶解,加热至65 ℃,再流加到超声波作用下的纯化水中,保持超声状态,使其爆发成核,形成晶体。结晶完毕,将结晶液过滤、干燥,得到伊维菌素结晶粉即晶种9.2 g。
粗粉重结晶:称取伊维菌素粗粉100 g,用450 mL乙醇在75 ℃下加热溶解并保温,向溶液中加入晶种2 g,养晶1 h,再缓慢降温至15 ℃,使结晶完全。结晶液过滤、洗涤、干燥,得到伊维菌素精粉90 g。
1.4 色谱条件
Unitary C18 色谱柱(4.6 mm×250 mm,5 μm),流动相为乙腈-甲醇-水(60∶23∶17,体积比),检测波长245 nm,流速1.5 mL·min-1,进样量10 μL。
2 结果与讨论
2.1 阿维菌素加氢反应条件优化
2.1.1 料液比的选择
称取阿维菌素原粉4份各100 g,分别加入反应釜中,再分别加入300 mL、400 mL、500 mL和600 mL甲苯,进行催化加氢反应,考察料液比(1∶3、1∶4、1∶5、1∶6,g∶mL,下同)对伊维菌素收率和质量的影响,结果见表1。
由表1可知,在催化剂用量一定的条件下,随着料液比的增大,即溶剂甲苯用量的减少,加氢反应速率加快,但四氢阿维菌素含量也逐渐增加。综合考虑成本与生产周期,加氢反应中料液比选择1∶(3~5)为宜。

表1 料液比的选择
2.1.2 催化剂用量的选择
称取阿维菌素原粉5份各100 g,分别加入反应釜中,再加入300 mL甲苯,在氮气搅拌下加入不同量(0.5 g、1.0 g、1.5 g、2.0 g、2.5 g)的催化剂RhCl(Ph3P)3进行催化加氢反应,考察催化剂用量对伊维菌素收率和质量的影响,结果见表2。

表2 催化剂用量的选择
由表2可知,在一定时间内,随着催化剂用量的增加,阿维菌素转化率逐渐升高,但副产物四氢阿维菌素含量也逐渐增加,选择性降低。综合考虑阿维菌素转化率、选择性、产品质量和成本,加氢反应中催化剂用量选择1.0~1.5 g即1.0%~1.5%为宜。
2.2 伊维菌素粗粉纯化工艺优化
2.2.1 晶种粒度的选择
称取伊维菌素粗粉4份各50 g,分别使用不同平均粒度D[4,3]的晶种进行伊维菌素粗品重结晶实验,结果见表3。

表3 晶种粒度的选择
由表3可知,晶种平均粒度较小时,结晶速度快,杂质去除效果差。综合考虑结晶收率和产品质量,选择晶种的平均粒度D[4,3]为40~60 μm。
2.2.2 结晶降温控制的优化
过饱和度是物质结晶的动力,过饱和度越大,生长速率越快,结晶选择性越低。在控温结晶过程中,要兼顾晶体成长速率,如果降温速度过快,晶体成长不能及时消耗其过饱和度,就会自发生成晶核,从而使控温结晶失败。采用自动降温控制系统,实现了伊维菌素结晶过程的梯度降温控制(图2),伊维菌素的晶体形态见图3。
由图3可知,通过梯度降温控制获得了晶型均一、稳定的晶体,有效改善了晶体外观和产品质量,利于包装和贮存。
2.3 工艺验证
在最优制备工艺条件下进行3批次伊维菌素验证生产,结果见表 4、表5。

图2 伊维菌素梯度降温控制曲线Fig.2 Gradient cooling control curve of Ivermectin
由表4可知,3批次伊维菌素验证生产所得伊维菌素精粉纯度均大于99%,收率均达到90%以上。
由表5可知,通过工艺条件优化,伊维菌素精粉质量符合USP标准,大大提高了伊维菌素的市场竞争力。

图3 伊维菌素的晶体形态(×400)Fig.3 Crystal morphology of Ivermectin(×400)
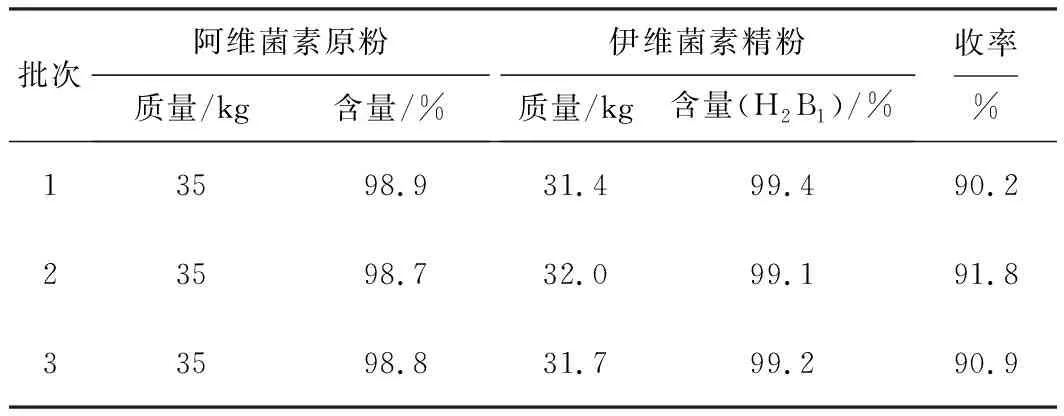
表4 伊维菌素精粉纯度及收率

表5 伊维菌素精粉质量/%
3 结论
以阿维菌素为原料、甲苯为溶剂,通过催化加氢反应得到伊维菌素粗粉,再通过重结晶纯化得到伊维菌素精粉,并优化了阿维菌素加氢反应条件及伊维菌素粗粉纯化工艺。确定阿维菌素加氢反应条件为:料液比1∶(3~5) (g∶mL)、催化剂用量1.0%~1.5%;再通过控制晶种粒度和梯度降温过程,有效改善了晶体外观和产品质量,所得伊维菌素精粉纯度大于99%,质量符合USP标准。该工艺简洁高效、质量可控,适用于伊维菌素的工业化生产。
