脑梗死后并发血管性痴呆的危险因素及血清VEGF、MMP-9 的早期预测价值
2021-03-25李光宗郑洪佳张月辉
李光宗,李 靖,朱 晨,郑洪佳,康 婕,张月辉
血管性痴呆是指缺血性或出血性脑卒中引发的记忆、认知以及行为等脑组织缺血、缺氧损伤所致的认知障碍综合征[1],临床表现以肢体、语言功能障碍为主,部分病人可伴神经心理或精神行为异常等。血管性痴呆是痴呆的第二诱因,仅次于阿尔茨海默病[2]。血管性痴呆具有发病突然,疾病呈阶梯性进展,并且病程漫长、易反复发作,多数病人与脑梗死并发。早期预测对于血管性痴呆防治具有重要意义,已有研究结果显示,血管内皮生长因子(vascular endothelial growth factor,VEGF)、基质金属蛋白酶-9(matrix metalloprotein-9,MMP-9)等血清指标在脑梗死后存在明显变化[3]。本研究分析脑梗死病人并发血管性痴呆的影响因素,并观察VEGF、MMP-9水平对血管性痴呆发生的预测价值。
1 资料与方法
1.1 一般资料 选取2016 年2 月—2018 年6 月在成都市第六人民医院接受治疗的脑梗死病人150 例为研究对象。纳入标准:年龄≥50 岁;根据临床表现和相关检查确诊为脑梗死;无其他系统严重疾病。排除标准:临床资料不全者;合并其他神经或精神系统疾病者。其中合并血管性痴呆30 例(20%),男17 例,女13 例,年龄54~78(64.25±3.98)岁;未合并血管性痴呆120例(80%),男80例,女40例,年 龄52~78(64.23±4.12)岁。本研究获得我院伦理委员会批准。
1.2 研究方法 抽取病人空腹状态下的外周静脉血4 mL,选用广州吉迪仪器有限公司生产的JIDI-6RH 落地式低速大容量冷冻离心机以4 000 r/min(8 cm 半径)离心10 min,取上清液采用ELISA 法检测VEGF、MMP-9,检测试剂盒由美国R&D 公司提供,操作参照说明书进行。分析脑梗死病人合并血管性痴呆的危险因素,分析VEGF、MMP-9 对脑梗死后并发血管性痴呆的预测价值。
1.3 统计学处理 应用SPSS 11.5 统计软件进行统计分析。计量资料以均数±标准差(±s)表示,采用t检验;计数资料采用χ2检验;使用Logistic 回归分析法分析脑梗死病人发生血管性痴呆的危险因素。以P<0.05 为差异有统计学意义。
2 结 果
2.1 脑梗死病人发生血管性痴呆的单因素分析 脑梗死合并血管性痴呆病人吸烟史、饮酒史、糖尿病史占比及VEGF、MMP-9 水平与未合并血管性痴呆病人比较差异均有统计学意义(P<0.05)。详见表1。
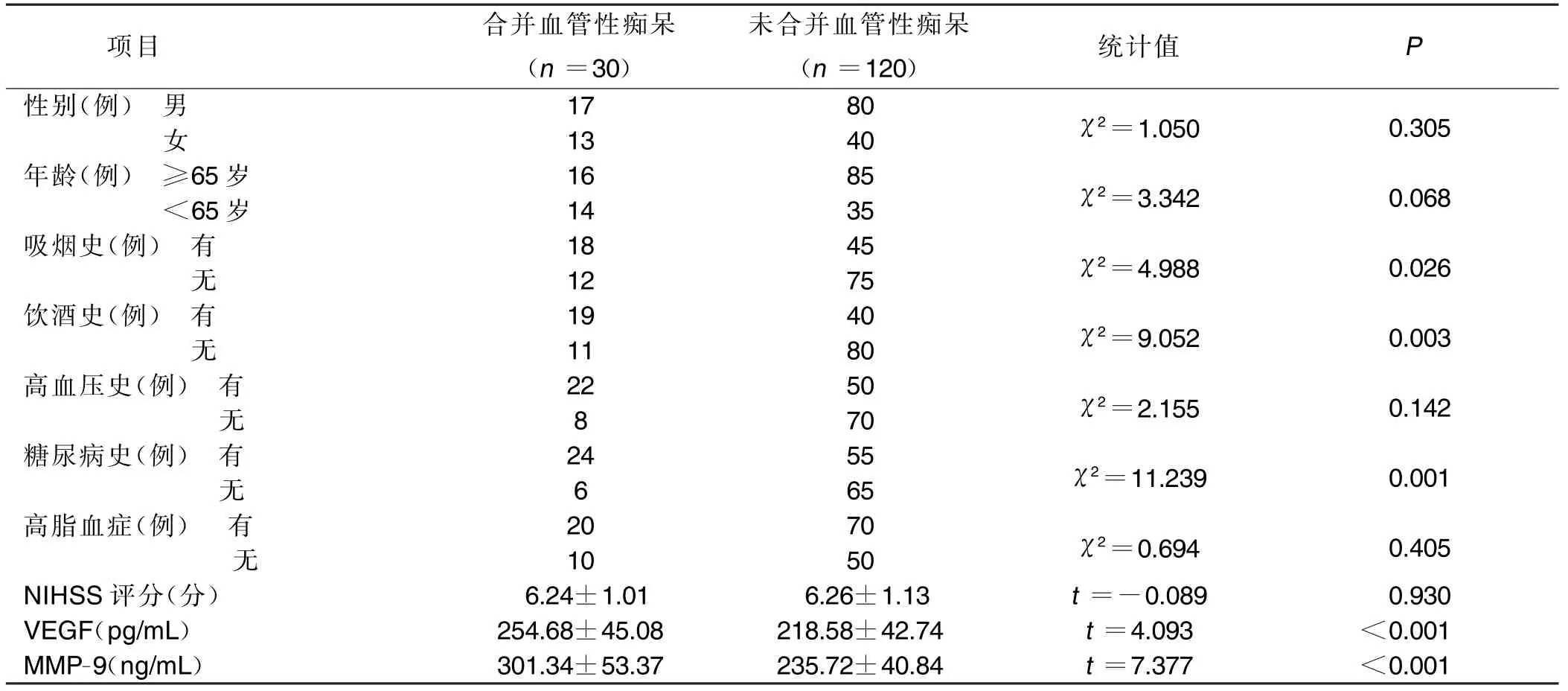
表1 脑梗死病人发生血管性痴呆的单因素分析
2.2 脑梗死病人发生血管性痴呆的多因素Logistic 回归分析 将单因素分析中有统计学意义的吸烟史、饮酒史、糖尿病史、VEGF、MMP-9 作为自变量,脑梗死病人发生血管性痴呆作为因变量,进行Logistic 回归分析。结果显示,糖尿病、VEGF、MMP-9 水平进入回归方程,提示糖尿病、VEGF、MMP-9 水平为脑梗死病人发生血管性痴呆的危险因素。详见表2。

表2 脑梗死病人发生血管性痴呆的多因素Logistic 回归分析
2.3 VEGF、MMP-9 对脑梗死合并血管性痴呆的预测价值分析 受试者工作特征曲线(ROC)分析显示,VEGF 以236.87 pg/mL 为截断值预测脑梗死后并发血管性痴呆的ROC 曲线下面积(AUC)=0.854,约登指数为0.709,灵敏度为0.867,特异度为0.842;MMP-9以259.64 ng/mL 为截断值预测脑梗死后并发血管性痴呆的AUC=0.786,约登指数为0.584,灵敏度为0.767,特异度为0.817。VEGF 预测的各效能参数均高于MMP-9。详见图1、图2。

图1 VEGF 对脑梗死合并血管性痴呆预测的ROC 曲线图

图2 MMP-9 对脑梗死后血管性痴呆预测的ROC 曲线
3 讨 论
血管性痴呆病机与动脉狭窄、闭塞诱导的脑组织低灌注介导的神经元细胞凋亡有关[4]。脑梗死后血管性痴呆起病急、发展快,通过临床表现诊断并不准确,应结合血清学指标及影像学资料早期诊断。
VEGF 是具有生物活性的一种功能性蛋白,具有促血管内皮细胞迁移、增殖,诱导细胞外基质变性以及促血管生成等作用[5]。VEGF 活性可被多种因素诱导,其中缺氧是VEGF 的首位诱导因素,脑梗死引发的脑组织缺氧可诱导神经元、神经胶质细胞合成大量的VEGF 及其受体[6]。本研究发现,脑梗死合并血管性痴呆病人VEGF 水平高于未合并血管性痴呆病人(P<0.05),提示血清VEGF 表达水平与脑梗死后血管性痴呆密切相关。有研究通过多因素研究发现,血清VEGF 浓度与脑梗死后血管性痴呆有关,并且VEGF是脑梗死后血管性痴呆的独立危险因素[7]。脑梗死急性期,VEGF 可通过减轻神经元细胞缺血缺氧损伤来形成神经保护效应,并且VEGF 介导的血管、神经生成有利于改善病人远期神经功能[8]。有研究发现,增强VEGF 浓度可提升血管新生能力,并增强缺血脑组织微小血管密度,降低脑组织梗死面积,保护脑神经功能[9]。本研究还发现,有吸烟史、糖尿病史的脑梗死病人血管性痴呆发生率较高,提示吸烟、糖尿病也可能是脑梗死后血管性痴呆的危险因素,但脑梗死合并血管性痴呆病人年龄、性别、饮酒史、高血压史与未合并血管性痴呆病人比较差异均无统计学意义(P>0.05)。
MMP-9 是基质金属蛋白酶家族成员之一,人体内的MMP-9 多以酶原形式存在。活化后的MMP-9 具有多种功能,可与明胶、Ⅳ型胶原及Ⅴ型胶原相互作用[10]。MMP-9 还可促使细胞外基质降解,并以此损伤细胞结构,导致细胞凋亡。大量研究表明,MMP-9 是脑梗死发生、发展的重要因子[11-12]。首先,MMP-9 可影响动脉粥样硬化斑块稳定性,促使斑块破碎并引发脑梗死。其次,MMP-9 可通过降解细胞外基质来增强微血管通透性,破坏血脑屏障,导致炎性因子入侵,引发血管源性脑水肿及神经损伤[13]。脑梗死后的MMP-9高表达还将引发出血性转化。本研究结果显示,脑梗死合并血管性痴呆病人MMP-9 水平明显高于未合并血管性痴呆病人(P<0.05),提示MMP-9 表达水平与脑梗死后血管性痴呆密切相关。有研究发现,慢性血管性痴呆造模大鼠海马区MMP-9 表达水平明显升高,并且其水平与大鼠神经认知功能密切相关[14]。还有研究通过单因素、多因素回归分析发现,血清MMP-9表达水平与脑梗死后血管性痴呆有关,MMP-9 高表达是脑梗死后血管性痴呆的重要危险因素[15]。本研究通过单因素回归分析发现,糖尿病、VEGF、MMP-9 是脑梗死后血管性痴呆的危险因素,这与前述研究结论相似。进一步绘制ROC 曲线分析预测价值的结果显示VEGF、MMP-9 预测脑梗死后并发血管性痴呆的AUC 均>0.7,且VEGF 预测的AUC、约登指数、灵敏度、特异度均高于MMP-9,提示VEGF、MMP-9 对脑梗死后并发血管性痴呆均具有较高的预测价值,且VEGF 的预测效能优于MMP-9。
本研究发现VEGF、MMP-9 表达水平与脑梗死后血管性痴呆密切相关,临床可通过检测VEGF、MMP-9表达来预测、诊断脑梗死病人是否并发血管性痴呆。
综上所述,糖尿病、高VEGF 水平和高MMP-9 水平是脑梗死后血管性痴呆的危险因素,且VEGF、MMP-9 水平对血管性痴呆有较好的预测价值。
