冠状病毒受体的研究进展
2021-03-11袁一心赵福杰张驰胡慧
袁一心,赵福杰,张驰,胡慧
(1. 河南农业大学牧医工程学院,河南 郑州 450046;2. 河南省动物性食品安全重点实验室,河南 郑州 450046)
冠状病毒是一类属于套式病毒目(Nidovirales),冠状病毒科(Coronaviridae),正冠状病毒亚科(Orthocoronavirinae),冠状病毒属(Coronavirus)的单股正链RNA病毒,能够感染人、蝙蝠、猪、犬、猫、禽类等脊椎动物。国际病毒学分类委员会根据基因型和血清学特性将冠状病毒分为4个属:α、β、γ和δ[1]。目前已知能够感染人的七种冠状病毒中:人冠状病毒(human coronavirus 229E,HCoV-229E)、人冠状病毒(human coronavirus NL63,HCoV-NL63)是属于α冠状病毒属的成员,人冠状病毒(human coronavirus OC43,HCoV-OC43)、人冠状病毒(human coronavirus,HCoV-HKU1)、严重急性呼吸综合征冠状病毒(severe acute respiratory syndrome coronavirus,SARS-CoV)、中东呼吸综合征冠状病毒(Middle East respiratory syndrome coronavirus,MERS-CoV)、以及近期新发于武汉的严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)是属于β冠状病毒属的成员[2]。SARS-CoV、MERS-CoV和SARS-CoV-2能够引起人类的严重的呼吸道疾病,对人类的健康产生极大的威胁。其中SARS-CoV-2的流行情况最为严重,截止至2020年4月8日,世界卫生组织统计显示SARS-CoV-2已传播至全球201个国家和地区,导致1 353 361人感染,造成79 235人死亡。除感染人外,研究发现多种冠状病毒能够引起牲畜呼吸道,胃肠道疾病,如牛冠状病毒(bovine coronavirus,BCoV)、猪传染性胃肠炎(transmissible gastroenteritis virus,TGEV)、猪呼吸道冠状病毒(porcine respiratory coronavirus,PRCoV)、猪流行性腹泻病毒(porcine epidemic diarrhea virus,PEDV)、猪丁型冠状病毒(porcine deltacoronavirus,PDCoV)和猪急性腹泻综合征冠状病毒(swine acute diarrhea syndrome coronavirus,SADS-CoV)等,对养殖业带来巨大的经济损失[3]。
病毒受体是宿主细胞膜上能够与病毒特异性地结合,并介导和促进病毒侵入或感染细胞的正常组成成分或其胞外基质,其化学本质大多是蛋白质,还有一些是糖蛋白、蛋白聚糖、脂类或糖脂,具有特异性、高亲和性、饱和性以及独特的生物学活性等[4]。病毒感染需要吸附宿主细胞,这个过程包括静电吸附和特异性受体吸附。静电吸附是可逆的非特异性结合,而特异性受体的吸附是不可逆的特异性结合,因此病毒与其受体特异性的结合对其感染细胞起着至关重要的作用。研究表明,冠状病毒入侵细胞首先依赖于病毒表面S蛋白与细胞表面受体的特异性结合(见图1),然后经过膜融合或者胞吞途径进入细胞内进行增殖,从而达到感染的目的[5],因此对冠状病毒受体的研究有助于深入了解病毒的感染及跨种传播的机制,对新型抗病毒药物和特异性疫苗的研发及对冠状病毒感染的防控有重要意义。目前已发现的冠状病毒的受体主要包括血管紧张素2(the angiotensin converting enzyme 2,ACE2)、氨 基 肽 酶N(aminopeptidase N,APN)、二肽酰肽酶4(dipeptyl peptidase 4,DPP4)、唾液酸(sialic acid, SA)和癌胚抗原相关细胞黏附分子1(carcinoembryonic antigen-related cell adhesion molecule 1, CEACAM1)等(见表1)。
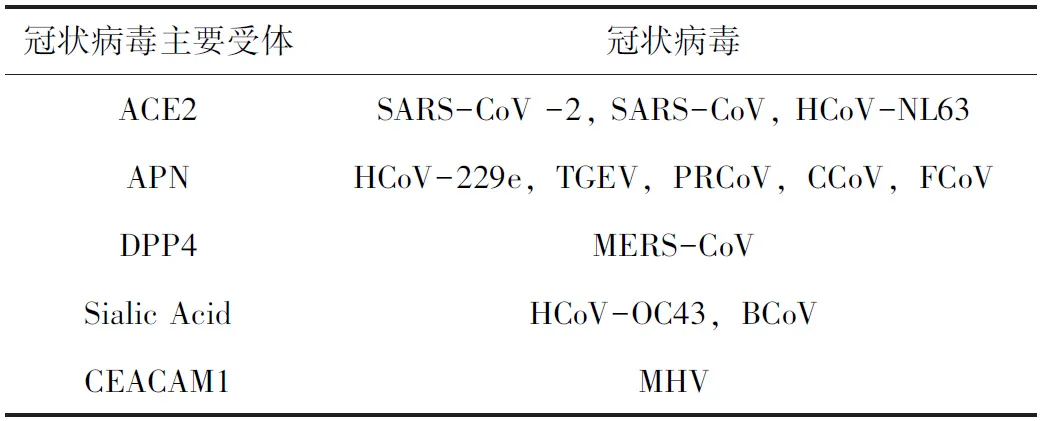
表1 冠状病毒主要受体与对应冠状病毒种类
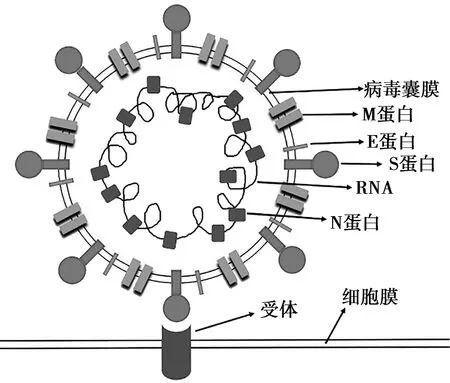
图1 冠状病毒S蛋白与受体结合示意图
1 ACE2
人ACE2是一种由位于x染色体上的基因编码的805个氨基酸残基组成的Ⅰ型跨膜糖蛋白,具有较大的N端胞外段,胞外部分可分为锌金属肽酶结构域(第19~611位氨基酸)和羧基端结构域(第612~740位氨基酸)。构成锌金属肽酶结构域的两个亚域之间的凹陷处可能作为病毒结合的位点[6]。早期研究发现ACE2具有羧肽酶活性,作为羧肽酶活性其作用底物主要是促血管生成素Ⅱ(angiopoietin Ⅱ,Ang Ⅱ)、缓激肽(des-arg-bradykinin)、神经降压素(neurotensin)和运动升压素(kinetensin),其生理功能主要表现为扩血管作用,与具有缩血管作用的ACE共同维持机体血压稳态。
冠状病毒的受体ACE2最早被发现是在2003年,研究发现SARS-CoV 的S1蛋白可与人ACE2特异性结合,而且可溶性的ACE2蛋白能够阻断SARS-CoV 的S1蛋白与其易感细胞Vero E6细胞的结合,转染并表达ACE2蛋白的293T细胞也可与表达SARS-CoV S蛋白的细胞形成多核合胞体。在表达ACE2的293T细胞中SARS-CoV能够有效地复制,抗ACE2的抗体则可阻止病毒的复制。使用可溶性酶促灭活的ACE2可以阻断SARS真病毒和假病毒的感染,提示ACE2酶的活性不影响病毒的入侵[7]。而通过研究SARS-CoV S蛋白不同片段与ACE2之间的亲和力,发现SARS-CoV的受体结合域(receptor binding domain,RBD)位于S1蛋白的C末端结构域1(C-terminal domain 1,CTD1)的第318-510位氨基酸,更短的片段则会丧失与ACE2的结合能力[8]。因此进一步证明ACE2是SARS-CoV的功能性受体。除此之外,2004年在荷兰发现的HCoV-NL63和2019年在武汉发现的SARS-CoV-2的受体也均是以ACE2作为其受体[9]。
对SARS-CoV S蛋白与ACE2复合物的晶体结构的研究发现受体结合域片段表面为微凹状,能够与ACE2的结合位置相适应,从而使其结合部位可紧密连接,便于SARS-CoV侵入细胞。其中第479位和第487位氨基酸在识别受体过程中起到了至关重要的作用,该位点的突变会改变SARS-CoV对不同物种ACE2的亲和力发生变化,从而导致病毒跨种传播的发生[10]。其CTD1的构象变化也同样会影响S蛋白与ACE2之间的结合,Gui等[11]发现CTD1紧靠在S2亚基的顶部时,其不具有结合受体的活性,当CTD1向上运动远离S2亚基时则会使S蛋白从受体结合的非活性状态变为活性状态。而SARS-CoV-2与SARS-CoV的S蛋白上受体结合域的结构十分相似,因此推测SARS-CoV-2的受体同样为ACE2,对它们的结构比较分析发现SARS-CoV识别ACE2的两个关键性位点第479位和第487位氨基酸分别对应SARS-CoV-2中的第394位和第501位氨基酸,从而使SARS-CoV-2能够有效的与人ACE2结合[12]。但HCoV-NL63的受体结合域结构与SARS-CoV相比则有较大的差异,因此HCoV-NL63与SARS-CoV在受体识别过程中有着明显的不同。HCoV-NL63的RBD的顶端形成的的空腔结构与人ACE2的结构形成互补,使其能够紧密连接。其中RBD上的11个氨基酸与人ACE2的16个氨基酸的直接相互作用介导它们之间的连接,但是其与ACE2的亲和力不如SARS-CoV的S蛋白,因此有研究认为HCoV-NL63的致病性弱与此有关[13]。
2 氨肽酶N类
氨基肽酶N是一类锌离子依赖性的膜结合Ⅱ型金属糖蛋白,主要功能是水解寡肽、酰胺和氨基酰胺等结构中的酰胺键,除去其中的N-末端氨基酸[14]。APN作用的天然底物包括血管作用肽(赖氨酸-缓激肽、血管紧张素Ⅲ)、神经肽激素(亮氨酸和蛋氨酸脑磷脂、神经激肽A)、细胞因子和免疫调节剂(IL-8、吞噬刺激素、胸腺肽)等,因此它能参与很多重要过程的深度反应,比如细胞生长、免疫调节和血压调节。研究表明APN对IL-8的降解,淋巴细胞参与机制,白细胞生长功能,降低T细胞对MHC Ⅱ型抗原决定簇的识别能力等方面都有很大的影响[15]。
研究表明,冠状病毒中以APN作为受体的主要是α属冠状病毒,包括:HCoV-229e,TGEV,PRCoV,犬冠状病毒(Canine coronavirus,CCoV),猫冠状病毒(Feline coronavirus,FCoV)[16]。而最近研究发现δ冠状病毒属的猪丁型冠状病毒(Porcine deltacoronavirus,PDCoV)也以APN作为其受体[17]。与其他冠状病毒相似,这些病毒也均以S蛋白识别受体,而且其在识别受体的过程中具有种属特异性,但研究发现猫氨肽酶N(Feline Aminopeptidase N,fAPN)可作为多种α类冠状病毒的受体。为了明确其选择宿主的原因,Tusell等[18]对fAPN的进一步研究发现:fAPN中3个小的不连续区域,第288~290位,732~746位(R1区)和764~788位(R2区)氨基酸在不同冠状病毒感染中起到重要作用。其中第288至290位氨基酸参与HCoV-229E感染过程,R1区参与TGEV感染过程,而FCoV和CCoV同时需要R1区和R2区才能完成入侵。对其中关键性位点分析发现R1区中的第742位天冬酰胺与TGEV,CCoV和FCoV的受体活性密切相关,而740位天冬酰胺则仅与CCoV受体活性的有关。
为了解这些冠状病毒与APN的结合方式,不同研究团队通过结构生物学方法分析它们之间的相互作用。其中对HCoV-229e和hAPN之间作用机制的研究最为深入,对其复合结构的解析发现HCoV-229e(第293~435位氨基酸)的RBD为6链的β-折叠结构域,其中的3个loop结构与hAPN直接接触,loop1(第308~325位氨基酸)中的第317~320位,loop2(第352~359位氨基酸)中的第359位以及loop3(第404~408位氨基酸)中的第404,407位氨基酸在结合过程中起到了重要作用[19]。而经过研究证实TGEV、PRCoV、CCoV和FCoV的RBD区高度同源,因此认为它们与受体pAPN结合时可能具有相似的原理。对PRCoV的RBD区以及pAPN的复合结构进行解析发现其RBD具有β-桶折叠结构,而pAPN则由四个结构域构成。在受体结合的过程中PRCoV RBD的顶端与pAPN胞外段远膜端区域相互作用,RBD中的第528位及571位氨基酸所在侧链与pAPN的结构域Ⅱ和结构域Ⅳ在空间上形成互补,使其能够紧密连接[20]。
3 DPP4
二肽基肽酶4是一种发现于1966年的Ⅱ型跨膜糖蛋白,属于丝氨酸蛋白酶S9B家族,具有丝氨酸蛋白酶活性,在啮齿类动物和人类体内广泛存在。人CD26基因定位于2号染色体长臂24区,编码了包含766个氨基酸的多肽链,是一个分布广泛的整合膜蛋白及分泌型蛋白[21]。除酶功能外,CD26可与细胞外基质蛋白(如纤连蛋白和胶原蛋白)互相作用,参与细胞的黏附、迁移和侵袭等过程[22]。在免疫调节中,CD26通过联合丝氨酸蛋白酶、成纤维细胞活化蛋白(fibroblast activation protein,FAP)和趋化因子受体4(chemokine receptor 4,CXCR4)等,参与细胞信号转导,从而起到T细胞活化标志物的作用[21]。
由于SARS-CoV和MERS-CoV的临床表现相似,所以早期认为MERS-CoV的受体也是人ACE2,但后续研究发现MERS-CoV不能像SARS-CoV一样感染表达人ACE2的非易感细胞,人ACE2的中和抗体也不能阻止MERS-CoV的感染[23]。经过进一步的研究发现MERS-CoV的S蛋白能够与可溶的人CD26结合,并能抑制MERS-CoV对Vero细胞的感染。通过转染表达人CD26蛋白的非易感细胞COS-7也能够被MERS-CoV感染,因此证明MERS-CoV的受体是CD26[24]。
早在MERS-CoV被发现前,即有不同团队对CD26的结构进行解析,发现其晶体结构为二聚体形式,并且每个亚基均由α/β-水解酶结构域和具有八个叶片的β-螺旋桨结构域组成。其中人CD26水解酶结构域由C端序列(第506~766位氨基酸)和一小段N端序列(第39~51位氨基酸)组装而成,β-螺旋桨结构域则由N末端(第55~497位氨基酸)组成。与人CD26进行结合的MERS-CoV的受体结构域则鉴定为S1的C端第367~606位氨基酸,其结构与SARS-CoV的RBD区具有一定的相似性[25]。对MERS-CoV受体结合域及人CD26的复合物晶体结构进行解析发现,MERS-CoV受体结合域绑定到人CD26螺旋桨结构的侧面,其能够识别出叶片IV和叶片V以及叶片相连处的一个小凸起螺旋,与之进行特异性结合。进一步分析发现MERS-CoV受体结构域的第499,501,502,510,513,539位氨基酸与人CD26的第336,286,288,317,344,267位氨基酸之间的相互作用在结合过程至关重要[26]。
4 唾液酸类
唾液酸最早由Blix从颌下腺黏蛋白中分离发现,是一类含9个碳原子的羧基化单糖酰化物的统称,其系统命名为5-氨基-3,5-二脱氧-D-甘油-D-半乳壬酮糖,根据5位碳上连接基团的不同可以分为N-乙酰神经氨酸(Neu5Ac)、N-羟乙酰神经氨酸(Neu5Gc)、去氨基神经氨酸(KDN)和神经氨酸(Neu)四类,而根据唾液酸第二个碳原子(C2) 与其他糖类(半乳糖、N-乙酰半乳糖胺或N-乙酰葡糖胺)的不同碳原子(C3、C6 或 C8)相连,又分为α2,3、α2,6或α2,8连接的唾液酸,其中是以α2,3或α2,6糖苷键的形式连接到半乳糖上,仅以α2,6糖苷键的形式连接到N-乙酰半乳糖胺,仅以α2,8糖苷键的形式连接到其他唾液酸上[27]。唾液酸主要作为细胞表面多糖的外端残基存在于脊椎动物体内,发挥着重要的生物学作用。研究发现,唾液酸对肿瘤的凋亡、肿瘤的转移、免疫反应的调节等方面[28]均有影响。
唾液酸是多种病毒的受体,在冠状病毒中HCoV-OC43,BCoV都被鉴定出使用9-O-乙酰基唾液酸作为受体,研究发现使用9-O-乙酰基唾液酸作为受体的流感病毒预处理禽红细胞后,能够抑制hCoV-OC43和BCoV对红细胞进行凝集,使用神经氨酸酶对红细胞进行处理后也能够减弱红细胞的凝集现象,在病毒感染细胞的过程中,与丙型流感病毒一样,去唾液酸化能够使细胞具有抗感染能力,而9-O-乙酰基唾液酸的再次唾液酸化则会恢复对细胞的易感性[29]。除此之外,TGEV和IBV则会利用唾液酸当作他们的辅助受体。TGEV S蛋白的唾液酸结合活性导致其的肠道嗜性的存在,其变异株,即PRCoV则由于S蛋白唾液酸结合位点区域缺失导致其无法在肠道中有效复制[30]。HCoV-HKU1虽然不能与9-O-乙酰基唾液酸结合,但近期发现其能够利用O-乙酰化唾液酸作为黏附受体附着在细胞的表面,但不能够作为入侵受体使用[31]。
对BCoV的受体结合域S蛋白NTD的结构进行了解析发现,其核心结构为三明治样的β-折叠,与人半乳糖凝集素的结构十分相似,并且确定了162位的酪氨酸,182位的谷氨酸,184位的色氨酸和185位的组氨酸在与唾液酸的结合中起到十分重要的作用,用丙氨酸取代任一位点都将显著降低BCoV的唾液酸亲和力,而取代掉loop10-11的部分则会完全丧失凝集活性[32]。与BCoV相似,HCoV-OC43的受体结合域同样具有类似人半乳糖凝集素的β-折叠结构,第27~32位氨基酸和第80~86位氨基酸组成的两个loop结构与第90位色氨酸侧链在空间上形成的两个口袋结构P1和P2,则是与9-O-乙酰基唾液酸结合的关键区域。在结合过程中,第9个碳原子上的O-乙酰甲基进入P1,其中的O-乙酰羰基则与第27位天冬酰胺之间形成氢键,第5个碳原子上的N-乙酰甲基插入到P2中,其氮原子与第81位赖氨酸形成氢键,第1个碳原子上的羧基与第81位赖氨酸形成盐桥,与第83位丝氨酸侧链羟基形成氢键,由此来保证受体与配体之间结合的稳定性与特异性[33]。
5 CEACAM1
CEACAM1又称为CD66, 是一种跨膜糖蛋白,属于癌胚抗原家族免疫球蛋白超家族。最初由Ocklind 和 Obrink 发现,并证明其与大鼠肝细胞间的粘附有关[34]。CEACAM1基因是其家族中最保守的,由于原始CEACAM1的mRNA存在复杂可变剪接,导致其至少存在11种剪接变体形式,因此CEACAM1 蛋白在其家族中具有最多的种类[35]。CEACAM1广泛地表达于所有哺乳动物白细胞,上皮细胞和内皮细胞膜上, 具有复杂的生物学功能,其在促进血管和淋巴管的形成,疾病的标记,抑制或促进肿瘤增殖,免疫的调控,介导信号传递等[36]方面有着重要的作用。
CEACAM1是多种病毒和细菌病原体的受体,包括流感嗜血杆菌(Haemophilusinfluenzae)、淋病奈瑟氏球菌(Neisseriagonorrhoeae)、脑膜炎奈瑟氏菌(Neisseriameningitidis)和β冠状病毒属的鼠肝炎病毒(murine hepatitis virus,MHV)[37]。最初研究发现转染并表达鼠CEACAM1a蛋白的人和仓鼠成纤维细胞能够感染MHV。通过用抗鼠CEACAM1a蛋白的抗体对细胞进行预处理,可以避免MHV的易感细胞小鼠成纤维细胞以及表达鼠CEACAM1a的人和仓鼠细胞免受MHV感染。除了鼠CEACAM1a蛋白之外,其等位基因编码的鼠CEACAM1b蛋白也可以作为MHV的受体,但其感染效率要远低于鼠CEACAM1a蛋白[38]。
为了解两种受体蛋白介导MHV入侵效率存在差异的原因,对两种蛋白的结构进行分析发现,结构域D1中连接两个β-折叠的的无规卷曲结构在与MHV结合过程起到重要作用,对两种蛋白中的这一关键性位点进行突变能够降低鼠CEACAM1a或者提高鼠CEACAM1b对MHV的感染效率[39]。而MHV S蛋白的受体结合域,即S蛋白N末端中第162位酪氨酸则在MHV感染过程中起到关键作用,通过对其受体结合域的结构进行解析,发现MHV NTD包含一个与人半乳糖凝集素相同的三明治样的β-折叠,但是与HCoV-OC43和BCoV中的半乳糖凝集素样NTD不同,其不能与糖结合,而是通过蛋白质之间相互作用结合鼠CEACAM1的结构域D1,其中MHV NTD中的14个残基与鼠CEACAM1中的17个残基的相互作用使MHV与鼠CEACAM1紧密结合,从而介导MHV入侵宿主细胞[40]。
6 结语
冠状病毒可引起人和多种动物发生疫病,给人类带来极大的损失。目前研究表明多种冠状病毒能够从其天然宿主传播到人类和其他动物中,在新宿主种群传播的过程中,S蛋白关键性氨基酸位点的突变使其能够适应新宿主受体,并引起大范围传播。目前针对一些冠状病毒仍没有的有效疫苗或者治疗方法,其频繁的跨种传播也使防控变得异常困难。因此冠状病毒受体的研究有助于了解冠状病毒的感染,致病以及跨种传播的机制,对冠状病毒病的防控,新型抗病毒药物或疫苗研发具有指导意义。
