食管癌患者营养支持治疗的药学监护有效预防再喂养综合征1 例
2021-03-10廖金花郑高崟陈小妹刘勇
廖金花,郑高崟,陈小妹,刘勇
赣州市肿瘤医院,江西 赣州 341000
再喂养综合征(refeeding syndrome,RFS)是指机体经长期饥饿或营养不良后,提供再喂养(包括经口摄食、肠内或肠外营养)后出现的以低磷血症为特征的电解质代谢紊乱及由此产生的一系列症状,包括水电解质失衡、葡萄糖耐受性下降、维生素缺乏及由此引发的神经、呼吸、消化、循环系统等并发症,严重者可导致死亡[1-2]。在很多文献中,与RFS 相关的最典型特征是低磷血症,实际上,它是一种更为复杂的综合征,具有高血糖,体液潴留,镁、钾和硫胺素的血浆水平降低等特征[3-4]。
本文以临床药师识别出食管癌患者RFS 的风险并给予营养干预的过程为例,阐述了临床药师给予营养支持治疗方案的药学监护以及识别、预防RFS的重要性。
1 病例资料
男,61 岁,因“外院诊断食管癌4 月余,吞咽困难。伴声音嘶哑1 周”入赣州市肿瘤医院(以下简称我院)治疗,自诉入院4 月前无明显诱因出现吞咽困难,进食梗阻,未予以重视,后吞咽困难加重,于外院诊断为(食管上段)鳞状细胞癌;十二指肠球部溃疡(H2 期),患者无手术指征,只能行姑息性放化疗,后患者未予以积极治疗,近期出现吞咽困难,求进一步治疗就诊我院。患者入院时饮食纳差,吞咽困难,饮水呛咳,反酸,嗳气,胸骨后灼烧感,4 个月来体质量下降20 kg。体格检查:身高体质量163 cm/46 kg,身体质量指数(BMI)17.3 kg/m2,体温36.9 ℃,脉搏110 次/min,呼吸20 次/min,血压149/97 mm Hg,患者步行入院,神志清楚,对答切题,余无特殊。实验室检查:血红蛋白(Hb)97 g/L,血清前血蛋白(PA)84 mg/L,白蛋白(ALB)27 g/L,镁0.71 mmol/L,磷0.62 mmol/L,钙1.98 mmol/L。入院后医生拟对该患者给予姑息性放射治疗,住院部护理人员采用NRS 2002 评分对该患者进行营养风险筛查,得分4 分,有营养风险,进一步对该患者采用主观全面营养评估量表(PG-SGA)评分进行营养评估,得分11 分,患者处于严重营养不良状态,需进行营养治疗。临床药师发现该患者在进行营养支持治疗的过程中有RFS 的风险,建议在营养支持治疗之前,调节电解质水平,超日常需要量给予维生素B1,患者从低热卡开始能量给予,并密切监测各项指标,第10 天患者在添加至目标能量时,体征正常,各项检查趋于正常,第15 天可以经口进食,白蛋白水平持续性增加,体质量也在持续性增加,并且放射治疗没有因此中断,患者成功避免了发生RFS。
2 营养治疗方案
患者入院时NRS 2002 评分4 分,有营养不良风险,使用PG-SGA 评分对病人的营养状态进行评估,提示患者处于重度营养不良状态,需尽快给予营养治疗。因患者食管梗阻,只能进食少量流食,拒绝进行管饲肠内营养治疗,所以给予该患者全肠外营养治疗。因患者入院前4 个月体质量丢失≥30%,入院前1 周只能进食少量流食,入院时身高163 cm,体质量46 kg,BMI 17.3 kg/m2,无水肿、腹水等症状,实验室检查:Hb 97 g/L,PA 62 g/L,ALB 27 g/L,镁0.71 mmol/L,磷0.73 mol/L,钙1.98 mmol/L。根据2020 年ASPEN《再喂养综合征》识别发生RFS 风险的标准[5],分为两个级别(中度风险、重度风险),该患者有发生RFS 的重度风险。该指南提出对于有中、重度风险发生RFS 的患者应该采取如下措施:(1)纠正电解质水平;(2)超常量补充维生素B1;(3)限制能量摄入;(4)复合维生素2 倍剂量补充;(5)严密监测各项指标。根据2018 年中国抗癌协会《恶性肿瘤放疗患者营养治疗专家共识》[6],推荐肿瘤患者目标能量为25~30 kcal·kg-1·d-1,蛋白质需要量为1.2~1.5 g·kg-1·d-1,计算出该患者能量需求约为1 300 kcal/d,蛋白质需要量约为60 g/d,液体需要量约为1 600 mL,该患者具体的营养干预方案见表1。
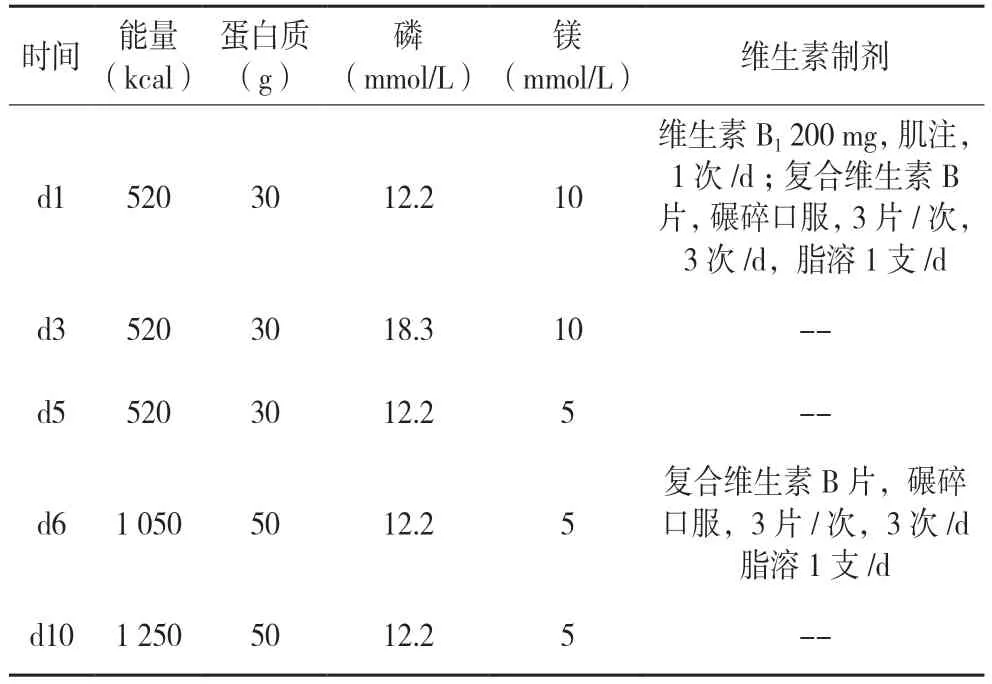
表1 患者营养干预方案
结果,患者的电解质水平在第5 天恢复到正常水平,患者在第5 天诉无力,查体后考虑是患者由于摄入不足且液体量不足引起,第6 日给予患者增加能量摄入,液体量增加,患者后诉无力感减少。第10 天达到患者目标能量,电解质水平正常,患者未诉其他不适。第15 天,随着放射治疗的效果,建议患者尝试口服肠内营养剂,服用后无不适。RFS一般发生在再喂养治疗的第3~4 天内,且无RFS 的症状[(1)循环系统、呼吸系统、神经系统症状;(2)钾<2.5 mmol/L,磷<0.32 mmol/L,镁<0.5 mmol/L。(3)外周水肿,急性液体积聚[7-8]],诊断该患者没有发生RFS。具体各项指标变化如表2。
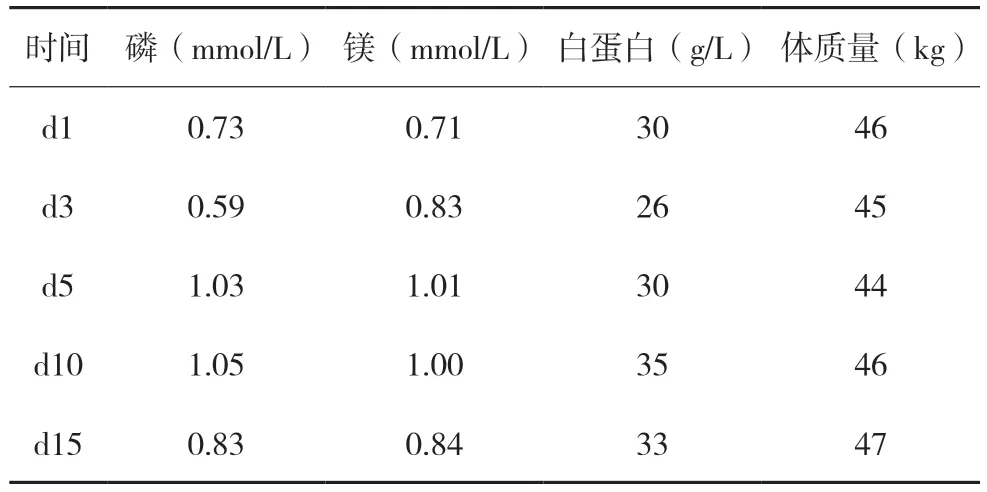
表2 各种指标的变化
3 讨论
识别出营养不良患者的RFS 的风险对于防治RFS 至关重要,这应该是团队合作的结果,其中包括在早期阶段和治疗过程中由专业营养师、专业的临床药师作为多学科的核心成员[8]。建立营养支持小组是推动营养支持在临床上有效、安全、合理应用的一种良好方式,它能使肠内、肠外营养引起的相关并发症减少,使营养支持治疗发挥最大的效能[5]。
为避免和降低发生RFS 风险,在电解质补给方面的建议如下:(1)再喂养前要检查电解质水平;(2)假如再喂养前患者电解质水平正常,不建议预防性补充电解质制剂;(3)假如电解质水平低则常规补充电解质制剂,所以该指南并没有明确给出具体给予电解质的方案,但是值得注意的是,再喂养前电解质水平低是需要常规补充电解质的。有文献指出,每个患者的干预方案应该是个体化的,应根据患者发生RFS 的风险程度、电解质水平给予个性化的调整[9]。
对于轻度低磷血症(0.61~0.8 mmol/L)的患者,建议口服0.3 mmol·kg-1·d-1磷酸盐或者在8~12 h内肌注0.3 mmol/kg 磷酸盐注射液[10-12]。该患者入院磷0.73 mmol/L,为轻度低磷血症,该患者在初始静脉给予12.2 mmol 的磷离子后,第3 天出现磷离子下降的现象,考虑是给予的量不足导致,后给予18.3 mmol 后,第5 天查电解质水平,均恢复正常,由于我院只有复合磷酸氢钾注射液,磷含量较低,且里面有钾离子,风险较大,有条件的话换成甘油磷酸钠注射液来补磷比较合理。
按照指南对于有高风险的患者,建议每12 小时监测电解质水平,由于患者不愿意频繁抽血,且医院条件有限,所以变成每3 天抽血化验一次。按照该指南患者应该在补充维生素B1的同时,应常规补充水溶性维生素,由于我院无水溶性维生素制剂,只能口服复合维生素B 片来补充水溶性维生素。按照原则个体化地给予干预方案。
总之,筛查出RFS 的风险且给予预防措施比治疗更为重要,在这个过程中,需要营养支持治疗小组的各个成员的参与,才能更好地制定合理安全的营养治疗方案。但本研究仅1 例,需要收集多些病例关于对临床药师参与营养支持治疗方案前后效果做一个对比研究,会更有说服力。
