磁性多孔碳基纳米棒的制备及催化硝基苯酚加氢反应性能
2021-03-08王舒璇董伟航杜春保欧阳韶晖
杨 涛,王舒璇,董伟航,杜春保,欧阳韶晖
(西北农林科技大学食品科学与工程学院,陕西 杨凌 712100)
1 前 言
硝基苯酚(NO2C6H4OH,NP)是农药的中间体,是一种常见于工业和农业废水中高毒性且难降解的有机污染物[1],其毒性对环境危害巨大。硝基苯酚有邻(2-NP)、间(3-NP)、对(4-NP)三种同分异构体,其中2-NP和4-NP很早就被美国环境保护总署列入“优先控制污染物名单”[2]。NP通过加氢反应可以被还原成氨基苯酚(NH2C6H4OH,AP),AP毒性小、易降解,是一种非常有价值的医药中间体,国内的需求量很大,市场坚挺。但是NP具有极强的生化稳定性,很难被自然降解或降解速率缓慢,导致其长期富集在环境中,危害人类健康。因此,迫切需要开发出一种高效的催化剂来加速NP还原反应。
金属有机骨架化合物(Metal-Organic Frameworks,MOFs)由于具有较大的比表面积、可设计的结构、可调节的孔径[3-4]、可控的性质、可接受的热稳定性及对反应物良好的聚集和传质作用,在设计和探索各种新型微孔或中孔催化剂方面表现出巨大的潜力。与对应的母体MOFs相比,这些催化剂有更强的活性,表现出一些新的性质。截止目前,已报道过多种金属/金属氧化物纳米颗粒(NPs)封装到MOFs中用于催化反应(例如选择性加氢[5-6],C-C偶联[7-8],CO2转化[9-10]),包括TiO2[11],Ag[12],Au[13],Pd[14],Pt[15],Co3O4[16]等。但是,关于具有碳基结构和磁性的MOFs衍生催化剂的报道却很少。这主要是由于以下两个因素:①由于有机配体的稳定性差,热解获得碳基结构将导致MOFs的三维结构在高温下坍塌;②其他磁性材料的掺入必然会干扰原有的催化活性位点,降低催化效率。目前解决这些问题仍然是一个很大的挑战。此外,大多数设计和研究的纳米催化剂通常仅用于4-NP的还原,很少用于其异构体2-NP和3-NP。因此,开发一种具有磁性的能有效还原2-NP,3-NP,4-NP的MOFs衍生催化剂是非常有前景的。
本研究首先采用溶剂热法制备了Ni基MOFs(MCF-61),然后通过简单的一步高温热解MCF-61制备了具有磁性和三维碳基结构的新型纳米棒状催化剂(MCF-61*)。接着采用一系列化学表征手段研究了MCF-61*的成分、形态、结构和化学特性,并研究了其对NP的催化性能。
2 实 验
2.1 试剂与仪器
实验用试剂有:氯化镁、2,4,6-三(4-吡啶基)-1,3,5-三嗪、草酸二甲酯、邻硝基苯酚、间硝基苯酚、对硝基苯酚、硼氢化钠及乙醇等,均为分析纯;实验用水为离子水。
X射线衍射仪(D8 Advance A25,XRD),X射线光电子能谱(Axis Ultra DLD,XPS),扫描电子显微镜(S-4800,SEM),透射电子显微镜(TF20 Joel 2100F,XPS),比表面积分析仪(ASAP2460),振动样品磁强计(LakeShore 7307)。紫外可见光分度计(UV-Vis2550,UV-Vis)。
2.2 纳米催化剂的制备
2.2.1MCF-61的合成 采用简单的溶剂热法合成MCF-61[Ni3(C2O4)3(TPT)2]。首先,NiCl2·6H2O(1.144 g,4.81 mmol)溶解在乙醇(288 mL)中形成均相溶液。然后在上述溶液中加入2,4,6-三(4-吡啶基)-1,3,5-三嗪(TPT,C18H12N6)(1.0 g,3.22 mmol)和草酸二甲酯(0.58 g,4.81 mmol),磁力搅拌30 min后,在高压反应器中120 ℃密封72 h。反应结束后,高压反应器自然冷却至室温。最后,经过温和过滤、乙醇重复洗涤、100 ℃真空干燥1 h,得到产率约88%的黄色产品MCF-61。
2.2.2MCF-61*的制备 将MCF-61放入管式炉中缓慢持续通入N230 min。然后,将MCF-61加热至500 ℃,加热速率为10 ℃/min,并连续通入N2。在500 ℃下保持2 h后,将管式炉冷却至300 ℃,冷却速率为10 ℃/min,并自然冷却至室温,最终得到活化后的黑色产物即为纳米催化剂,记为MCF-61*。
2.3 催化性能试验
分别称量1.7 mg的2-NP、3-NP和4-NP于100 mL超纯水中配成溶液(0.125 mmol/L),称量3.783 g的NaBH4于100 mL超纯水中配成溶液(0.1 mol/L),上述溶液用锡箔纸包装。分别取5.0 mL的NP溶液和200 μL的NaBH4溶液进行充分混合后,加入5.0 mg的MCF-61*,隔一定时间通过磁场快速分离,并使用UV-Vis分光光度计进行测量。
3 实验结果与分析
3.1 SEM观察
MCF-61和MCF-61*的SEM照片如图1所示。MCF-61是典型的纳米棒结构,轮廓光滑,表面致密,直径约100 nm且较均一。MCF-61热解后得到的MCF-61*为多孔结构,这可能是由于小分子和残留反应物的分解引起的;MCF-61*表面上具有接近球形的纳米颗粒,由第3.4节中Ni2pXPS光谱和TEM映射可知,该纳米颗粒是由于Ni2+的还原和迁移聚集造成的。尽管处理温度高达500 ℃,但是MCF-61*的基本骨架并未改变,说明纳米棒结构的稳定性。众多MOFs在热解后虽表现出类似沸石的永久性微孔,但在高温下除去溶剂时,往往会崩塌,很难保持原有的空间结构。然而,由于MCF-61的特殊性(存在两种有机配体,以及有机配体TPT的稳定性),尽管热解时有机分子发生了分解、重组或杂化,金属离子被还原并迁移,MCF-61经碳化所得到的纳米催化剂仍能很好的保持原始纳米棒结构。

图1 (a) MCF-61; (b) MCF-61*的SEM照片Fig.1 SEM images of (a) MCF-61 and (b) MCF-61*
3.2 XRD分析
图2为MCF-61及MCF-61*的XRD图谱。在MCF-61的XRD图谱中出现三处尖而窄的衍射峰,这与之前报道的研究结果[17]一致,说明成功合成了MCF-61,图谱中还存在其他较弱的衍射峰,这可能是由于溶剂没有完全排干净而导致的。经热处理后,MCF-61*在2θ=44.4°、51.7°、76.3°处有典型的衍射峰,分别为面心立方Ni(111)、(200)、(220)晶面的特征峰,表明Ni2+在热处理过程中被还原。此外,MCF-61*在26.0°和41.8°处出现了石墨(002)和(100)晶面的典型衍射峰,表明MCF-61*中存在丰富的碳基结构。
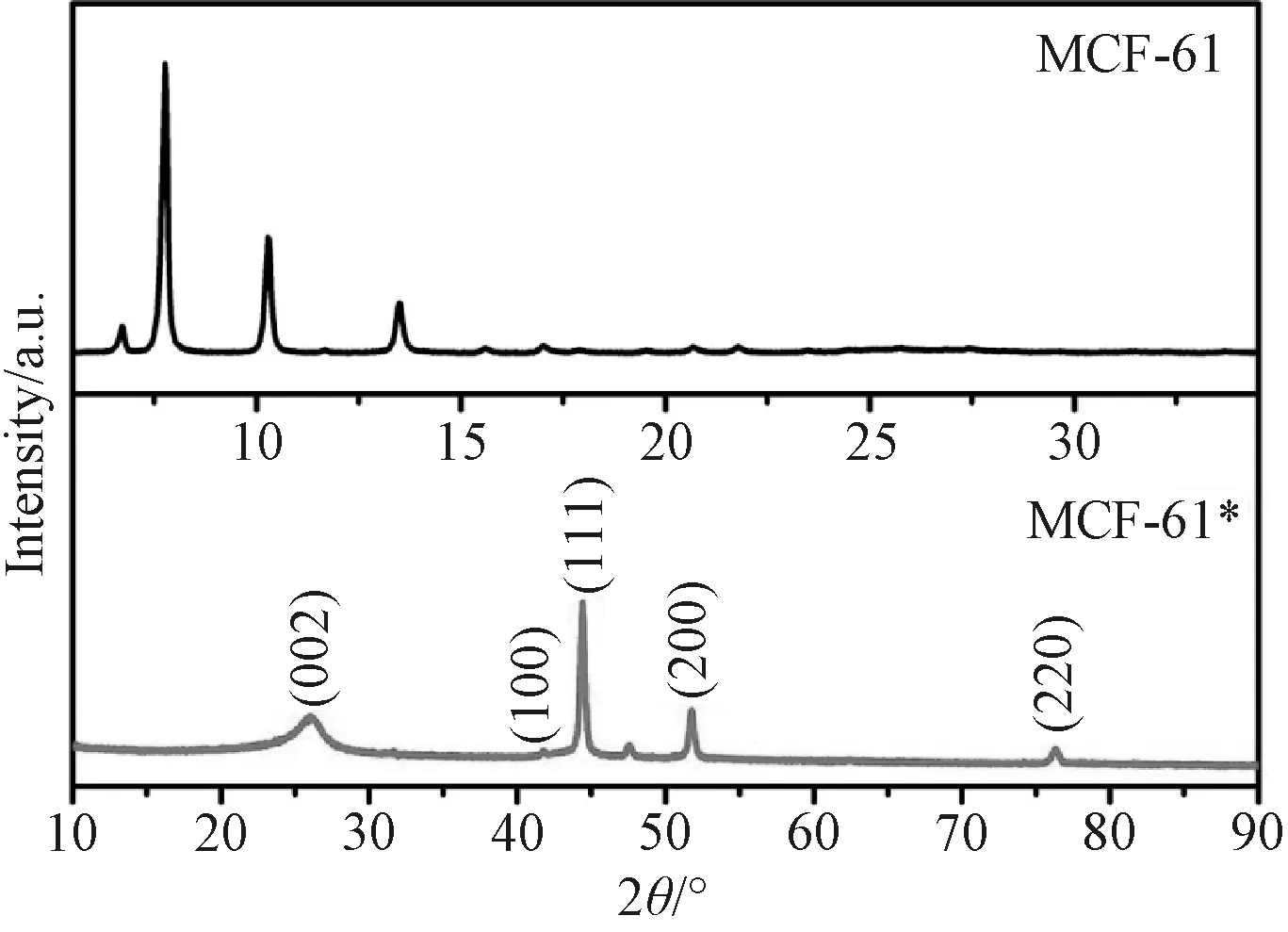
图2 MCF-61和MCF-61*的XRD图谱Fig.2 XRD patterns of MCF-61 and MCF-61*
3.3 XPS分析
图3是MCF-61和MCF-61*的XPS分析结果。由MCF-61和MCF-61*的XPS全谱图(图3(a))可以看出,这两种样品都是由C、O、N和Ni 四种元素组成。与MCF-61原子组成相比,MCF-61*中O的原子含量降低,197.0 eV左右的Cl2p峰消失,这是由于高温下小分子物质的分解和挥发而造成的。在MCF-61的Ni2pXPS光谱中(图3(b)),Ni元素的两个峰出现了相应的峰移(Ni2p3/2从855.5到852.9 eV,Ni2p1/2从872.6到871.2 eV),这表明在MCF-61的分解和还原过程中Ni的价态发生了显著的变化,部分Ni2+被还原为单质Ni。在N1sXPS光谱(图3(c))中,MCF-61在399.2和400.5 eV处的两个峰对应于TPT的N1s,而MCF-61*中N的化学状态由于形成了复杂的碳氮掺杂结构而不易被证实。MCF-61*和MCF-61的C1s的高分辨率XPS谱图(图3(d))均含有四种类型的化学键(C-C,C-N,N-C=N,O-C=O),表明MCF-61*具有与MCF-61相同的C化学状态,并且只有原子含量表现出轻微的变化,这进一步说明其骨架的稳定性。

图3 (a) MCF-61和MCF-61*的XPS全谱图(插图是不同元素的原子浓度); (b) MCF-61和MCF-61*的Ni2pXPS光谱; (c) MCF-61和MCF-61*的N1sXPS光谱; (d) MCF-61和MCF-61*的C1s XPS光谱(插图是C1s的不同化学状态的原子浓度)Fig.3 (a) XPS survey spectra of wide scan MCF-61 and MCF-61* (inset was the atomic concentrations of different elements); (b) Ni2p XPS survey spectra of MCF-61 and MCF-61*; (c) N1s XPS survey spectra of MCF-61 and MCF-61*; (d) C1s XPS survey spectra of MCF-61 and MCF-61* (insets was the atomic concentrations of different chemical states of C1s)

图4 MCF-61*(a)和MCF-61*(b)的TEM图片Fig.4 TEM images of MCF-61*(a) and (b) HRTEM
3.4 TEM观测
MCF-61*的低倍TEM照片(图4(a))更清楚的显示了MCF-61*的典型纳米棒结构,纳米棒的直径约为100 nm,验证了之前SEM的结果,同时纳米棒上出现了很多黑色颗粒,由之前的分析可知是Ni单质。图4(b)是MCF-61*的高分辨率透射电镜(HRTEM)照片,晶面间距为0.34和0.176 nm的两个晶格条纹分别对应MCF-61*中石墨的(002)晶面和元素Ni的(200)晶面,这进一步证实了骨架和纳米颗粒的组成元素。通过TEM mapping分析了元素分布,结果如图5所示:MCF-61*中,C、N、O元素分布在样品整个区域,构成了MCF-61*的基本骨架。从SEM图像、高角度环形暗场图(图5(f))、TEM图像和TEM元素成像来看,纳米棒表面存在大量的球形Ni纳米颗粒,这是Ni2+在高温下被还原并迁移聚集形成的。
以上分析表明成功制备了具有稳定结构的多孔纳米棒催化剂。
3.5 比表面积分析
图6为MCF-61*的氮气吸附-脱附等温线和孔径分布曲线。如图6(a)所示,MCF-61*的吸附曲线属于典型的IV型等温线,图中有一个明显的H1滞后环结构,在0.4~0.6的相对压力下,有一个明显的台阶,表明MCF-61*中存在中孔。通过BET(brunauer-emmett-teller)方法计算表明,MCF-61*的比表面积为119.9 cm2·g-1。通过BJH(barrett-joiner-halenda)模型求得样品孔径分布曲线(图6(b)),样品的孔径主要以中孔为主,分布范围较宽,平均孔径为11.6 nm。因此, PN分子可以顺利进入孔内,并与MCF-61*相互作用进行催化反应。同时极小的孔径使得在相同的体积内MCF-61*具有更大的比表面积,表明MCF-61*是良好的催化剂候选物。

图5 (a,b,c,d,e) TEM mapping图谱(从左至右依次为C-K、N-K、O-K、Ni-K、Ni-L); (f) MCF-61*的高角度环形暗场图Fig.5 (a,b,c,d,e) TEM mappings of MCF-61*(C-K, N-K, O-K, Ni-K, Ni-L from left to right); (f) High-angle annular dark field image of MCF-61*
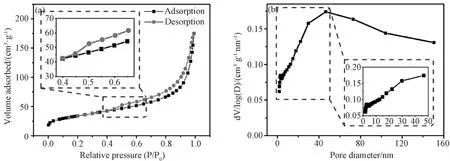
图6 (a) MCF-61*的N2吸附脱附等温线(77 K); (b) MCF-61*的孔径分布曲线Fig.6 (a) N2 adsorption/desorption isotherms of MCF-61*(77 K); (b) pore size distributions of MCF-61*
3.6 磁滞分析
图7的磁滞数据显示MCF-61*具有磁性,矫顽力为0.043 kOe,饱和磁化强度为0.0207 A·m2·g-1。如此低的矫顽力表明MCF-61*与典型的软磁体环路基本相同,具有大的磁导率,容易磁化也容易退磁;磁滞回线包围面积小,具有准超顺磁性,没有磁滞损耗,当移去外磁场后,剩磁很快消失,这有利于样品的分离和回收。通过施加外部磁场发现MCF-61对磁场没有响应(图8(a)),而MCF-61*可以很迅速地被磁场收集(图8(b),(c))。
3.7 催化性能分析
图9(a),(c),(e)为5.0 mg MCF-61*对初始浓度为0.125 mmol/L 的NP溶液在25 ℃下的降解曲线,随着NaBH4的加入,2-NP、3-NP和4-NP的紫外-可见吸收光谱从351.5、333.0和318.0 nm分别移动到416.0、393.0和401.0 nm。Wu等[18]和Li等[19]已证明2-NP、3-NP和4-NP的加氢反应即便延长反应时间也很难在没有催化剂的情况下发生。由于缺乏有效的催化位点,未经处理的MCF-61对2-NP、3-NP和4-NP没有明显的催化效果,而催化剂MCF-61*的加入使吸收光谱峰开始有规律地降低,在6 min内几乎可以催化2-NP、3-NP、4-NP的完全还原。与之相比,MCF-61对2-NP、3-NP和4-NP没有明显的催化反应,这些结果最终证明了热解的优越性。另外,使用伪一级动力学方程来评估MCF-61*对2-NP、3-NP和4-NP的催化效率,表示为ln(Ct/C0)=ln(At/A0)=-kt,其中Ct是时间t的NP浓度,At是NP在时间t的吸光度,k是表观速率常数。如图9(b),(d),(f)所示MCF-61*催化2-NP、3-NP和4-NP的速率常数(k)分别计算为0.7466、0.4945和0.51 min-1。整个催化过程是在快速重复磁分离和紫外可见检测下完成的,所以催化过程可以随时得到控制。同时,MCF-61*对NP的有效催化作用也归因于其对AP的低结合力,这使得催化位点容易暴露而有利于催化反应的进行。因此,MCF-61*同时满足了理想催化剂公认应具备的两个条件即反应物的高催化活性和产物易脱附性。和一些典型的催化剂相比[18-24],它表现出了优异的催化活性。此外,MCF-61*即使经过5个循环仍能保持较高的催化活性,说明MCF-61*骨架的稳定性和Ni纳米颗粒在多孔碳骨架上催化位点的稳定性 (图10)。同时,利用外加磁场进行循环试验,可以有效地从反应溶液中回收催化剂,不会造成明显的损失。因此,相信这项工作已证明了MCF-61*在绿色可持续催化化学中的潜力。

图7 MCF-61*的磁滞回线Fig.7 Magnetization curves of MCF-61*
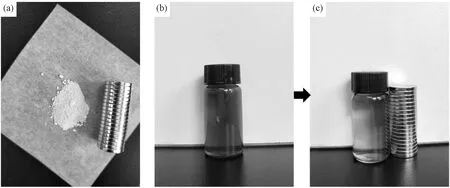
图8 MCF-61(a)和MCF-61*(b,c)对外界磁场的响应Fig.8 (a) Magnetic responsiveness of MCF-61; (b) MCF-61* aqueous solution without magneticfield; (c) magnetic responsiveness of MCF-61*
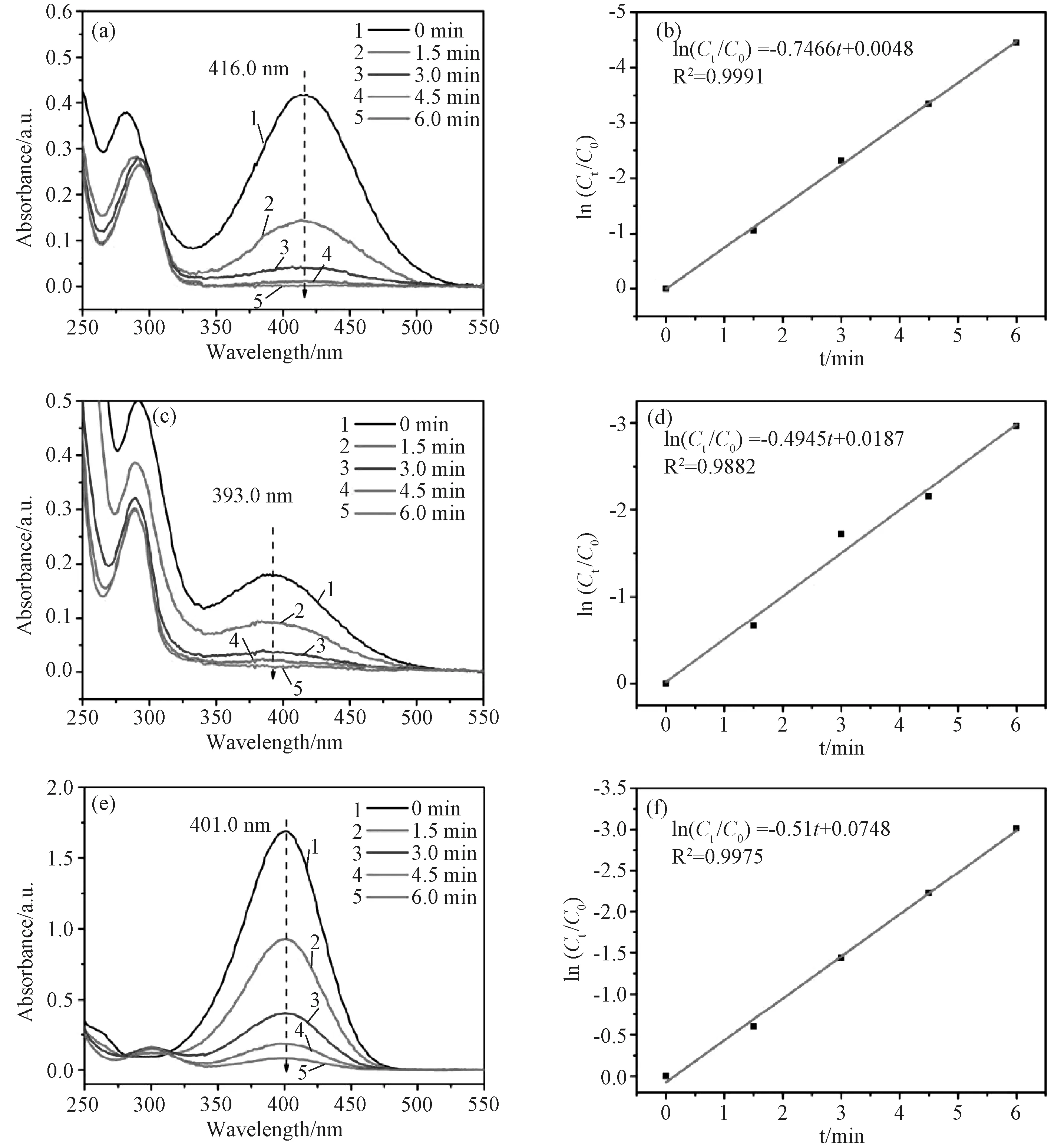
图9 2-NP(a),3-NP(c),4-NP(e)的紫外光谱图;2-NP(b),3-NP(d),4-NP(f)的催化反应动力学曲线(其中NP溶液(5.0 mL,0.125 mmol/L),NaBH4(200 μL,0.1 mol/L),MCF-61*(5.0 mg),反应在25℃下进行)Fig.9 UV-Vis spectra of 2-NP solution(a), 3-NP solution (c), 4-NP solution (e) (NP aqueous solution (5.0 mL, 0.125 mmol/L) and NaBH4 (200 μL, 0.1 mol/L)) over MCF-61* (5.0 mg) at 25 ℃. Plots of ln(Ct/C0) against t of 2-NP solution (b), 3-NP solution (d), and 4-NP solution (f) over MCF-61*
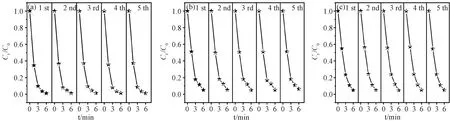
图10 催化剂MCF-61*(5.0 mg)催化2-NP(a),3-NP(b),4-NP(c)溶液的重复降解曲线(NP水溶液(5.0 mL,0.125 mmol/L)和NaBH4(200 μL,0.1 mol/L),反应在25 ℃下进行)Fig.10 Recycling runs in catalysis of MCF-61* for 2-NP solution(a), 3-NP solution (b), 4-NP solution (c) (NP aqueous solution (5.0 mL, 0.125 mmol/L) and NaBH4 (200 μL, 0.1 mol/L)) with the catalyst of MCF-61* (5.0 mg) at 25 ℃
4 结 论
本研究利用简单的一步热解方法成功构建了具有较高密度和分散均匀的催化活性位点的Ni基纳米催化剂,该催化剂可以实现对2-NP、3-NP和4-NP的快速催化还原,催化反应均遵循伪一级动力学方程,且能通过外界磁场快速分离催化剂来控制反应进程,在循环使用5次后,仍能保持较高的催化活性。该催化剂表现出的绿色可持续的特点,增加了其在工业生产和环境治理中大规模应用的潜力。
