电感耦合等离子体质谱法测定左氧氟沙星片中8种元素杂质的含量
2021-03-05孙滨滨黄祝刚李亚囡孟亚楠
孙滨滨,黄祝刚,李亚囡,唐 彬,孟亚楠
(山东齐都药业有限公司药物分析研究室,山东淄博 255400)
电感耦合等离子体质谱(ICP-MS)是20世纪80年代发展起来的一种分析测试技术,是以独特的接口技术将电感耦合等离子体的高温电离特性与四极杆质谱仪灵敏、快速扫描的优点结合而成的一种新型的元素和同位素分析技术。近年来,ICP-MS不仅应用于地质科学研究,还迅速拓展到医药卫生、食品科学、生物科技、卫生防疫、环境分析、冶金工业、石油和核材料分析等领域[1-2]。
左氧氟沙星为第三代氟喹诺酮类抗菌药,为氧氟沙星的左旋异构体,可作用于细菌DNA旋转酶和(或)拓扑异构酶Ⅳ,抑制DNA的合成与复制,从而导致细菌死亡,具有抗菌谱广、抗菌作用强的特点[3]。在左氧氟沙星片的生产和储存过程中可能会生成、加入或无意中引入元素杂质,这些元素杂质可能存在于原料药、辅料、制剂中的催化剂和环境污染物(如通过与生产设备[4]、密闭容器或包装材料相互作用产生)。因为元素杂质不具有任何治疗作用,所以它们在药品中的含量需要被控制在可接受的限度范围内。
基于元素毒性及在药品中出现的可能性,将元素杂质分为3类[5]。第1类:砷(As)、镉(Cd)、汞(Hg)和铅(Pb),对人体有毒,药品生产中不得使用或限制使用,通常来源于矿物赋形剂。因此,所有给药途径的风险评估中都必须评估这4种元素。第2类:该类元素毒性的大小与药物的给药途径有关,根据出现在药品中概率的大小将该类元素进一步分级为2A类和2B类。2A类元素包括钴(Co)、镍(Ni)、钒(V),这些元素在制剂中出现的可能性较高,需要对所有潜在的来源和给药途径进行风险评估。2B类元素包括银(Ag)、金(Au)、铱(Ir)、锇(Os)、钯(Pd)、铂 (Pt)、铑(Rh)、钌(Ru)、硒(Se)、铊(Tl),这些元素在自然界中稀少,与其他材料共分离可能性较低,在药品中出现的可能性较低。第3类:该类元素口服毒性低, 包括钡(Ba)、铬(Cr)、铜(Cu)、锂(Li)、钼(Mo)、锑(Sb)、锡(Sn)。如果在原料药、赋形剂或药品的其他组分生产中有意添加,则需要进行风险评估。
根据《人用药品注册技术国际协调会(ICH)Q3D元素杂质指导原则》口服制剂评估要求[6],对药品生产过程中非有意添加的1类和2A类共7种元素杂质进行评估,考虑到在左氧氟沙星片的生产过程中容易引入铁(Fe)元素,故增加了对Fe元素的研究。欧洲药品审评局(EMEA)《关于金属催化剂和金属试剂残留量限度规定的指导原则》中将Fe归为第3类金属[7],这一类金属无明显毒性,安全隐患小,口服给药的每日允许暴露量(PDE)为13 mg/d,静脉给药的PDE为1.3 mg/d。
1 材 料
1.1 仪器 7900电感耦合等离子体质谱仪[安捷伦科技(中国)有限公司];Med-C型微波消解仪(屹尧科技有限公司);SQP型十万分之一电子天平[赛多利斯科学仪器(北京)有限公司]。
1.2 药品和试剂 硝酸[67%~70%,痕量金属级,赛默飞世尔科技(中国)有限公司];盐酸(37%,优级纯,默克股份两合公司);异丙醇(色谱纯,天津市科密欧化学试剂有限公司);Cd、Pb、Hg、Co、V、As、Ni单元素标准溶液(1000 μg/ml)和Fe单元素标准溶液(10 mg/ml,国家有色金属及电子材料分析测试中心);内标标准溶液(Te 25 μg/ml,Sc 10 μg/ml,Ge、In、Lu、Bi 25 μg/ml)、调谐液(Ce、Co、Li、Mg、Tl、Y 1 μg/L)均购自安捷伦科技(中国)有限公司;左氧氟沙星片(规格0.5 g/片,批号181209、181210、181211,山东齐都药业有限公司);左氧氟沙星片参比制剂[规格0.5 g/片,批号BT066G1,第一三共制药(北京)有限公司]。
2 方法和结果
2.1 元素杂质限度的确定 参照《ICH Q3D元素杂质指导原则》和EMEA《关于金属催化剂和金属试剂残留量限度规定的指导原则》要求,左氧氟沙星片中待测元素Cd、Pb、As、Hg、Co、V、Ni、Fe的PDE值见表1。每日摄入不超过10 g的药品以10 g计算药品中每种组分的目标元素通用允许浓度[6],即限度值,根据限度值及消解过程计算得到目标元素的限度浓度,各目标元素的限度值及限度浓度见表1。
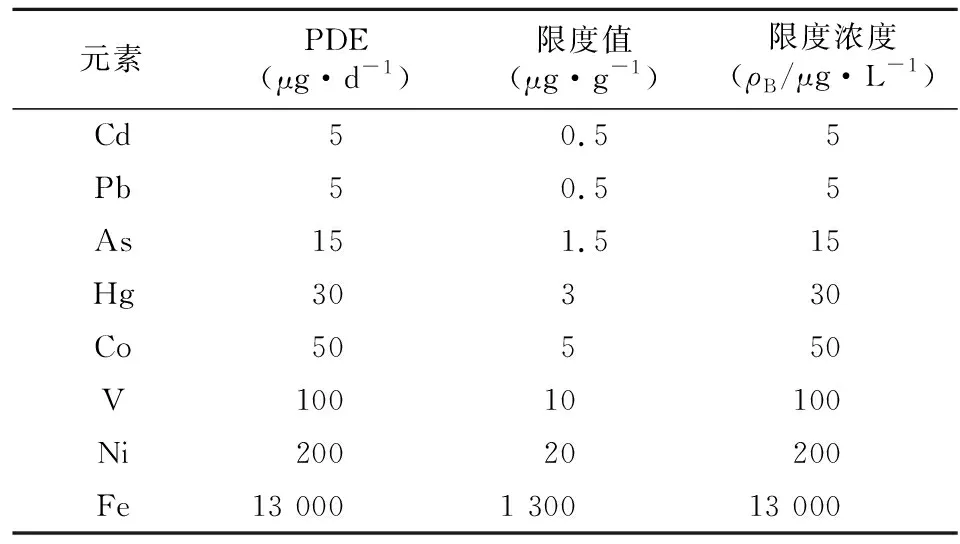
表1 目标元素的每日允许暴露量、限度值及限度浓度Table 1 Target element daily permissible exposure,limit value and limit concentration
2.2 仪器工作条件 等离子体模式为通用模式,射频(RF)功率1550 W,采样深度10.0 mm,等离子气流量15.0 L/min,雾化气流量1.03 L/min,辅助气流量0.90 L/min,蠕动泵转速0.10 r/min,雾化室温度2 ℃,测定模式为He模式。
2.3 溶液制备
2.3.1 供试品溶液 取左氧氟沙星片10片,用研钵研细,作为供试品,精密称取供试品0.2 g于消解罐中,加5 ml硝酸,按表2消解程序和条件进行微波消解,消解后于115 ℃赶酸至0.5 ~ 1.0 ml,用超纯水将其转移至20 ml量瓶中,稀释至刻度,摇匀后用0.45 μm滤膜过滤除去辅料,得供试品溶液。不加供试品,同法制备空白溶液。

表2 微波消解程序和条件Table 2 Microwave digestion program
2.3.2 内标溶液 精密量取内标标准溶液1 ml于50 ml量瓶中,加25 ml异丙醇,然后用2%硝酸和1%盐酸的混合溶液稀释至刻度,摇匀。
2.3.3 线性溶液 精密量取Cd、Pb、As、Hg、Co、V、Ni、Fe单元素标准溶液25、25、75、150、250、500、1000、650 μl于100 ml量瓶中,用2%硝酸和1%盐酸的混合溶液稀释至刻度,摇匀,作为多元素储备液。由于口服制剂中Fe元素限度较大,若按其限度配制线性溶液将超出仪器检测范围,故按注射剂中Fe元素限度浓度配制线性溶液。
根据《ICH Q3D元素杂质指导原则》,将药品既定PDE值的30%定义为控制阈值,作为元素杂质水平显著性的衡量指标,控制阈值可用于判断是否需要额外的控制[6]。分别精密量取0.3、0.5、1.0、1.5、2.0 ml多元素储备液于50 ml量瓶中,用2%硝酸和1%盐酸的混合溶液定容至刻度,摇匀,作为0.3J、0.5J、1.0J、1.5J、2.0J线性溶液(Fe元素J值为注射剂中的限度浓度,其他元素J值为口服制剂中的限度浓度),各元素线性溶液浓度见表3。

表3 各元素线性溶液浓度Table 3 Linear solution concentrations of each element (ρB/μg·L-1)
2.4 测定方法 通常选择供试品中不含,且质量数和第一电离能均与待测元素接近的元素作为内标元素[8]。依据上述内标选择原则,本研究选取45Sc、72Ge、115In、209Bi为内标元素,其中51V、56Fe以45Sc为内标,59Co、60Ni、75As以72Ge为内标,111Cd以115In为内标,201Hg、208Pb以209Bi为内标。仪器调谐后,将内标管插入内标溶液中,样品管放入空白溶液中,待系统稳定后依次引入空白溶液及线性溶液,以各元素线性溶液浓度为横坐标,待测元素与内标元素响应值比值(ratio值)为纵坐标做标准曲线。将样品管插入供试品溶液中,根据3次平均ratio值计算得到供试品溶液中各元素杂质的含量。
2.5 方法学验证
2.5.1 线性和范围 设计0J、0.3J、0.5J、1.0J、1.5J、2.0J共6个线性溶液浓度点,考察各元素浓度与ratio值的线性关系。将各线性溶液依次引入ICP-MS,以各元素浓度为横坐标、ratio值为纵坐标绘制标准曲线,得到各元素线性方程和相关系数,结果见表4。由表4可见,各元素线性相关系数均>0.999 0,表明线性关系良好。

表4 各元素线性实验结果Table 4 Linear test results of each element
2.5.2 检测限和定量限 取空白溶液连续测定11次,根据空白溶液的响应值计算其标准偏差(SD),根据公式:检测限(LOD)=3.3SD/K、定量限(LOQ)=10SD/K(K为各元素浓度与响应值线性关系斜率)计算各元素检测限和定量限[9]。结果见表5,各元素检测限和定量限均低于限度值的10%,能够满足限度测试要求。
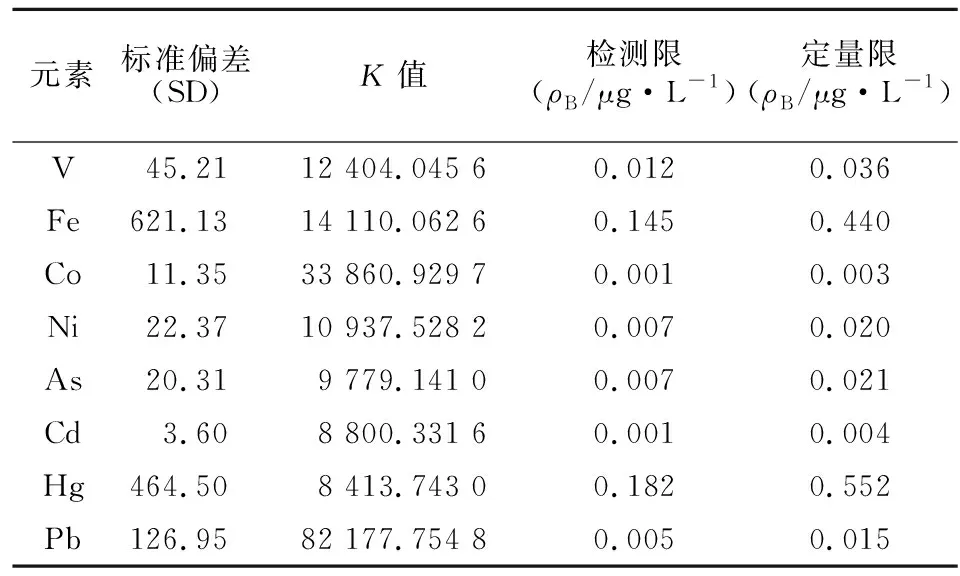
表5 各元素检测限和定量限实验结果Table 5 Limit of detection and limit of quantitative test results of each element
2.5.3 加样回收率实验 参照2.3.1项下方法平行制备9份供试品溶液,将供试品溶液分成3组,分别加入0.5、1.0、1.5 ml多元素储备液后定容至刻度,摇匀,作为50%、100%、150%限度的低、中、高浓度加标供试品溶液。对上述3组加标供试品溶液进行加样回收率实验,验证方法的准确性,要求每个浓度3个平行样品的加样回收率在70%~150%,结果各元素杂质低、中、高浓度下的回收率在90.21%~103.58%,RSD均<5%(n=3),表明该方法准确性良好。
2.5.4 重复性实验 参照2.3.1项下方法平行制备6份供试品溶液,分别加入1.0 ml多元素储备液后定容至刻度,摇匀,进样分析,计算各元素连续6次检测结果的RSD,考察其重复性,要求各元素重复性RSD≤20%。结果左氧氟沙星片中各元素重复性RSD均<1%(n=6),符合重复性要求,表明该方法重复性良好。
2.5.5 内标回收率实验 ICP-MS法测定元素杂质要求内标元素回收率在80%~120%。左氧氟沙星片元素杂质检查方法学验证结果表明,内标元素45Sc、72Ge、115In、209Bi的回收率均在80%~120%,该方法检测结果准确可靠。
2.6 样品检测 在2.2项仪器工作条件下,按2.3.1项下方法制备供试品溶液,对左氧氟沙星片1批参比制剂和3批供试品中的8种元素杂质含量进行测定,结果见表6。由表6可见,各批次样品中元素杂质含量均小于控制阈值(限度浓度的30%),且3批供试品中的元素杂质与参比制剂相近,表明样品中所测元素杂质无风险,无需额外控制。

表6 左氧氟沙星片样品中各元素含量测定结果Table 6 Results of content determination of each element in sample (μg·g-1)
3 讨 论
本研究所选溶剂为2%硝酸和1%盐酸的混合溶液,采用盐酸作为样品基体的目的是减少Hg元素因吸附而产生的记忆效应问题[10],使测定结果准确可靠。异丙醇作为基体改进剂,可提高仪器灵敏度,消除含碳有机物对目标元素的增敏作用,解决无基体改进剂标准溶液响应值低而导致样品测定结果偏高的问题[11]。
本研究建立了ICP-MS法测定左氧氟沙星片中8种元素杂质含量,并进行了方法学验证。检测结果显示,3批供试品中Fe元素含量低于参比制剂,其他元素与参比制剂相当,8种目标元素含量均小于限度值且低于控制阈值,符合ICH Q3D和EMEA《关于金属催化剂和金属试剂残留量限度规定的指导原则》中对元素杂质的限度要求,因此左氧氟沙星片中元素杂质无风险,无需对元素杂质进行额外控制。本研究建立了ICP-MS法测定左氧氟沙星片中8种元素杂质含量,为固体制剂中元素杂质的测定和风险评估提供了参考依据。
