高电压钴酸锂(LCO)正极材料研究现状
2021-03-04孙宏达周森苏畅
孙宏达,周森,苏畅
(东北大学 冶金学院,辽宁 沈阳 110068)
随着社会的进步和科技的发展,人们生活水平得到了很大的提高,随之所需要的能源消耗也逐渐增加。就目前我国资源利用情况来看,传统的能源(煤、石油、天然气等不可再生资源)正面临严峻的考验,同时这类资源在燃烧的过程中会产生许多的有害物质和温室气体二氧化碳,造成自然环境污染和全球气候变暖等问题。因此开发和探索新型可再生资源迫在眉睫,而太阳能、风能、核能、潮汐能等这类能源拥有可再生、来源广泛等优点,因此深受学术界的科研人士的喜爱。但这些能源的利用离不开化学电源。钴酸锂电池作为常用化学电源,被广泛应用于生产和生活中。本文将着重介绍高电压钴酸锂(LCO)电池正极材料的研究现状。
1 LCO 研究存在的问题及分析
1980年牛津大学教授GOODENOUGH 提出了可逆脱嵌锂离子的过度金属氧化物LiCoO2,这种材料具有R-3M 空间群锂离子与钴离子交替排列,在氧阴离子构成的骨架当中具有二维的锂离子传输通道。这一发现为锂离子电池的发展提供了新的道路,1991年钴酸锂电池正式走上历史舞台。
锂离子电池的发展带动了钴酸锂电极材料的发展研究以及商业化应用,这也缓解了人类目前所面临的资源短缺、环境破坏问题。然而虽然钴酸锂电极材料已经研究了20 多年,但是仍然存在许多未被解决的难题,其中最为关注也是最重要的便是高电压钴酸锂的探索。
在对钴酸锂的早期探索中,当电压高于4.25 V时,电池的循环性能便会出现快速的衰减,此时钴酸锂材料六方晶相开始向单斜相转变。通过研究表明相变过程中材料体积变化的同时会导致材料性能发生改变,因为相变是不可逆的,从而会导致容量衰减、内部结构遭到破坏、副反应加剧等问题。目前高电压钴酸锂的研究仍然存在以下4 个难题需要突破:固液相副反应以及CEI 的生成、晶格氧参与电荷补偿、相变过程与体积形变、材料表面的结构变化[1-5]。
1.1 固液相副反应以及CEI 的生成
图1 为钴酸锂正极容量衰减机制示意图。
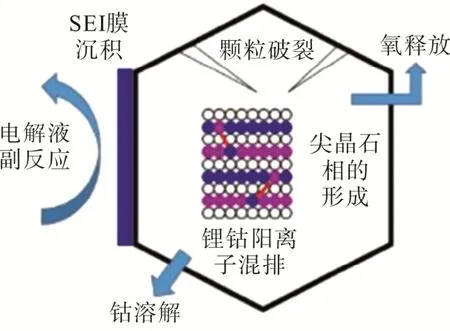
图1 钴酸锂正极容量衰减机制示意图
锂电池在工作的时候其固液相界面发生副反应是不可避免的,目前所使用的非水有机电解液化学窗口通常低于4.4 V,当充电截止电压高于4.4 V 时,电解液便会发生氧化分解,这将导致电池容量急剧下降,同时反应产物将会附着在电极材料表面从而增大内阻。游离过渡金属元素催化表面副反应产物分界使电极材料维持高位活性状态带来隐患。
1.2 晶格氧参与电荷补偿
钴元素与氧元素具有强相互作用,随着充电电压的升高,电荷补偿过程中,当钴元素的电子不足时,将会促使氧元素参与其中,从而会使材料的架构发生改变,稳定性也随之发生改变。与此同时,如果O 参与电解液的氧化反应,那样将会加速材料表面CEI 膜的生成。
1.3 相变过程与体积形变
钴酸锂材料升压的主要影响因素是电压为4.5 V 左右时O3→H1-3→O1 相变。当电压达到甚至高于4.6 V 时材料的相变将难以控制,这种难以控制主要包括:相变动力学变差导致内阻在高电位下增加;材料内部结构发生巨大改变,其中的O3 结构消失;晶胞参数剧烈膨胀收缩使材料颗粒体积膨胀及收缩,同时颗粒变化还将导致电芯衰减;因为滑移相变是不完全可逆的,因此将导致容量电压的衰减。
1.4 材料表面的结构变化
因为材料表面存在悬挂键和不饱和的配位关系,反应活性明显高于体相。当对钴酸锂电池进行充电时,会发生以下过程:①正极材料自表面开始脱锂;②脱锂发生后,Li 层氧原子间失去阻隔产生排斥,导致表面结构不稳定;③持续脱锂促进表面晶格活性发生气体溢出;④溢出气体导致表面Co原子稳定性变差、溶解;⑤溶解的高价Co 元素也会氧化电解液参与电解液化学反应。而现在高电压钴酸锂应用所面临的最大困难是难以通过45 ℃的循环测试,期间会有大量的金属溶解、释放氧气以及材料发生的相变。

图2 层状材料表面结构演示图
1.5 电池正极材料的改进
提高充电电压后会使其发生一系列副反应,产生的CO2等气体会导致电池本身膨胀、漏液,更严重的则会发生火灾。目前主要有两个解决方法:着手电解液的研究或电池材料自身的完善,电解液的研究能够抑制电解液在材料界面反应或形成固态界面膜(SEI 膜);从材料本身出发,可以通过表面修饰以及表面包覆来隔断反应的进行。常用的包覆材料是氧化物类包覆材料,如MgO、TiO2、Al2O3、ZrO2、AlPO4、CoAl2O4。若利用Li2TiO3、Li1.3Al0.3Ti1.7(PO4)3、LiZr2(PO4)3这类锂离子导体包覆材料,能够有效地提升材料倍率性能[6]。
2 电解液的研究
电解液是制约锂离子电池发展的关键性因素,因此目前研究高电压电解液也是提高LiCoO2高电压下的电化学性能的重要途径之一。齐爱[7]通过添加剂对电解质物化性能的影响以及作用机理的研究发现噻吩(T)、2-甲基噻吩(DMT)、2-噻吩甲腈(TC)、苯并噻吩(BT)及一种高电压溶剂氟代碳酸乙烯酯(FEC)这类添加剂。采用量子化学计算、循环伏安法、交流阻抗、恒流充放电、材料表面形貌分析、成分分析、结构分析等方法研究添加剂以及高电压溶剂对LiCoO2在高电压下电化学性能的影响。
如果在电解液中添加噻吩(0.1%),LiCoO2高电压下的循环性能和高温性能会发生巨大改善,但是当电流过大时便会出现过冲现象。噻吩在4.3 V 发生氧化聚合,在正极材料表面形成低LiF致密的聚合噻吩膜,这样将阻止电解液持续氧化,减小循环后的电荷转移阻抗,同时形成的聚噻吩膜有利于Li+的脱嵌,同时噻吩对负极材料的循环性能没有不良影响。
LiDEOB 与BT 构成的复合添加剂共同参与正极表面成膜,有效提高首次效率,因此在保持优秀的循环性能的同时还提高了放电比容量。因此可以发现复合添加剂将会成为未来电解液研究的重要方向。但是它也存在一定的弊端,那就是会影响负极材料的循环性能。FEC 作为溶剂可以提高电解液的稳定性。FEC 分解的中间产物VC 能够在正极材料表面形成一层富含烷基锂盐的膜。LiF 含量降低,这就间接地减小了循环阻抗。因此含10%FEC 电解液能够显著提高电池的循环性能和倍率性能。
3 钴酸锂(LiCoO2)的制备
在锂电池的组成成分来看,正极材料是其中最为重要的组成部分,也是影响电池电化学性能的决定性因素。目前钴酸锂、磷酸铁锂、磷酸钒锂是最为常见的3 种正极材料。其中钴酸锂具有3.7 V 平均输出电压,它的能量密度有140 mAh·kg-1,并且具有良好的循环性能和良好的热稳定性。这些优点使得钴酸锂被认为是最具有发展前景的正极材料[8]。
LiCoO2的制备方法主要有:高温固相法、低温共沉淀法和凝胶法等,本文将主要介绍目前应用较多的高温固相法和浸出法。
3.1 高温固相法
目前合成技术比较成熟的是高温固相法,反应物选用钴的(碱式)碳酸盐或氧化物等与碳酸锂两种进行反应。将Li2CO3与CoCO3按n(Li)/n(Co)=1 的比例混合,然后在空气气氛下于700 ℃ 烧结而成;或将Co3O4与Li2CO3为原料,按化学计量比混合后在600 ℃烧结5 h,然后在900 ℃烧结10 h,可制得稳定的LiCoO2。热重曲线和XRD 物相分析表明,在200 ℃ 以上CoCO 开始分解生成Co3O4、Co2O3,300 ℃时其主体仍为Co3O4,在高于此温度的钴氧化物与Li2CO3进行固相反应生成LiCoO2[9]。
3.2 浸出法
浸出法是通过废弃钴酸锂中提取钴并制备钴酸锂,其具体实验流程为:首先用酸和还原剂将钴锂浸出,得到浸出液;然后利用化学法将浸出液中的Cu、Fe、Al、Ca、Mg 等杂质除去;利用碳酸盐沉淀的方法将钴锂沉淀并得到碳酸钴锂;将碳酸钴锂干燥,并且根据钴锂比配入相应的钴元素和锂元素;最后煅烧得到钴酸锂成品[10]。
4 钴酸锂(LiCoO2)材料的改性
通过目前的研究可知,对于钴酸锂材料的改性,目前应用较为广泛的方法是元素掺杂和表面包覆,当然二者协同作用将会起到更好的改良效果。掺杂、包覆以及复合改性在高电压钴酸锂正极材料的研究开发中起着越来越重要的作用,其中复合包覆以及复合改性将是高电压钴酸锂正极材料重点研究开发方向。运用不同的改性方法可以有效抑制钴酸锂在高电压下的结构变化,提升钴酸锂晶体结构的稳定性和界面稳定性,从而提高钴酸锂在高电压下的克比容量、热稳定性、循环稳定性和倍率性能,并使得锂离子电池各项性能得到改善,为更高电压钴酸锂正极材料的商业化打下坚实的基础[11]。
靳佳[6]等采用固相烧结法制备正极材料钴酸锂,并且采用异丙醇铝(AIP)对其表面进行包覆,通过电化学性能测试发现AIP 包覆可有效改善材料的循环性能,提高材料的放电比容量、库仑效率和倍率性能。
彭邦恒[12]等利用高温固相法对LiCoO2进行 Mg掺杂改性,稳定 LiCoO2结构,然后再通过球磨法对掺杂后的 LiCoO2进行石墨包覆,最后又采用磁控溅射技术对商用 LiCoO2电极片进行溅射包覆改性,从而提高其电化学性能。实验考察了不同Mg 掺杂浓度下LiCo(1-x)MgxO2的电化学性能。当掺杂浓度为x=0.02 时,获得的 LiCo0.98Mg0.02O2具有最优的循环性能,在4.5 V 截止电位下循环60 周后容量保持率为62.2%。石墨包覆Mg掺杂处理后的LiCo0.98Mg0.02O2循环性能优于 LiCoO2和石墨包覆 LiCoO2,循环60 周之后的比容量仍有146.15 mAh·g-1,容量保有率为78.7%,从而可以发现二者起到了协同作用。然后采用磁控溅射法对 LiCoO2极片进行了Li0.33La0.56TiO3(简写 LLTO)薄膜包覆处理,通过控制溅射时间,研究了最佳包覆厚度并探讨改性机理。LLTO 包覆层最佳厚度约 10 nm,此时 LiCoO2电极在 3~4.5 V 电压范围、0.2 C 条件下首周充放电比容量达184.61 mAh·g-1,循环80 周后其容量保有率为 71.9%。但他团队认为还需要寻找更加合适的包覆材料、掺杂元素或者二者的组合。
李春流[13]等首先采用固相烧结法,在不同烧结工艺的条件下对 LiCoO2进行纳米级钛白粉、氢氧化铝和氢氧化镁表面复合包覆,在充放电 3.0~4.35 V电压区间,以 0.5、1.0 C 放电,复合包覆改性钴酸锂的比容量、平台率和循环性能都有明显的提高。
张杰男[5]等通过利用Ti、Mg、Al 痕量共掺杂的方法对钴酸锂在高电压 (4.6 V)下的电化学循环性能进行了优化改性,因为Al 元素能够提高材料在电化学循环过程中的稳定性,Mg 元素可以提高材料的电子电导,Ti 元素能够提高材料的首周效率与放电比容量,3 种元素的掺杂对于材料的影响相辅相成,且互不影响。同时,掺杂元素能够显著提高材料表面阴离子的稳定性,从而提高材料在高电压循环下的稳定性。
5 结束语
在对钴酸锂材料作为正极的40年研究进程中可以发现LiCoO2中近 70%的Li 可在最先进的锂离子电池中可逆使用。能否继续提高Li 的利用率呢?可使用Li 的实际上限和分层 LCO 的工作电压是什么?这些问题都是未来对于钴酸锂的着重研究内容。此外,还需要对不同掺杂元素的实际工作机制进行定量评价。LCO 通常还需要高级功能电解质才能形成稳定的阴极电解质(CEI)。显然,未来采用新型添加剂和分子组装在LCO 上设计稳定的CEI,需要借助先进的光谱技术进行更精确的控制和定量表征。未来对于高能量密度LIB 的应用有两点是非常重要的,第一是固态电解质将会逐渐被应用于锂电中,要么用作LCO 的涂层材料,要么用更少的有机溶剂提高电解质的离子电导率;第二则是利用其他新开发的分层阴极材料,如富镍的NCM 来代替LCO。此外,石墨阳极向含硅或含锂阳极的转换将成为主要发展趋势。在未来对其研究和改善后,LCO的理论容量以及工作电压限制都将得到质的改善。当然这些问题都要在漫长的科研道路上不断探索才能实现的[14]。
