废旧锂电池正极材料剥离工艺研究
2020-05-07游孟醒
刘 宇, 徐 军, 王 翔, 游孟醒
(1.四川长虹电器股份有限公司, 四川 绵阳 621000; 2.清华大学 机械工程系, 北京 100084)
0 引言
锂离子电池(LIB)是目前综合性能最好的电池体系,具有高比能量、高循环寿命、体积小、质量轻、无记忆效应、无污染等特点,并迅速发展成为新一代储能电源,用于信息技术、电动车和混合动力车、航空航天等领域的动力支持。 钴、锂等作为生产锂离子电池的原材料,在自然界中蕴藏很少。 钴是资源稀少、价格较贵的金属,绝大多数是伴生矿,主要伴生在铁、铜、镍等矿床中,开发难度大且品位低,其平均品位仅为0.02%。 各国金属钴主要靠从金属冶炼过程中提取以及从废旧含钴材料中回收。 我国的钴资源比较稀缺,地质储量约87 万吨,但是贫矿多,独立成矿的钴矿物仅占5%,每年需从国外进口钴约1000~1200 吨。 因此,对废旧锂电池的正极材料的回收有着十分重要的意义。
废旧锂电池结构主要包括正极、负极、电解质、外壳、隔膜组成,其中待回收部分主要是正极材料,包括钴酸锂及其他锂三元化合物,废旧电池中钴的回收目前主要工艺包括预处理、正极材料处理、浸出等工序[1]。其中,废旧锂电池的预处理的目的是将电池中的正极、 负极、 电解质、外壳、隔膜各组分进行分离,同时消除电池中化学品的活性[2]。 其中正极材料与铝箔的分离对金属钴和锂的回收有着直接影响,因此本文采用实验的方式对废旧锂电池正极材料的剥离工艺进行了研究,对破碎后经过水浮选的正极材料采用酸性和碱性搅拌剥离的剥离率进行了研究。
1 水洗浮选分离
将机械破碎后的废旧锂离子电池置于孔径为0.63mm 的筛网中,然后将筛网和电池一起放入水中,浮选时有少量电解质挥发的气味,有气泡产生,大部分的有机隔膜浮在水面,用刮板将其刮除,剩下的少量有机隔膜与金属夹杂在一起没有浮起, 电池塑料外壳与金属混杂在一起。 浮选前后的电池如图1 所示。
从图1 可以看出,经过浮选,废旧锂离子电池中的有机隔膜已经基本被除去,浮选效果良好。

图1 锂离子电池浮选前后照片(左:浮选前,右:浮选后)Fig.1 Photos of lithium-ion battery before and after flotation(left:before flotation,right:after flotation)
通过浮选可以在溶液表面分离有机隔膜,同时使电解液中的六氟磷酸锂和大部分有机溶剂进入水中,能抑制六氟磷酸锂的分解和有机溶剂的挥发,使得操作环境大为改善;除此之外,有机隔膜被浮选除去后,使得溶液的过滤性能得到极大的改善,抽滤时间从57min 缩短至6min,能够快速的将其过滤;机械破碎后的电池经水中振动筛分可以将铜箔表面的碳粉剥离下来,同时也有21.4%的钴酸锂从铝箔上脱落,剩余的钴酸锂粉末仍然残留在铝箔上。
2 酸性溶液下的剥离分离
采用实验研究的方式,研究温度、搅拌方式和硫酸浓度对钴酸锂剥离率的影响。
2.1 温度和搅拌方式对钴酸锂剥离率的影响
称取一定量的破碎后的正极材料 (粘附有钴酸锂的铝箔),按固液比1g:50mL 加入0.5mol/L 的H2SO4,以磁力加热搅拌器搅拌辅助剥离钴酸锂。 在不同温度下获得的实验结果如表1 所示。
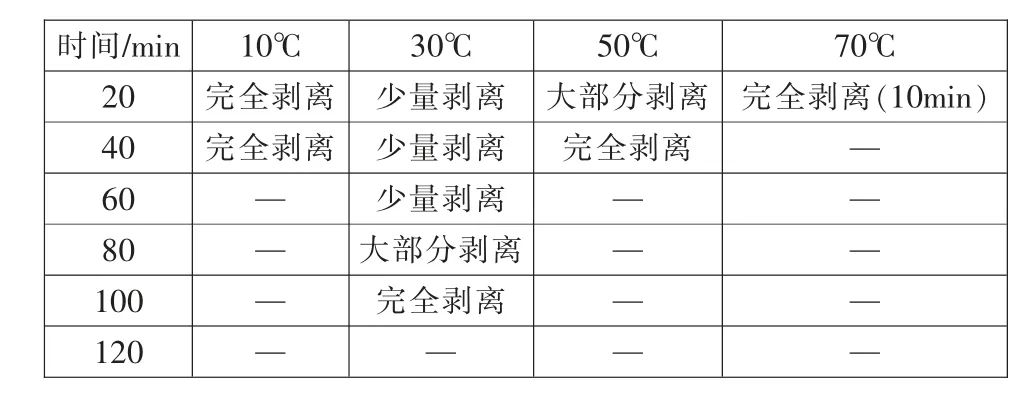
表1 样品在硫酸介质中搅拌剥离情况Tab.1 Stripping of samples by stirring in sulfuric acid medium
称取一定量的正极材料 (粘附有钴酸锂的铝箔),按固液比1g:50mL 加入0.5mol/L 的H2SO4,以40kHz 超声波辅助剥离钴酸锂。 在不同温度下的实验结果如表2 所示。
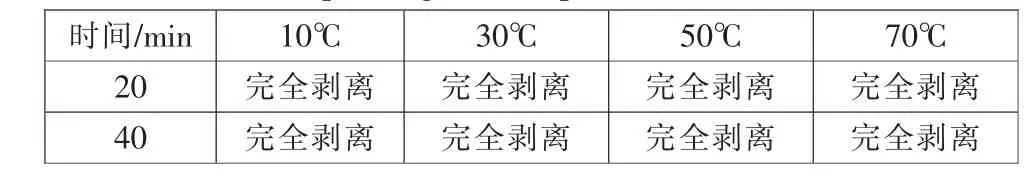
表2 样品在硫酸介质中超声波剥离情况Tab.2 Ultrasonic peeling of samples in sulfuric acid medium
实验用硫酸的浓度为0.5mol/L,即pH 值为0,固液比1g:50mL,剥离后溶液的pH 值约为0.5,对比以上实验结果可知:
(1)在硫酸介质中,约10℃的室温条件下,使用搅拌或超声波剥离钴酸锂的效果都较好;且温度越高,钴酸锂剥离时间越短,当温度升高到50℃时,在20min 内钴酸锂已完全剥离,继续升高温度对缩短剥离时间的影响已不明显。
(2)在稀硫酸介质中使用搅拌或超声波能加速铝箔表面的钴酸锂剥离,在室温(约10℃)下,20min 即可达到非常良好的效果。
2.2 硫酸溶液浓度对剥离影响
在室温(约20℃)、剥离时间为20min 的条件下,考察硫酸的浓度对钴酸锂剥离效果的影响, 硫酸浓度分别为0.1mol/L、0.2mol/L、0.3mol/L、0.4mol/L、0.5mol/L,在剥离的同时使用超声波,剥离实验之后过滤并取滤渣,用王水溶解滤渣,ICP 定量分析滤液和滤渣中钴的含量。 实验结果如表3 所示。

表3 硫酸浓度对钴酸锂剥离的影响Tab.3 The effect of sulfuric acid concentration on the stripping of lithium cobaltite
由表3 的结果可知,当硫酸浓度为0.4mol/L 时,Co 的剥离效率最高为68.9%,结合浮选分离结果,破碎后的电池在水中振动浮选筛分时钴酸锂的剥离率为21.4%,因此经破碎-振动筛分-稀硫酸剥离后, 钴酸锂总的剥离率为90.3%(钴酸锂的剥离率包括两部分: 水中剥离率21.4%,稀硫酸中剥离率68.9%)。 硫酸浓度从0.1mol/L 增加到0.5mol/L 时, 约有24%~29%钴酸锂溶于硫酸中;实验结果表明, 在剥离过程中钴酸锂容易被硫酸浸出进入溶液,造成剥离下来的钴酸锂粉末大量损失。 剥离钴酸锂后的铝箔表面的SEM 图像 和 能 谱(EDS)分析结果分别如图2、图3 和表4所示:

图2 铝箔表面SEM 图(左:剥离前,右:剥离后)Fig.2 SEM of aluminum foil surface(left:before stripping,right:after stripping)
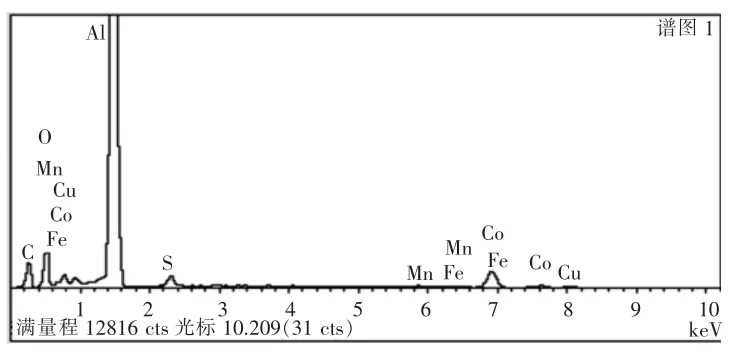
图3 铝箔表面EDS 图谱Fig.3 EDS Atlas of aluminum foil surface
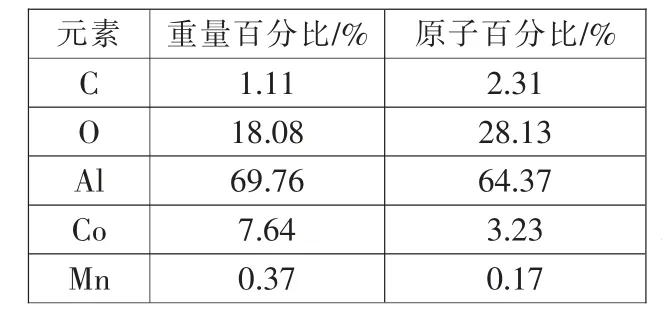
表4 EDS 分析结果Tab.4 EDS analysis results
从图2中对比剥离前后铝箔表面发现,经过稀硫酸剥离后,铝箔表面的钴酸锂除了少量残留在铝箔上外, 大部分被剥离下来;从图3 和表4中的EDS 分析结果可知, 经硫酸处理后,还有7.64%的钴酸锂残留在铝箔上,钴酸锂的剥离率大于92%,与ICP 分析测试的结果相近(ICP 测试结果为90.3%)。 表4 中O 的含量比较高,其原因在于Al 箔表面在空气中被氧化,生成了Al2O3。
在室温(约20℃)下,用稀硫酸剥离钴酸锂的最佳条件为:硫酸浓度0.4mol/L,固液比1g:50mL,超声波频率40kHz,时间20min,钴酸锂总的剥离率大于90.3%。
3 碱性环境下剥离
每次称取5g 经机械破碎、水中振动筛分的废旧锂离子电池作为实验样品, 与氢氧化钠溶液按固液比为1g:50mL 加入到烧杯中,设计氢氧化钠溶液浓度、温度的单因素实验, 观察剥离的效果, 确定钴酸锂的最佳剥离条件,计算钴酸锂的剥离率。其中温度为室温(约20℃)和冰浴(约0℃,模拟冬季气温)。
3.1 温度、氢氧化钠浓度对钴酸锂剥离的影响
氢氧化钠的浓度分别为0.5%、1%、2%、3%和5%,在室温(20℃)下边搅拌边反应,记录钴酸锂完全剥离的时间,实验结果如表5 所示。
氢氧化钠的浓度分别为0.5%、1%、2%、3%和5%,溶液在冰浴中边搅拌边反应,记录钴酸锂完全剥离的时间,实验结果如表6 所示。
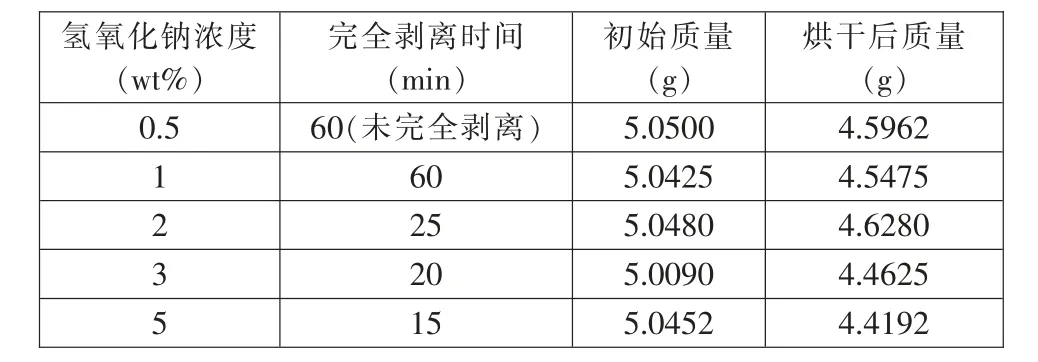
表5 不同氢氧化钠浓度下钴酸锂剥离情况(室温,约20℃)Tab.5 Stripping of lithium cobaltite with different sodium hydroxide concentration
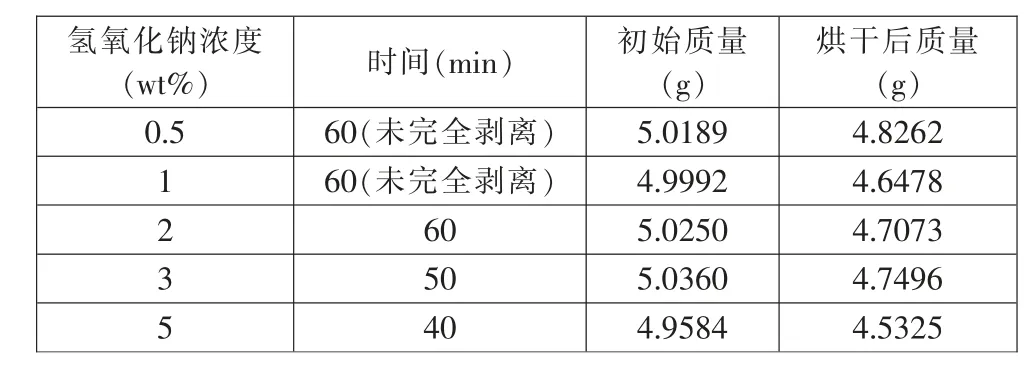
表6 不同氢氧化钠浓度下钴酸锂剥离情况(冰浴,约0℃)Tab.6 Stripping of lithium cobaltite under different sodium hydroxide concentrations(ice bath,about 0 ℃)
从表5 可以看出,室温(约20℃)下,随着氢氧化钠浓度的增加,钴酸锂完全剥离的时间减少。当氢氧化钠浓度为0.5%时,搅拌剥离60min 后,钴酸锂仍未被完全剥离,氢氧化钠浓度从1%增加到5%时, 钴酸锂完全剥离的时间从60min 缩短为15min;从表6 可知,溶液在冰浴(约0℃)中,随着氢氧化钠浓度的增加,钴酸锂完全剥离的时间也逐渐减少,但时间的变化不如室温(约20℃)下明显,当氢氧化钠浓度低于1%时,搅拌剥离60min 后,钴酸锂仍未被完全剥离,氢氧化钠浓度从2%增加到5%时,钴酸锂完全剥离的时间从60min 缩短为40min。结合表5 和表6 可知,相同氢氧化钠浓度下,溶液在冰浴(约0℃)中钴酸锂完全剥离的时间约为室温(约20℃)下钴酸锂完全剥离的时间的2.5 倍。
3.2 钴酸锂剥离效率
将剥离完钴酸锂的氢氧化钠溶液过滤,滤渣烘干过筛,筛分出铜箔和铝箔的混合物, 将铜箔和铝箔的混合物溶于40mL 的王水中,过滤后定容到500mL 用ICP 检测未被剥离的Co 的量,计算钴酸锂的剥离率。 结果如表7 和表8 所示。

表7 室温(约20℃)下钴酸锂的剥离效率Tab.7 Stripping efficiency of lithium cobaltite at room temperature(about 20 ℃)
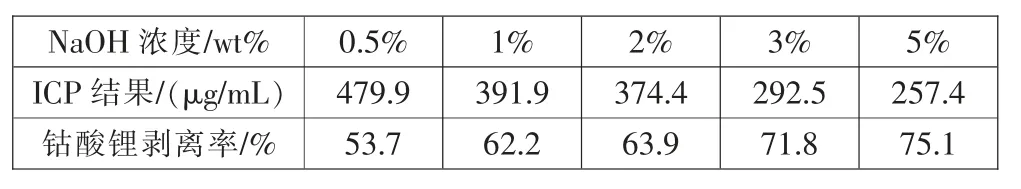
表8 冰浴(约0℃)中钴酸锂的剥离效率Tab.8 Stripping efficiency of lithium cobaltite in ice bath(about 0 ℃)
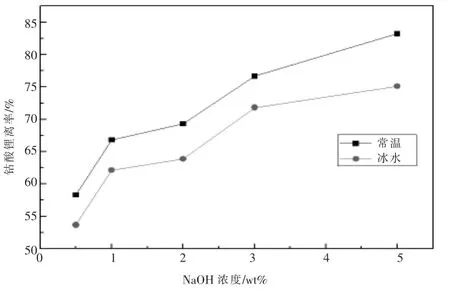
图4 钴酸锂在氢氧化钠溶液中的剥离效率Fig.4 Stripping efficiency of lithium cobaltite in sodium hydroxide solution
从表7 和表8 以及图4可知:氢氧化钠的浓度越高,钴酸锂剥离的时间越短,钴酸锂的剥离效率也越高。 室温(约20℃)下,当氢氧化钠浓度从0.5%增加到5%时, 钴酸锂的剥离效率从58.3%上升到83.2%;溶液在冰浴(约0℃)中,当氢氧化钠浓度从0.5%增加到5%时,钴酸锂的剥离效率从53.7%上升到75.1%。 破碎后的电池在经过浮选分离钴酸锂的剥离率为21.4%,当氢氧化钠浓度为3%和5%时,室温(约20℃)下钴酸锂总的剥离率分别为98.1%和104.6%,冰浴(约0℃)中钴酸锂总的剥离率分别为93.2%和96.5%(钴酸锂的剥离率包括两部分:水中的剥离率21.4%和氢氧化钠中的剥离率)。其中氢氧化钠浓度为5%时,室温(20℃)下钴酸锂总的剥离率大于100%,其原因主要有两个,一是分析检测时仪器引起的误差,二是锂电池品牌繁多,品牌之间成分各异,造成实验样品组分不均一。
用SEM 和能谱(EDS)对剥离钴酸锂后的铝箔表面进行分析,结果如图5、图6 和表9 所示:
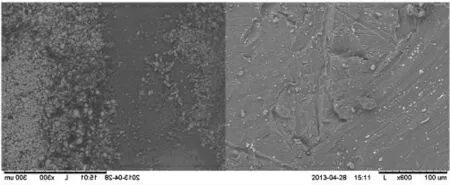
图5 铝箔表面SEM 图(左:剥离前,右:剥离后)Fig.5 SEM of aluminum foil surface(left:before stripping,right:after stripping)
从图5 中对比剥离前后铝箔表面发现, 经过氢氧化钠剥离后,铝箔表面的钴酸锂除了少量残留在铝箔上外,基本都被剥离下来; 从图6 和表9 中的EDS 分析结果可知,经氢氧化钠处理后,有1.99%的钴酸锂残留在铝箔上,钴酸锂的剥离率大于98%, 与ICP 分析测试的结果吻合(ICP 测试结果为98.1%)。 表9中O 的含量比较高,原因是Al 箔表面在空气中被氧化,生成了Al2O3。
从实验结果来看,当氢氧化钠浓度增加到3%时, 室温(20℃) 下 钴 酸锂总的剥离率达到98.1%,冰浴(0℃)中钴酸锂总的剥离率也达到了93.2%,已能够满足剥离钴酸锂的需求,因此用氢氧化钠剥离钴酸锂的最佳浓度为3%。
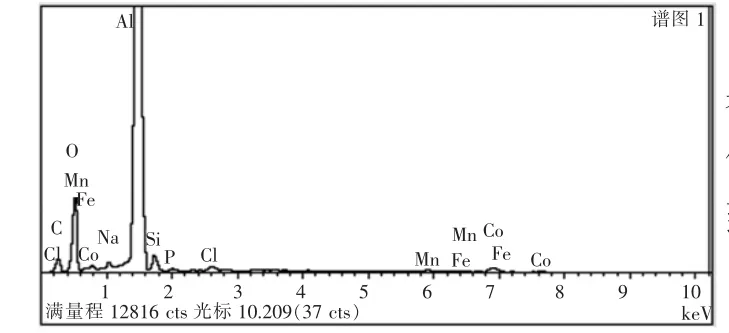
图6 铝箔表面EDS 图谱Fig.6 EDS Atlas of aluminum foil surface
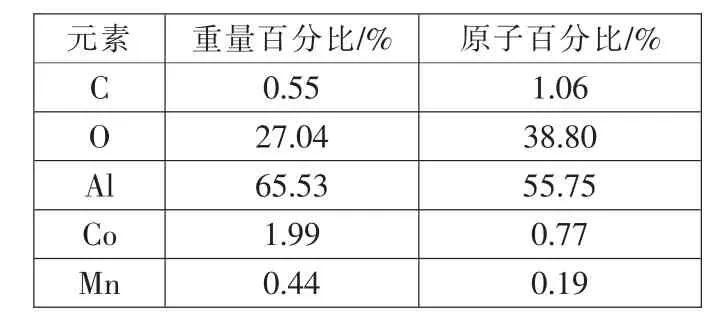
表9 EDS 分析结果Tab.9 EDS analysis results
3.3 铝箔溶解率
将剥离完钴酸锂的氢氧化钠溶液过滤, 取滤液定容到500mL,用ICP 检测滤液中Al 的含量,计算铝箔的溶解率。 结果如表10 和表11 所示。
由表10 和表11 及图7 可知: 铝箔的溶解率随着氢氧化钠浓度的升高而升高,室温(约20℃)下,当氢氧化钠的浓度从0.5%增加到5%的过程中, 铝箔的溶解率从47.3%上升到69.6%;溶液在冰浴(约0℃)中,当氢氧化钠的浓度从0.5%增加到2%的时候,铝箔的溶解率从20.2%上升到40.7%,继续增加氢氧化钠浓度至3%时,铝箔的溶解率下降至31.9%,当氢氧化钠浓度增加到5%时,铝箔溶解率又上升至53.2%。 冰水中,当氢氧化钠浓度为2%和3%时,铝箔溶解率突然上升,然后又下降的原因可能是实验用的样品不均匀以及分析测试时产生的误差。结合钴酸锂的剥离效率来看,铝箔的溶解率越高,钴酸锂的剥离效率越高。 氢氧化钠剥离钴酸锂时直接通过浸蚀铝箔,导致钴酸锂从铝箔上脱落,以此达到剥离钴酸锂的目的。
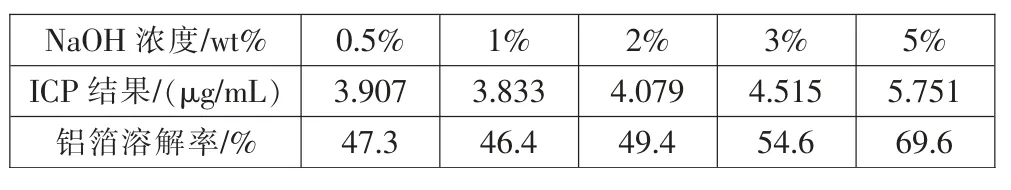
表10 室温(约20℃)下铝箔溶解率Tab.10 Dissolution rate of aluminum foil at room temperature(about 20 ℃)
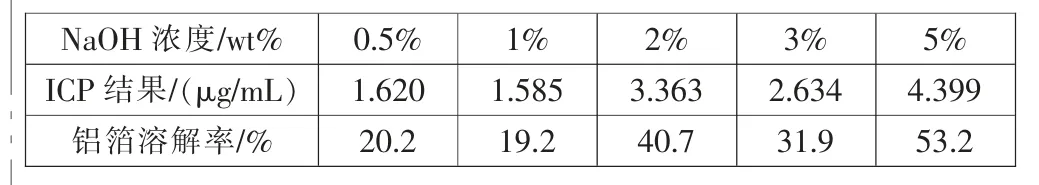
表11 冰浴(约0℃)中铝箔溶解率Tab.11 Dissolution rate of aluminum foilin ice bath(about 0℃)
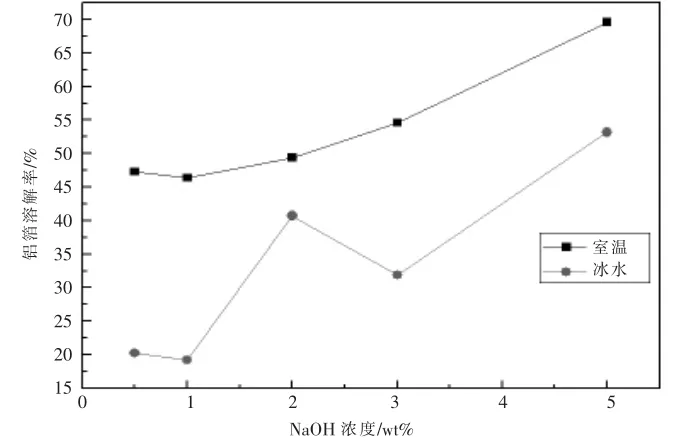
图7 铝箔在氢氧化钠溶液中的溶解率Fig.7 Solubility of aluminum foil in sodium hydroxide solution
4 结论
对废旧钴酸锂正极材料钴酸锂的剥离工艺进行了研究,研究发现,在碱性溶液氢氧化钠的搅拌剥离的剥离率大于酸性溶液。 同时,钴酸锂的剥离率和铝箔的溶解率都随着氢氧化钠浓度的升高而升高,温度的升高也有利于钴酸锂的剥离。氢氧化钠的最佳浓度为3% ,在此浓度、搅拌、室温(约20℃)条件下,钴酸锂总的剥离率可达98.1%,铝箔溶解率为54.6%;冰浴(约0℃)中钴酸锂总的剥离率可达93.2%,铝箔溶解率为31.9%。
