小分子GLP-1R激动剂对骨质疏松模型小鼠的改善作用
2021-03-02周颖王宁陈周刘焕李汾魏明李萍
周颖 王宁 陈周 刘焕 李汾 魏明 李萍

摘 要 目的:探討小分子胰高血糖素样肽1受体(GLP-1R)激动剂6,7-二氯-2-磺酰烷基-3-仲烷氨基喹喔啉(DMB)对骨质疏松模型小鼠的改善作用。方法:将C57BL/6J小鼠随机分为假手术组、模型组、阳性对照组(17β-雌二醇,10 μg/kg)和DMB组(1 mg/kg),每组10只。假手术组小鼠行双侧剖腹术但不摘除卵巢,其余各组小鼠行双侧卵巢切除术以复制骨质疏松模型。术后第4周,假手术组、模型组小鼠灌胃等体积橄榄油,各给药组小鼠灌胃相应药物,每日1次,连续8周。末次给药后,采用计算机断层扫描(Micro-CT)仪检测各组小鼠股骨骨微结构、骨矿密度(BMD)、骨矿含量(BMC)及骨形态参数[骨组织体积分数(BV/TV)、骨小梁厚度(Tb.Th)、骨小梁数(Tb.N)和骨小梁间距(Tb.Sp)];采用酶联免疫吸附试验法检测各组小鼠血清中骨形成指标[骨特异性碱性磷酸酶(BALP)、骨保护素(OPG)]和骨吸收指标[抗酒石酸酸性磷酸酶(TRAP)和Ⅰ型胶原蛋白C末端交联肽(CTX-Ⅰ)]的表达水平;采用三点弯曲试验法检测各组小鼠股骨的生物力学参数(最大载荷、刚度、应力和杨氏模量)。结果:假手术组小鼠股骨的骨小梁数量多、壁厚、形态结构完整、排列紧密有序、呈网状,骨微结构和骨量正常。与假手术组比较,模型组小鼠股骨的骨小梁数量减少、厚度变薄、扭曲或断裂,且骨小梁间隙增大,骨微结构恶化,骨量减少;BMD、BMC、BV/TV、Tb.Th、Tb.N和股骨的生物力学参数均显著降低,Tb.Sp和血清中BLAP、OPG、TRAP、CTX-Ⅰ水平均显著升高(P<0.05或P<0.01)。与模型组比较,阳性对照组和DMB组小鼠骨量增加,骨小梁数量、厚度、形态等部分恢复;BMD、BMC、BV/TV、Tb.Th、Tb.N和股骨的生物力学参数均显著升高(P<0.05或P<0.01),Tb.Sp和血清中BLAP、OPG水平均显著升高(P<0.01),TRAP、CTX-Ⅰ水平均显著降低(P<0.05或P<0.01)。结论:DMB可通过增加骨量、改善骨微结构、升高骨形成相关指标的表达和骨生物力学参数以及降低骨吸收相关指标的表达,来发挥改善小鼠骨质疏松的作用。
关键词 6,7-二氯-2-磺酰烷基-3-仲烷氨基喹喔啉;胰高血糖素样肽1受体;受体激动剂;骨质疏松症;小鼠
中图分类号 R965 文献标志码 A 文章编号 1001-0408(2021)03-0284-05
DOI 10.6039/j.issn.1001-0408.2021.03.06
ABSTRACT OBJECTIVE: To explore the improvement effects of small-molecule glucagon-like peptide-1 receptor (GLP-1R) agonists (6,7-dichloro-2-methylsulfonyl-3-N-tert-butylaminoquinoxaline, DMB) on osteoporosis model mice. METHODS: C57BL/6J mice were randomly divided into sham operation group, model group, positive control group (17β-estradiol, 10 μg/kg) and DMB group (1 mg/kg), with 10 mice in each group. The sham operation group received bilateral laparotomy without ovariectomy, and the other groups received bilateral ovariectomy to reproduce the osteoporosis model. At 4th week after operation, sham operation group and model group were given constant volume of olive oil intragastrically; administration groups were given relevant medicine intragastrically, once a day, for consecutive 8 weeks. After last medication, Micro-CT was used to detect the femur microstructure, bone mineral density (BMD), bone mineral content (BMC) and bone morphometric parameters [bone tissue volume ratio (BV/TV), trabecular thickness (Tb.Th), trabecular number (Tb.N) and trabecular spacing (Tb.Sp)]. ELISA assay was used to detect the expression of bone formation indexes [bone specific alkaline phosphatase (BALP), osteoprotegerin (OPG)] and bone resorption indexes [tartrate resistant acid phosphatase (TRAP) and C-terminal cross-linked telopeptides of type Ⅰ collagen (CTX-Ⅰ)]. Three-point bending test was used to detect biomechanical parameters (maximum load, stiffness, stress and Youngs modulus) of femur of mice in each group. RESULTS: In sham operation group, trabeculae were numerous, thick, complete in morphological structure, well-organized and reticular; bone microstructure and bone mass were normal. Compared with sham operation group, the number of trabecular bone decreased, the thickness became thinner, twisted or broken, and the trabecular space increased; the bone microstructure deteriorated and the bone mass decreased; BMD, BMC, BV/TV, Tb.Th, Tb.N and biomechanical parameters of femur were decreased significantly, while Tb.Sp and serum levels of BLAP, OPG, TRAP and CTX-Ⅰ were increased significantly in model group (P<0.05 or P<0.01). Compared with model group, the bone mass of positive control group and DMB group were increased, while the number, thickness and shape of trabecular bone partially recovered; BMD, BMC, BV/TV, Tb.Th, Tb.N and biomechanical parameters of femur were increased significantly (P<0.05 or P<0.01); Tb.Sp, serum levels of BLAP and OPG were increased significantly (P<0.01), while the levels of TRAP and CTX-Ⅰ were decreased significantly (P<0.05 or P<0.01). CONCLUSIONS: DMB can improve osteoporosis by increasing bone mass, improving bone microstructure, increasing the expression of bone formation related indexes and biomechanical parameters and decreasing bone resorption related indexes.
KEYWORDS 6,7-dichloro-2-methylsulfonyl-3-N-tert-butylaminoquinoxaline; Glucagon-like peptide-1 receptor; Receptor agonist; Osteoporosis; Mice
相关研究发现,肠促激素胰高血糖素样肽1(GLP-1)及其受体(GLP-1R)可参与成骨细胞和破骨细胞的分化与功能调节,影响机体骨代谢平衡[1-2],故GLP-1R激动剂已成为治疗骨质疏松的候选药物。然而,骨质疏松是一种慢性的、老年性疾病,患者需要长时间使用药物进行治疗[3]。现有的天然GLP-1及肽类GLP-1R激动剂的稳定性差、制备困难且价格昂贵,加之需要注射给药,使得其临床应用受到一定限制[4-5]。6,7-二氯-2-磺酰烷基-3-仲烷氨基喹喔啉(6,7-dichloro-2- methylsulfonyl-3-N-tert-butylaminoquinoxaline,DMB)是一种小分子GLP-1R激动剂,其合成工艺简单、稳定性好、可口服,体内外研究均提示其具有降糖活性[6-7];另有研究发现,其还能促进内源性GLP-1与其受体结合,增强GLP-1的体内活性[7]。本课题组前期预实验结果显示,DMB可显著降低去卵巢诱导的骨质疏松模型小鼠的骨吸收标志物水平,并上调骨形成标志物水平。然而,DMB是否与肽类激动剂类似,可参与骨代谢的调节,目前尚未见相关研究报道。基于此,本研究探讨了DMB对骨质疏松模型小鼠骨微结构、骨矿密度(BMD)、骨矿含量(BMC)、骨形态参数、骨形成和骨吸收相关指标及骨生物力学参数的影响,以期为小分子GLP-1R激动剂治疗骨质疏松症提供参考依据。
1 材料
1.1 主要仪器
本研究所用的主要仪器有:AL104型万分之一电子天平(瑞士 Mettler Toledo 公司)、SmarT-R17型高速冷冻离心机(韩国Hanil公司)、ELx800型全自动酶标仪(美国BioTek公司)、Inveon型微计算机断层扫描(Micro- CT)仪(德国Siemens公司)、MTS BioNix 858 Ⅱ型万能材料测试仪(美国MTS公司)。
1.2 主要药品与试剂
本研究所用的主要药品与试剂有:DMB对照品(北京亿思研科技开发中心,纯度≥98%),戊巴比妥钠原料药、17β-雌二醇(E2)原料药(美国Sigma公司,批号分别为127K1005、E-8875,纯度均不低于98%),RNA微量提取试剂盒(美国Promega公司,批号Z3100),逆转录试剂盒、SYBR Premix Ex Taq酶(日本TaKaRa公司,批号分别为BK1501、AKA906),橄榄油(国药集团化学试剂有限公司,批号20170422),血清骨特异性碱性磷酸酶(BALP)酶联免疫吸附试验(ELISA)试剂盒(上海远慕科技有限公司,批号20180124),抗酒石酸酸性磷酸酶(TRAP)ELISA试剂盒(上海酶联生物科技有限公司,批号180223),骨保护素(OPG)ELISA试剂盒(深圳子科生物科技有限公司,批号181031),Ⅰ型胶原蛋白C末端交联肽(CTX-Ⅰ)ELISA试剂盒(南京信帆生物技術有限公司,批号180411),去离子水;其余试剂均为分析纯或实验室常用规格。
1.3 动物
本研究所用的动物为SPF级雌性C57BL/6J小鼠,6周龄,体质量为13~15 g,由空军军医大学实验动物中心提供,动物生产许可证号为SCXK(陕)2014-002。所有小鼠均饲养于温度(21±2) ℃、相对湿度50%、12 h光暗交替的环境下,并自由进食、饮水。
2 方法
2.1 分组、造模与给药
将小鼠适应性喂养1周后,取40只腹腔注射戊巴比妥钠(40 mg/kg)进行麻醉,然后分为假手术组、模型组、阳性对照组(E2,10 μg/kg)和DMB组(1 mg/kg),每组10只。其中,假手术组小鼠行双侧剖腹术但不摘除卵巢,其余各组小鼠行双侧卵巢切除术以复制骨质疏松模型。术后第4周,阳性对照组和DMB组小鼠灌胃相应药物溶液10 mL/kg(以橄榄油为溶剂配制,剂量参考文献[7]及本课题组前期预实验结果),假手术组和模型组小鼠灌胃给予等体积橄榄油,每日1次,连续给药8周。
2.2 小鼠股骨骨微结构、BMD、BMC和骨形态参数检测
各组小鼠末次给药后,腹腔注射戊巴比妥钠(40 mg/kg)进行麻醉,并通过Micro-CT仪扫描其股骨的微结构,并导出图片;然后采用Inveon Research Workplace 2.2软件分析扫描数据并进行三维(3D)重建小鼠股骨干骺端,获取小鼠股骨的BMD、BMC和骨形态参数[包括骨组织体积分数(BV/TV)、骨小梁厚度(Tb.Th)、骨小梁数(Tb.N)和骨小梁间距(Tb.Sp)]。
2.3 小鼠血清中骨形成和骨吸收指标检测
采用ELISA法进行检测。“2.2”项实验结束后,各组小鼠摘眼球取血适量,于4 ℃下以3 000 r/min离心20 min,分离血清。采用酶标仪检测各组小鼠血清中骨形成指标(BALP、OPG)和骨吸收指标(TRAP、CTX-Ⅰ)的水平,严格按照相应试剂盒说明书方法操作。
2.4 DMB对骨质疏松模型小鼠股骨骨生物力学参数的影响考察
采用三点弯曲试验法进行检测。各组小鼠取血后脱颈椎法处死,剥离股骨,并用浸有生理盐水的纱布包裹,于-80 ℃冻存。临检测时,将股骨样品解冻1 h后,置于万能材料测试仪的支架上(跨距设置为10 mm),向股骨施加载荷(速度设置为1.2 mm/min)直到骨折;然后采用Test Star Ⅱ软件绘制小鼠股骨载荷-变形曲线,并分析其最大载荷、刚度、应力和杨氏模量等骨生物力学参数。
2.5 统计学方法
使用GraphPad Prism 5软件对数据进行统计分析。计量资料以x±s表示,组间比较采用方差分析。P<0.05表示差异有统计学意义。
3 结果
3.1 DMB对骨质疏松模型小鼠股骨骨微结构的影响
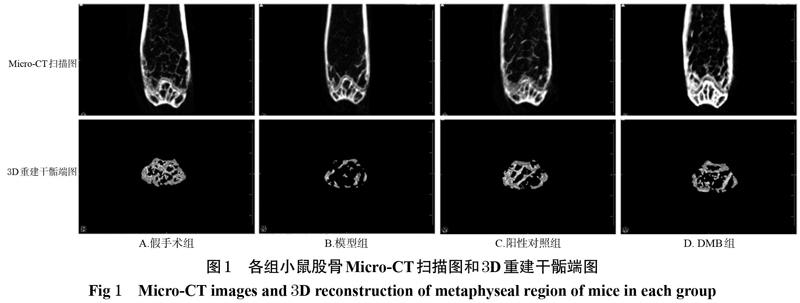
假手术组小鼠股骨的骨小梁数量多、壁厚、形态结构完整、排列紧密有序、呈网状,骨微结构和骨量正常;与假手术组比较,模型组小鼠股骨的骨小梁数量减少、厚度变薄、出现扭曲或断裂,且骨小梁间隙增大,骨微结构恶化,骨量减少;与模型组比较,阳性对照组和DMB组小鼠骨量增加,骨小梁数量、厚度、形态等部分恢复,详见图1。
3.2 DMB对骨质疏松模型小鼠股骨BMD、BMC和骨形态参数的影响
与假手术组比较,模型组小鼠的BMD、BMC、BV/TV、Tb.Th、Tb.N均显著降低,Tb.Sp显著升高(P<0.05或P<0.01);与模型组比较,阳性对照组和DMB组小鼠的BMD、BMC、BV/TV、Tb.Th、Tb.N均显著升高(P<0.05),Tb.Sp显著降低(P<0.05),详见表1。
3.3 DMB对骨质疏松模型小鼠血清中骨形成和骨吸收指标的影响
与假手术组比较,模型组小鼠血清中的BALP、OPG、TRAP、CTX-Ⅰ水平均显著升高(P<0.05或P<0.01);与模型组比较,阳性对照组和DMB组小鼠血清中BALP、OPG水平均显著升高(P<0.01),TRAP、CTX-Ⅰ水平均显著降低(P<0.05或P<0.01),详见表2。
3.4 DMB对骨质疏松模型小鼠股骨骨生物力学的影响
与假手术组比较,模型组小鼠股骨的最大载荷、刚度、应力、杨氏模量均显著降低(P<0.01);与模型组比较,阳性对照组和DMB组小鼠股骨的上述骨生物力学指标均显著升高(P<0.05),详见表3。
4 讨论
目前,肽类GLP-1R激动剂如艾塞那肽、利拉鲁肽、索马鲁肽等,主要用于2型糖尿病的临床治疗,其给药方式主要是皮下或肌内注射,但患者使用不便且依从性很差[5,8]。虽然在2019年9月索马鲁肽的口服制剂被批准上市,但是其药物剂量约是皮下注射剂量的数十倍,且价格非常昂贵[9]。现有GLP-1R激动剂中,根据化学结构可分为一氧二氮杂蒽类、硝基吡唑类、喹喔啉硫醚类、亚胺噻唑烷酮类、环丁烷类和喹喔啉类等,体外研究显示,一氧二氮杂蒽类、硝基吡唑类和喹喔啉硫醚类化合物均能与GLP-1R竞争性结合[10],但尚无体内活性的研究报道。此外,亚胺噻唑烷酮类化合物本身并无任何活性,但当其与GLP-1R结合后,可增加GLP-1的生物活性[10-11];环丁烷类化合物(如Boc5)虽然具有体内降糖活性,但是其合成制备工艺复杂[11],因此开发价值有限;喹喔啉类化合物DMB可通过激活GLP-1R,促进胰岛细胞系分泌胰岛素和改善正常小鼠糖耐量,同时还可增加GLP-1对其受体的亲和力[6-7],具有一定的开发潜力。
研究发现,GLP-1及其受体的信号转导通路参与了骨代谢过程[12-14],如GLP-1受体激动剂可通过激活胰岛素样生长因子1/磷脂酰肌醇3-激酶/蛋白激酶B(IGF-1/ PI3K/Akt)信号通路,促进大鼠衰老成骨细胞的增殖[12];利拉鲁肽可刺激小鼠前成骨细胞MC3T3-E1或人骨髓基质细胞向成骨细胞的分化[13];GLP-1(7-36)酰胺和艾塞那肽对骨吸收均具有抑制作用[13]。但小分子GLP-1R激动剂DMB是否也参与骨代谢的调节尚不明确。
经双侧卵巢切除术建立的模型小鼠是研究中老年女性绝经后骨质疏松较好的动物模型[15]。有研究指出,骨质疏松患者由于生理性骨转换功能的改变,会降低骨骼中BMC的水平,从而增加骨折的风险[16];BMD可反映骨质疏松的程度,也是预测骨折风险的重要依据之一[4];此外,骨微结构的恶化也是导致骨强度下降和骨折风险增加的重要因素[3]。BALP、OPG是骨形成的标志物,其中OPG由成骨细胞分泌,能调节破骨细胞的分化;TRAP、CTX-Ⅰ是骨吸收标志物,TRAP可反映破骨细胞活性及骨吸收状态,CTX-Ⅰ常用于评价抗骨吸收药物的治疗效果[17-18]。在骨质疏松发生的过程中,上述生化指标也会发生变化。
本课题组前期预实验结果发现,DMB(0.2、1、5 mg/kg)可随剂量增加而增加/降低骨质疏松模型小鼠血清中BALP/TRAP水平,这提示其可影响小鼠的骨代谢水平。基于此,本研究进一步探讨了DMB改善骨质疏松的作用。结果显示,模型组小鼠经双侧卵巢切除后,其骨量流失、骨微结构恶化,BMC、BMD和骨生物力学参数均显著降低(P<0.05或P<0.01),血清中BALP、OPG、TRAP、CTX-Ⅰ水平均显著升高(P<0.05或P<0.01),这是由于小鼠经双侧卵巢切除术后其体内雌激素缺乏,从而会刺激骨形成、骨吸收指标水平的升高[10];经E2和DMB干预后,小鼠骨量增加,骨微结构改善,BMC、BMD、骨生物力学参数和血清中BALP、OPG水平均显著升高,而血清中TRAP、CTX-Ⅰ水平均显著降低(P<0.05或P<0.01)。此结果与已报道的GLP-1R激动剂在多种动物模型中的促成骨作用相一致[19-21]。
综上所述,DMB可通过增加骨量、改善骨微结构、升高骨形成相关指标的表达和骨生物力学参数以及降低骨吸收相关指标的表达来发挥改善骨质疏松的作用。由于DMB是小分子化合物,其空間结构和肽类激动剂不同,可能使其与GLP-1R的亲和力和内在活性与肽类激动剂存在差异[22]。目前,多条信号通路已被证实与GLP-1R介导的骨代谢调节作用有关,如蛋白激酶C-β2(PKC-β2)[2]、IGF-1/IGF-1受体 [12]、PI3K/Akt和细胞外因子/β-联蛋白[13]通路等,而DMB改善骨质疏松作用是否直接通过激动GLP-1R受体,或通过上述信号通路参与骨代谢调节还有待进一步研究。
參考文献
[ 1 ] GIRDHAR K,DEHURY B,KUMAR SINGH M,et al. Novel insights into the dynamics behavior of glucagon- like peptide-1 receptor with its small molecule agonists[J].J Biomol Struct Dyn,2019,37(15):3976-3986.
[ 2 ] WANG Z,WANG X,ZHANG L,et al. GLP-1 inhibits PKC-β2 phosphorylation to improve the osteogenic diffe- rentiation potential of hPDLSCs in the AGE microenvironment[J]. J Diabetes Complications,2020. DOI:10.1016/J.JDIACOMP.2019.107495.
[ 3 ] JACOME-GALARZA CE,PERCIN GI,MULLER JT, et al. Developmental origin,functional maintenance and genetic rescue of osteoclasts[J]. Nature,2019,568(7753):541-545.
[ 4 ] PARIZAD N,BAGHI V,KARIMI EB,et al. The prevalence of osteoporosis among Iranian postmenopausal women with type 2 diabetes:a systematic review and meta-analysis[J]. Diabetes Metab Syndr,2019,13(4):2607- 2612.
[ 5 ] KNUDSEN LB,KIEL D,TENG M,et al. Small-molecule agonists for the glucagon-like peptide 1 receptor[J]. Proc Natl Acad Sci USA,2007,104(3):937-942.
[ 6 ] CHEONG YH,KIM MK,SON MH,et al. Two small mo- lecule agonists of glucagon-like peptide-1 receptor modulate the receptor activation response differently[J]. Biochem Biophys Res Commun,2012,417(1):558-563.
[ 7 ] IRWIN N,FLATT PR,PATTERSON S ,et al. Insulin-releasing and metabolic effects of small molecule GLP-1 receptor agonist 6,7-dichloro-2-methylsulfonyl-3-N-tert-butylaminoquinoxaline[J]. Eur J Pharmacol,2010,628(1/2/3):268-273.
[ 8 ] 芦志伟,孙浩,李莹,等.长效GLP-1受体激动药索马鲁肽治疗2型糖尿病疗效和安全性的系统评价[J].中国药房,2019,30(7):969-975.
[ 9 ] 李艳梅,唐祎偌,夏旋.索马鲁肽口服剂:开启GLP-1受体激动剂的新时代[J].药品评价,2019,16(24):1-3.
[10] GRAAF CD,DONNELLY D,WOOTTEN D ,et al. Glucagon-like peptide-1 and its class BG protein-coupled receptors:a long march to therapeutic successes[J]. Pharmacol Rev,2016,68(4):954-1013.
[11] ZHOU C,ZHOU Y,WANG J,et al. Emergence of Chinese drug discovery research:impact of hit and lead identification[J]. J Biomol Screen,2015,20(3):318-329.
[12] ZHANG M,XIE Y,ZHOU Y,et al. Exendin-4 enhances proliferation of senescent osteoblasts through activation of the IGF-1/IGF-1R signaling pathway[J]. Biochem Biophys Res Commun,2019,516(1):300-306.
[13] GAO L,LI SL,LI YK. Liraglutide promotes the osteoge- nic differentiation in MC3T3-E1 cells via regulating the expression of Smad2/3 through PI3K/Akt and Wnt/beta- catenin pathways[J]. DNA Cell Biol,2018,37(12):1031- 1043.
[14] NISSEN A,MARSTRAND S,SKOV-JEPPESEN K,et al. A pilot study showing acute inhibitory effect of GLP-1 on the bone resorption marker CTX in humans[J]. JBMR Plus,2019. DOI:10.1002/JBM4.10209.
[15] YOUSEFZADEH N,KASHFI K,JEDDI S,et al. Ovariectomized rat model of osteoporosis:a practical guide[J]. EXCLI J,2020. DOI:10.17179/EXCLI2019-1990.
[16] SANGHANI-KERAI A,MCCREARY D,LANCASHIRE H,et al. Stem cell interventions for bone healing:fractures and osteoporosis[J]. Curr Stem Cell Res Ther,2018,13(5):369-377.
[17] SZULC P. Biochemical bone turnover markers in hormo- nal disorders in adults:a narrative review[J]. J Endocrinol Invest,2020,43(10):1409-1427.
[18] DIEMAR SS,MOLLEHAVE LT,QUARDON N,et al. Effects of age and sex on osteocalcin and bone-specific alkaline phosphatase-reference intervals and confounders for two bone formation markers[J]. Arch Osteoporos,2020.DOI:10.1007/S11657-020-00715-6.
[19] LEI T,LIANG Z,LI F,et al. Pulsed electromagnetic fields (PEMF) attenuate changes in vertebral bone mass,architecture and strength in ovariectomized mice[J]. Bone,2018. DOI:10.1016/J.BONE.2017.12.008.
[20] SCHIELLERUP SP,SKOV-JEPPESEN K,WINDEL?V JA,et al. Gut hormones and their effect on bone metabolism. Potential drug therapies in future osteoporosis treatment[J]. Front Endocrinol (Lausanne),2019. DOI:10. 3389/FENDO.2019.00075.
[21] ZHANG Y,LIU MW,HE Y,et al. Protective effect of resveratrol on estrogen deficiency-induced osteoporosis though attenuating NADPH oxidase 4/nuclear factor kappa B pathway by increasing miR-92b-3p expression[J]. Int J Immunopathol Pharmacol,2020. DOI:10.1177/205873- 8420941762.
[22] WOOTTEN D,MILLER LJ. Structural basis for allosteric modulation of class BG protein-coupled receptors[J]. Annu Rev Pharmacol Toxicol,2020. DOI:10.1146/ANNUREV-PHARMTOX-010919-023301.
(收稿日期:2020-08-18 修回日期:2020-11-05)
(編辑:唐晓莲)
