氢氧化钠标准溶液的配制与标定信息化教学设计
2021-03-01牛飞伦西北工业学校陕西兴平713100
牛飞伦(西北工业学校,陕西 兴平 713100)
1 教学分析
1.1 教材分析
本教材在结构上采用的是传统的编写方法,系统性非常强,难易程度适合学生学习。前面两章均为理论知识,实践操作内容均安排在后面几章。理论知识和实际操作各自独立,不利于学生学习。所以这次把学生要掌握的内容中的理论知识和动手操作知识整合成一个整体,作为一个有机的整体内容来完成。
在企业的分析检测中心,标准溶液的配制及标定时化学检验员的一项日常工作,要求个人必须独立完成,所以本次学习内容是酸碱滴定的核心内容,也是整个滴定分析必不可少的学习内容[1]。
《氢氧化钠标准溶液的配制与标定》选自高等教育出版社《分析化学》通用类第四章酸碱滴定法第五节标准溶液的配制和标定的实验项目之一。为了更好地辅助课堂教学,我们选择了中国大学慕课《化学分析技术》中的《认识标准溶液》《标准溶液的配制》《基准物质称量范围的计算》《减量称量法—固体》《分析天平的操作》《滴定管的检漏》《滴定管操作》《滴定管滴定速度的控制》和《氢氧化钠标准溶液的标定》等微课视频作为学生课前预习的学习资源。
1.2 目标分析
1.2.1 素质目标
(1)培养细心、认真的科学态度;(2)激发学习化学的兴趣;(3)培养学生互帮互助的团队精神。
1.2.2 知识目标
(1)掌握标定氢氧化钠标准溶液的标定方法;(2)了解如何选择合适的指示剂;(3)掌握酸碱滴定分析的实验步骤及注意事项;(4)能够熟练进行滴定操作,并正确把握滴定终点。
1.2.3 能力目标
(1)培养学生用所学化学思想来解决实际问题的才能;(2)会正对数据进行记录和;(3)把现实生活中的问题会用课本中的知识来解决。
1.3 重点和难点
(1)重点。①用邻苯二甲酸氢钾标定氢氧化钠的实验过程;②氢氧化钠标准溶液的配制。
(2)难点。①滴定管的操作方法;②滴定终点的判断及控制。
1.4 学情分析
目前中职院校学生整体状况为:多数学生基础差,没考上高中才来中职学校。他们普遍厌学,痴迷于网络游戏,但是他们有着活跃的思维,对新鲜事物好奇心十足。
这门课程的授课主体是我校二年级化学工艺专业的学生,《基础化学》这门课在一年级已经开设过了,本学期新开设《分析化学》,通过前面几周的学习,已经了解了滴定分析中的相关计算问题。滴定分析的基本操作已经进行了为期两周的集中训练,多数学生已经学会了滴定分析仪器的基本操作,但是操作还不熟练,应在后续具体项目中教师进行演示并指正操作问题[2]。
整体来说本班学生学习态度不太好,只有少数学生能主动细心学习;大部分学生能在老师的催促下学习;有近三分之一的学生基础较差,对学习没有积极性和主动性。
2 设计思路和教学策略
采用线上线下混合教学模式,充分利用“一端三平”开展教学。课前学生利用手机登录平台观看相关微课,完成检测题目。教师则利用平台督促学生自主学习,根据学生自学情况优化课堂设计。理论教学借助超星平台发起抢答,课堂练习,小组讨论展示分享实验方案,使学生实验原理有了充分的理解,能给出实验的具体操作步骤,能列举实验所需物品;实操部分教师演示纠正学生操作问题,小组合作探究,互动评价。教师在教学的整个过程中起到了引导作用,可以使学生学习的积极性充分发挥出来。
3 教学环境
理论授课地点为化工实训楼502,教室有触控交互的一体机,一体机有千兆网络连接,师生使用4G网络的智能手机,课堂教学基于超星的学习通平台,有利于手机投屏,展开教学活动。
实训授课地点为化工实训楼分析实验室和分析天平一室,这两个实验室都有符合本项目所用的仪器和试剂,完全满足教师演示和学生实操项目的进行。
4 教学过程
(1)引入。利用学习通平台推送练习题:分别给出多种浓度的溶液,让学生快速判断出哪些是标准溶液。
(2)设计意图。进一步了解标准溶液的准确浓度如何表示。
(3)师生探讨教师提出以下问题,学生回答
①要配制一瓶标准溶液,你怎样来做?
②怎样来配制氢氧化标准溶液?原因是什么?
③实验室是如何来标定氢氧化钠溶液?
④那些基准试剂可以标定氢氧化钠溶液?
⑤基准试剂邻苯二甲酸氢钾和草酸比较有哪些优点?
(4)设计意图。对学生课前自学遗留的问题进一步讲解,解开了学生心中的疑虑。
(5)课堂练习教师通过学习通平台推送随堂练习:计算0.1摩尔每升氢氧化钠标准溶液在标定时所需要称量的基准物质的质量?要求学生做完后拍照上传,请三位学生上台讲解自己的计算过程,其它同学可以补充。
(6)学生活动。①写出化学反应方程式;②做出相应计算;③拍照上传计算过程至学习通平台。④上台讲解自己如何计算的。
(7)设计意图。锻炼了学生的表达能力的同时增强了他们的自信心
(8)师生探讨。教师提出问题:当基准物质为邻苯二甲酸氢钾,应如何选择指示剂?
引导学生考虑理论终点时的pH值。
教师为学生讲解邻苯二甲酸钠钾溶液pH值的计算方法。
(9)学生活动。在老师的引导下确定出化学计量点时溶液的pH值,并且能从常用的几种酸碱指示剂中确定出所用的指示剂为酚酞,且能说出终点时溶液的颜色变化。
(10)设计意图。弱化了学生对于溶液pH计算的难度,增强学生学习的自信心。
(11)完成实验方案。在已经明白了实验原理的基础上,教师要求学生以小组为单位以思维导图的形式列出实验步骤以及实验所需的仪器和试剂。
(12)学生活动。小组讨论,完成方案的制定,并将本组的思维导图上传至平台。
(13)设计意图。①最大程度发挥小组协作能力;②思维导图明了易懂,促进了组内,组间的相互学习。
(14)完善实验方案
任务一:氢氧化钠标准溶液的配制。称取固体氢氧化钠110 g置于烧杯中,加水100 mL,注入塑料桶中,密封放置至溶液澄清;吸取2.5 mL上层清液注入500 mL无二氧化碳的水,转移到试剂瓶中,并盖上橡皮塞,摇匀并贴上标签。
任务二:氢氧化钠标准溶液的。将试样称于锥形瓶中,加20~30 mL无CO2蒸馏水使其溶解,若溶解不完全,可稍微加热。加酚酞指示剂2~3滴,用待标定的NaOH溶液滴定至呈微红色并保持半分钟不褪色即为终点。并将实验过程中所用的氢氧化钠溶液的体积在实验记录单上,平行标定三次[3]。
(15)讲述。①减量法称量过程中容易出现的问题。②滴定管的读数。读数时,视线应与凹液面最低处成水平。视线高于凹液面最低处,读数将偏低;反之,读数偏高。③在滴定操作时,常用中速,慢速及半滴操作。滴定前将滴定管尖悬挂的液滴靠在锥形瓶外壁上。滴定开始时,应一边滴定一边摇锥形瓶,滴定速度不能太快,为中速滴定。切记不能流成“水线”。临近滴定终点时,滴定速度应十分缓慢,为慢速滴定,应一滴-滴地加入,防止过量。最后再加半滴,直至终点为止。④实验安全。如有NaOH接触立刻用自来水冲洗后涂上硼酸软膏。
(16)学生活动。①认真观看老师规范动作演示,能分辨出错误操作。②让三名同学在全体同学面前操作,其余同学观察并指出错误的操作。③提出自己的问题,听老师讲解。
(17)设计意图。①通过让学生参使学生感受到准备实验工作的辛苦和繁琐,进而减少学生对实验药品的浪费,让学生获得成功感,在潜移默化中使学生的节约意识有了提升,并加强学生对实验成本的计算能力。②培养学生实验过程中的安全意识,对比分析问题的能力。
(18)方案实施。①巡视指导学生,并对学生中出现的错误操作进行纠正。②解答学生在操作过程中发现的问题,对次数出现较多的问题进行补充讲解。③解决突发问题。④记录评价各组表现。
(19)学生活动。①各小组按照修改后的实验步骤进行操作;②对实验数据进行记录,并对测定结果进行计算。③设计意图,培养学生学以致用能力,实操能力,发现问题、分析问题和解决问题的能力。
(20)数据处理。①原始数据记录单(学生自行设计)。②氢氧化钠标准溶液浓度的计算:
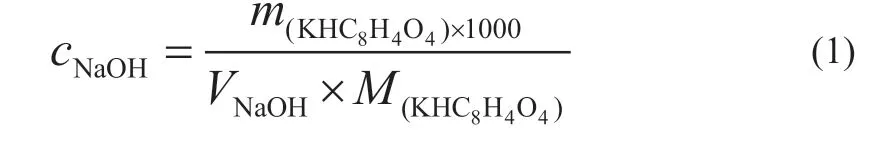
(21)总结评价。①评价各小组完成实验操作的情况;②讲评学生在本次学习的活动中可能出现的问题及发现的优点进行总结。
(22)教学反思。借助信息化手段,打破了传统教学中学生的被动地位,使学生学习的积极性有了大幅度的提高;从课前的自主学习,到课中的随堂练习学生参与的积极性明显增高,教师对学生点评打分使得学生之间有了竞争意识,活跃了课堂气氛。
充分发挥学生为主体,教师为主导的教学理念,将实验准备工作安排给学生,让学生感受到了准备工作的辛苦与繁琐,进而懂得节约,培养了他们认真细致考虑问题的能力[4]。互帮互助的小组协作方式,既培养了学生的团队合作能力,多种不同的评价让学生更清楚自己是教学的目标任务,并感受了什么是客观的评价。学生演示,同学提示、教师点评活跃课堂。提升课堂教学效果教师及时巡视、纠错,给予指导,做一个有用的配角和教学组织者;学生的参与性积极性得到了充分发挥,增强了学生团队合作的思想;现场考核、分析讨论、总结拓展。教学手段丰富,形式多样。再次突破重、难点。优化教学效果,培养了学生规范化的职业素。
5 结语
本次课的不足之处是在课堂教学中教师考虑到了滴定突跃概念的抽象与难理解,为了降低难度只是有针对性的为学生讲解了以邻苯二甲酸氢钾为基准试剂时指示剂的选择,基于学以致用教师在后期教学中应该不断学生加强学生的滴定分析的运算能力,以应用到实际工作中。
