1,2-二苯基-1-丙醇的合成及表征
——由Grignard反应合成醇教学实验的改进
2021-02-28林欣瑛封飞艳邵周强
陈 红,林欣瑛,封飞艳,邵周强,施 梅
(南京晓庄学院 环境科学学院,江苏 南京 211171)
0 引言
立体化学内容既是有机化学教学的重点,也是教学中的难点.与之相关的手性中心、对映体、非对映体、非对映选择性、dr值等概念在医药、材料科学、生命科学等领域均有极其重要的应用.不对称反应的研究越来越受到人们的重视,并已成为有机化学的前沿领域之一,可谓是有机合成的灵魂.但与此不相称的情况是,目前本科阶段的有机化学实验教材,缺少展示立体化学概念和不对称合成方面的实验项目,从而造成学生所学实验知识和技能与实际科研需要脱节[1].为了解决这一问题,我们参考教材中的相关实验,更换其反应原料,引入具有非对映选择性特征的格氏反应.通过学习实验原理、亲手操作实验过程以及对实验结果的分析论证,使学生对立体化学知识产生直观的体会和明确的印象.
现行面向本科生的有机化学实验教材中[2-4],由Grignard反应合成醇类化合物的实验,如“三苯甲醇的合成”“2-甲基-2-丁醇的制备”等,产物均为不含手性中心的化合物.我们通过更换反应原料,对该实验进行了改进.其中第一步格氏试剂的制备,与教材中相同;第二步加成反应中,选用含有手性中心的2-苯基丙醛作原料,替代原格氏反应中的丙酮或二苯甲酮等反应物,目的是通过反应物中已有不对称中心来不对称诱导产生新的手性中心.
整个实验的反应条件以及操作过程与原有实验类似,但所包含的内容却更加多元和丰富.从实验原理看,包含了不对称合成中的重要规则Cram规则的运用,并引入了手性中心、对映体、非对映体、非对映选择性、dr值等立体化学概念.从实验操作技能上看,除了无水无氧操作,还训练了薄层色谱、柱色谱等实验技术,并运用红外及核磁氢谱对所得产物进行表征.通过比较手性中心氢的积分面积,得到两对对映体物质的量之比,即反应产物的dr值.
1 实验部分
1.1 实验原理

图1 格氏试剂与羰基发生加成反应示意图
若醛、酮的α-碳为手性碳,手性碳上连有大小不同的三个基团,分别用L(最大基团)、M(中等基团)、S(最小基团)表示.旋转羰基碳与α-碳之间的单键,可得无数个构象(图1).当格氏试剂与羰基发生加成反应时,格氏试剂中的Mg须与羰基氧配位,因此羰基氧原子一端空间位阻增大,导致α-碳上的最大基团(L)与羰基处于反式,故R与L处于重叠型为反应的优势构象[5].

图2 Cram规则示意图
根据Cram规则(图2),格氏试剂中的烃基R′从羰基旁空间位阻较小的基团(S)一边接近分子,所得加成产物是主要产物,从中等大小的基团(M)一边接近分子,由于位阻较大,所得加成产物是次要产物.

图3 1,2-二苯基-1-丙醇合成路线
本实验中,先由溴苯和金属镁在无水乙醚中反应,制备格氏试剂苯基溴化镁;然后将其与2-苯基丙醛加成,经水解得产物1,2-二苯基-1-丙醇(图3)[6-8].
反应物2-苯基丙醛的α-碳为手性碳,当其与格氏试剂苯基溴化镁加成时,根据Cram规则,该反应具有非对映选择性,即:格氏试剂中的苯基从羰基旁空间位阻小的氢一边接近分子,所得加成产物是主要产物;从甲基一边接近分子,由于位阻较大,所得加成产物是次要产物.

图4 2-苯基丙醛和苯基溴化镁反应结果示意图
本实验中,考虑试剂成本,使用的是2-苯基丙醛的外消旋混合物.外消旋体中的(S)-对映体经反应生成非等量的(1R,2S)和(1S,2S)-1,2-二苯基-1-丙醇两种异构体.同样,外消旋体中的(R)-对映体经反应也生成非等量的(1S,2R)和(1R,2R)-1,2-二苯基-1-丙醇两种异构体(图4).因为反应物2-苯基丙醛由等量的(S)和(R)-异构体组成,两组产物正好互相平衡,即(1R,2S)和(1S,2R)等量组成一对对映体,(1S,2S)和(1R,2R)也等量组成一对对映体,其中前者为反应的主要产物.
1.2 试剂或材料
反应所用无水乙醚为市售乙醚,经无水硫酸钠干燥除水,再加入钠粒干燥;镁条为高纯试剂;其余试剂均为市售分析纯,未经处理直接使用.
1.3 仪器和表征方法
红外光谱仪(美国Nicolet iS50,Thermo Fisher),核磁共振仪(瑞士Bruker Biospin AVANCE III HD 600 MHz).
1.4 实验步骤
1.4.1 格氏试剂的制备
用经过充分干燥的仪器搭建实验装置.将3.2 mL(4.71 g,0.03 mol)溴苯以及15 mL无水乙醚混合均匀,加入恒压滴液漏斗,然后将一小粒碘和0.81 g(0.033 mol)剪碎的镁条加入三颈烧瓶中.自滴液漏斗加2~3 mL混合液于反应瓶内,浸没镁条.约5 min后,反应引发,溶液微沸,碘颜色消失.继续滴加其余混合液,并开动搅拌,保持反应液微沸.滴加完毕,40 ℃油浴加热回流30 min,反应液呈棕灰色澄清液体.格氏试剂制备完成.
1.4.2 格氏试剂与2-苯基丙醛的加成
将反应装置改为冰盐浴冷却,并用氮气气球保护.在制备格氏试剂时,所用溶剂乙醚在反应温度下有较大蒸汽压,能够排除反应体系中的大部分空气,从而消除空气中的氧气和水蒸气对实验的影响.改用冰盐浴后,反应温度降低,乙醚蒸汽压下降.为了防止外界空气和水蒸气侵入反应体系,使用氮气气球进行保护.
取2-苯基丙醛3.5 mL(3.49 g,0.026 mol)、无水乙醚15 mL,混合均匀,加入恒压滴液漏斗.在-5 ℃下逐滴加入反应瓶.滴加完毕,冰盐浴下继续反应30 min,反应液呈乳白色浑浊.TLC(V(乙醚)∶V(石油醚)= 1∶1展开)显示原料点消失,反应完全.
1.4.3 后处理及提纯
在冰浴冷却下,通过滴液漏斗缓慢加入20 mL饱和氯化铵溶液淬灭反应,并加入少量蒸馏水溶解产生的沉淀.将反应混合物转移至分液漏斗,分液,用乙醚(3×10 mL)萃取,合并有机相,无水硫酸钠干燥.蒸除溶剂后,得粗品,为一黄色油状物.硅胶柱层析(V(石油醚)∶V(乙酸乙酯)=15∶1→10∶1梯度洗脱)分离,得产物,浅黄色油,3.62 g,产率68%.
2 结果与讨论

图5 产物的红外谱图
2.1 薄层色谱分析
对粗产物进行薄层色谱分析,254 nm紫外灯下观察,发现展开后分为两个点,其一比原料2-苯基丙醛的极性小,推测为制备格氏试剂时的副产物联苯;另一比原料醛的极性大,推测为目标产物1,2-二苯基-1-丙醇.
由于所得粗产物中除联苯外,其它副产物极少,曾尝试用水蒸气蒸馏法来除去联苯,后经对馏出液的乙醚萃取液点板分析,发现部分目标产物也被蒸馏了出来,故改用硅胶柱层析法对粗产物进行提纯.作为教学实验,也可以直接对粗产物进行核磁氢谱表征,具体可根据教学时长安排及学生对柱色谱分离技术的熟练情况,选做该部分内容.
2.2 红外光谱分析
红外光谱(图5)分析表明,产物结构与预期化合物1,2-二苯基-1-丙醇一致.IR(cm-1):3406(羟基O—H伸缩振动),3061, 3028(苯环上=C—H伸缩振动),2967, 2876(饱和C—H伸缩振动),1603, 1495, 1450(苯环骨架振动),762, 694(单取代苯环).
2.3 核磁氢谱分析
1H NMR(CDCl3, 600 MHz),δ:7.34~7.12(m,10H,Ar-H),4.79~4.64(d,1H,1-H),3.10~3.00(m,1H,2-H),1.85(s,1H,OH),1.30~1.06(d,3H,CH3).核磁氢谱(图6)分析表明,所得产物与目标化合物结构相符.其中,δ4.79处双峰与δ4.64处双峰的积分面积比约为9∶1;同样,δ3.10处五重峰与δ3.00处五重峰的积分面积比,以及δ1.30处双峰与δ1.06处双峰的积分面积比,均约为9∶1.结合之前对反应原理的讨论,可以确定产物组成如图7所示.产物由两对对映体组成,每对对映体组成一种外消旋体.这两对对映体的物质的量之比,即产物的dr值,为9∶1.
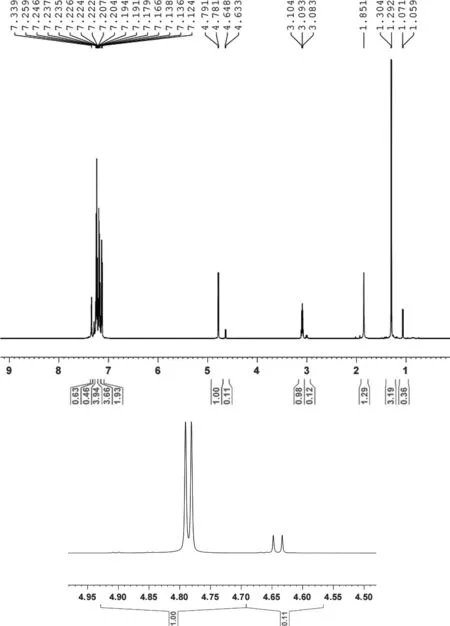
图6 产物的核磁氢谱谱图

图7 反应产物组成示意图
3 结语
在设计理念方面,本实验内涵丰富、机理清晰,强化了手性合成、Cram规则等相关立体化学知识的应用,弥补了现行实验教材的不足;对实验原理的介绍,能够激发学生对不对称合成和相关理论的学习兴趣,使学生可以在基础教学实验室体验有机合成的科研过程.在实验操作方面,本实验条件温和、操作简单、产率高,实验结果直观明显,产物的核磁氢谱表征直接表明了该反应的非对映选择性.在实验推广方面,本实验所用仪器设备均为本科教学实验室常见的,所用药品也是常见化学试剂,无需昂贵的手性试剂,实验成本低,利于本科教学推广.总之,通过对原有实验项目中反应原料的替换,使本实验升华为一个集知识性、可操作性、先进性于一体,简单高效的实验,值得本科教学推广.
