双膦酸盐抗骨质疏松症研究进展*
2021-02-26谢青青综述李梦兰周菊帅世全审校
谢青青 综述 李梦兰 周菊 帅世全 审校
(南充市中心医院风湿免疫科·川北医学院第二临床医学院,四川 南充 637000))
骨质疏松症(Osteoporosis,OP)是多种原因引起的一种全身性骨骼疾病,以骨强度下降和骨折风险增加为特征,其病理生理主要表现为骨吸收增加和(或)骨形成减少,发病以中老年为主,且近年来有年轻化的趋势[1-2],因此OP的防治非常重要。OP的治疗方案是综合性的,包括药物及营养治疗等,而有效的药物治疗必不可少。双膦酸盐(Bisphosphonate,BPS)是国内外多个指南推荐的首选抗OP药物,为焦磷酸盐的类似物,含P-C-P基本结构,是其产生抑制骨吸收活性的必要条件,具有 R1 和R2 两个侧链,R1中的羟基对羟基磷灰石晶体具有高亲和力,R2是生物活性组成部分,当其烷基链上存在氮分子或环状结构时,能使BPS抑制骨吸收的能力显著增加[3]。根据侧链含氮量分为不含氮双膦酸盐(非N-BPS)和含氮双膦酸盐(N-BPS),本文选取了4种代表性的BPS,对比了它们在抗OP机制、疗效等方面的不同,现就近年来的一些研究做一综述。
1 依替膦酸盐
依替膦酸盐(Etidronate)是以羟基和甲基作为侧链的第一代BPS,为非N-BPS,在高剂量时,依替膦酸盐既能抑制骨吸收,又能抑制骨形成,当低剂量给药治疗OP时,只抑制骨吸收,而不影响骨形成[4],其化学结构式,见图1。

图1 依替膦酸盐化学结构式
研究表明,骨保护素(Osteoprotegrin,OPG)/核因子κB受体激活剂(Receptor activator of nuclear factor kappa B,RANK)/RANK配体(RANKL)系统参与了破骨细胞与成骨细胞平衡的调剂,OPG与RANKL竞争性与RANK结合,且OPG与RANK的结合能力比RANKL更强,从而抑制破骨细胞分化、成熟,影响骨重建,起到抗OP的作用,国外文献报道OPG基因可能是众多药物修复OP相关骨折的关键因子[5]。徐晓峰等[6]在OP大鼠骨缺损模型中的研究表明,依替膦酸盐可能通过上调骨组织中OPG的含量,阻止破骨细胞异常分化,增加骨矿物质密度(Bone mineral density,BMD),促进大鼠骨缺损的修复,发挥抗OP效应。另外,在一些动物试验中发现,依替膦酸盐在抑制骨吸收的同时可能通过与神经元相互作用而发挥有效的、不依赖于抗骨吸收的独特镇痛作用,且依替膦酸盐的镇痛效果似乎优于N-BPS[7]。
既往的研究表明,在绝经后OP、男性OP以及糖皮质激素诱导的OP(Glucocorticoid-induced osteoporosis,GIO)患者中,间歇性使用依替膦酸盐可以提高BMD,降低椎体骨折的发生率,但是依替膦酸盐减少骨吸收的剂量与导致骨矿化的剂量接近,长时间高剂量使用可能导致骨软化和骨折,加之其抗骨吸收作用明显劣于含氮的第二代或第三代BPS[8],因此在治疗OP方面已逐渐被其他N-BPS所取代[9]。而近年来研究发现,以依替膦酸盐为代表的非N-BPS没有N-BPS的炎症坏死作用,在过去几年中,由于N-BPS的炎症坏死作用,约有上千例颌骨骨坏死(Osteonecrosis of jaw bone,ONJ)怀疑与N-BPS的使用有关[10]。而有学者报道,依替膦酸盐似乎可以减轻N-BPS的炎症作用,因此他们提出,对于接受过N-BPS治疗的ONJ风险患者,依替膦酸盐可能是一种有用的替代药物[11]。另外,Fujita等[12]在临床研究中,比较了依替膦酸盐、阿仑膦酸盐(Alendronate)及利塞膦酸盐(Risedronate)三种BPS对OP患者的镇痛效果,结果显示依替膦酸盐的镇痛效果最好。因此,基于依替膦酸盐可能在降低ONJ风险方面具有价值以及抗OP的独特镇痛作用,所以值得我们重新评价它们治疗OP的安全性与有效性。
2 阿仑膦酸盐
阿仑膦酸盐(Alendronate)是活性最强的第二代BPS,以侧链含氨基为主要特点,即N-BPS,不仅可抑制破骨细胞活性,减少骨吸收,阿仑膦酸盐还可刺激成骨细胞分化,防止或减轻骨细胞和成骨细胞凋亡[13],其化学结构式,见图2。

图2 阿仑膦酸盐化学结构式
有研究显示,干扰素-β(IFN-β)/信号转导与转录激活因子1(Signal transducer and activator of transcription 1,STAT1)信号通路的激活与OP的发生和发展相关,用IFN-β刺激该通路可显著抑制破骨细胞,而OP的进展受STAT1的表达和磷酸化水平的调节[14]。Ma等[15]在OP大鼠模型中研究发现阿仑膦酸盐通过刺激IFN-β的表达显著抑制了破骨细胞的活性,而且还提高了破骨细胞中STAT1的表达和磷酸化水平,增强了成骨细胞的活性与分化,研究证实了阿仑膦酸盐可以通过上调IFN-β/STAT1信号通路来调节破骨细胞与成骨细胞的功能,影响大鼠OP进展。
阿仑膦酸盐已广泛用于OP的治疗。在一项荟萃分析中,Xu[16]评估了阿仑膦酸盐治疗男性OP的疗效,结果显示阿仑膦酸钠可以有效提高腰椎、股骨颈和全髋部BMD,以及降低新椎体骨折的发生率。在另一项荟萃分析中,Wang等[17]评价了阿仑膦酸盐治疗GIO的有效性与安全性,分析得出阿仑膦酸盐能显著增加GIO患者腰椎和股骨颈的BMD,但似乎不能降低骨折的风险,而在Kan等[18]的系统分析中也有类似的结果。但由于关于GIO骨折发生率的报道相对不足,统计存在缺陷,因此需要进行更多的试验来确定阿仑膦酸盐预防GIO骨折的疗效。研究显示,长时间使用BPS可能会增加非典型性股骨骨折(Atypical femoral fractures,AFF)的风险[19],在丹麦的一项全国性研究中,Bo等[20]探讨了OP患者长期(≥为10年)使用阿仑膦酸盐的骨骼安全性和有效性,发现即使假设100%的转子下骨折和股骨干骨折是由于使用阿仑膦酸盐导致的AFF,但AFF的数量仍然太少,不足以抵消长期使用阿仑膦酸盐对预防髋部骨折的好处,当然,我们仍然需警惕AFF的发生。虽然阿仑膦酸盐作为一种有效的抗骨吸收剂,在国际治疗中被强烈推荐用于治疗OP,但其口服生物利用度非常差,伴随的副作用也不能忽略,例如最常见的胃肠道反应,以及坐骨神经痛,皮疹和哮喘等[21]。因此,基于口服阿仑膦酸盐的不良反应及对患者依从性的影响,不少学者研究并提出了一些新型给药制剂,包括阿仑膦酸盐泡腾片、溶液制剂[22]以及近些年研究的口服凝胶[23],临床研究发现这些新型制剂具有同传统片剂一样的抗OP效应,而其不良反应比片剂组少,且患者依从性更高,相信随着越来越多新型制剂的研究,阿仑膦酸盐还能发挥更好的治疗效果。
3 利塞膦酸盐
利塞膦酸盐(Risedronate)是一种用途广泛的强效第三代含吡啶基N-BPS,在吸收后的第一小时内,利塞膦酸盐可以选择性地结合并被骨矿表面摄取,并在给药后长时间在骨表面保持活性,有效抑制骨吸收,同时也会影响成骨细胞系的活性,促进骨形成[24],其化学结构式,见图3。

图3 利塞膦酸盐化学结构式
近年的研究显示,骨髓脂肪细胞参与和调节了骨代谢[25]。如前所述,RANKL/RANK系统是近年来发现的在破骨细胞分化过程中一个重要的经典信号通路。而有研究发现脂肪细胞同样可以表达RANKL,并可通过表达RANKL促进破骨细胞分化[26],从而影响骨重建。有学者在动物研究中发现利塞膦酸盐可显著抑制OP大鼠骨髓内脂肪堆积,同时抑制脂肪细胞RANKL蛋白的表达,通过 RANKL/RANK系统,抑制破骨细胞的分化及功能,最终达到抗OP功效[27]。而且更多的研究还发现利塞膦酸盐在骨形成中也有积极的作用,Valenti等[28]发现利塞膦酸盐可能通过上调环氧化酶2(cyclooxygenase 2,COX-2),从而影响骨代谢,而有研究表明,COX的抑制与体内骨形成减少和延迟骨折愈合相关。
许多OP患者患有糖尿病(Diabetes mellitus,DM)、高血压(Hypertension,HT)和血脂异常(Dyslipidemia,DL),在日本一项三期试验的数据分析中显示利塞膦酸盐对伴有DM、HT和/或DL的骨质疏松症患者具有一致的安全性和有效性,可抑制骨转换和增加骨密度[29],然而,这些合并症是否会影响OP治疗效果还需要更多的临床数据予以支持。虽然有研究显示,每月口服一次利塞膦酸盐75mg在抑制原发性OP伴轻中度慢性肾功能不全(Chronic kidney disease,CKD)患者的骨转换和增加骨密度方面显示出一致的安全性和有效性[30]。但是,学者也提及轻中度CKD患者报道数量少,因此结论尚需谨慎。虽然BPS总体安全性较好,但BPS约60%以原形从肾脏排泄,对于肾功能异常的患者,应慎用此类药物或酌情减少药物剂量,而对伴有慢性肾功能不全[(CKD)4 期(肌酐清除率<35 mL/min)以上]的老年OP患者,应禁用BPS[31]。在肝硬化患者中,OP的发病率也较高,尽管BPS由于其潜在的消化道黏膜损伤风险一直被避免用于食管静脉曲张患者中,而一项研究显示,在内镜监测下,利塞膦酸盐可以安全地用于出血风险较低的伴有食管静脉曲张的肝硬化,以恢复OP患者的骨量[32]。
研究表明,在中国绝经后OP或骨量减少的绝经后妇女中,口服利塞膦酸盐每周35 mg和每日5 mg给药方案在改善BMD和骨转换生化指标方面具有相似的疗效[33],国外有学者的研究发现每月一次利塞膦酸盐的给药方案也具有与每日一次相似的疗效与耐受性[34],这也许提示我们可制定对患者来说更方便的用药方案,但仍需要更多的临床数据证实方案的可行性。在男性OP患者中,每周口服利塞膦酸盐或阿仑膦酸盐都是有效和安全的治疗方案,但一项研究中,利塞膦酸盐在男性患者似乎比阿伦膦酸盐更受欢迎[35]。Yano等[36]在临床研究中比较了二者的抗OP差异,发现利塞膦酸盐在提升BMD上虽不如阿仑膦酸盐,但对骨质量和骨硬度的改善比阿伦膦酸盐更有效。尽管利塞膦酸盐抗OP的功效众所周知,但和阿仑膦酸盐类似,其口服生物利用度也较差[37],口服毒性大,近年来,学者也研究了一些新型给药制剂,包括口服的纳米制剂[38],以及避开口服而通过皮肤[39]、鼻腔和肺部等途径局部传递利塞膦酸盐的给药制剂[40],这些新型制剂均在动物试验中被证实具有良好的抗OP效应,相信在未来的临床治疗上一定会具有广阔的前景。
4 唑来膦酸盐
唑来膦酸盐(Zoledronate)在侧链上含有一个咪唑环,对骨矿物质具有高亲和力,是迄今为止确定的最有效的第三代N-BPS,同阿仑膦酸盐和利塞膦酸盐一样,不仅对破骨细胞具有抑制活性,对成骨细胞系也有积极影响,与上述几种BPS不同的是,唑来膦酸盐是通过静脉给药的抗OP药物,其化学结构式,见图4。
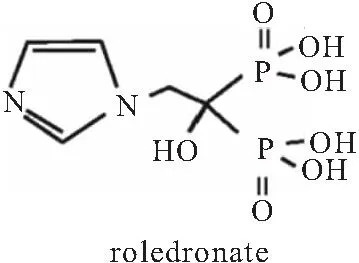
图4 唑来膦酸盐化学结构式
研究发现,腺苷活化蛋白激酶(Activated protein kinase,AMPK)、活化T细胞核因子C1(Nuclear factor of activated T-cells cytoplasmic 1,NFATc1)、碳酸酐酶Ⅱ(Carbonic anhydrase Ⅱ,CAⅡ)等物质在破骨细胞形成过程中都存在一定影响,且上述物质也都涉及于RANKL/RANK系统之中[41]。Wei等[42]的研究表明唑来膦酸盐可能通过AMPK途径影响骨重建;Nakagawa等[43]发现唑来膦酸盐可能通过对CAII和NFATc1的抑制作用阻止破骨细胞分化发挥抗OP作用,上述的研究均提示唑来膦酸盐可能也通过调节RANKL/RANK通路中相关的物质活性来发挥其抗骨吸收作用。同样,也有研究证实了唑来膦酸对成骨细胞系活性的积极影响,其可能通过增强骨髓间充质干细胞的成骨分化[44],从而发挥抗OP效应。
临床试验显示,每年接受一次5mg唑来膦酸盐静脉注射治疗可以有效地防止OP患者过度的骨丢失,并增加BMD,降低骨折风险[45]。最新一项研究还首次证实了唑来膦酸盐对体重也有显著影响,结果表明唑来膦酸盐可以预防与年龄相关的绝经后OP患者脂肪减少[46]。虽然唑来膦酸盐抗OP疗效显著,没有严重的胃肠道副作用,具有良好的安全性,但有时仍有不良反应发生,最常见的是流感样症状,如发热、寒战、骨痛和肌痛等[47],而且需警惕N-BPS严重的ONJ副作用。既往有研究显示,ONJ的发生率随着BP治疗时间的延长而增加,OP患者口服BPS治疗的前4年ONJ患病率为0.04%,继续治疗后ONJ患病率上升至0.21%,在药物引起的OP患者中,每年接受2-4次静脉BPS,患病率上升到1%[48]。因此,唑来膦酸盐作为静脉给药的BPS,合理制定用药方案对于预防ONJ并且达到良好的抗OP效果具有重要意义。尽管唑来膦酸盐已被批准用于临床治疗OP多年,但它的最佳给药方案尚不确定,Grey等[49]在早期的临床试验中,发现静脉注射唑来膦酸盐1mg和2.5mg剂量可产生至少两年的抗吸收作用。给药两年后,2.5mg唑来膦酸盐诱导的骨骼效果类似于5mg剂量诱导的。在进一步研究中,他们发现1 mg、2.5 mg或5 mg唑来膦酸盐分别持续抑制骨吸收约2年、4年和5年[50]。另一项唑来膦酸盐的III期试验分析报告说,在3年内,每年接受3次5mg剂量的参与者和只接受一次5mg剂量的参与者,他们的骨折风险降低程度是一致的[51]。相信随着越来越多临床试验证据的提出,可以指导医生为OP患者制定最佳治疗剂量与频率,提高患者接受度并降低每位患者的治疗成本,同时不影响甚至增强治疗效果。
5 小结与展望
OP作为一种全球性健康问题,其药物治疗十分重要,而BPS在治疗OP上具有显著的临床意义。虽然BPS的抗OP机制十分复杂,而且每种BPS在抗OP的机制和疗效上也存在差异,各有其优缺点,但相信随着越来越多的药物基础试验与临床研究,可以让我们更加深入地了解每种BPS的抗OP作用位点及机制,给临床医生提供更多更有效的药物剂型选择,指导医生为OP患者制定最有利的用药方案。
