固相萃取分离-电感耦合等离子体质谱(ICP-MS)法测定海产品中的无机砷
2021-02-23李林川吴建伟胡建西毕晨曦
李林川 吴建伟 胡建西 毕晨曦 苏 众
(云南同创检测技术股份有限公司,昆明 650106)
前言
砷是一种常见的有毒元素,过量摄入会引起砷中毒,长期低量接触也会引起慢性砷中毒,诱发各种疾病。随着毒理学的研究不断深入,结果表明砷的毒性与其存在的形态密切相关。目前已经发现了30余种不同形态的砷化合物[1],海产品中砷形态多样,主要以无机砷As(Ⅴ)和As(Ⅲ)、二甲基砷酸盐(DMA)、甲基砷酸盐(MMA)、砷胆碱(AsC)和砷甜菜碱(AsB)形式存在[2]。有机砷通常被认为是低毒或是无毒的,无机砷的毒性远高于有机砷,其中As(Ⅲ)毒性最强高达As(Ⅴ)的60倍以上[3]。因此,对于总砷含量较高的海产品其无机砷形态的分析比砷总量的测定更有意义,以砷的形态对其安全性进行评价更为科学严谨。
目前砷的形态主要以HPLC-ICP-MS或HPLC-AFS作为其分析手段,利用色谱分离技术可同时检测砷的多种形态,两者都具有选择性好灵敏度高等优点[4-10],但其设备昂贵,联用液相色谱设备不易维护,在实际样品检测中需要配置流动相、还原剂、平衡色谱柱等一系列操作。在食品检测时GB/T 2762—2017中规定“对于制定无机砷限量的食品可先测定其总砷,当总砷水平不超过无机砷限量值时,不必测定无机砷;否则,需再测定无机砷”[6],对于海产品其总砷水平一般较高,往往需要先测定完总砷水平后还需要再次实验,进行无机砷的测定,同一样品需要两种独立的检测方法才能完成实验。HPLC与ICP-MS或AFS联用测定无机砷的方法,耗时较长实际样品检测效率不高。
介孔二氧化硅作为一种常见的吸附材料,对其进行表面修饰或改性引入官能团后可选择性吸附不同的物质,已应用于环境、检测等多个领域[11-12]。固相萃取(SPE)作为一种常见的前处理技术已广泛应用于食品中农药残留、色素等检测。氨基功能化的硅胶整体柱与ICP-MS联用用于环境水样中无机砷的测定也见报道[12]。相比于环境水样,海产品作为一种常见砷总量较高的食品,其基体较为复杂。本研究拟在前期工作的基础上,分别以N-(β氨乙基)--氨丙基三甲氧基硅烷(AEAPTMS)、3-巯丙基三甲氧基硅烷(MPTMS)与四乙氧基硅烷(TEOS)水解共聚制备氨基功能化和巯基功能化的固相萃取小柱,拟将色谱分离过程手动化用于As(Ⅴ)和As(Ⅲ)的富集与分离,结合ICP-MS测定砷含量。在检测总砷时可同时进行无机砷的测定,为食品砷形态分析及安全评价提供一种快速、高效的手段。
1 实验部分
1.1 试剂与仪器
实验所用主要试剂与仪器见表1,实验用水均为去离子水,来自Mili-Q(18.2 MΩ·cm),其他试剂为优级纯。砷形态分析标准溶液于冰箱-18 ℃保存,其他低浓度标准溶液实验当天用去离子水稀释得到。
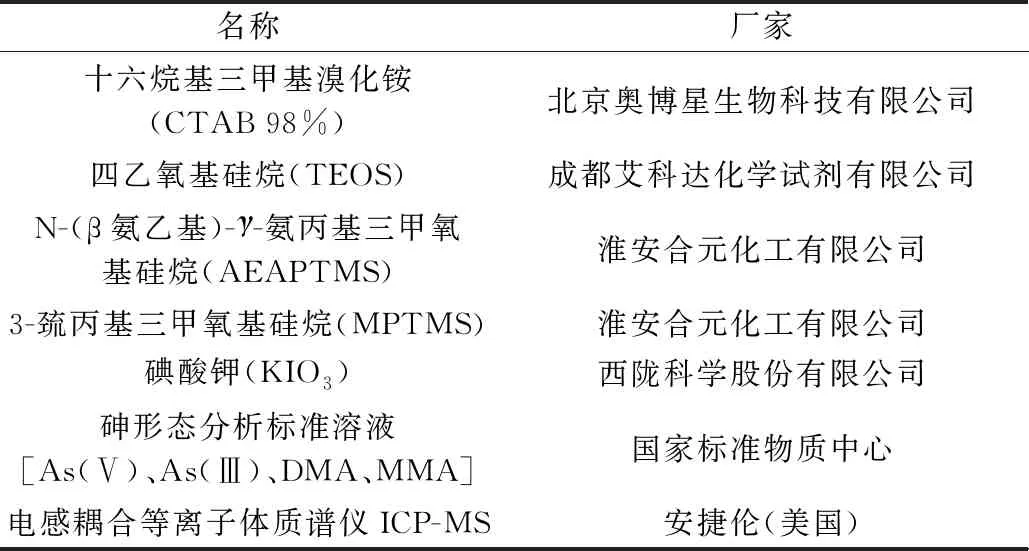
表1 主要试剂与仪器
1.2 氨基功能化固相萃取小柱的制备
称取0.176 g CTAB于20 mL离心管中加入1.8 mL无水乙醇,0.6 mL去离子水涡旋溶解完全,移取1.2 mL TEOS加入离心管中涡旋30 s,再移取0.4 mL AEAPTMS加入离心管中涡旋混合得到均一透明溶液,在室温下(20~30 ℃)反应20 h。反应完毕用乙醇-水(1∶1V/V)涡旋离心洗涤5次,除去未反应试剂后于50 ℃烘箱中烘干研细得到氨基键合硅胶材料。二氧化硅研细过筛选取74~96 μm粒径物,用硝酸(20%)溶液浸泡20 h后用去离子水洗涤至中性,烘干备用。
称取一份质量的氨基键合硅胶材料与两份质量的二氧化硅均匀混合,填充于6 mL固相萃取小柱(或5 mL医用注射器)中,填料厚度1 cm以填实紧压为准,备用。使用前依次用甲醇、水活化。
1.3 巯基功能化固相萃取小柱的制备
称取0.176 g CTAB于20 mL离心管中,加入0.5 mL乙醇、1.0 mL甲醇、1.0 mL乙酸溶液(0.2 mol/L),涡旋至CTAB溶解。移取1.2 mL TEOS、0.4 mL MPTMS加入离心管中,涡旋得到均一透明的溶液在50 ℃烘箱中水解2 h(期间如分层需涡旋振荡混匀)。
水解完毕,取出离心管冷却至室温,滴加氨水溶液(10%,V/V)至碱性,继续于50 ℃烘箱中反应1 h使TEOS和MPTMS水解产物快速聚合,反应完毕依次用甲醇、去离子水涡旋离心洗涤5次,于50 ℃烘箱中烘干研细得到巯基键合硅胶材料。
称取一份质量的巯基键合硅胶材料与两份质量的二氧化硅均匀混合,填充于5 mL固相萃取小柱(或5 mL医用注射器)中,填料厚度1 cm以填实紧压为准,备用。使用前依次用甲醇、水活化。
1.4 样品检测
准确称取1.00 g经粉碎的样品,加入20 mL硝酸溶液(0.15 mol/L)摇匀放置过夜。于90 ℃恒温箱中浸提2.5 h,每0.5 h摇匀1 min,提取完毕,冷却至室温。8 000 r/min离心15 min。取上层清液置于离心管中加入5 mL正己烷,震摇1 min后8 000 r/min离心15 min,弃去上层正己烷,按此步骤重复一次[7]。将氨基功能化SPE小柱与巯基功能化SPE小柱按图1所示连接。移取10 mL试液调节pH值注入SPE小柱中,调整真空泵压力使试液以0.5 mL/min的流速通过两段SPE小柱。吸附完毕SPE小柱经少量去离子水洗涤后,分别用3 mL硝酸(1.5%)溶液以0.5 mL/min的流速洗脱氨基化小柱3次,用3 mL KIO3(0.1 mol/L)+硝酸(1.5%)溶液以0.5 mL/min的流速洗脱巯基化小柱3次,流出液分别用10 mL容量瓶接取,定容以ICP-MS分别检测As(Ⅴ)与As(Ⅲ)含量。
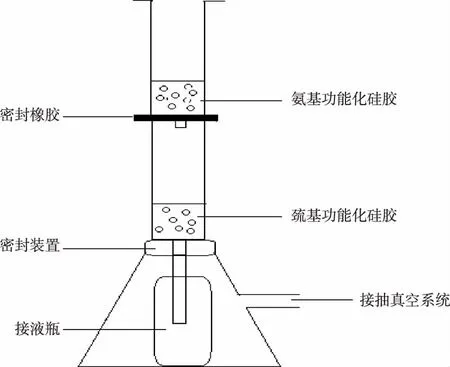
图1 吸附装置连接示意图
2 结果与讨论
2.1 氨基功能化固相萃取小柱的性能
四乙氧基硅烷作为共缩聚前体,水解后产生乙氧基、硅羟基,N-(β氨乙基)--氨丙基三甲氧基硅烷,由于自身两个氨基化官能团的存在无需其他碱性溶剂的存在也能自发水解产生硅羟基、甲氧基。在反应溶液中乙氧基、硅羟基、甲氧基之间相互缩合,形成硅烷链,两个功能化氨基也由甲氧基而键合到了硅烷链中,从而使硅胶材料具备了氨基的功能。
2.1.1 选择性
在pH<4的溶液中As(Ⅴ)以负离子的形式存在而被吸附到氨基化材料中,而MMA、DMA、As(Ⅲ)在此条件下以中性条件存在不能被萃取。实验中考察了氨基键合硅胶材料在不同pH值条件下对100 ng/mL四种形态砷标准溶液的吸附率(如图2所示)。在pH=2~9,材料对As(Ⅴ)的吸附率均在90%以上,对As(Ⅲ)吸附率均在7%以下。pH<4的条件下,MMA、DMA在溶液中难电离而不容易被材料吸附,随着pH值增大,MMA、DMA逐渐变为阴离子形式存在,材料对其吸附率逐渐增大。
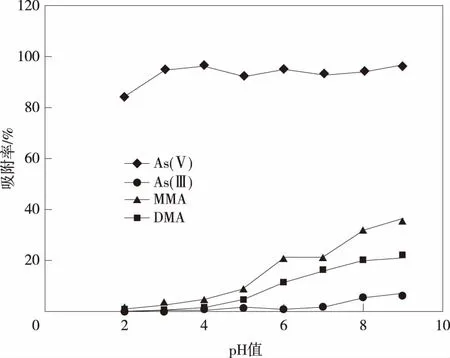
图2 不同pH值下氨基材料对砷的吸附率趋势图
2.1.2 洗脱液的选择
溶液pH值对砷的形态及吸附机理均有一定影响,在pH=3~8时,As(Ⅴ)能以静电吸附力被吸附到硅烷链末端的氨基官能团上。随着pH值的减小,As(Ⅴ)在溶液中难以电离,吸附率逐渐变小。实验以不同pH值,浓度为50 ng/mL的As(Ⅴ)标准溶液进行吸附(结果见表2)。表2结果可见当pH<3时,SPE小柱对As(Ⅴ)吸附开始减小,pH<1时,吸附率小于20%。因此考虑可用pH值较小的稀酸溶液进行洗脱,后续ICP-MS法测定时硝酸浓度一般为2%,因此选用硝酸(2%)作为洗脱液洗脱As(Ⅴ)。
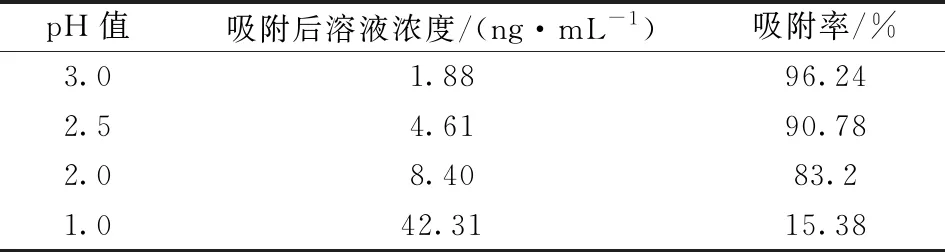
表2 不同pH值对As(Ⅴ)吸附率影响
2.2 巯基功能化固相萃取小柱的性能
氨基官能团对五价砷有良好的吸附性能,而巯基官能团则对三价砷有较好的螯合作用。与氨基键合硅胶材料类似,MPTMS通过水解得到了硅羟基与甲氧基,在碱催化条件下与TEOS水解产物发生缩聚反应,成功将巯基官能团键合到了硅烷链中。材料中存在的巯基官能团对As(Ⅲ)的螯合作用,其他官能团存在较弱的静电吸附力,随着pH值增大,As(Ⅴ)、MMA、DMA逐渐电离从而能被材料吸附。
2.2.1 选择性
对不同pH值的As(Ⅲ)、As(Ⅴ)、MMA、DMA标准溶液进行吸附试验(结果见图3),pH=2~9,巯基键合的硅胶材料对As(Ⅲ)都有较好的选择性,吸附率达到了90%以上,随着pH值增大,材料对As(Ⅴ)、MMA、DMA吸附率逐渐增大。在pH<4的条件下,材料对其他3种形态的砷均无吸附作用,吸附率均在6%以下。
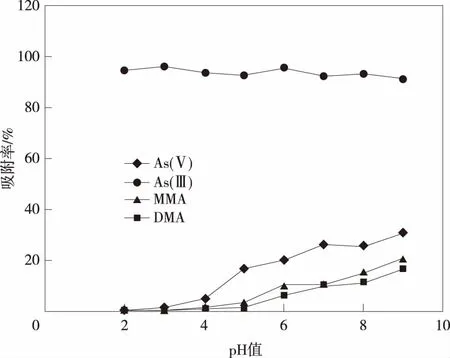
图3 不同pH值下巯基材料对砷的吸附率趋势图
2.2.2 洗脱液的选择
巯基官能团对As(Ⅲ)的吸附机理为螯合作用,无法像As(Ⅴ)一样通过减小洗脱液pH值对As(Ⅲ)进行洗脱。采用2%、3%、5%硝酸溶液(V/V)均无法将As(Ⅲ)从巯基SPE小柱上洗脱。利用洗脱液中巯基与巯基键合材料中巯基相互争夺As(Ⅲ)的原理,采用巯基乙醇(10%)+硝酸溶液(3%)洗脱,回收率也只达到60%。最终,用含KIO3(0.1 mol/L)稀硝酸溶液洗脱,利用碘酸钾将硅烷链末端-SH氧化,使材料失去吸附作用的原理,洗脱回收率达到了96%(结果见表3)。因此,结合ICP-MS法检测,最终选取As(Ⅲ)洗脱液为KIO3(0.1 mol/L)+硝酸(2%)。

表3 不同洗脱液As(Ⅲ)的回收率
2.3 实际样品检测
2.3.1 pH值及样品流速
样品经0.15 mol/L稀硝酸提取砷后,溶液pH值较低,氨基功能化SPE小柱在pH<3的条件下吸附率有所下降。氨基功能化SPE小柱和巯基功能化SPE小柱在pH<4的条件下能选择性吸附As(Ⅴ)与As(Ⅲ),排除了有机砷干扰。因此选择在移取10 mL试样溶液后,用0.1 mol/L的氢氧化钠溶液调节移取的溶液pH值至3~4再进行吸附。
样品的流速也会影响不同形态砷在材料上的保留行为,流速过高溶液保留时间过短,萃取不完全;流速过低则使检测速度变慢效率较低。实验中所制备的氨基、巯基键合硅胶材料粒径较小填充后溶液通过性较差,因此制备了粒径稍大的SiO2粉末混合于硅胶材料填充,在不影响吸附率的前提下提高了溶液的通过性。实验考察了不同流速下,As(Ⅲ)和As(Ⅴ)的回收率(结果见图4)。结果表明溶液流速在0.1~1 mL/min时,回收率可达到90%以上,随着流速继续增大,回收率变低。考虑到实际样品基质的影响,为了使样品溶液中砷能够被充分萃取,选择了0.5 mL/min作为样品溶液的流速及洗脱流速。
2.3.2 样品检测结果对比与加标回收率
为验证方法的实用性与准确性,利用所建立的固相萃取小柱分离富集三种不同基质的样品:紫菜、扇贝粉、小鱼干中As(Ⅲ)和As(Ⅴ),SPE-ICP-MS测定三种基质样品无机砷含量均低于100 μg/kg,6次重复实验相对平均偏差在4.1%~30.6%(结果见表4),除较低含量样品外该方法精密度(RSD)均在20%以下满足日常检测需求。
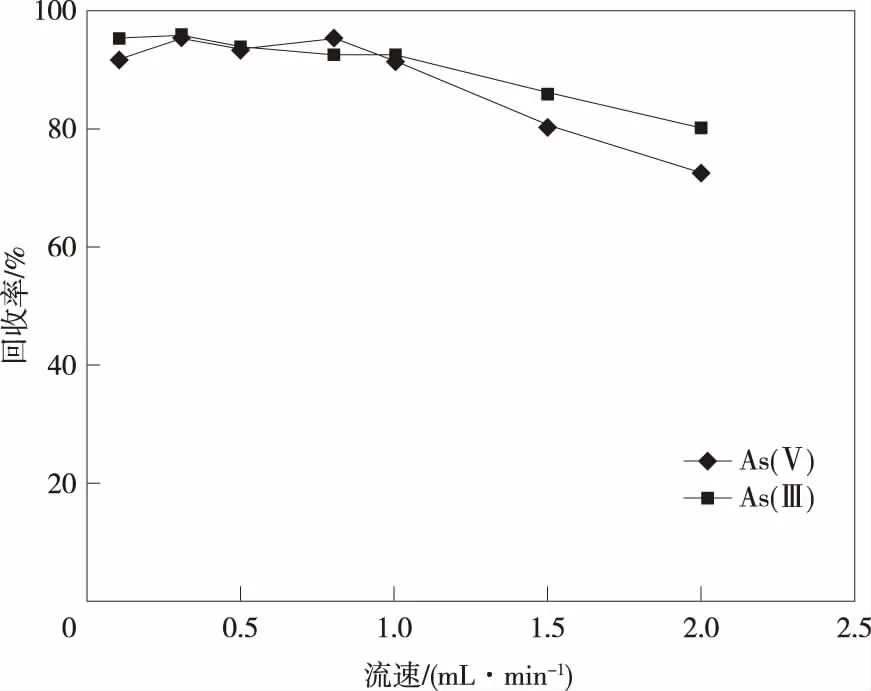
图4 不同流速下As(Ⅲ)和As(Ⅴ)的回收率
ICP-MS法检测结果与HPLC-AFS法检测结果进行比较(见表5),结果表明三种基质样品用不同方法检测结果基本一致,相对标准偏差小于20%。实验采用加标回收的方式考察所检测样品结果的准确性(见表6),加标回收率在72.3%~102%,表明方法用于海产品中无机砷的检测结果准确。

表4 SPE-ICP-MS法精密度结果

表5 不同方法检测结果对比

表6 实际样品检测加标回收结果
3 结论
利用各类硅烷试剂水解、缩聚的原理,将氨基官能团与巯基官能团键合到了硅烷链中,成功制备了能够选择性吸附无机砷的硅胶材料。分段式氨基化小柱与巯基化小柱联用能够排除有机砷以及As(V)与As(Ⅲ)之间的相互干扰,所建立的固相萃取小柱-电感耦合等离子体质谱法测定无机砷的方法通过手动分离可以实现样品总砷与无机砷快速同时检测,方法相对标准偏差小于20%,样品加标回收率在72.3%~102%。该方法用于海产品中无机砷形态的测定结果准确,操作简单,提高效率的同时降低了检测成本,可作为食品检测与安全评价的另一种检测手段。
