阿比特龙联合多西他赛对前列腺癌患者的有效性及安全性评价
2021-02-15金姗静陈海飞王建新
金姗静 陈海飞 王建新
[摘要] 目的 探讨阿比特龙联合多西他赛临床治疗前列腺癌(PCa)患者的有效性及安全性。 方法 选择2018年4月至2019年3月在我院接受治疗的70例前列腺癌患者,依据随机数字表法分为联合组、对照组,各35例,两组均给予常规口服泼尼松片,对照组在此基础上静脉滴注多西他赛,联合组在对照组基础上加用阿比特龙片进行治疗。比较两组患者治疗前后的特异性前列腺抗原(PSA)、血清白蛋白(ALB)、血清前蛋白(PA)及中性粒细胞计数、谷丙转氨酶及睾酮水平,观察两组患者临床疗效及不良反应发生情况。 结果 两组治疗前PSA、ALB、PA、中性粒细胞、谷丙转氨酶、睾酮指标比较,差异无统计学意义(P>0.05);与治疗前比较,两组治疗后ALB、PA、谷丙转氨酶指标升高,PSA、中性粒细胞计数、睪酮指标降低,差异有统计学意义(P<0.05);与对照组比较,联合组ALB、PA、中性粒细胞计数水平较高,PSA、谷丙转氨酶、睾酮水平较低,差异有统计学意义(P<0.05);对照组临床有效率低于联合组,但差异无统计学意义(P>0.05);联合组不良反应总发生率高于对照组,差异无统计学意义(P>0.05)。 结论 阿比特龙联合多西他赛治疗前列腺癌患者临床效果优秀,优化患者各项指标表达,且安全性更高,值得临床应用推广。
[关键词] 阿比特龙;多西他赛;前列腺癌;特异性前列腺抗原
[中图分类号] R737.25 [文献标识码] B [文章编号] 1673-9701(2021)36-0097-04
Efficacy and safety of abiraterone combined with docetaxel in patients with prostate cancer
JIN Shanjing1 CHEN Haifei1 WANG Jianxin2
1.Operating Room, Taizhou First People's Hospital in Zhejiang Province, Taizhou 318020, China; 2.Uropoiesis Surgical Department, Taizhou First People's Hospital in Zhejiang Province, Taizhou 318020, China
[Abstract] Objective To investigate the efficacy and safety of abiraterone combined with docetaxel in the clinical treatment of patients with prostate cancer (PCa). Methods A total of 70 patients with prostate cancer treated in our hospital from April 2018 to March 2019 were selected. They were divided into the combination group and the control group using random number table method, with 35 patients in each group. Both groups were given conventional oral prednisone tablets. The control group were given additional intravenous docetaxel, and the combination group were given additional abiraterone tablets combined with intravenous docetaxel. The specific prostate antigen (PSA), serum albumin (ALB), serum proprotein (PA), neutrophil count, alanine aminotransferase and testosterone before and after treatment were compared between the two groups. The clinical efficacy and incidence of adverse events were observed in both groups. Results There were no significant differences in PSA, ALB, PA, neutrophils, alanine aminotransferase, and testosterone indicators between the two groups before treatment,the difference was not statistically significant (P>0.05). After treatment, the ALB, PA, and alanine aminotransferase indicators were increased in both groups, and PSA, neutrophil count, and testosterone indicators were decreased in both groups, the difference was statistically significant (P<0.05). The levels of ALB, PA, and neutrophil count in the combination groups were higher than those in the control group, and the levels of PSA, alanine aminotransferase, and testosterone in the combination group were lower than those in the control group, the difference was statistically significant (P<0.05). The clinical effective rate in the control group was lower than that in the combination group, but the difference was not statistically significant (P>0.05). The total incidence of adverse events in the combination group was higher than that in the control group, the difference was not statistically significant (P>0.05). Conclusion Abiraterone combined with docetaxel has excellent clinical effects in the treatment of patients with prostate cancer. It can optimize expression of various indicators with higher safety. It is worthy of clinical application and promotion.
[Key words] Abiraterone; Docetaxel; Prostate cancer; Prostate specific antigen
前列腺癌(Prostatecancer,PCa)属于泌尿科男性比较常见的恶性肿瘤疾病,患病初期没有明显症状,后期治愈难度大,且死亡率高[1]。目前前列腺癌患者接受的治疗方式主要是用药、手术抑制,但绝大部分患者在治疗后,会由激素敏感性前列腺癌发展为去势抵抗性前列腺癌,治疗难度变高[2]。阿比特龙片作为一种高选择性、高亲和力的CYP17酶抑制剂,其自身具有起效快的药物作用,能够轻松阻断前列腺组织、睾丸、肾上腺组织中癌细胞、病原体的合成[3-4]。多西他赛作为一种有丝分裂抑制剂药物,其主要在微管/微丝蛋白系统中起作用,使微管/微丝蛋白形成稳定非功能性微管束,起到抑制癌细胞增殖的作用[5-6]。基于上述研究背景,在本研究中前列腺癌采用阿比特龙联合多西他赛治疗,前列腺癌患者使用阿比特龙联合多西他赛是否更优,对患者细胞因子功能产生如何影响,现报道如下。
1 对象与方法
1.1 研究对象
选择2018年4月至2019年3月我院收治的70例前列腺癌患者,年龄22~70岁,按照随机数字表法将其分为联合组、对照组各35例。两组患者一般资料比较见表1。本研究所有患者及其家属均知情并签署知情同意书,经过我院医学伦理委员会批准,自愿参与本研究。纳入标准:①符合《前列腺癌早期诊断专家共识》[7]诊斷标准;②年龄≥18周岁的男性;③未进行过放、化疗者;④前4周内未使用酮康唑治疗者。排除标准:①有病毒性肝炎史或肝功能异常者;②隐睾、单侧睾丸或缺失睾丸等先天缺陷者;③肾上腺皮质或垂体功能减退者;④近6个月内进行过重大手术者;⑤高血压、转氨酶水平异常及恶性肿瘤者。
1.2 治疗方法
两组均给与常规口服泼尼松片(浙江仙琚制药股份有限公司,国药准字H33021207)5 mg,2次/d;对照组在常规基础上采用静脉滴注多西他赛注射液(江苏奥赛药业股份有限公司,批号H20064301)150 mL,2次/d;联合组在对照组基础上给予阿比特龙片(西安杨森制药有限公司,国药准字J20150112,规格:0.25 g×120片)0.25 g,3次/d,空腹口服。3周为1个疗程,治疗总疗程为6周。
1.3 检测方法
1.3.1 样本采集 两组患者接受治疗后在晨起空腹状态下,进行抽血采样9 mL,离心12 min,收集血清备用,放于5℃低温箱中保存、待检;每日采集患者尿液10 mL,放于5℃低温箱中保存、待检。
1.3.2 两组治疗前后PSA、ALB、PA、谷丙转氨酶水平表达检测方法 采用酶联免疫吸附法检测PSA、ALB、PA、谷丙转氨酶指标,样本采集、保存参照1.3.1;提前30 min取出西卡林试剂盒(SIKARU,加拿大),放置室温;将浓缩洗涤液以1∶30的比例用双蒸水稀释;配置酶结合物工作液,用试剂稀释液稀释浓缩酶结合物(1∶100)产生酶结合物工作液;打开试剂盒,将试剂稀释液混合样本添加于西卡林试剂盒酶标板孔中,放置10 min,观察数值并记录样本浓度;将不同浓度样本加入样本孔中,在每个样本孔中加入5 μL样本稀释液和样本,再依次加入50 μL生物素化抗体工作液,使用封板胶纸密封反应孔,放置30 min,读取数值;清洗酶标板孔5次,每孔加洗涤液350 μL,30 s后清理孔内液体,用吸水纸干燥;使用普卡自动微粒免疫器(PUKEI日本)再次测试样本PSA、ALB、PA、谷丙转氨酶浓度并记录;对PSA、ALB、PA、谷丙转氨酶指标进行检测,在酶标仪上450 nm波长下调节、读取指标数值。
1.3.3 两组治疗前后中性粒细胞、睾酮水平表达检测方法 使用免疫组织化学法检测,从低温箱中取出患者尿液样本,接着将所有器具经高压灭菌处理后,收集总RNA并由其逆转录生成cDNA,利用样本尿液配备浓度3 μL的RNA反应体系,准备mmvl、dNTPS、5rt缓冲溶液0.78 L、132 μL、0.26 μL,在室温下,反应30 min。然后,配备RT-PCR反应测定体系,其包括cDNA、引物及探针化合物、无核酸酶水、一般化合物分别为1.79 μL、7.46 μL、1.98 μL、120 mL,内参基因为睾酮指标。上游:5’-GCCTCTCCAAGGAAGAATCC-3’,下游:5’-TCCTGTTGTTGGACAGGTCA-3’,开始化学反应,97℃下反应0.3 h,之后降至56℃,再反应120 s,反复50次。中性粒细胞、睾酮表达量经2-△△ct计算得到。
1.3.4 疗效评价标准 参考世界卫生组织(WHO)实体肿瘤评价标准,完全缓解(CR):病灶完全消失且未出现新的肿瘤;部分缓解(PR):病灶直径减少>50%;稳定(SD):病灶直径减少<50%或者增大<20%,未出现新的肿瘤;进展(PD):原有病灶增大或者出现新的病灶。总有效率=(CR例数+PR例数+SD例数)/总例数×100%。记录两组患者治疗期间低血钾、高血糖、体液潴留、脱发等不良反应发生情况。
1.4 统计学方法
采用SPSS 26.0统计学软件进行数据分析处理。计量资料采用均数±标准差(x±s)描述,组间比较采用独立样本t检验,计数资料采用[n(%)]表示,组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组患者一般资料比较
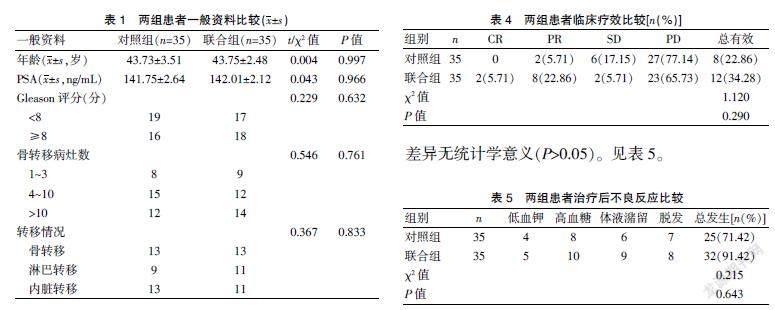
两组患者年龄、PSA、Gleason评分、骨转移病灶数、转移情况相比较,差异无统计学意义(P>0.05)。见表1。
2.2 两组患者治疗前后PSA、ALB、PA表达比较
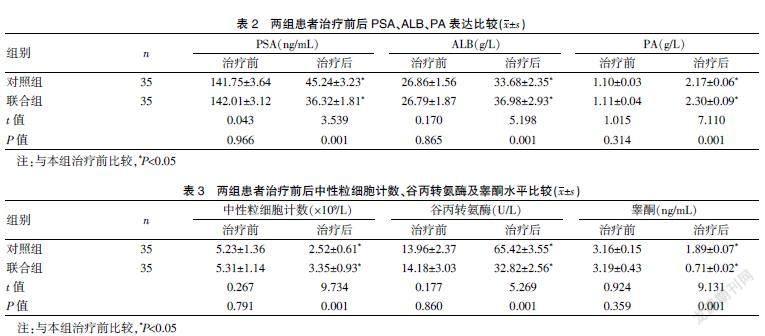
两组治疗前PSA、ALB、PA比较,差异无统计学意义(P>0.05);与治疗前比较,两组治疗后ALB、PA指标升高,PSA指标降低,联合组ALB、PA水平高于对照组,PSA水平低于对照组,差异有统计学意义(P<0.05)。见表2。
2.3 两组患者治疗前后中性粒细胞、谷丙转氨酶、睾酮表达比较
两组治疗前中性粒细胞、谷丙转氨酶、睾酮比较,差异无统计学意义(P>0.05);与治疗前比较,两组治疗后中性粒细胞计数、睾酮指标降低,谷丙转氨酶指标升高,联合组中性粒细胞计数指标高于对照组,谷丙转氨酶、睾酮指标低于对照组,差异有统计学意义(P<0.05)。见表3。
2.4 两组患者临床疗效比较
对照组临床总有效率略低于联合组,差异无统计学意义(P>0.05)。见表4。
2.5 两组患者治疗后不良反应比较
联合组治疗后不良反应总发生率稍高于对照组,差异无统计学意义(P>0.05)。见表5。
3 讨论
前列腺癌在癌症发病率中名列前茅,属于前期隐蔽性非常高的恶性肿瘤疾病[9-11]。引起前列腺癌的主要原因是癌细胞内被雄激素持续刺激所致,故前列腺癌发病快,死亡率高,给患者及家属带来经济、心理上的双重压力[12]。目前临床上已有研究将阿比特龙联合多西他赛应用于前列腺癌患者的治疗追踪,结果发现,阿比特龙联合多西他赛可明显改善前列腺癌患者临床症状,促进疾病恢复。
细胞色素P45017A1(CYP17A1)酶在雄激素合成的生化途徑上是催化生成合成雄激素所必须的前提产物,并且是肾上腺及前列腺癌细胞合成雄激素的重要途径[13]。PSA作为前列腺管分泌的一种无活性特异性蛋白,其水平的高低可以用来辨别前列腺组织是否发生病变[14]。而前列腺组织分泌的特异性前列腺抗原进入血液循环中后与发生病变所引起的局部炎症组织反应,从而引起淋巴细胞与上皮细胞受损[15]。血浆中大量存在着ALB、PA,其主要参与脏器和组织修复过程,其水平的高低主要反映全身炎症程度表现,导致ALB、PA水平指标异常的原因为前列腺癌导致部分脏器损坏而引起病原菌侵入[16]。本研究结果表明,两组治疗后ALB、PA指标升高,PSA指标降低,联合组ALB、PA水平高于对照组,PSA水平低于对照组。结果表明,阿比特龙联合多西他赛治疗前列腺癌效果显著,两者联合可改变患者免疫功能,起到提升抵抗力等作用。
多西他赛作为一种细胞毒性化疗药物,可以诱导肿瘤细胞代谢、凋亡[17-19];阿比特龙作为一种细胞色素酶抑制剂,完全抑制睾丸所分泌的雄激素,同时阿比特龙对细胞色素酶CYP17的活性产生抑制效果,进一步抑制肾上腺及前列腺组织中癌细胞合成分泌雄激素,从而延缓疾病进展[20-22]。本研究结果中,联合组治疗后的中性粒细胞计数、谷丙转氨酶水平、睾酮水平均得到明显改善,部分使用阿比特龙联合多西他赛治疗的患者出现高血糖、脱发等药物不良反应,但大多不良反应并不需要临床干预,采用阿比特龙联合多西他赛治疗前列腺癌安全性很高。本研究结果显示,阿比特龙联合多西他赛治疗能显著延长前列腺癌患者的终点指数(总生存时间),阿比特龙联合多西他赛治疗前列腺癌临床具有可行性,能有效抑制疾病进展。
综上所述,治疗前列腺癌使用阿比特龙联合多西他赛效果明显,优化患者各指标表达,有效缓解临床症状,促进细胞免疫功能指标恢复,安全性很高,值得临床应用推广。
[参考文献]
[1] 潘悦,郑克文,陈伟.CIP2A在高危局限性前列腺癌中的表达及临床意义[J].中国现代医生,2020,58(2):49-51.
[2] 胡玉洁,潘虹,蒋梦捷,等.戈舍瑞林联合比卡鲁胺治疗转移性前列腺癌术后患者的临床效果[J].中国现代医生,2020,58(24):17-20.
[3] 杨涛,那扎罗.阿比特龙药物代谢在前列腺癌治疗中的意义及研究进展[J].中国男科学杂志,2021,35(1):60-63.
[4] 苏梦,宋娟,张伶俐.阿比特龙联合泼尼松治疗晚期转移性去势抵抗性前列腺癌的疗效观察[J].浙江临床医学,2021,23(6):871-872,875.
[5] 秦庆伟,李那,王胜,等.多西他赛化疗对局限期高危前列腺癌疗效及安全性的荟萃分析[J].中华泌尿外科杂志,2019,40(11):853-858.
[6] 段丽群,张曲,刘三河,等.多西他赛再挑战治疗转移性去势抵抗性前列腺癌的疗效及预后因素[J].肿瘤防治研究,2019,46(9):819-824.
[7] 中华医学会泌尿外科学分会前列腺癌联盟.中国前列腺癌早期诊断专家共识[J].中华泌尿外科杂志,2015, 36(8):561-564.
[8] 徐梓宁,黄敬君,周娟,等.程序性死亡受体-1单抗在肝动脉化疗栓塞辅以分子靶向药物治疗后进展期肝细胞癌的疗效分析[J].中华内科杂志,2021,60(7):630-636.
[9] 王俊涛,王悬,于洁,等.益肾化痰方联合伊班膦酸钠治疗前列腺癌骨转移疼痛的临床观察[J].中医药学报,2021,49(2):67-70.
[10] 彭世荣,马晓明,李泽安,等. 神经胶质瘤肿瘤抑制因子候选区基因1对前列腺癌细胞增殖及迁移能力的影响[J]. 中华实验外科杂志,2021,38(6):1053-1055.
[11] 何清柳,张建育,颜醒愚.伊班膦酸钠与唑来膦酸治疗前列腺癌骨转移的临床疗效分析[J].中国现代医生,2019,57(30):83-85.
[12] Miyahira AK,Sharp A,Ellis L,et al. Prostate cancer research:The next generation; report from the 2019 Coffey-Holden Prostate Cancer Academy Meeting[J].Prostate,2020,80(2):113-132.
[13] Lu S,Zhong J,Zhang Y,et al. CYP17A1 polymorphisms are linked to the risk of coronary heart disease in acase-control study[J]. J Cardiovasc Pharmacol,2019,74(2):98-104.
[14] 李梅桂,黄国定,刘海剑,等.间歇性内分泌辅以中药治疗晚期前列腺癌的疗效及对PSA、VEGF和免疫功能的影响[J].肿瘤药学,2021,11(3):337-341.
[15] 王雅丽,红华,吴国柱,等.前列腺钙化、PSA、Gleason评分与前列腺癌骨转移的相关性分析[J].中国超声医学杂志,2020,36(5):458-462.
[16] 林鑫,翟泰宇,孙轶华.血清C-反应蛋白与血清白蛋白的比值与恶性肿瘤患者预后评估的关系[J].标记免疫分析与临床,2019,26(10):1778-1781.
[17] 魏松长,杨红琪,张宏娟,等.RON蛋白与CXC趋化因子受体4蛋白的表达与去势抵抗型前列腺癌患者阿比特龙耐药的相关性[J].中国临床药理学与治疗学,2021,26(4):414-422.
[18] 黄荏钊,郑锐年,梁镇锋,等.阿比特龙联合泼尼松治疗非转移性去势抵抗性前列腺癌的对比研究[J].新医学,2021,52(5):365-370.
[19] 胡林军,李长岭,寿建忠,等.多西他赛治疗转移性去势抵抗性前列腺癌的耐受剂量及其与预后的关系[J].中华泌尿外科杂志,2019,40(1):31-36.
[20] 赵宏毅,王亮.唑来膦酸联合多西他赛治疗雄激素非依赖性前列腺癌[J].实用医学杂志,2019,35(16):2633-2636.
[21] 李鑫钊,刘大闯,梁清,等. 醋酸阿比特龙、多西他赛分别联合泼尼松治疗转移性去势抵抗性前列腺癌疗效比较[J]. 山东医药,2021,61(20):79-81.
[22] 王慧,趙善坤,刘世雄,等. 再次服用阿比特龙治疗转移性前列腺癌的价值[J]. 中国全科医学,2021,24(26):3387-3391.
(收稿日期:2021-08-09)
