亚临界水快速合成MoVOx复合金属氧化物及其催化苯甲醇气相氧化性能研究
2021-02-11刘永威李双明卢自轩邓璐瑶李鹏飞于三三
刘永威,李双明,卢自轩,邓璐瑶,李鹏飞,张 旭,于三三
(沈阳化工大学 化学工程学院, 辽宁 沈阳 110142)
在化学化工等领域,选择性氧化是一类极为重要的反应[1-2],通过该过程可制取一系列种类繁多的化工产品,如烯烃、醛、酮、酸、酯等[3-7].因此,该反应过程无论在工业生产还是科学研究中都受到了广泛的关注.对于氧化脱氢反应,其工艺的核心在于催化剂,这也是该领域一直以来的研究热点.迄今为止,各种不同类型的催化剂被用于该反应过程[1,8-9],其中,Mo-V基复合金属氧化物在丙烷氧化制丙烯酸、氨氧化制丙烯腈[10-13]、甘油氧化脱水制丙烯酸[14-15],以及乙烷氧化制乙烯[16]等诸多氧化反应中,均表现出了优越的催化性能,已成为目前最具发展前景和研究价值的一类选择性氧化催化剂[17].
研究表明:Mo-V基复合金属氧化物的性质在很大程度上取决于晶相、形貌等微观结构,而这些微观结构又与催化剂的制备方法息息相关[2,18-19].目前,用于制备Mo-V基复合金属氧化物的方法包括水热合成法[20]、溶胶法[21]、共沉淀法[22]和溶剂热法[6]等.水热合成法是其中应用最广泛的方法.Ishikawa等人使用水热合成法制备了正交晶系、纤维棒状结构的MoVO晶体[16].Konya等使用水热合成法制备了正交、三角及四方晶系的MoVO晶体[23].Zhang等使用水热合成法,通过控制前驱体溶液的酸碱度,选择性地合成了正交或三角晶系具有棒状结构的MoVO催化剂[24].然而,无论采用哪种方法,制备所得样品均需经过后续高温煅烧处理才能形成所需晶相.例如:Yun等采用水热法制备的前驱体在N2气氛、600 ℃条件下煅烧处理2 h获得了MoVTeNbCeO催化剂[25];Rasteiro等将水热法制得的催化剂前体在500 ℃氧化气氛中热处理2 h合成了Mo4.65V0.35O14、MoV2O8晶相[15].
相较于上述方法,本文采用一种无需高温煅烧处理的亚临界水技术合成MoVOx复合金属氧化物,并考察体系温度以及Mo与V物质的量的比对产物晶相组成、形貌、氧化还原能力、比表面积等微观结构和催化性能的影响.通过该方法反应1 h即可获得主晶相为V0.95Mo0.97O5的产物,且在苯甲醇气相选择性氧化制苯甲醛的反应中表现出了优异的催化性能.
1 实验部分
1.1 原料与试剂
四水合钼酸铵[(NH4)6Mo7O24·4H2O]、偏钒酸铵(NH4VO3)、苯甲醇(C7H8O)、苯甲醛(C7H6O)均为分析纯,国药集团化学试剂有限公司;去离子水(H2O)为实验室自制;甲苯(C7H8)、苯甲酸甲酯(C8H8O2),天津恒兴化学试剂制造有限公司.
1.2 MoVOx的制备
按照一定的Mo与V物质的量的比,称取一定量钼酸铵[(NH4)6Mo7O24·4H2O]和偏钒酸铵(NH4VO3),于80 ℃下搅拌,溶解于25 mL去离子水中,得到橙黄色透明前驱液.将该前驱液转移至高温反应釜中,密闭后将反应体系加热至一定温度,并在该温度下保持1 h.反应结束后将反应体系进行抽滤、去离子水洗涤2~3次,所得样品在60 ℃下充分干燥,经压片、破碎、筛分得到20~40目催化剂成品.
1.3 结构表征
采用X射线衍射仪(D/max-2200型,日本理学公司)表征MoVOx复合金属氧化物的晶相结构(XRD),Cu靶、Kα射线,管电压40 kV,管电流30 mA,扫描速度2 (°)/min,扫描范围2θ=10°~80°,步长为0.02°.N2吸附脱附分析(BET)采用布鲁克公司的D8 Advance型仪器进行测试,样品测试前于120 ℃下真空处理5 h.SEM分析采用日本日立公司的S-4800型场发射扫描电镜.程序升温还原(H2-TPR)采用美国康塔全自动程序升温化学吸附仪(ChemBET Pulsar)进行测试,试样用量均为0.1 g,在Ar气氛下升到500 ℃,维持30 min,以便脱除吸附水和二氧化碳等,随后降至30 ℃,切换为体积分数为10%的H2-Ar混合气体,并以10 ℃/min升至900 ℃.
1.4 催化测试
采用连续式反应器进行催化测试,在固定床不锈钢反应器(内径为8 mm,长400 mm)中进行苯甲醇脱氢氧化.将0.15 g MoVOx复合金属氧化物装入反应器中部,苯甲醇经过微量泵(LC3000型,北京创新通恒科技有限公司)泵入汽化炉,汽化后与氧气、氮气等原料气混合进入反应器.其中,n(苯甲醇)∶n(氧气)∶n(氮气)=1∶1.1∶4.4,反应温度控制在220~300 ℃.反应产物经冷凝后收集,以乙醇为溶剂、苯甲酸甲酯为内标物,使用高效液相色谱(安捷伦1260,美国)进行分析,检测波长为250 nm,检测器为DAD.
2 结果与讨论
2.1 XRD分析
图1(a)为在亚临界水体系400 ℃条件下、不同Mo与V物质的量的比制备的MoVOx的XRD结果.从图1(a)中可以看出:制备所得样品中的主要晶相为V0.95Mo0.97O5(PDF 77-0649),在2θ为14.63°、21.94°、24.96°、26.36°、29.51°、32.64°、33.43°、36.91°和44.93°的衍射峰分别对应于V0.95Mo0.97O5结构的(1 0 0)、(0 1 0)、(-1 0 1)、(-1 1 0)、(2 0 0)、(-2 0 1)、(0-1 1)、(-2 1 0)和(3 0 0)晶格平面.除V0.95Mo0.97O5晶相外,在Mo与V物质的量的比为1∶1.1、1∶1.3和1∶1.5的样品衍射图中,还出现了明显的VO2(PDF 44-0253,2θ为27.68°、37.12°、55.36°)衍射峰.由MAUD分析晶相含量结果[图1(b)]可知:当Mo与V物质的量的比为1∶0.4时,V0.95Mo0.97O5晶相含量(摩尔分数,以下同)最高,为99.09%;而随着Mo与V物质的量的比的减小,V0.95Mo0.97O5晶相含量呈明显下降趋势,VO2含量则由0.91%[n(Mo)∶n(V)=1∶0.4]增加到24.11%[n(Mo)∶n(V)=1∶1.5].结合图1(a)和图1(b)分析可知:利用亚临界水制备MoVOx时,前驱液中Mo与V物质的量的比对产物的晶相组成有显著的影响.通过调整Mo与V物质的量的比可获得V0.95Mo0.97O5和VO2不同比例的复合晶相.
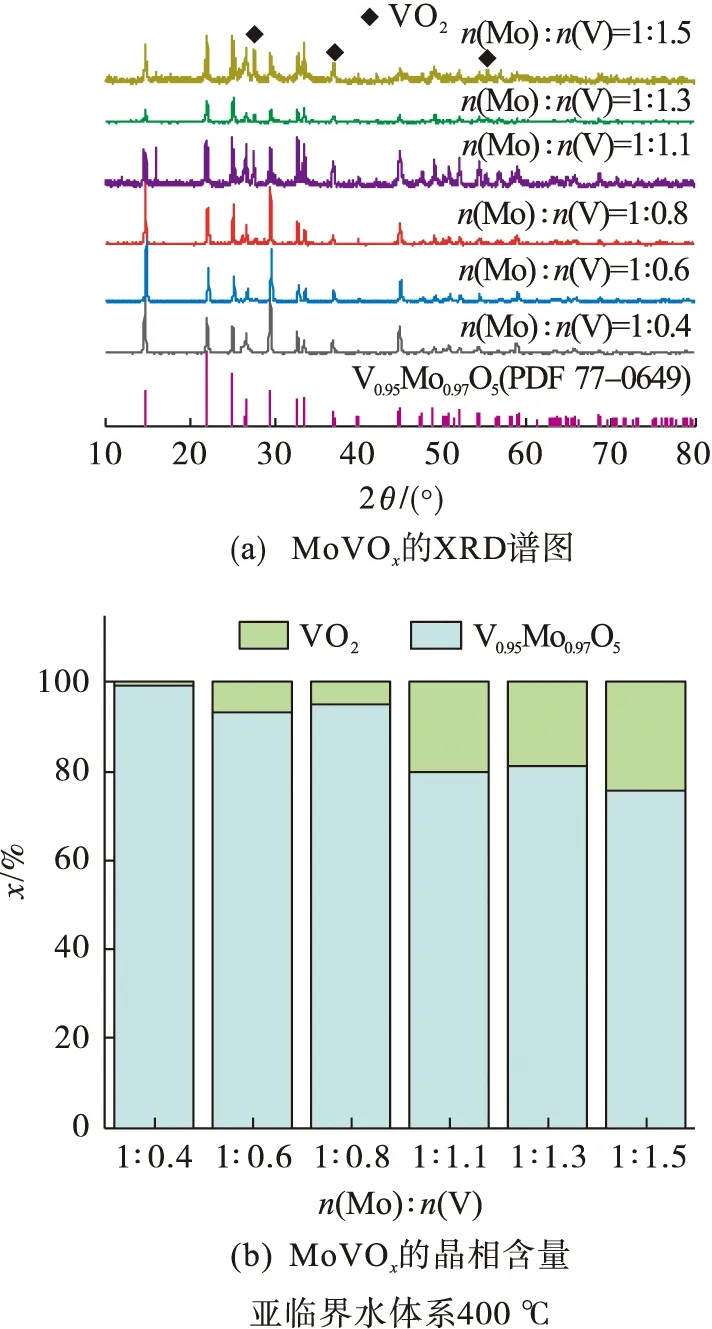
图1 不同Mo与V物质的量的比制备的MoVOx的XRD谱图和晶相含量Fig.1 XRD spectra and crystal phase composition of MoVOx prepared with different molar ratio of Mo to V
图2(a)和2(b)为Mo与V物质的量的比为1∶0.4在不同亚临界水体系温度下制备的MoVOx样品的XRD谱图和相应晶相含量结果.图2结果表明:亚临界水体系温度对制备产物的物相组成具有显著的影响.当体系温度较低(320 ℃)时,产物中含有V0.95Mo0.97O5、V2O5(PDF53-0538)、Mo8O23(PDF84-1248)和VO2四种晶相,含量分别为66.69%、26.28%、6.08%和0.95%;温度升高至340 ℃和360 ℃时,Mo8O23衍射峰消失;而当体系温度为380 ℃和400 ℃时,产物中则只有V0.95Mo0.97O5和V2O5两种晶相.由此可知,当Mo与V物质的量的比一定时,亚临界水体系温度越高越有利于MoVOx复合金属氧化物的形成,在400 ℃条件下,几乎可以定量地获得MoVOx(V0.95Mo0.97O5),相反则会出现较多的单金属氧化物.

图2 不同亚临界水体系温度下制备的MoVOx样品的XRD谱图和晶相含量Fig.2 XRD patterns and crystal phase composition of MoVOx prepared at different subcritical water system temperatures
2.2 SEM分析
图3为Mo与V物质的量的比为1∶0.4在不同亚临界水体系温度下制备的MoVOx样品的SEM图.由图3可知:制备的样品均展现出多层纳米片状和棒状结构.在亚临界水体系温度为320 ℃时,MoVOx以棒状结构为主,同时还有少量的片层结构;随着亚临界水体系温度的升高,样品分散性得到明显提高,尤其在360 ℃时,MoVOx样品表现出较为均匀的片层结构[图3(c)];而在380 ℃时,样品主要由不规则的片状结构组成[图3(d)];在400 ℃时,MoVOx呈现出由多个纳米片层叠加而形成的棒状结构[图3(e)、(f)].


n(Mo)∶n(V)=1∶0.4图3 不同亚临界水体系温度下制备的MoVOx样品的SEM图Fig.3 SEM images of MoVOx prepared at different subcritical water system temperatures
图4为亚临界水体系400 ℃下以不同Mo与V物质的量的比制备的MoVOx的SEM图.由图4可知:在一定的亚临界水体系温度下,Mo与V物质的量的比的改变对MoVOx的形貌具有显著的影响.当Mo与V物质的量的比为1∶0.6时,合成的MoVOx产物具有较长的棒状结构,表面光滑,长度约为3~9 μm,表面有少量的晶粒附着;随着Mo与V物质的量的比减小,棒状结构的长度逐渐减小,在Mo与V物质的量的比为1∶1.1时,约为1~3 μm,且分布均匀;而在Mo与V物质的量的比为1∶1.5时,MoVOx出现了明显的团聚现象.


图4 不同Mo与V物质的量的比制备的MoVOx的SEM图Fig.4 SEM images of MoVOx prepared with different molar ratio of Mo to V
2.3 H2-TPR测试分析
催化剂的氧化还原性是影响其催化性能的重要因素,而且在氢气还原过程中,还原温度的高低能在一定程度上反映金属氧化物内部晶格氧的移动速度.图5(a)为亚临界水体系温度为400 ℃、不同Mo与V物质的量的比制备的MoVOx的H2-TPR图.图5(b)为不同亚临界水体系温度下Mo与V物质的量的比为1∶0.4时制备的MoVOx样品的H2-TPR图.从图5中可以看出:所有样品都有一个明显的还原峰.根据文献报道[26],温度在600~750 ℃的还原峰主要是由Mo6+→Mo4+、V5+→V4+的还原引起的.改变Mo与V物质的量的比,其H2-TPR曲线发生了显著的变化,还原温度随Mo与V物质的量的比的减小而出现降低趋势.当Mo与V物质的量的比为1∶0.6时,还原温度为751 ℃,在651 ℃存在一个宽峰;当Mo与V物质的量的比为1∶0.8时,还原温度为691 ℃,同时在634 ℃存在1个肩峰;当Mo与V物质的量的比为1∶1.3时,还原温度为621 ℃,表明活性中心变得更加活跃.在Mo与V物质的量的比为1∶0.4的条件下,改变亚临界水体系温度对还原温度影响不大,只有亚临界水体系温度在380 ℃时制备的样品的还原温度出现了下降.

图5 MoVOx样品的H2-TPR图Fig.5 H2-TPR diagrams of MoVOx sample
2.4 BET测试分析
图6为在不同条件下制备的MoVOx样品的N2吸附/脱附等温线.
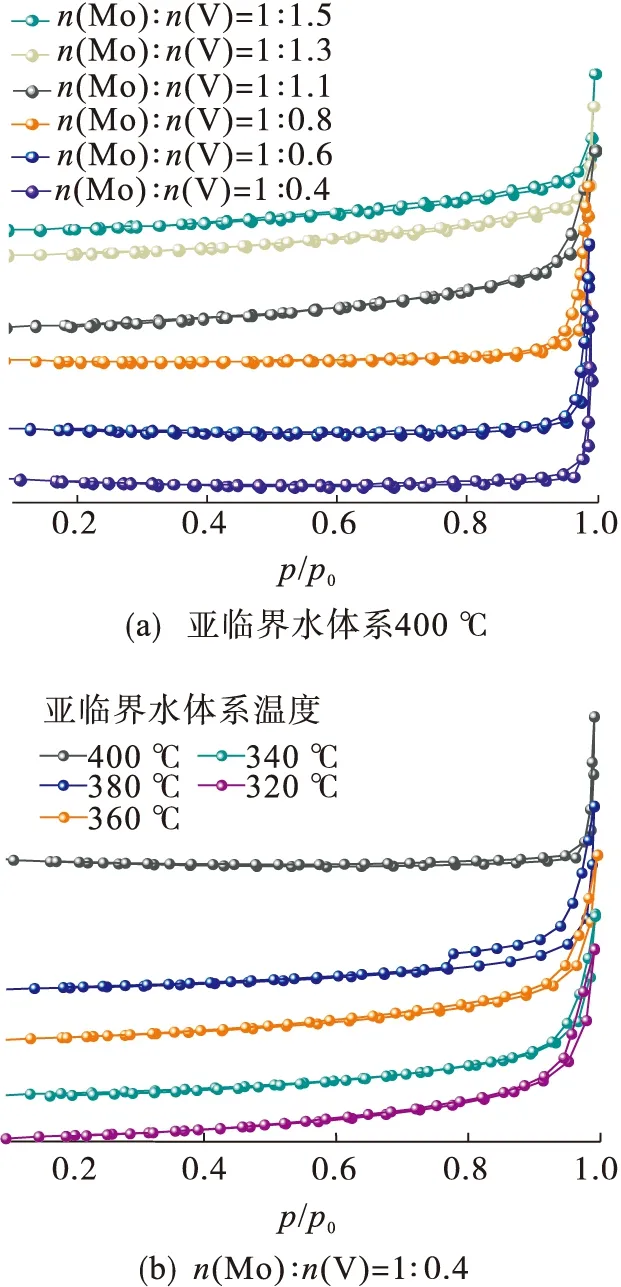
图6 MoVOx样品的N2吸附/脱附等温线Fig.6 N2 adsorption-desorption isotherms of MoVOx sample
由图6(a)可知:MoVOx样品具有Ⅲ型的等温线.相对压力较低时,均为单分子层吸附,表现为典型微孔吸附; 在 0.78
0.8时均变陡,吸附量突然增大.此外,380 ℃下制备样品的回滞环面积要明显大于其他温度,说明该样品中除了微孔外,可能还存在一些介孔或大孔结构.
不同条件下制备的MoVOx复合金属氧化物的比表面积和孔特性参数如表1所示.从表1中可以看出:当Mo与V物质的量的比为1∶0.4时,随着亚临界水体系温度的增加,MoVOx样品的比表面积先增加后减小,比表面积由6.16 m2/g(320 ℃)先增加至6.96 m2/g(360 ℃),然后又下降到4.14 m2/g(400 ℃);孔容积由0.046 cm3/g(320 ℃)增加到0.053 cm3/g(400 ℃),平均孔径在15~27 nm.当亚临界水体系温度为400 ℃时,随着Mo与V物质的量的比的减小,MoVOx样品的比表面积也表现出先增大后减小的趋势,比表面积由4.14 m2/g(Mo与V物质的量的比为1∶0.4)增加到8.97 m2/g(Mo与V物质的量的比为1∶0.8),平均孔径在12~32 nm之间,孔容积在Mo与V物质的量的比为1∶1.5时最小,为0.038 cm3/g.

表1 不同亚临界水条件下制备的MoVOx样品的比表面积和孔特性Table 1 Specific surface area and pore properties of the MoVOx as prepared under different subcritical water conditions
2.5 催化性能测试
不同Mo与V物质的量的比制备的MoVOx选择性氧化苯甲醇的催化性能如图7所示.由图7 可以看出:在不同的催化温度下,随着Mo与V物质的量的比的减小,苯甲醇的转化率呈现出不同的变化趋势,Mo与V物质的量的比为1∶0.8的样品在300 ℃时转化率达到最高,为55%[图7(d)];对苯甲醛的选择性在59%~98%之间,其中Mo与V物质的量的比为1∶0.4的样品,在反应温度250 ℃时表现出最大的选择性,这可能与其含有高含量V0.95Mo0.97O5(99.09%)晶相有关(图1).此外,催化剂的活性很大程度上也受比表面积的影响,比表面积较大有利于增加催化剂与反应物接触,提高MoVOx的活性.由图7和表1可知:苯甲醇在280 ℃、300 ℃反应温度下的转化率趋势与MoVOx样品比表面积的变化趋势一致,Mo与V物质的量的比为1∶0.8样品的比表面积最大是其苯甲醇转化率最大的原因之一.有文献表明[27],催化剂的还原性对其催化性能也有一定的影响.结合H2-TPR结果(图5)分析,Mo与V物质的量的比的减小使MoVOx的还原温度降低,进而对转化率产生了有利影响.

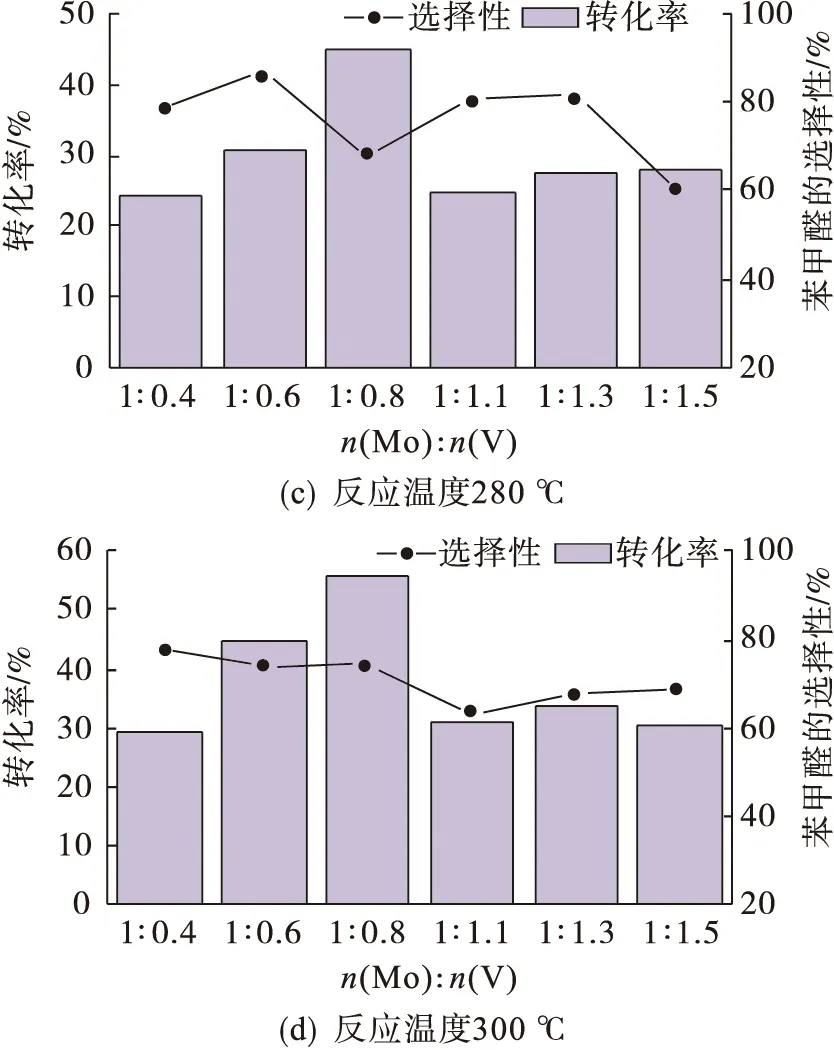
图7 在亚临界水体系400 ℃条件下不同Mo与V物质的量的比制备的MoVOx催化氧化苯甲醇结果Fig.7 Results of catalytic oxidation of benzyl alcohol by MoVOx prepared with different molar ratio of Mo to V when the subcritical water is 400 ℃
图8为不同亚临界水体系温度制备的MoVOx,在不同反应温度下对苯甲醇催化氧化结果.从图8中可以看出:在不同的催化温度下,随着亚临界水体系温度的升高,苯甲醇的转化率呈现出不同的变化趋势.其中,亚临界水体系温度380 ℃的样品在催化温度300 ℃时转化率达到最高,为40.0%[图8(d)].由BET结果分析可知:该样品具有包含微孔、介孔的特殊结构,可能对苯甲醇的转化率产生有利的影响.此外,由图2(b)可知:在不同亚临界水体系温度下制备的MoVOx样品的晶相组成明显不同.在320 ℃下制备的MoVOx含有V0.95Mo0.97O5、V2O5、Mo8O23和VO2四种混合晶相,单金属氧化物,尤其是Mo8O23晶相含量较大,这可能是导致其苯甲醇转化率偏低的主要原因.苯甲醛的选择性在77.0%~98.0%之间,高于不同Mo与V物质的量的比制备样品的苯甲醛选择性,说明在亚临界水制备体系中,与制备温度相比,Mo与V物质的量的比对产物苯甲醛选择性的影响更加显著.

图8 在Mo与V物质的量的比为1∶0.4条件下不同亚临界水体系温度制备的MoVOx催化氧化苯甲醇结果Fig.8 Results of catalytic oxidation of benzyl alcohol by MoVOx prepared at different water system subcritical temperatures when the molar ratio of Mo to V is 1∶0.4
3 结 论
采用亚临界水快速合成了MoVOx复合金属氧化物,并将其作为催化剂应用于苯甲醇选择性氧化脱氢反应.与传统水热法相比,亚临界水技术制备时间短,且无需经过后续高温煅烧处理即可获得所需晶相.研究结果表明:Mo与V物质的量的比和亚临界水体系温度对MoVOx晶相组成、形貌、氧化还原性和比表面积等微观结构有显著影响.制备所得MoVOx复合金属氧化物的主要晶相为V0.95Mo0.97O5,减小Mo与V物质的量的比,VO2晶相逐渐增多;而降低亚临界水体系温度,会产生V2O5和Mo8O23晶相.在亚临界水体系温度为400 ℃、Mo与V物质的量的比为 1∶0.4体系下,合成的MoVOx中V0.95Mo0.97O5晶相含量为99.09%,该样品在苯甲醇选择性氧化脱氢反应中,对苯甲醛的选择性达到98.0%.
