妊娠SD大鼠血糖指标值的系统评价和单组连续变量Meta分析*
2021-02-10江心泳赖玉婷黄萍萍庞书勤于红虹
江心泳 葛 莉 赖玉婷 黄萍萍 陈 凡 庞书勤 于红虹
(福建中医药大学护理学院,福州 350122)
随着我国二胎政策放开,高龄产妇和经产妇人群数量不断增加,2004—2018年妊娠期糖尿病(gestational diabetes mellitus,GDM)的总体患病率高达12.85%,远超国际水平,并且呈持续增长趋势[1]。根据钟婕等[2]报道,GDM不仅可增加早产、巨大儿、胎儿畸形等不良妊娠结局的发生率,而且增加母亲和其子代患代谢性疾病的风险。由于开展临床研究困难性大,因此应用相关实验动物开展研究尤显重要。洪雅青等[3]和李鑫等[4]研究发现SD大鼠因其具有孕期适中(21 d)的特点,且支持短期内大量复制GDM模型而被广泛应用于相关实验研究。动物血液生化指标是动物实验重要而敏感的指标,也是药物安全性评价实验中必不可少的检测项目[5]。空腹血糖(fasting blood glucose,FBG)和血清空腹胰岛素(fasting serum insulin,FINS)是检测妊娠大鼠罹患GDM的重要指标[6-7]。目前大多数研究判断患GDM的SD大鼠,FBG为6.7~16.7 mmo/L,差值范围大且缺乏统一标准。另外,FINS作为协助FBG判断GDM的指标仍未有明确范围[7-9]。因此,本研究通过对妊娠SD大鼠血糖FBG和FINS的Meta分析,旨在探讨二者的参考值上限,为患GDM 的SD大鼠模型的构建及FBG和FINS指标的标准区间提供参考。
1 材料和方法
1.1 文献检索
计算机检索中国知网、维普、万方、Web of Science、Cochrane Library、Scopus、PubMed、EMBase和MEDLINE共9个数据库中与妊娠SD大鼠血糖相关的文献,检索时限为2014年1月—2020年12月,采用主题词和自由词结合的方式进行检索,并根据不同数据库特征进行检索式调整以确定最终的检索方式。英文检索词包括“Rat*”、“Rattus”、“Rattus norvegicus”、“Rats, Norway”、“Rat*, Laboratory”、“Laboratory Rat*”、“Blood Glucose”、“Diabetes Mellitus”、“Diabetes, Gestational”、“Blood Sugar”、“Sugar, Blood”、“Glucose, Blood”、“Pregnanc*”、“Gestation”及“Gravidit*”;中文检索词包括“大鼠”、“血糖”、“糖尿病”、“妊娠期糖尿病”和“妊娠”。
1.2 纳入与排除标准
纳入标准:研究对象为妊娠 SD大鼠,实验观察指标包含妊娠期FBG和FINS。排除标准:会议报告、病例报告、综述、个案报道和以人为对象的实验研究、重复发表或结局指标不全、无法获取全文的文献及干预中应用改变大鼠生理状态药物的文献。
1.3 文献筛选与资料提取
由两名研究者通过阅读文章题目、摘要及全文,严格按照纳入与排除标准独立进行文献筛选,完成后提取相关资料并交叉核对。如遇分歧,由双方讨论或与第三名研究者讨论,形成统一意见。资料提取主要包括第一作者、发表年份、国家、样本量、入组周龄、体质量、FBG、FINS、禁食时间、血液采集部位和实验所用血糖仪厂家。
1.4 文献质量评价
由两名研究者采用SYRCLE动物实验偏倚风险评估工具(SYRCLE’s risk of bias tool for animal studies)[10]进行文献质量评价,如有争议则与第三名研究者讨论,形成统一意见。该工具评价内容包括10个条目、22个亚条目以及随机序列的生成、基线特征、分配隐藏、动物安置随机化、盲法(实施偏倚)、随机性评估结果、盲法(测量偏倚)、结局指标完整性、选择性报告研究结果和其他偏倚来源。该工具评估结果最终以“是”、“否”和“不确定”表示,其中“是”代表低风险偏倚,“否”代表高风险偏倚,“不确定”代表不确定风险偏倚。
1.5 数据分析方法
1.5.1单组连续变量Meta分析:应用STATA15.0软件进行Meta分析,收集原始研究数据中已直接报告的SD大鼠FBG和FINS的均值和标准差,以加权均数差(Weighted Mean Difference,WMD)和95%可信区间(Confidence Interval,CI)为合并统计量。通过I2对文献进行异质性检验,当I2<50%且P≥0.1认为不存在异质性,采用固定效应模型;若I2>50% 且P<0.1则采用随机效应模型进行分析,同时对存在异质性的研究进行亚组分析,寻找可能造成异质性的因素[11]。

2 结果
2.1 文献检索结果
初步检索共获取文献2 359篇,剔除重复文献644篇,通过阅读文献标题和摘要,排除1 428篇;通过阅读全文,排除250篇,最终纳入37篇文献,文献筛选流程如图1。

图1 文献筛选流程图
2.2 纳入文献基本特征及质量评价
本研究共纳入文献37篇,包括29篇中文文献和8篇英文文献;32篇来自中国,其余5篇来自美国、沙特阿拉伯、坦桑尼亚、马来西亚和伊朗。文章共包括428只SD大鼠,最大样本量为20只,最小样本量为5只。纳入的文献中,8篇检测了妊娠第0周的FBG;23篇检测了妊娠第1周的FBG和FINS;22篇检测了妊娠第2~3周的FBG和FINS。纳入研究的基本特征,具体见表1。
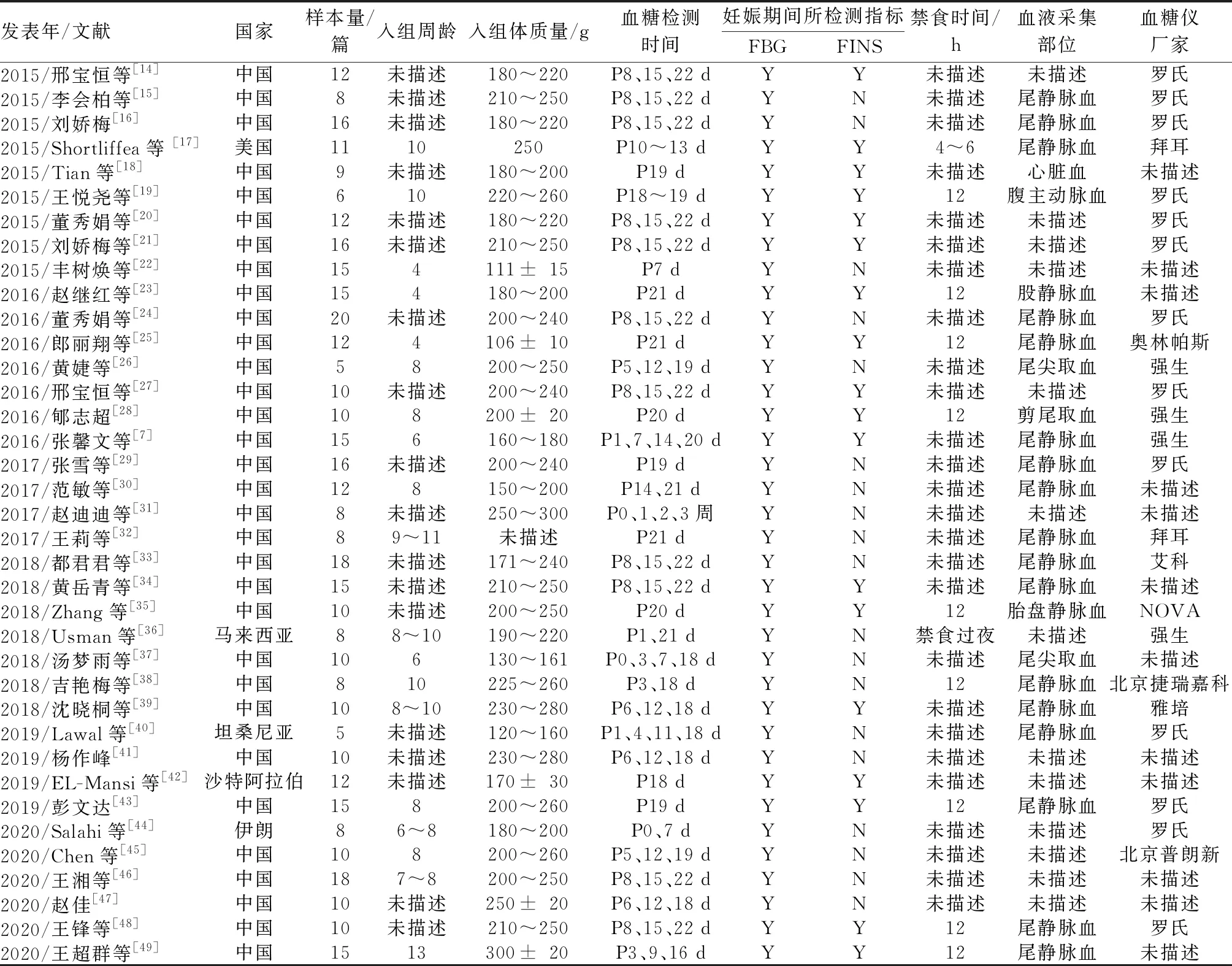
表1 纳入文献基本特征
2.3 文献质量评价
风险评估结果如图2,纳入的37篇研究中,6篇[7,22-23,34-35,49]明确表示采用随机数字表法进行序列生成,8篇[15-16,20-21,24,27,29,39]未采用随机方式产生序列;37篇基线特征均衡;两篇研究[34,49]采用分配隐藏,12篇[14-16,20-21,24,26-27, 32,42,47-48]未实现分配隐藏;6篇[19,26-28,35,42]未提供完整数据,另有张馨文等[7]一篇提供完整数据但未说明失访理由。纳入的所有文献在动物安置随机化,盲法(实施/测量偏倚)和随机性结果评估中均未有明确报告。

图2 风险评估
2.4 数据分析结果
2.4.1妊娠期间SD大鼠FBG参考值上限
2.4.1.1妊娠第0周FBG参考值上限:共7篇文献检测大鼠妊娠第0周的FBG[7,21,27,31,38,40,49],异质性检验结果P=0.000 < 0.1,I2=98.6%,异质性高。

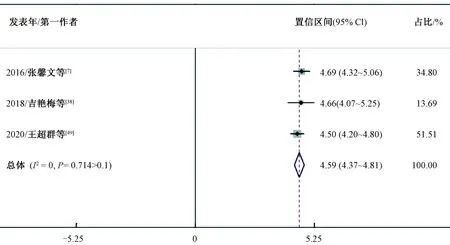
图3 妊娠第0周尾静脉取血FBG森林图


图4 妊娠第1周尾静脉取血FBG森林图

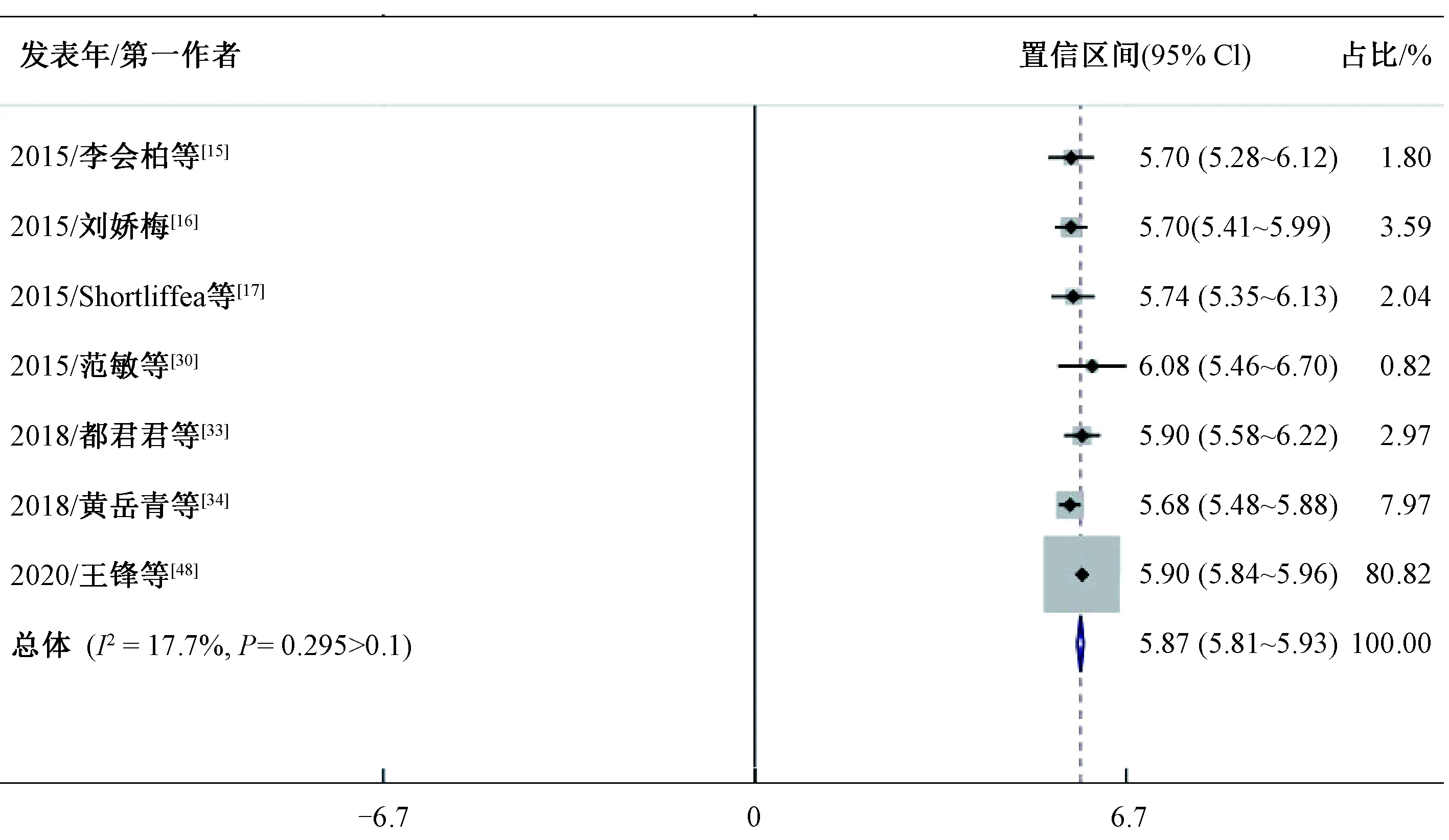
图5 妊娠第2周尾静脉取血FBG森林图
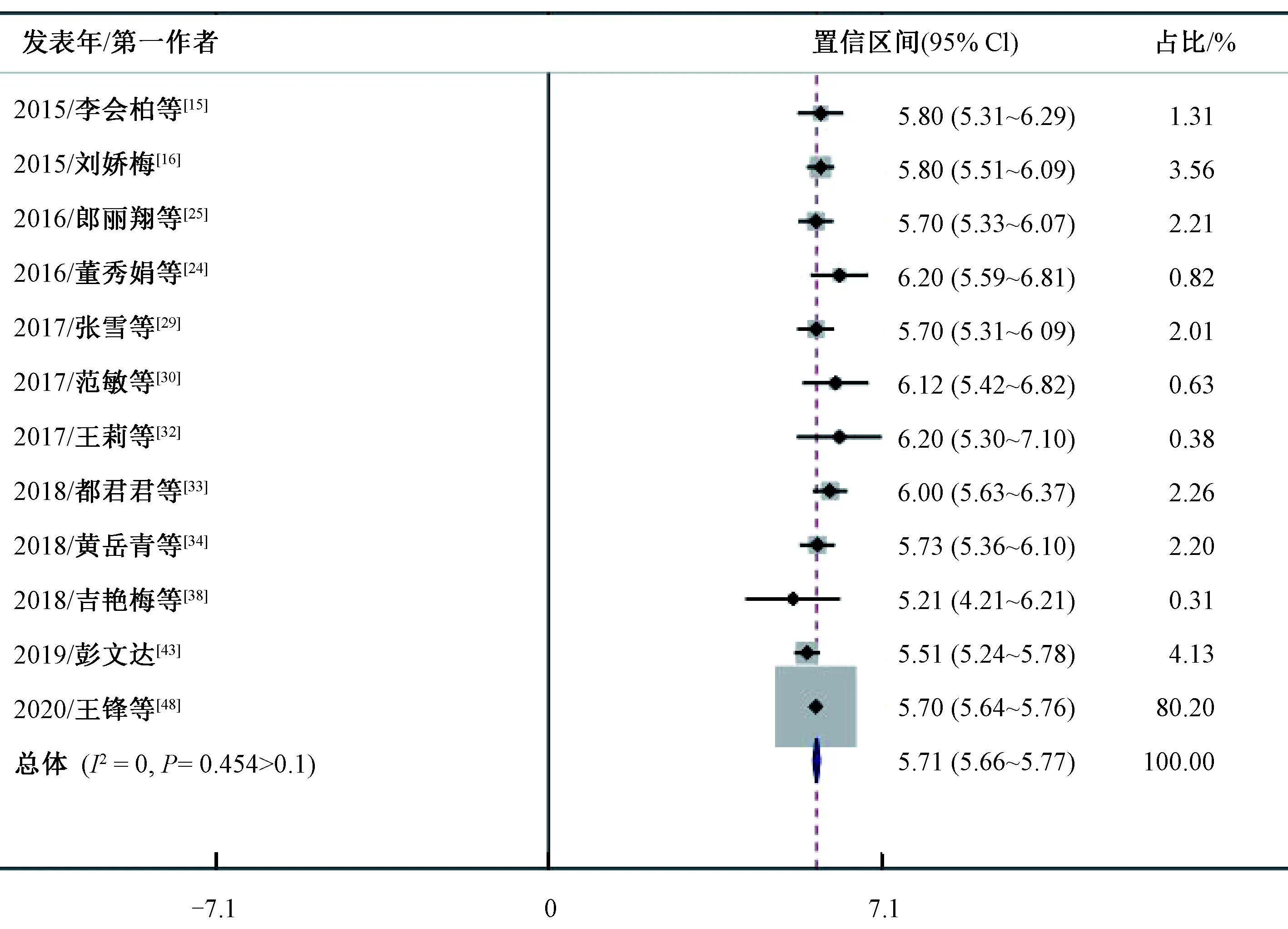
图6 妊娠第3周尾静脉取血FBG森林图
2.4.2妊娠期间SD大鼠FINS参考值上限


图7 妊娠第1周FINS森林图

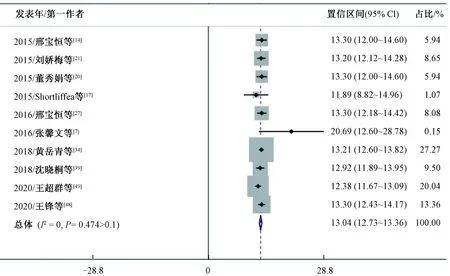
图8 妊娠第2周FINS森林图


图9 妊娠第3周FINS森林图
3 讨论
3.1 FBG对GDM大鼠成模判断的意义
FBG是判断妊娠大鼠是否罹患GDM最直观的动物血液生化学指标,也是临床上用于检测GDM的常规指标[6,50]。FBG作为一项容易测量且数值直观的指标,应用于判定GDM大鼠模型是否成模。例如:蒋静等[51]、李佳等[52]和税迎春等[53]研究均采用FBG作为判断GDM大鼠成模的标准。因此,本研究对FBG进行系统评价和Meta分析以得出其成模标准。
3.2 FBG和FINS结果影响因素
研究发现,不同采血部位的FBG检测结果存在明显差异。本研究纳入的37篇文献中,有17篇采取尾静脉取血的方式检测FBG,而其余部位较少。张秀青[54]发现,静脉采血结果较末梢采血稳定。同时,尾静脉取血操作简单,对实验动物造成的损伤极小,可多次重复测量大鼠模型FBG值。因此,SD大鼠尾静脉采血用于检测FBG,可作为判定GDM大鼠的成模标准。大鼠体质量也会影响FBG,而且大部分研究仅对入组时的大鼠体质量进行了描述,缺乏对妊娠期间体质量数据。程臻等[55]研究显示,超重及肥胖与血糖指标的结果密切相关。Thamban等[56]的研究结果显示,GDM发生的危险性会随着妊娠前的BMI的升高而增大。此外,肥胖可导致炎性细胞因子增多,促炎性和抗炎性细胞因子表达失衡,从而导致IR或GDM[57]。禁食时间的长短也可影响FBG和FINS结果。王超群等[49]和汤琦等[58]研究表明,实验动物禁食时间过长会影响正常的糖代谢,引起低血糖反应。因此,在今后研究中应完善妊娠期间体质量的描述,明确大鼠在妊娠前未出现体质量过高的情况,同时明确禁食时间和采血部位以稳定FBG检测结果。
3.3 GDM SD大鼠的FBG成模标准的确立
汤梦雨等[37]、蒋静等[51]及祁秀茹等[59]研究判断SD大鼠患GDM时FBG为6.7~16.7 mmol/L,差值范围大且缺乏统一标准。因此,本研究通过对纳入文章中的数据Meta分析,得出妊娠期间4个阶段的FBG成模标准。同时,因不同采血部位的检测结果存在明显差异,故本研究FBG成模标准主要为尾静脉取血,不明确采血部位的结果予以排除,FBG结果分别为第0周5.51 mmol/L,第1周6.92 mmol/L,第2周6.64 mmol/L以及第3周7.04 mmol/L。同时,根据系统评价结果显示,GDM大鼠的成模判断时间多在妊娠第1周时进行[14-15]。因此,本研究选取妊娠第1周异质性低的结果数据合并,GDM的SD大鼠模型的成模标准为FBG>6.92 mmol/L,即妊娠SD大鼠FBG检测结果>6.92 mmol/L即可判断为出现GDM。
3.4 不足之处
本研究对符合纳入标准的37个动物实验依据进行质量评价,发现存在4方面不足,如下:①在随机序列的产生中,21.6%的研究,随机分配方法出现高风险及62.2%的研究未对随机分配方法进行描述;②对动物研究方法的介绍中,32.4%的研究在分配隐藏的描述中显示了高风险,62.2%研究分配隐藏方法不确定,仅5.4%的研究介绍了分配隐藏方法;③所有研究均未报道动物安置随机化、盲法以及随机性结果评估;④18.9%的研究未对失访动物是否会对结局造成偏倚进行评估。以上不足会对本研究结果带来偏倚风险。
综上所述,本研究共纳入428只妊娠SD大鼠。首次进行妊娠SD大鼠FBG系统评价和Meta分析,初步确认SD大鼠在妊娠第0~3周的FBG和FINS参考值上限。FBG,第0周:5.51 mmol/L;第1周:6.92 mmol/L;第2周:6.64 mmol/L;第3周:7.04 mmol/L。FINS,第0周:无统计数据;第1周:15.66 mIU/L;第2周:15.98 mIU/L;第3周:15.63 mIU/L。以上FBG和FINS参考值上限的确定可能为今后SD大鼠相关实验提供指标参考,减少不同实验中因参考值标准不同而带来的实验误差。
