机器人辅助袖状胃切除术操作指南(2020年版)
2021-02-06中国研究型医院学会微创外科学专业委员会中国医药教育协会代谢病学专业委员会
中国研究型医院学会微创外科学专业委员会,中国医药教育协会代谢病学专业委员会
肥胖症与糖尿病是严重危害人类健康的两种密切相关的慢性疾病,发病率逐年上升。目前,中国有超过9 000万的肥胖症、超过1亿的糖尿病患者,数量均居世界第一,其中超重与肥胖人群的糖尿病患病率已达12.8%与18.5%[1-3]。袖状胃切除术在显著减轻患者体重的同时可有效改善糖尿病等肥胖相关的合并症。袖状胃切除术与传统胃旁路术手术效果相当,且具有操作简单、手术时间短、并发症少等一系列优点,现已成为主流的减重与代谢手术方式。2016年袖状胃切除术在北美(57.18%)、亚洲(64.65%)、中国(64.61%)均是使用频率最高的减重与代谢手术方式[4-5]。随着我国腹腔镜技术的逐渐普及,袖状胃切除术多在腹腔镜下完成。而达芬奇手术机器人系统在继承腹腔镜技术微创特点的同时,完美模拟了人类的3D视野及人手关节的灵活性,消除了人手颤抖,增加了操作稳定性,在肥胖患者关键部位的操作中可有效降低手术难度,增加手术安全性。Sudan等于2007年报道了机器人胆胰分流并十二指肠转位术,其中机器人辅助袖状胃切除术作为手术的一部分被首次提出,此后得到同行专家的认可与学习[6]。我国大陆地区机器人辅助袖状胃切除术于2015年初陆续开展,处于快速增长期[7]。但国内外仍缺少相应的规范手术操作指南[8-9]。为进一步推动机器人辅助袖状胃切除术操作的规范化与标准化进程,国内相关领域专家共同编写首版《机器人辅助袖状胃切除术操作指南(2020版)》,以保证机器人辅助袖状胃切除术的安全性与疗效。本指南主要针对机器人辅助袖状胃切除术操作进行详细探讨,关于手术适应证、禁忌证及术前术后全程化的管理请参考腹腔镜袖状胃切除术[10-11]。
1 机器人袖状胃切除术步骤
1.1 患者体位、腹腔探查、Trocar布局、机器人的连接
1.1.1 患者体位、腹腔探查 因术中不便于更改体位,在机械臂就位前,应先进行腹腔镜探查并调整患者体位。患者取仰卧位,于脐孔上缘或下缘穿刺Trocar作为观察孔,置入机器人光学镜探查。注意穿刺孔下方有无脏器损伤、脂肪肝、大网膜堆积等情况,并观察是否存在食管裂孔疝及脏器表面有无肿瘤或其他病变。如果胃腔内气体、胃液较多,建议先经口置入胃引导管或电子胃十二指肠镜将气体、胃液排除干净,以利于显露、操作。如有腹腔粘连,可在腹腔镜下先处理粘连,再调整机器人体位。探查完毕后,患者取头高脚低15°~20°并躯体向右侧旋转15°~20°[12]。根据助手的操作习惯,助手可立于患者两侧。麻醉医生立于患者头侧,器械护士立于第一助手的右下方。
1.1.2 Trocar布局 根据术中使用手术机器人系统机械臂的数量可将手术分为4+1模式、3+2模式。4+1模式是指术者操控四枚机械臂,助手操作一枚腹腔镜器械;3+2模式是指术者操控三枚机械臂,两个助手各操作一枚腹腔镜器械。
1.1.2.1 U形法(5孔) 见图1A。4+1模式:脐孔上缘或下缘穿刺Trocar作为观察孔,置入机器人光学镜。左、右腋前线肋缘下2 cm处穿刺Trocar,置入机械臂。左、右锁骨中线平脐水平线上方2 cm处穿刺Trocar,置入机械臂或腹腔镜器械。相邻Trocar间距>8 cm,避免机械臂相互干扰。3+2模式:左、右锁骨中线平脐水平线上方2 cm的Trocar均置入腹腔镜器械。
1.1.2.2 U形法(4孔) 可根据术者习惯及机器人操作系统类型,减少左或右锁骨中线平脐上2 cm处的Trocar,其余与五孔U形法相同。
1.1.2.3 W形法(5孔) 见图1B。4+1模式:脐孔上缘或下缘穿刺Trocar作为观察孔,置入机器人光学镜。左、右腋前线肋缘下2 cm处穿刺Trocar,置入机械臂。左、右锁骨中线平脐下2 cm处穿刺Trocar,置入机械臂或腹腔镜器械。相邻Trocar间距>8 cm,避免机械臂相互干扰。3+2模式:左、右锁骨中线平脐水平线下方2 cm的Trocar均置入腹腔镜器械[13]。
1.1.2.4 W形法(4孔) 可根据术者习惯及机器人操作系统类型,减少左或右锁骨中线平脐下2 cm处的Trocar,其余与五孔W形法相同。
1.1.2.5 斜N形法(5孔) 见图1C。脐上缘或下缘穿刺Trocar作为观察孔,置入机器人光学镜;右侧腋前线与脐水平线交点穿刺Trocar,置入腹腔镜器械;右侧锁骨中线与脐上5 cm水平线交点处穿刺Trocar,置入机械臂;左侧锁骨中线与脐上3 cm水平线交点处穿刺Trocar,置入腹腔镜器械;左侧腋前线与剑突、脐连线中点水平线交点处穿刺Trocar,置入机械臂[14]。
1.1.2.6 L形法(5孔) 见图1D。脐上偏左穿刺Trocar作为观察孔,置入机器人光学镜;右腋前线与观察孔水平线交点上方2 cm处穿刺Trocar,置入机械臂。左锁骨中线、左腋前线与观察孔水平线处穿刺Trocar,置入机械臂。右腋前线的Trocar与观察孔连线的中点穿刺Trocar,置入腹腔镜器械。
1.1.2.7 L形法(4孔) 如果术中利用吊线或其他方法进行肝脏暴露,可在L形法(5孔)基础上减少左腋前线与观察孔水平线处的Trocar。
以上方法均可根据术者操作需要决定是否置入牵拉器或用悬吊法牵拉左肝外侧叶,以显露术野。
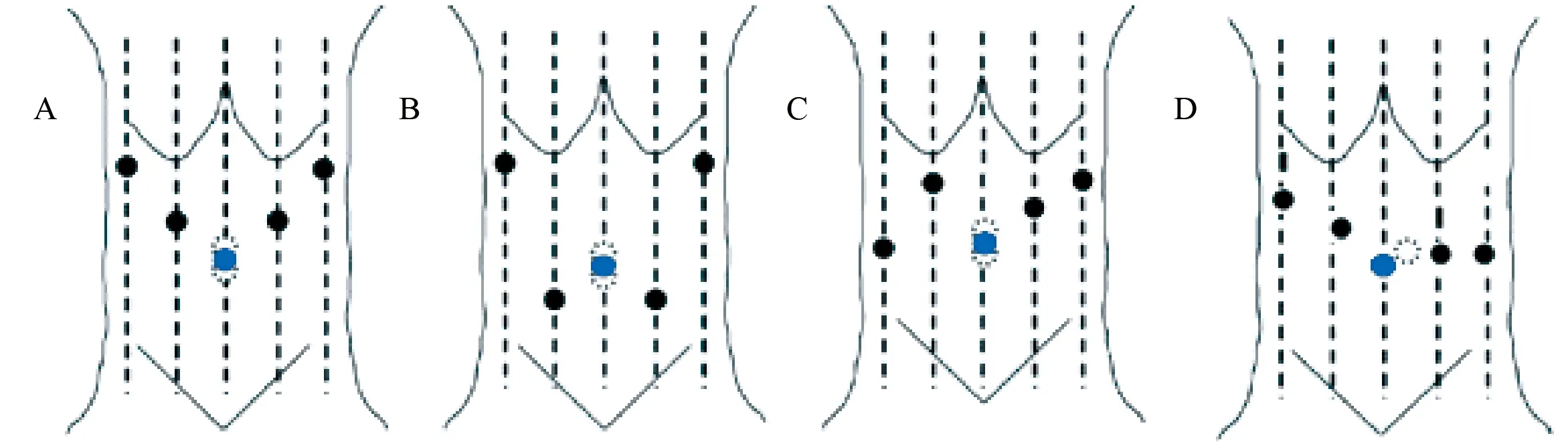
图1 Trocar布局(A:U形法布局;B:W形法布局;C:斜N形法布局;D:L形法布局;黑球为Trocar位置,蓝球为脐部,虚线为观察孔位置,A~C可根据患者情况放置脐上或脐下)
1.2 显露幽门、游离胃大弯 显露并识别幽门管或幽门前静脉,顺大弯侧向头侧方向用标尺测量2~6 cm,确定切割起始点(图2A、2B)。由起始点沿胃大弯、于网膜血管弓内用超声刀开始游离。进入网膜囊后(图2C、2D)向上依次离断胃大弯侧弓内的血管及胃短血管,完全游离胃大弯(图2E、2F)。
手术要点及难点对策:游离起始点可选择距幽门近端2~6 cm,此处多为胃网膜及结肠系膜融合处,应注意解剖层次;也可选择胃角对侧作为游离起始点,此处大网膜较薄,便于进入小网膜囊后再向胃底及幽门方向游离。
处理胃短血管时,有时胃短血管过短,用超声刀分离时应靠近胃壁进行,以免损伤脾脏导致出血。
1.3 游离胃底、胃后壁,显露His角 将胃壁向患者右上方牵拉或挑起胃后壁,适当处理胃胰韧带、胃后壁与胰腺被膜的粘连带,充分游离胃底及胃后壁,充分显露左侧膈肌脚,同时处理胃后血管,保证His角的完全显露(图3)。
手术要点及难点对策:(1)胃胰韧带、胃后壁与胰腺被膜的粘连带是导致胃后壁显露困难的重要原因,应充分分离,便于显露。此处也会遇到胃后血管或左膈下血管向胃的分支,应注意识别与处理。(2)术中应充分显露左膈肌脚,避免处理完胃底与脾脏上极粘连后即认为分离完成,导致出现由His角分离不完全而引起的胃底残留。(3)游离胃后壁时,超声刀工作面避免直接接触,以防止超声刀热损伤胃壁。(4)术中应注意有无食管裂孔疝的情况,如果合并食管裂孔疝,且满足以下条件时需联合处理,否则会减弱减重效果:①诊断明确的Ⅱ~Ⅳ型食管裂孔疝;②药物治疗效果不明显或出现其他并发症的滑动型食管裂孔疝[15]。可行胃底折叠联合部分袖状胃切除术或Nissen胃底折叠联合袖状胃成形术[16-17]。
1.4 袖状胃切除术 请台下助手经口置入32~40 Fr胃支撑管或电子胃镜,贴近胃小弯通过幽门进入十二指肠,如通过幽门环困难,也可将胃支撑管或电子胃镜贴近胃小弯靠近幽门处,并调整胃支撑管或胃镜位置,使其贴近小弯侧(图4A)。建议距幽门2~6 cm处作为切割起始点(图4B)。调整钉仓尖端方向,沿距胃支撑管0.8~1.0 cm连续切割,切割线的末端需离贲门左侧1.0~1.5 cm(图4C~4F)。

图2 显露幽门、游离胃大弯(A:显露幽门;B:确认起始点(箭头所指位置);C、D:打开胃结肠韧带;E、F:于血管弓内游离胃大弯)

图3 游离胃底及胃后壁
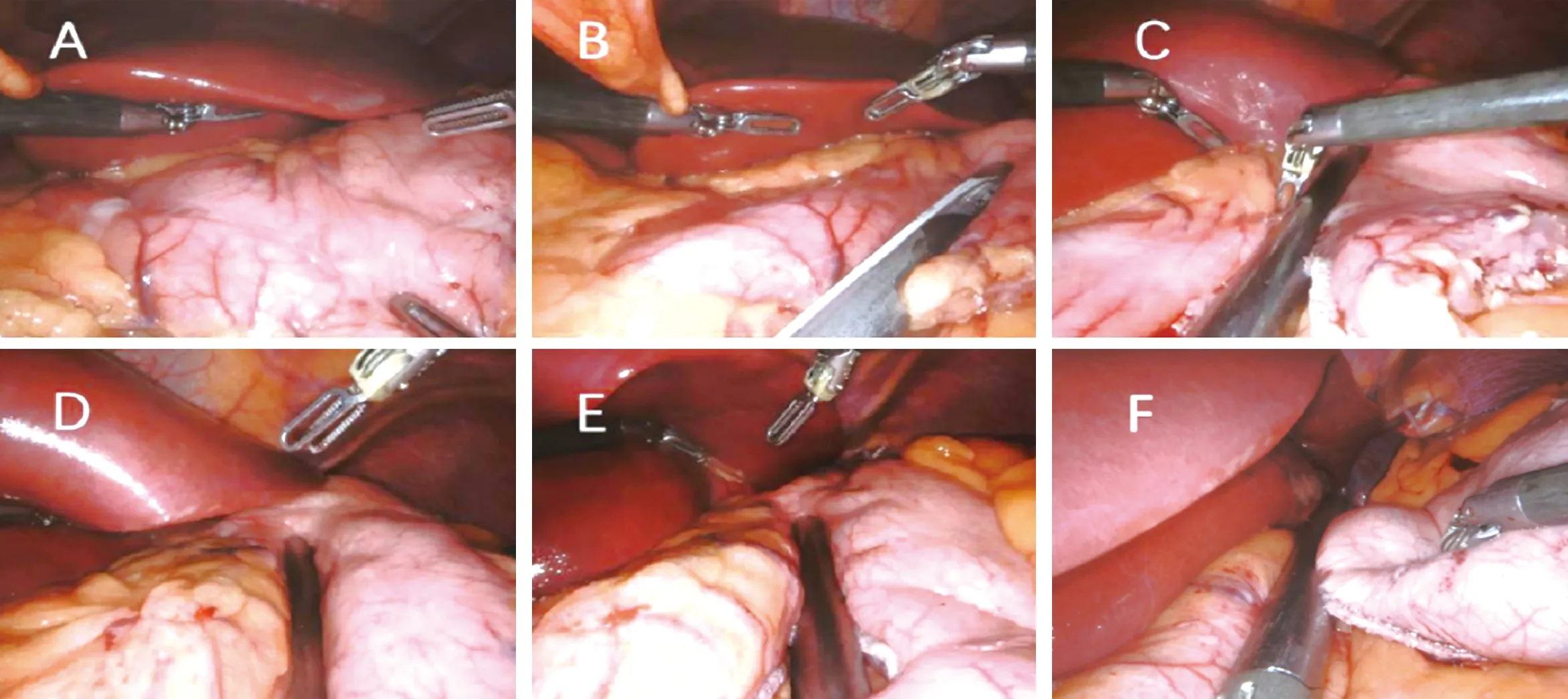
图4 胃壁切割(A:置入支撑管或胃镜;B:距幽门2~4 cm处作为切割起始点;C、D、E:第二次之后的切割应注意靠近支撑管或胃镜,但不可紧贴,调整钉仓方向与之平行;F:切割线的末端需要离贲门左侧1~1.5 cm)
手术要点及难点对策:(1)根据胃壁厚度选择钉仓,胃窦部建议使用成钉高度2.0 mm及以上的钉仓,胃体建议使用成钉高度1.5 mm及以上的钉仓。推荐在切割闭合器咬合组织15 s后激发,以减少出血或“爆钉”的情况发生。如果为修正手术,既往手术造成的增厚胃壁区域应选择成钉高度为2.0 mm及以上的钉仓。(2)切割胃壁时,沿胃大弯侧牵拉胃壁,将胃壁展平。距胃支撑管或胃镜8 mm用切割闭合器夹闭并切断胃壁。第一次切割钉仓应与胃角切线平行,胃角处距切割线的距离应为1.5~2.0 cm,切不可将钉仓尖端紧贴胃支撑管(胃镜)或指向胃角,否则在第一、二次切割交点位置容易出现狭窄,引起术后胃梗阻。
1.5 切缘处理、渗漏测试及大网膜复位 袖状胃切除术是否需要加固缝合胃切缘目前仍存有争议。2020年一项纳入148篇共40 653例患者的系统评价结果显示,胃切缘加固缝合相较不加固缝合可降低术后胃瘘的风险[18]。而Berger等基于代谢与减肥手术鉴定质量改善计划数据库(MBSAQIP)的大宗临床数据研究显示胃切缘缝合加固后增加了胃瘘的风险[19],但其具体原因不明确。本指南专家组建议拔除支撑胃管后采用3-0可吸收缝线或倒刺线连续全层或浆肌层缝合的方法加固切缘(图5A~5C)。切缘处理完成后进行渗漏测试。使用胃支撑管或术中胃镜,采用注气或注液法。术中胃镜检查可观察切缘是否出血。
大网膜是否需要复位目前也存有争议,参考腹腔镜袖状胃切除术操作指南(2018版),专家组多数认为复位大网膜可恢复胃结肠韧带形态,减少术后袖状胃扭转、向胸腔移位的风险,利于胃排空,减少术后呕吐、切缘出血及瘘的风险。可将大网膜缝合至袖状胃切缘,间断缝合2~4针;也可连续全程缝合[5,20-21]。
1.6 取出标本、关腹 仔细检查胃切缘、网膜断端有无出血。将标本置入标本袋,提起胃窦端将标本经12 mm戳孔取出(图5D、5E)。是否放置腹腔引流管尚存在争议,如放置引流管,其头端应置于胃食管结合部附近,此处是最容易发生切线漏的位置(图5F)。手术完成后撤除Trocar,务必于镜下观察戳孔有无活动性出血。解除气腹,关闭操作孔,防止戳孔疝发生。
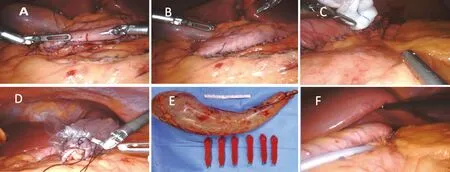
图5 加固胃切缘(A:可吸收缝线或倒刺线加固胃切缘;B、C:确认加固后的切缘无活动性出血;D、E:取出标本;F:放置腹腔引流管)
2 机械臂与腹腔镜结合模式
目前临床上主要使用的手术机器人操作系统分为三、四代达芬奇机器人手术系统。两代机器人手术系统机械臂的分布略有不同:三代机术者右手操作1号臂,左手操作2、3号臂,而光学镜位于1、2号臂之间;四代机机械臂原理功能基本相同,光学镜一般位于2号或3号臂,根据术者习惯,右手操作3、4号臂,左手操作1号臂或左手操作1、2号臂,右手操作4号臂。一般主力手为右手,进行超声刀、双极电凝等主要器械的操作,而左手负责辅助牵拉显露,一般操作无损伤抓钳等。
在助手操作孔选择方面,使用三代达芬奇机器人系统时,4+1模式助手操作孔多位于左锁骨中线处,3+1及3+2模式助手操作孔可位于左或(和)右锁骨中线处。而在使用四代达芬奇机器人系统时,三种模式助手操作孔可位于左或(和)右锁骨中线处。
2.1 4+1模式 这种模式是术者操控四枚机械臂,助手操作一枚腹腔镜器械。术者负责视野的暴露、组织的分离及超声刀的切割;助手帮助术者进行视野的显露及使用切割闭合器行袖状胃成形。这种模式的优点是可完全展现出机器人操作的防颤抖及高活动度的优势,完成各项精细操作。同时也有部分缺点:(1)四枚机械臂同时使用,增加了机械臂耗材的费用;(2)术者左手或右手控制2枚机械臂,需来回切换,增加了术者的操作难度;(3)机器人操作系统缺少牵拉的力量反馈机制,机械臂间进行组织的对抗牵拉,容易造成损伤;(4)部分操作过程中,各机械臂在腹腔内或腹腔外容易相互影响。如改为由助手使用普通腔镜超声刀进行胃的游离,可降低部分手术费用。
2.2 3+2模式 这种模式是术者操控三枚机械臂、两个助手各操作一枚腹腔镜器械进行手术。术者及第二助手负责视野的暴露、组织的牵拉,第一助手使用超声刀及切割闭合器负责组织、脏器的分离与切割。选取第一助手位置时,考虑到胃大、小弯生理弧度,右侧锁骨中线处更容易使用切割闭合器进行胃壁的切割。这种模式由于减少了一枚机械臂的使用,在降低手术费用的同时术者不必频繁切换左手或右手的操作器械,简化了手术过程;而由第二助手负责与术者进行对抗牵拉,以显露手术视野,部分解决了机器人系统无力反馈而易导致组织器官损伤的问题。
2.3 3+1 模式 这种模式是术者操控3枚机械臂、助手操作一枚腹腔镜器械进行手术[22-23]。但由于少了一个助手的辅助,在进行视野暴露方面增加了难度,可能需要采用悬吊法或牵拉器牵拉左肝,以帮助显露视野。
3 小 结
与腹腔镜袖状胃切除术相比,虽然机器人在精细操作上更具优势,但相关临床研究罕有报道[24-26]。在手术效果及安全性等方面,尚无大量临床证据证实机器人袖状胃切除术明显优于腹腔镜袖状胃切除术[27-28]。但随着机器人工程技术的迭代升级及5G通讯技术等智慧医疗建设的不断完善,在减重与代谢外科医师的不断开拓创新、大样本多中心的临床研究成果不断积累下,本指南委员会还会定期对其进行讨论、修订与更新。相信在不久的未来,机器人手术操作系统的应用可能成为减重与代谢外科发展的新方向。
《机器人辅助袖状胃切除术操作指南(2020年版)》编审委员会成员名单
执笔:胡三元
审校:赵玉沛
编写人员:赵玉沛 胡三元 张忠涛 王存川 刘金刚 朱晒红 龚航军 姜可伟 姜 涛 金佳斌
康博雄 梁 辉 刘 昶 刘雁军 孙世波 孙喜太 陶凯雄 童卫东 吴良平 赵高平
