酯交换法制备生物柴油的研究
2021-02-05荣俊锋程茜朱永全张晔李伏虎王金明刘铭
荣俊锋,程茜,朱永全,张晔,李伏虎,王金明,刘铭
(安徽理工大学 化学工程学院,安徽 淮南 232001)
以可再生的植物油或动物油为原料油,通过酯交换工艺可制成生物柴油[1-2]。生物柴油是可再生能源,发展潜力大[3-5]。目前生物柴油制备方法主要有:直接混合法、微乳液法、高温裂解法和酯交换法。其中酯交换法因其反应所需仪器简单易得,原料来源广泛,方法更为有效[6-11],是一种更有效、简单且可行性更高的方法,本文选用酯交换反应进行生物柴油的制备[4,12-14]。
1 实验部分
1.1 材料与仪器
大豆油,由淮南市吉福粮油有限公司提供;甲醇、氢氧化钾、乙醇(95%)、乙醚、酚酞、乙酸、碘化钾、硫代硫酸钠、环己烷、可溶性淀粉、氯化碘、硫酸银、硫酸汞、浓硫酸、重铬酸钾、硫酸亚铁铵、七水合硫酸亚铁、邻菲罗啉、活性炭、氢氧化钠、氯化钠、盐酸、邻苯二甲酸氢钾均为分析纯。
HI 88703高精度台式浊度测定仪;DF-II数显集热式磁力搅拌器;PTF-A电子天平。
1.2 实验原理
在碱催化剂的作用下,油脂与甲醇可以发生酯交换反应,生成产物脂肪酸酯和甘油。酯交换反应为可逆反应,是分步进行的,如下所示:

CH2—OOCR1CH2—OH||CH—OOCR2+ 3ROH催化剂→CH—OH+R1(R2,R3)—COOR||CH2—OOCR3CH2—OH
式中 R1、R2、R3——C12~C24的饱和或不饱和直链烃基;
ROH——低级醇,多为甲醇。
该反应实际上可分为三步:
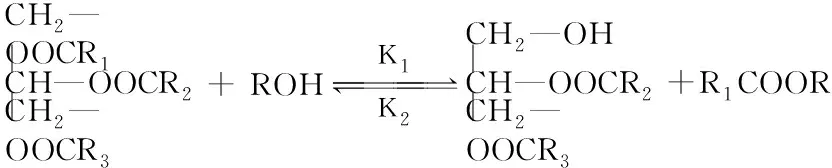
CH2—OOCR1CH2—OH||CH—OOCR2+ ROH K1 K2 CH—OOCR2+R1COOR||CH2—OOCR3CH2—OOCR3

CH2—OHCH2—OH||CH—OOCR2+ ROH K3 K4 CH—OH+R2COOR||CH2—OOCR3CH2—OOCR3

CH2—OHCH2—OH||CH—OH+ ROH K5 K6 CH—OH+R3COOR||CH2—OOCR3CH2—OH
由于有机物空间效应对反应过程存在影响,所以在酯交换反应发生时,所选醇的碳链越短其空间位阻越小,反应所受的空间效应的影响就越小,使得反应活性越高。甲氧基是最活泼的烷氧基,也因为是最小的基团,所以甲醇是酯交换反应中最合适的醇。反应过程中,甲醇中的甲氧基和甘油三酸酯中的某一个脂肪酸结合后,生成长链脂肪酸甲酯并从甘油三酸酯上脱落,与此同时生成甘油二酸酯;然后甲醇中的甲氧基再继续与甘油二酸酯中的某一个脂肪酸结合后,生成长链脂肪酸甲酯,并从甘油三酸酯上脱落后,同时生成甘油单酸酯;最后甲醇中的甲氧基则继续与甘油单酸酯的脂肪酸结合,并生成长链脂肪酸甲酯从甘油三酸酯上脱落,同时生成甘油。以上反应过程表明,经过转酯化反应之后甘油三酸酯最终分裂生成了3个单独的脂肪酸甲酯,以减短碳链的长度,同时形成了有用的副产物甘油。
1.3 实验方法
准确称取所需质量的大豆油后,装入三口烧瓶后加入合适型号的搅拌子,放入已设置实验所需温度的水浴锅中。中间口和右口用塞子塞好,左口连接温度计,调节搅拌子旋转速度,注意观察温度计读数。分别准确称取所需质量的甲醇和氢氧化钾,将氢氧化钾溶于甲醇,待大豆油达到所需温度后,从三口烧瓶中间口加入氢氧化钾甲醇混合液。将球形冷凝管连接于中间口,记录反应开始时间和反应体系温度。反应一定时间后,将搅拌子转速降为0,停止反应。将反应器内液体倒入分液漏斗,进行分液。上层浅黄色清液为目标产品生物柴油,下层棕色浊液为甘油。对生物柴油各项指标进行分析。
1.4 性能测试
酸值按GB/T 14489.3—93测定,碘值按GB 5532—85测定,水分按GB 6283—86(卡尔-费休氏法)测定,运动黏度按GB/T 265—88测定,浊度采用高精度浊度分析测定仪测定。红外分析通过制作溴化钾压片,将生物柴油产品薄涂于压片表面后,放入样品槽中进行样品采集,采集结束后保存数据即可。
2 结果与讨论
2.1 反应时间和甲醇用量对酸值及碘值影响
表1是在大豆油44 g,氢氧化钾0.88 g,60 ℃水浴条件下,不同反应时间、不同甲醇用量对应的酸值、碘值数据。

表1 不同反应时间下不同甲醇用量对应的酸值及碘值Table 1 Acid value and iodine value corresponding todifferent methanol dosage at different reaction time
由表1可知,生物柴油的酸值及碘值会根据醇油比的改变而发生改变。醇油比增加使酸值增加,碘值下降。
2.2 大豆油用量对酸值及碘值的影响
表2是在甲醇12.8 g,氢氧化钾0.88 g,60 ℃水浴条件下,反应2 h不同大豆油用量对应的酸值、碘值数据。

表2 不同大豆油用量对应的酸值及碘值Table 2 Acid value and iodine value of differentsoybean oil dosage
由表2可知,甲醇用量不变,随着大豆油用量增加,可能有部分大豆油未反应,酯交换反应进行不彻底,酸值和碘值有所增大。
2.3 催化剂用量对生物柴油性能影响
在60 ℃水浴条件下,取反应2 h所得生物柴油进行性能测试,研究催化剂用量对浊度、黏度、酸值及碘值的影响,结果见图1、图2。

图1 催化剂用量对浊度及黏度的影响Fig.1 Effect of catalyst dosage on turbidity and viscosity
由图1可知,催化剂KOH用量超过0.88 g之后,浊度随催化剂含量的增加而增加,在0.8~0.88 g 之间,浊度出现最低值。由黏度曲线可知,黏度波动不大,故催化剂用量对生物柴油的黏度性能影响不大。

图2 催化剂用量对产品酸值及碘值的影响Fig.2 Effect of catalyst dosage on acid value and iodine value
由图2可知,酸值随着催化剂用量的增加波动较大。催化剂用量在0.90~0.94 g范围内,酸值较低。碘值曲线表明,碘值随催化剂用量的变化呈先上升后下降的趋势,在0.8 g和0.94 g处出现最低值,在0.88 g处出现最高值。
2.4 反应时间对生物柴油性能影响
在60 ℃水浴条件下,原料配比相同条件下(大豆油44 g,甲醇12.8 g,氢氧化钾0.8 g),研究反应时间对浊度、黏度、酸值、碘值及水分的影响,结果见图3~图5。

图3 反应时间对浊度及黏度的影响Fig.3 Effect of reaction time on turbidity and viscosity
由图3可知,反应时长的改变对生物柴油的浊度及黏度影响很大。随着反应时间的增加,生物柴油的浊度逐渐降低,性能逐渐增强。而黏度呈现微小先降低后增加的趋势。

图4 反应时间对酸值及碘值的影响Fig.4 Effect of reaction time on acid value and iodine value
随着反应时长的增加,可以使得原料充分反应,酯交换反应充分进行。由图4可知,随着反应时间的增加,酸值大致呈现增长趋势,可能是脂肪酸的累计所导致的酸值增加。因此,制备生物柴油时,应选择合适的反应时间,以防止酸值过高。而碘值则随反应时间的增加而呈现降低的趋势。

图5 反应时间对水分的影响Fig.5 Effect of reaction time on water content
由图5可知,随着反应时间的增加,水分含量为先增加后减少的趋势,反应12 h后,含水量约为0.026%。水分同样会影响生物柴油的燃烧性能,生物柴油中的水可以促进微生物生长,导致储罐腐蚀,参与乳液的形成,以及引起水解或水解氧化。
2.5 红外分析
选取制备得到的性能指标较好的四种生物柴油样品,进行红外分析,结果见图6。
由图6样品4曲线可知,在3 650~3 590 cm-1以及3 350 cm-1处出现很强很宽的峰,说明检测样品中存在游离态的醇羟基或酚羟基以及多聚态的醇或酚;在3 300~2 500 cm-1范围内出现较为宽散的谱带,说明可能存在二聚体羧基;3 300~2 700 cm-1之间的峰值说明存在不饱和和饱和碳氢伸缩振动;图中1 639 cm-1处的峰在1 690~1 630 cm-1之间,存在碳氧双键和碳碳双键;1 405 cm-1处峰值在 1 420~1 300 cm-1之间,为碳氧伸缩振动;612 cm-1处的宽峰说明存在碳卤键。综合上述分析,该样品中含有羟基、羧基、酯基、双键、羰基、醚键、C—I键和C—Cl键等。其他3条曲线分析同上。对比四条曲线谱图可知,产品特征峰基本相同,只有吸光度存在一定差值。

图6 生物柴油样品红外对比图Fig.6 Infrared contrast map of biodiesel samples
样品1.大豆油44 g,催化剂0.8 g,甲醇12.8 g,反应3 h;
样品2.大豆油44 g,催化剂0.8 g,甲醇12.8 g,反应10 h;
样品3.大豆油44 g,催化剂0.8 g,甲醇14.7 g,反应8 h;
样品4.大豆油44 g,催化剂0.8 g,甲醇12.8 g,反应12 h
3 结论
在氢氧化钾均相碱催化作用下,大豆油和甲醇进行酯交换反应制备生物柴油。通过对产品酸值、碘值、浊度、黏度及水分等指标的分析测定,研究了甲醇用量、大豆油用量、催化剂用量、反应时间等因素对各项指标的影响。通过实验表明,改变原料配比可直接影响生物柴油的收率及性能,而改变反应时间可影响其性能结果。碘值随反应时间的增加呈下降趋势,而酸值呈上升趋势。本文的研究将为生物柴油的制备及性能测定提供一定的借鉴。
