静脉联合局部应用氨甲环酸对减少腰椎手术失血的有效性及安全性
2021-02-03陈思
陈思
作者单位: 430000 武汉市,湖北六七二中西医结合骨科医院
随着人口老龄化问题的日趋严峻,腰椎退行性疾病患者明显增多,可引起患者出现下腰痛、下肢放射痛、下肢麻木、间歇性跛行等症状,对患者的日常生活造成严重干扰[1]。腰椎后路减压内固定融合术是治疗该类疾病的重要手段,可有效解除神经根压迫,缓解患者的临床症状,但该术式切口较深长,术中失血在所难免,若术中失血过多会增加切口感染、急性硬膜外血肿等并发症发生风险,同时导致脏器灌流不足,造成靶器官损伤,患者面临输血治疗,会增加交叉感染、排斥反应等不良反应,影响治疗效果[2]。因此在手术过程中应减少患者失血,以稳定患者的病情,提高临床疗效。TXA是临床手术常见的一种抗纤溶剂,能降低纤维蛋白的溶解,减少出血,效果确切[3]。但目前将该药静脉联合局部用药应用于腰椎手术中的研究较少,鉴于此,本研究观察静脉联合局部应用TXA对减少腰椎手术患者失血的有效性和安全性,并与同时期采用生理盐水的患者进行比较,现报道如下。
1 资料与方法
1.1 一般资料 选择2017年1月-2020年5月在湖北六七二中西医结合骨科医院接受腰椎后路减压内固定融合术治疗的患者88例,按抽签法随机分为研究组44例和对照组44例。研究组男24例,女20例;年龄44~68(56.08±5.06)岁;病程3个月~15年,平均病程(7.52±2.16)年。对照组男25例,女19例;年龄43~69(56.45±5.12)岁;病程6个月~15年,平均病程(6.98±2.02)年。2组基础资料比较无显著差异(P>0.05),具有比较价值。本研究经医院伦理委员会批准。
1.2 选择标准 纳入标准:(1)单节段或双节段行手术治疗;(2)知情同意本研究;(3)无药物过敏史;(4)初次腰椎手术。排除标准:(1)血常规异常者;(2)凝血功能异常者;(3)术中发生脑脊液漏者;(4)既往存在血栓病史者;(5)对本研究药物成分过敏者。
1.3 方法
1.3.1 手术方法:2组患者均采取腰椎后路减压内固定融合术治疗,由同1名医师主刀完成。全麻;患者取俯卧位,保持腰椎段后伸;研究组于手术切皮前15 min给予TXA(厂家:贵州圣济堂制药;批准文号:国药准字H20063068;规格:5 ml ∶0.5 g)500 mg加入生理盐水100 ml中稀释后静脉滴注;对照组给予生理盐水100 ml静脉滴注。以伤椎为中心作一长约10 cm正中切口,剥离双侧椎旁肌,并促使手术节段上下棘突均充分暴露;借助G型臂X线机,在椎弓根准确置入螺丝钉,满意后将相应阶段棘突、椎板切除;椎管、侧隐窝减压;观察神经根与椎间盘位置关系,并切除突出明显或脱出的髓核组织。术中研究组使用TXA浸湿的方纱对切口内出血部位进行浸润压迫止血,对照组使用生理盐水浸湿的方纱进行压迫止血。完成骨块复位后,置入引流管,并连接美国CBC-Ⅱ自体血回输器;使用吸收线进行缝合。
1.3.2 术后处理:术后6 h内引出血性液体经CBC-Ⅱ自体血回输器进行自体血回输,并观察患者是否出现输血反应;引流情况较好者可于术后24~58 h拔除引流管;术后第1、3天检查血常规、血生化、凝血功能等。
1.4 观察指标与方法 (1)手术失血情况:以总失血量、隐性失血量、显性失血量、术中失血量及术后引流量作为观察指标。结合患者的身高、体质量、红细胞压积,采用Cross方程、Nadler方程计算总失血量;显性失血量=术中失血量+术后引流量;隐性失血量=失血总量-术中失血量-术后引流量;术中失血量=吸引器中液体总量-术中冲洗用水量+纱布含血量[4]。(2)输血情况:输血率、术中输血量、术后6 h自体血回输量。(3)血液学指标:比较2组术后第1、3天血红蛋白(HGB)、红细胞压积(HCT)、凝血酶原时间(PT)。(4)不良反应(头痛、恶心、呕吐、腹泻等)。

2 结 果
2.1 手术失血情况比较 2组隐性失血量比较无显著性差异(P>0.05);研究组总失血量、显性失血量、术中失血量、术后引流量均少于对照组(P<0.01)。见表1。
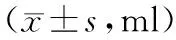
表1 2组手术失血情况比较
2.2 输血情况比较 研究组输血率低于对照组,术中输血量、术后6 h自体血回输量均少于对照组(P<0.01)。见表2。

表2 2组输血情况比较
2.3 术后第1、3天血液学指标比较 术后第1天,2组HGB、HCT、PT比较无显著性差异(P>0.05);术后第3天,研究组HGB、HCT均高于对照组(P<0.01),2组PT比较无显著性差异(P>0.05)。见表3。

表3 2组术后第1、3天血液学指标比较
2.4 不良反应比较 2组切口均一期甲级愈合,无头痛、恶心、呕吐、腹泻等不良反应。
3 讨 论
暴露手术节段上下棘突剥离椎旁肌过多、椎管内操作损伤静脉丛、椎管减压时松质骨面出血、术后切口引流出血等是腰椎后路减压内固定融合术失血过多的主要原因[5],此时机体凝血系统被激活,产生的血凝块中的纤维蛋白吸附纤溶酶原及其激活物,导致血凝块被大量的纤溶酶溶解而增加出血,引起较多并发症,延长患者住院时间,甚至危及患者生命[6]。因此,明确影响腰椎手术围术期失血的因素,并采取针对性止血措施对于改善治疗效果、提高治愈率具有重要意义。多年来临床医师从术式改进、术前应用增加止血的药物、及时干预内科疾病、控制低血压、缩短手术时间等多方面进行研究,但仍有部分患者因失血量过多而需进行异体输血治疗[7]。
TXA是一种人工合成的抗纤维蛋白溶酶药,目前已在心脏手术及骨关节外科手术中得到广泛应用,已有大量的临床研究证明,其在术中因纤溶激活而引起的出血中止血效果显著,且安全性高[8-9]。张永远等[10]在腰椎手术中局部应用TXA,即于术中主要步骤完成后使用TXA浸泡的术腔纱布填塞1 min,于所有步骤完成后再次填塞3 min,并于缝合筋膜后于术腔注射TXA溶液10 ml,结果显示,与生理盐水(使用方法与氨甲环酸相同)相比,该组在术中及术后止血、住院时间、并发症发生情况均表现出优势。TXA止血的作用机制主要是该药的化学结构与赖氨酸相似,可竞争性地阻止纤溶酶、纤溶酶原在纤维蛋白上吸附,从而防止纤溶酶原激活,避免纤维蛋白被纤溶酶降解和溶解,增强凝血功能,达到良好的止血效果[11];另外,在临床应用中导致血栓形成的发生率极低,还不会增加心脑肾出血的风险[12]。但目前对于在脊柱手术中使用TXA的具体方法尚未明确,有学者证明切皮前15 min静脉用药10 mg/kg,或术中1 mg/kg维持量至术毕均具有较好的疗效和安全性。也有研究证明术中局部用药靶向针对性更强,可促使局部在短时间内达到较好的药物浓度,有效减少局部出血[13]。本研究中将术前15 min TXA静脉滴注与术中局部用药结合,结果发现,与生理盐水相比,TXA组总失血量、显性失血量、术中失血量、术后引流量均减少,同时还能降低输血率,且减少术中输血量及术后6 h自体血回输量,说明TXA静脉联合局部用药在腰椎手术中具有明显的止血优势。隐性失血是由各种原因引起的隐匿性失血,在腰椎手术中多由纤溶系统平衡被破坏、红细胞溶血等原因造成,而TXA的优势在于能够稳定血凝块,避免血肿形成,不仅能有效减少显性失血,在减少隐性失血方面也具有优势。将TXA静脉用药与局部用药结合,一方面通过调节低亢进的纤溶系统、改善HGB、HCT指标而有效止血,另一方面通过局部针对性强的止血效果有效控制切口出血,可在一定程度上减少静脉用药的剂量,从而减少不良反应。本研究结果显示,2组用药后伤口均愈合良好,且无明显的不良反应,提示TXA在起到显著的止血效果的同时还不会增加不良反应,安全性较高。
在TXA用药剂量方面,目前临床上也尚未统一,不同剂量的TXA均可起到良好的止血效果,减少出血的发生,控制出血程度,但在最低使用剂量上尚无明确标准。既往有研究表示,手术初始静脉予TXA 15 mg/kg,随后予1 mg·kg-1·h-1维持,与对照组相比止血程度无显著差异[14]。本研究中于术前予TXA 500 mg静脉滴注,剂量小于既往的研究,但本研究优势在于结合局部用药的方式,结果显示止血效果较优,提示静脉联合局部用药效果较佳。
综上所述,在腰椎手术中采取TXA静脉联合局部用药方案不仅具有良好的止血功能,有效减少手术失血量及输血量,而且不会增加不良反应,具有较高的安全性。但本研究的缺陷在于:(1)未对TXA使用剂量进行详细的分析对比,缺乏对TXA疗效佳、安全性高的最低剂量进行研究,这也是今后工作的研究方向;(2)选取的样本量较少,故应在今后的工作中扩大样本量以进一步证明本研究结论;(3)在TXA使用时间上未进行详细对比,缺乏对术前、术中TXA使用时机的探讨。
