医疗器械生产企业质量检验信息化系统的研发和应用
2021-02-03林定余郭永兵朱清
林定余,郭永兵,朱清,
1 宁波戴维医疗器械股份有限公司,宁波市,315700
2 浙江医药高等专科学校,宁波市,315100
0 引言
中国医疗器械产业发展迅速,已成为全球第二大医疗器械市场[1],然而国内众多医疗器械企业的质量管理体系依旧存在诸多不足[2]。质量管理体系的良好运行是产品质量与安全的保障[3]。国内法规要求医疗器械生产企业应按照《医疗器械生产质量管理规范》的要求,建立健全与所生产医疗器械相适应的质量管理体系并保证其有效运行[4]。随着国内外监管从上市前监管转向产品全生命周期的监管[5-6],对生产企业的质量管理体系提出了更高的要求。新时代的医疗器械监管更加注重过程控制,包括对产品、过程和检验设备等方面的控制,而不单纯只强调检测。产品检测内容方面,包括对原材料、过程、成品质量的检验。要求工厂产品检验(或验证)应符合“技术要求”的全部项目[7]。
2016-2017年,原国家食品药品监督管理局在国内医疗器械生产企业飞行检查中发现,生产企业质量管理体系缺陷主要存在于文件和记录控制、生产管理、采购等环节中[8-9]。其中,文件管理不当的缺陷项是监管部门日常监督检查或飞行检查中发现的高频问题之一。这类问题部分是由于企业管理层对质量管理体系理解不到位,没有妥善保管质检文件;或由于企业跨部门间沟通效率低,没有及时记录检验数据、更新仓储数据;或由于一线检验人员对法规、标准理解不到位等原因造成的[10]。为了解决上述问题,本公司研发了一套质量管理检验信息化系统,并应用到企业管理中,用以提高企业的质量体系管理水平。
1 系统设计
1.1 系统框架
质量管理检验信息化系统分为用户界面层、应用服务层、数据接口层和数据库等四层。用户界面层包含检验人员的移动客户端操作界面和PC客户端操作界面。应用服务层为产品生产检验业务流程模块的构建。数据接口层负责连接检验数据和ERP数据,以及信息化系统业务模块之间的数据交互。数据库包括检验标准化数据储存和ERP系统数据库,两个数据库的数据动态链接,实时更新产品检验过程数据,如图1所示。
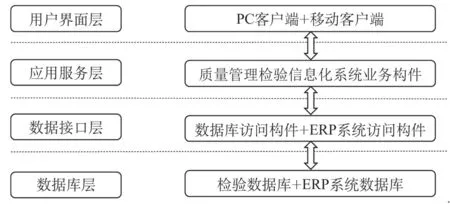
图1 质量管理检验信息化系统总体结构图Fig.1 Structure chart of quality inspection information system
1.2 用户界面层
用户界面层面向检验人员、复检人员、审核人员、产品放行审批人和仓储管理人员五类人员。
(1)检验人员:采用移动终端扫描采购件、中间品或成品二维码,通过电子检验登记单输入检验结果。对于定量检验,检验人员只需要输入检验结果,系统将自动将检验结果与该检验项目指标的标准进行比较。如果检验结果在标准值允许的范围内,系统自动判断为合格;如果检验结果不符合标准值,系统自动判断为不合格,并自动产生一条复检记录。
(2)复检人员:查看产品的不合格项目指标,并对采购件、中间品或成品的不合格项进一步复查,给出复检结果和复检结论,并做好复查记录。
(3)审核人员:需要根据检验人员的检验记录单和复检人员的复检记录单,审核产品是否全部符合检验和试验规范要求,并给出产品检验的最终结论。
(4)产品放行审批人:成品由制造部发起产品放行审批单,采购物资由采购部门发起产品放行审批单。系统根据预先流程设置,相关部门分别在流程中对产品放行的必要条件逐一进行确认,最终由公司制定的产品放行审批人进行最终审批。
(5)仓储管理人员:接收到放行审批单后,采用移动终端扫描产品二维码并确认产品实物,系统会自动在ERP系统中生成入库单,对产品库存数据实施自动更新,仓储管理人员按法规要求在仓储区域进行分类放置、标识和管理。
1.3 应用服务层
应用服务层根据业务流程设计开发,整体上可分为基础性业务工作和常规性业务工作两类。
基础性业务工作包括建立产品数据库、导入产品质检方案和关联产品检验项目指标等三个步骤。首先,依照企业内产品品种或型号建立标准化的产品数据库;然后,根据产品的品种或型号导入对应的产品质检方案;最后,根据产品质检方案,梳理对应产品项目指标清单、检验操作流程/规范和检验合格的标准值范围。基础性业务工作如无变更,一般只需填报一次。
常规性业务工作包括产品检验登记、检测数据结果、复检、放行审核和产品入库等工作环节。常规性业务工作可直接调用基础性业务工作的相关数据库。
第一步,检验人员扫描每批/台的产品二维码,系统根据基础性业务工作中的产品数据库,生成该产品的电子检验记录表。如该产品品种或型号不在产品数据库中,则需要在基础性业务工作中对该产品的数据进行补充。
第二步,检验人员核对系统生成的检验方案,并根据该方案的项目指标完成对应的采购物料、中间品和/或成品的所有检验项目。检验人员将完成检验的该台/批产品检验记录单提交至最终审核人。审核人员对检验内容和项目进行核查,如出现复检项,还要对复检结果进行核查。经核查所有检验项目全部符合检验和试验规范要求后,方能通过审核。
第三步,产品放行审批人根据产品的检验登记表和检验报告单,判断产品是否符合放行条件。仓储管理人员根据产品的最终放行审批单,按法规要求在仓储区域进行分类放置、标识和管理。
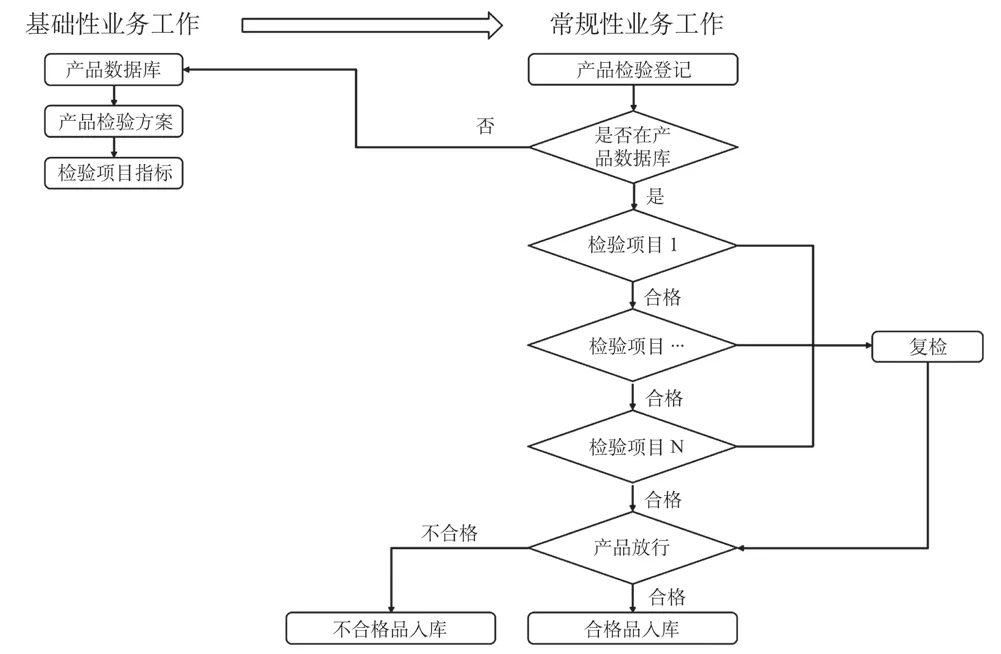
图2 质量管理检验信息化系统业务流程图Fig.2 Business flow chart of quality inspection information system
1.4 数据库层
数据库包括检验数据库和ERP系统数据库。检验数据库的物料领用和产品检验信息,与ERP数据库的进存销数据保持动态连接,以保证物料和成品库存数据可随生产和检验过程实时更新。
检验数据库层包括产品信息、基础数据档案、质检方案、检验项目指标、关键元器件和检验装置,以及每批/台设备的检验信息、复检信息和放行信息等。产品信息包括产品类型型号等,该信息与产品实物之间通过二维码实现关联。每个产品一旦进入生产环节,将生产一个二维码作为该产品的“身份证”,保证产品和二维码之间唯一对应。通过扫描产品的二维码,能够关联产品生产和检验的所有信息,包括产品的生产日期、检验项目、检验人员、检验数据和结果等信息。基础数据档案包括检验用的仪器、设备的状态、校准日期等信息;质检方案包括文件版本号、方案内容、生效日期和检验操作指导书等;项目指标包括产品出厂检验需要检测的项目清单、技术要求等。
调用的ERP系统数据库包括物料采购信息、物料库存、库存等信息。ERP系统数据库与检验系统数据库之间存在数据的流向如下:通过ERP系统从供应商处采购物料,检验人员完成进货检验并上传检验系统。合格的物料进入ERP物料库存,不合格的进行退货或销毁。当生产车间开始产品生产时,从仓库领用物料,ERP系统对应核减。在产品生产中或生产完后,对中间品或产成品进行检验和复检。管理人员对合格产品放行进入仓库,不合格产品放置于不合格区,同时在ERP系统中生成记录,如图3所示。
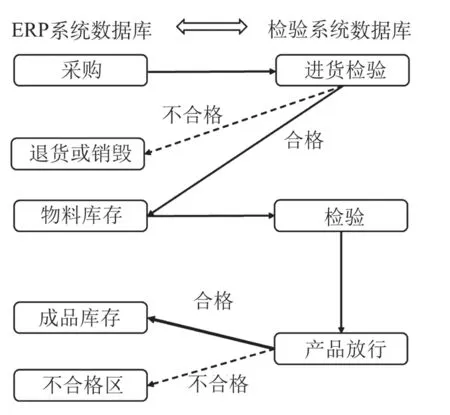
图3 ERP系统数据库与检验系统数据库的数据交换示意图Fig.3 Sketch map of data exchange between ERP system database and inspection system database
1.5 系统研发
质量管理信息化系统采用C/S架构,由SQL Server数据库、服务端和客户端组成,适用于Win7/Win10操作系统。
根据业务流程,管理人员和检验人员PC端界面的菜单栏包含基础数据档案维护、项目指标总清单、质检方案档案、质检项目登记、产品检验登记、产品检验审核、复检记录保持、质检报告打印和查询、质检数据搜索和统计分析等功能,各功能视实际需求开放给所需人员。具体操作界面,如图4所示。
图4 管理人员和检验人员的操作界面,包括产品检验登记、检验复核、复检记录等Fig.4 Operation interface of management personnel and inspection personnel,including product inspection registration,inspection review,re-inspection records,etc.
2 应用成效
质量检验信息化系统的研发始于2018年3月,并于2020年4月在本公司中实际投入使用,覆盖企业全部的医疗器械产品,共计16类品种、78个型号。质量检验信息化系统的应用不仅实现所有产品检测过程信息化和可视化,而且与ERP系统实时联动,从而保证物料、中间品和成品数据的准确性。
2.1 凸显质量管理的重要性
医疗器械生产企业质量管理检验系统研发的最大难点,往往并不仅仅在于系统开发硬件上的难点,还在于企业思想上的“软件”问题[10]。信息化系统的研发过程,需要打破企业传统的工作模式和工作习惯。在短期内增加企业员工的工作量,必然引起一部分企业工作人员对于信息化系统的抵触。因此,要推进信息化系统的研发和应用,需要改变生产企业过往的“重理论、轻质量”“重生产、轻质检”的理念,要重新激发企业的内在创新动力。信息化系统研发的过程,帮助企业管理层重新认识产品质量管理对于企业发展的重要性,提高了企业的技术研发人员、生产车间人员等对质检作用的重视,督促企业投入资金和技术用以加强产品质量体系建设,最终在企业内形成产品生产和质检“两手都要抓,两手都要硬”的新氛围。
2.2 完善质量管理的追溯体系
质量管理检验信息化系统实现了质检方案、检验记录等数据的电子化,有利于企业发现产品质量管理中可能存在的问题或漏洞,帮助企业追溯问题产品的根源。
质检方案是企业产品检验的“宪法”,是质量体系的基石,是保障产品安全有效的重要组成。大部分生产企业的质检方案一般采用纸质文件的形式保存。纸质文件会因为保存时间跨度过长、原保管人员的离职、企业生产地址搬迁等众多因素而损坏或遗失。质检方案电子化后可将其保存在企业云端,从而打破空间和时间的局限性,可供企业和监管部门随时随地调取、检索和翻阅,提高工作效率。而且,电子化的质检方案即使经过多个版本的变更或修订,历史的版本都可以进行有效追溯,方便企业对质量体系建设过程和历史进行总结和回顾性的评价。
检验记录的电子化,将所涉及检验的人员、检测时间地点、使用的检验仪器、检测原始数据等重要信息均保存在云端。一方面,如果产品出现故障或不良事件,可快速追溯、重现该设备的生产、检验的过程,有利于分析和排查导致不良事件发生的原因。另一方面,电子化检验数据有利于企业从时间轴上分析比较各批次产品的检验数据,查找趋势性变化,通过专家会诊或大数据分析的方法,排查质量体系中可能存在的不足。
2.3 提高产品质检效率和准确性
以往产品检验采用纸质记录方式,不同的检验项目会有多份纸质检验登记表。如果多品种、多型号、多批次的产品同时需要检验,容易造成登记表混淆,且不方便登记表的管理。随着信息化系统的应用,产品的种类、型号、批次信息可通过扫描产品的二维码直接生成。因此提高了检验工作效率和准确率。既避免了同一产品多个项目的重复填写,也保证实际检验的产品和检验登记表相一致。
扫描产品的二维码,不仅能获得对应产品的基本信息,还能提供产品的质检方案和项目清单。检验人员根据移动终端的提示,开展项目检测并填写检验数据。系统根据检验结果和项目清单自动判断该项目是否合格,从而减少人为判定的误差。这使得检验人员可更专注于检验的过程,提高检验效率。
2.4 顺应新时代医疗器械数字化监管的趋势
一方面,随着人民的生活水平提高和对医疗服务需求的多样化,国内药械化企业发展迅速,企业数量和产品种类日益增加,使得药监部门的监管压力不断增加。因此,通过打造智能监管系统,提高监管效能,已经成为国家药械化监管的大趋势[11]。多个省市的监管部门已加快推进“数字药监”的建设和应用。生产企业的基本数据监管和生产业务数据是构建“数字药监”的一个重要组成部分,为“数字药监”风险预警模型提供所需的数据源,增强风险预警系统的预判性[12]。
另一方面,监管部门的检查人员到企业现场检查的过程中,有不少精力和时间浪费在质量体系文档、产品生产检验原始记录和仓储文档等纸质文件上查找和比对信息。信息化系统整合ERP和检验数据库,可以为检查人员提供便捷的搜索功能。通过关键词搜索,找到对应的文档进行核对和数据校验;当检查员到车间检查产品生产和检验过程时,检查人员可通过移动终端扫描产品的二维码,立即获得产品的所有检验信息。这提高了现场检查的效率和有效性。
3 总结和展望
医疗器械生产企业质量检验信息化系统能够将生产质检过程透明化,有利于企业扁平化管理,明确职责,提高企业内部协同效率。然而,一套系统是否能顺利运作,不仅仅靠系统本身,还与企业内参与系统使用者息息相关。企业需要统一思想,做好系统使用培训,切实将质量控制从线下转到线上线下相结合的模式,让信息化系统发挥真正的作用。未来,随着工业4.0智能制造设备和5G物联网的推进应用,检验设备能够自动完成检验和数据上网[13],将进一步提高检验效率,减少人为误差以及人为篡改数据的可能性。
