高分辨率磁共振管壁成像对缺血性卒中病因的精准诊断价值
2021-02-02李文君刘翠翠刘俊艳
李文君,刘翠翠,刘俊艳
缺血性卒中病因的精确分型对于临床医师选择恰当的急性期治疗措施及二级预防方案,从而改善患者预后至关重要。目前被临床广泛应用的CIS S 分型标准将缺血性卒中病因分为大动脉粥样硬化(l a r g e artery atherosclerosis,LAA)、心源性栓塞(cardiogenic stroke,CS)、穿支动脉疾病(penetrating artery disease,PAD)、其他病因(other etiology,OE)及病因不确定(undetermined etiology,UE)型[1]。传统的血管影像学检查方式包括TCD、MRA、CTA及DSA等,因仅能提供管腔狭窄程度信息,对于颅内动脉狭窄闭塞性疾病的病因诊断价值有限。另外,上述影像学检查方式对血管低度狭窄的诊断亦不准确,致使PAD型卒中被过高估计[2]。HR-MRI技术因能显示管壁细微结构及未造成管腔明显狭窄的微小斑块而有助于明确缺血性卒中的病因诊断[3]。随着影像学技术的发展,其临床应用越来越广泛。基于此,本研究探讨HR-MRI对缺血性卒中病因精准化诊断的价值。
1 研究对象与方法
1.1 研究对象 回顾性纳入2014年5月-2019年5月就诊于河北医科大学第三医院神经内科的急性缺血性卒中患者。入组标准:①年龄≥18岁;②发病2周内入院;③依据《中国急性缺血性脑卒中诊治指南2018》[4]诊断为急性缺血性卒中;④住院过程中完善了责任血管或责任血管载体动脉的HR-MRI扫描。排除标准:①存在明确的颈动脉易损斑块或严重狭窄者;②伴随心房颤动、心脏瓣膜病等可能产生心源性血栓者;③HR-MRI图像不清晰无法分析者。
1.2 研究方法 收集入组患者的临床及影像学资料,依据CISS分型标准,分别于HR-MRI扫描前后对入组患者进行病因分型。上述结果由2名从事脑血管病研究的神经内科医师和1名影像科医师共同判定并达成一致。
1.2.1 HR-MRI成像技术方法及参数设定
使用3.0T MR扫描仪(Verio;Siemens,Erlangen,Germany)及8通道头颅线圈,应用2D或3D成像技术完成入组患者的HR-MRI。
2D成像序列包括:T1加权、T2加权和质子加权。相应成像参数分别为:①T1加权(TSE序列):重复时间(repetition time,TR)/回波时间(echo time,TE)=1060/26 ms,视野(field of view,FOV)=150 mm×150 mm,矩阵256×256,层厚2 mm;②T2加权:TR/TE=2500/76 ms,FOV=150 mm×150 mm,矩阵256×256,层厚2 mm;③质子加权:TR/TE=2400/16 ms,FOV=150 mm×150 mm,矩阵384×384,层厚2 mm。扫描长度约3 cm(14层)。扫描时间分别为:T1加权3 min 28 s,T2加权3 min 10 s,质子加权4 min 19 s。
3D成像序列包括平扫和增强3D T1加权SPACE(TSE序列)成像,成像参数为:TR/TE=900/15 ms,FOV=200 mm×180 mm,分辨率0.6 mm,采集方位斜冠状位,扫描时间8 min。平扫结束后,静脉注射对比剂,后进行增强扫描,扫描时间8 min。
1.2.2 HR-MRI图像解读 图像分析经工作站(SyngoVia;Siemens,Erlangen,Germany)进行。在质子或T1加权图像上,手动描绘病变及参考血管的内外壁,经半自动方法定量测量病变及参考血管的管腔及血管面积。其中病变血管为最大管腔狭窄截面;参考血管为狭窄截面近端或远端正常血管截面。动脉狭窄程度及重构指数的计算方法如下[5]:
动脉狭窄程度=1-病变管腔面积/参考管腔面积。
重构指数=病变处血管面积/参考处血管面积。根据重构指数可进一步定义正、负性重构:重构指数≥1.05定义为正性重构,≤0.95定义为负性重构。
1.3 统计学方法 采用SPSS 13.0统计软件进行分析。符合正态分布的计量资料以表示;偏态分布的计量资料以M(P25~P75)表示。计数资料以频数(%)表示。
2 结果
共入组139例患者,年龄28~85岁,平均57.5岁。其中男性99例(71.2%),高血压113例(81.3%),糖尿病43例(30.9%),既往卒中史36例(25.9%),饮酒51例(36.7%),吸烟56例(40.3%)。
有学者对形成EKC机理的收入效应和结构效应提出了质疑。从收入效应看,当环境资源的消费不具有排他性时,人们很难有意愿以可持续发展的方式使用环境资源,此时对环境资源消费需求的增加,必定会导致生态环境质量的恶化。从结构效应看,产业结构的改变只是影响经济的产出结构,消费结构如果没有随之改变,资源密集型产品(包括环境污染密集型产品)的需求只有通过进口来满足,也就是说,资源密集型产业只是在国际间转移,本国生态环境压力的下降实际上是以他国生态环境压力的上升为代价的,[16]因此,用结构效应解释EKC难于有说服力。
入组患者的HR-MRI成像,95例经2D成像技术完成,44例经3D成像技术完成,成像血管分布如下:颈内动脉7例(5.0%),大脑中动脉78例(56.1%),大脑前动脉1例(0.7%),椎动脉4例(2.9%),基底动脉43例(30.9%),大脑后动脉6例(4.3%)。
2.1 HR-MRI扫描前CISS分型结果 HRMRI扫描前的分型为:LAA型89例;PAD型45例(穿支动脉供血区梗死且TCD/MRA检查未发现载体动脉狭窄者);OE型3例:烟雾病2例,系统性红斑狼疮(systemic lupus erythematosus,SLE)继发血管炎1例;UE型2例:其中1例有高血压及类风湿关节炎病史,既往血压控制不佳,此次病前因停用抗风湿药致风湿活动,颅脑MRA提示其双侧颈内动脉末端、大脑中动脉、大脑前动脉重度狭窄,可见烟雾状血管,另1例患SLE多年,但实验室检查提示其血糖、血脂代谢异常。
2.2 HR-MRI扫描后CISS分型结果 经HRMRI扫描后,89例LAA型卒中患者均于责任血管发现偏心性管壁增厚,或非均匀的环形增厚,动脉管壁最薄处直径不足最厚处直径的50%,表明粥样硬化斑块存在[6],证实为动脉粥样硬化性疾病。其中包含载体动脉病变累及穿支动脉40例。
原诊断为PAD型的45例卒中患者,经HRMRI扫描仅27例证实为穿支动脉本身病变。其余18例于责任血管的载体动脉发现粥样硬化斑块,证实为载体动脉病变累及穿支动脉的LAA型卒中(图1),其中12例载体动脉狭窄程度≤36%,6例载体动脉存在正性重构。经HRMRI明确病因分型的穿支动脉供血区梗死患者病变特点见表1。
原诊断为OE型3例卒中患者:2例烟雾病患者经HR-MRI扫描于基底节区均可见多发血管流空影,提示新生穿支血管出现,但其中1例于闭塞血管近端可见不规则偏心性管壁增厚,考虑为动脉粥样硬化性烟雾综合征(图2);另外1例SLE继发血管炎患者经HR-MRI扫描发现责任血管向心性狭窄伴管壁明显强化,证实为继发性血管炎。
原诊断为UE型2例卒中患者中,1例于闭塞动脉近端管壁发现偏心性管壁增厚,其斑块密度欠均匀;另1例未见偏心性管壁增厚,但基底节区可见多发血管流空影(图3)。两者增强扫描后均未见明显强化,结合患者的病史、辅助检查及治疗反应得以明确诊断。

表1 经HR-MRI明确病因分型的穿支动脉供血区梗死患者病灶特征比较[单位:例(%)]
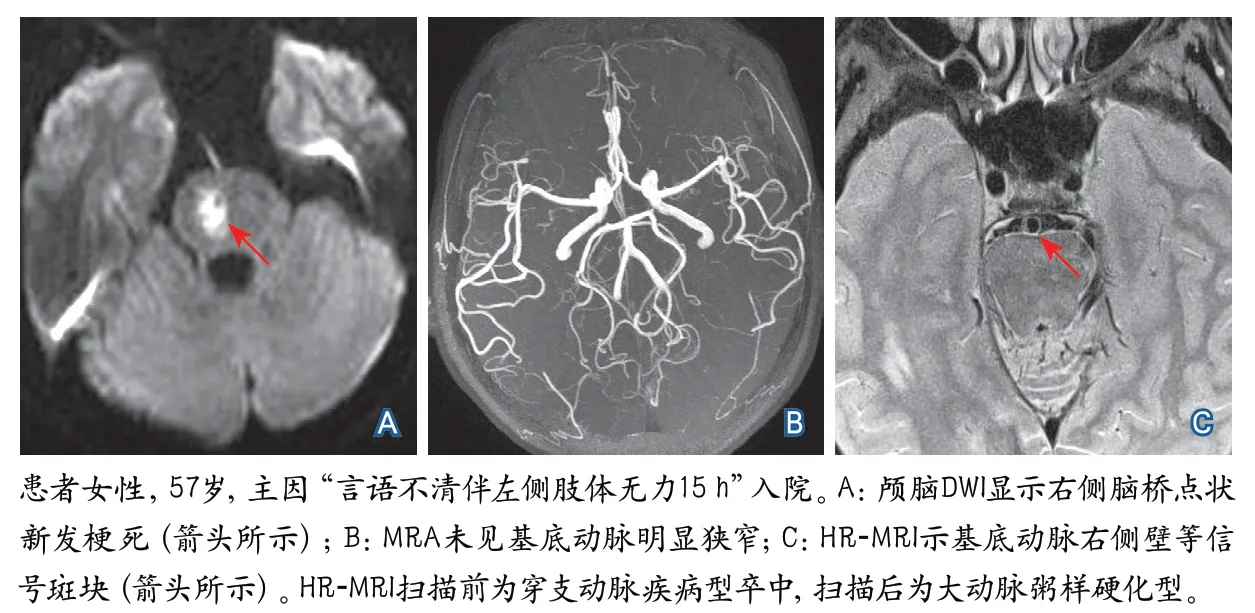
图1 典型病例:微小载体动脉斑块累及穿支动脉开口
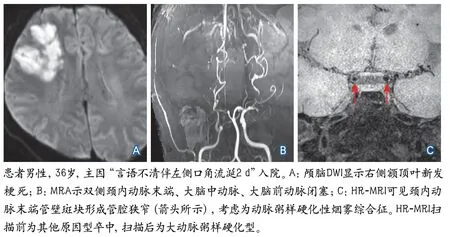
图2 典型病例:动脉粥样硬化性烟雾综合征

图3 典型病例:烟雾病
3 讨论
本研究共入组患者139例,分别于HRMRI扫描前后依据CISS标准对入组人群进行病因分型,得出的结果相差甚远,表明依据传统血管影像学进行的CISS分型存在较大误差,而HR-MRI可同时提供动脉管壁及管腔信息,有利于CISS分型的精确化。
余18例穿支动脉供血区梗死依据TCD/MRA诊断为PAD的卒中患者,经HR-MRI扫描后发现载体动脉粥样硬化斑块,明确病因分型为LAA。其中12例载体动脉狭窄程度≤36%,6例载体动脉存在正性重构。正性重构作为不稳定动脉粥样硬化斑块的影像学特征,经由TCD、MRA等传统血管影像学难以检出。且多项研究表明,正向重构有利于维持管腔,但与大脂质核心、薄纤维冒、斑块内炎症等不稳定特性相关,更多见于症状性缺血性卒中患者[8-9]。此外,体积微小未造成动脉管腔明显狭窄的粥样硬化斑块亦可为不稳定斑块。以往利用HRMRI对颈动脉斑块进行的研究发现大量高危斑块存在于狭窄程度<50%的颈动脉中[10]。这提示动脉管腔的狭窄程度对于斑块稳定性的预测价值有限[11-12]。
烟雾病是一种病因未明的进行性闭塞性脑血管疾病,多见于儿童与青年,其引起动脉狭窄的原因为平滑肌细胞或内皮细胞增殖导致的内膜增厚,表现为颈内动脉末端及其分支的严重狭窄或闭塞伴广泛侧支形成[13]。动脉粥样硬化性烟雾综合征为其重要的鉴别诊断之一。传统血管影像学主要显示管腔狭窄程度,难以区分两者,而HR-MRI管壁成像除可显示管腔狭窄程度外尚可显示管壁病变性质,在其鉴别诊断方面有重要价值。两者主要的HR-MRI鉴别点在于动脉粥样硬化表现为不均质的偏心性管壁增厚,而烟雾病表现为均质的环形管壁增厚,增强表现为无明显强化或轻度环形强化[13-14],且由于重构方式的不同,烟雾病患者的血管外径明显小于动脉粥样硬化性狭窄者[15]。本研究中2例烟雾病患者经HR-MRI扫描于其中1例闭塞血管近端发现不规则偏心性管壁增厚,明确其为动脉粥样硬化性烟雾综合征。
中枢神经系统血管炎在常规血管影像学上的表现与动脉粥样硬化等其他原因所致的管腔狭窄相似。但在HR-MRI管壁成像上,不同于粥样硬化性狭窄的偏心性管壁增厚及增强,其表现为受累管壁光滑、均匀一致的向心性增厚及炎性管壁的弥漫性增强[16]。但这种影像学表现亦可见于因上游血管重度狭窄或闭塞而致下游血管管壁水肿者[17],提示临床医师需结合MRA、CTA等进行综合分析,以免误诊。
2例UE型卒中患者中1例有高血压及类风湿病史,均控制不佳,颅脑MRA提示前循环多血管狭窄伴烟雾状侧支形成,HR-MRI显示基底节区多发血管流空影,无偏心性管壁增厚及强化,且激素冲击治疗无效,故考虑其为烟雾病而非动脉粥样硬化或血管炎。另1例患者患SLE多年,糖脂代谢异常,HR-MRI发现颈内动脉末端偏心性管壁增厚,表明其并存动脉粥样硬化。既往研究证实SLE患者更易发生动脉粥样硬化,其原因与糖皮质激素所致的糖脂代谢障碍及异常的炎症、免疫状态相关[18]。但患者对激素治疗的良好反应提示其责任血管病变原因为系统性血管炎而非动脉粥样硬化。而增强扫描无强化,推测与扫描前已应用激素冲击相关。结合患者的病史、辅助检查及治疗反应,对于存在多重血管病危险因素的患者,HR-MRI管壁成像亦可为临床医师探究责任血管病变原因提供帮助,以指导其制订更为准确的防治方案,从而改善患者预后。
虽然本研究为回顾性研究,存在非连续性入组患者、OE及UE型卒中患者例数较少等局限性。但本研究表明,与传统血管影像学相比,HR-MRI具有同时显示管壁细微结构及管腔大小的优势,有利于临床医师对于卒中病因的精确分型及卒中患者的精准化诊治。结合患者的临床特征、实验室及其他影像学检查结果,可实现对穿支动脉梗死病因的分析,颅内动脉狭窄闭塞性疾病的鉴别,以及具有多重血管病危险因素患者责任血管病变原因的明确诊断。
【点睛】应用HR-MRI显示颅内动脉管壁细微结构特征,可协助临床医师明确卒中病因分型,实现临床医师对卒中患者的精准化诊治。
