钼靶结合超声乳腺影像报告和数据系统分类对微小乳腺癌的诊断价值
2021-01-29牛晓仙郭卫红李金利
牛晓仙,郭卫红,李金利,冯 丽
焦作市第二人民医院超声诊断科,河南 焦作 454001
微小乳腺癌是指肿瘤直径≤0.5 cm病灶,其一般缺乏乳腺癌典型表现,因此易被忽视[1]。但有研究指出,随乳腺病灶直径的增大,肿瘤扩散转移的风险会不断增高,其预后越差,因此提高微小乳腺癌的早期诊断是改善乳腺癌预后的关键点。现影像学检查是其主要检查方式,钼靶对钙化的检出率较高,易于乳腺癌早期病变的发现;而超声对结节诊断率较高,能清楚地显示肿块的大小、边界、回声。通过BI-RADS分类,大大提高了微小乳腺癌的检出率,优势明显[2]。本研究以病理结果为金标准,探讨钼靶结合超声BI-RADS分类对微小乳腺癌的诊断价值,以期为临床微小乳腺癌的早期诊断提供参考。
1 资料与方法
1.1 一般资料
选取2017年8月—2019年8月焦作市第二人民医院诊治的208例乳腺病变患者,共216个微小乳腺病灶为研究对象。纳入标准:(1)乳腺癌符合《中国抗癌协会乳腺癌诊治指南与规范》[3]诊断标准;(2)乳腺病灶直径≤0.5 cm者;(3)乳腺癌钼靶、超声检查前均未行手术、穿刺活检、药物治疗者;(4)无检查禁忌者;(5)临床资料完整者。排除标准:(1)严重心、肝、肾等功能障碍;(2)钼靶、超声检查禁忌者;(3)合并有其他恶性肿瘤者;(4)血液系统疾病;(5)合并其他感染性、炎症性疾病;(6)妊娠或哺乳期妇女。入选患者中,年龄22~68岁,平均年龄(45.35±6.42)岁;体质量指数(body mass index,BMI) 19~28 kg/m2,平均体质量指数(23.32±3.26) kg/m2。本研究征得医院医学伦理委员会批准,研究对象均知情同意。
1.2 检查方法
钼靶X线摄片:采用美国GE Senographe Essential全数字乳腺摄影机摄片,常规摄双乳头尾位和内外斜位,并进行加压,乳房压至30~50 mm的厚度,在全自动曝光条件下,采集受试者的图像并上传到工作站中进行处理。观察乳腺体的结构、位置、大小、形态及钙化情况。
超声检查:采用PHILIPSIU22超声诊断仪,设置线阵探头为L12-5,频率为8~14 MHz。患者行仰卧姿势,在双侧乳房及腋下充分暴露情况下,以乳头位中心对患者乳腺部位进行横切、纵切、斜切等扫描。发现病灶后,从各个切面及角度对病灶的位置、大小、形态、边界、纵横比内部回声、钙化情况等进行观察,并按照BI-RADS分类标准进行分类。
1.3 观察指标及评判标准
(1)超声BI-RADS分级:按肿块形态、边缘、回声等,超声图像分低度和高度恶性可疑:①低度恶性可疑:肿块形态表现为圆形或分叶状、横纵比>1、边缘模糊、内有液体无回声、后方回声衰减等。其中以上特征中包含一项即可为BI-RADS 4级。②高度恶性可疑:肿块不规则、边缘呈毛刺状或角征、内部回声伴微钙化等。以上特征中包含其中两项即可为BI-RADS 5级;若含有其中一项至少列为BI-RADS 4级,可结合临床检查部分列入BI-RADS 5级[4]。钼靶BI-RADS分级以病灶肿块、钙化、非对称致密性、结构扭曲、腋窝淋巴结肿大等进行评估。
(2)BI-RADS分类标准:①1类:评估不完全,需要结合其他影像学检查共同评估。②2类:阴性,未发现病灶。③3类:良性病灶可能大,无恶性特征显现,恶性可能≤2%。④4类:可疑恶性病变大(恶性率2%~95%之间),建议穿刺活检。可分为4 a、4 b、4 c级,其中4 a为轻度恶性(3%~30%),4 b为中度恶性(31%~60%),4 c为高度恶性(61%~95%)。⑤5类:高度恶性(>95%)。⑥6类:穿刺活检证实为恶性病灶。其中0~2类为良性,3~5类为恶性。
1.4 统计学方法
所有数据采用SPSS 22.0统计软件进行处理,计数资料用例数和百分比(%)表示,行χ2检验;采用受试者工作特征曲线(receiver operator characteristic curve,ROC曲线)评估临床价值,曲线下面积(area under curve,AUC)0.7~0.9表示有一定准确性,>0.9准确性较高。以P<0.05为差异有统计学意义。
2 结果
2.1 乳腺病变患者病理类型及例数情况
208例患者经穿刺或手术证实,良性组89例(92个病灶),恶性组119例(124个病灶),见表1。

表1 乳腺病变患者病理类型及例数情况
2.2 钼靶、超声BI-RADS分类及两者联合对微小乳腺癌的诊断结果
结果显示:对216个病灶按照钼靶、超声BI-RADS分类进行评估,钼靶诊断微小乳腺癌的阳性预测值、阴性预测值分别为79.03%、89.13%,超声为90.32%、93.48%,钼靶、超声联合为95.16%、97.83%,联合诊断准确率大于单一方法,见表2。
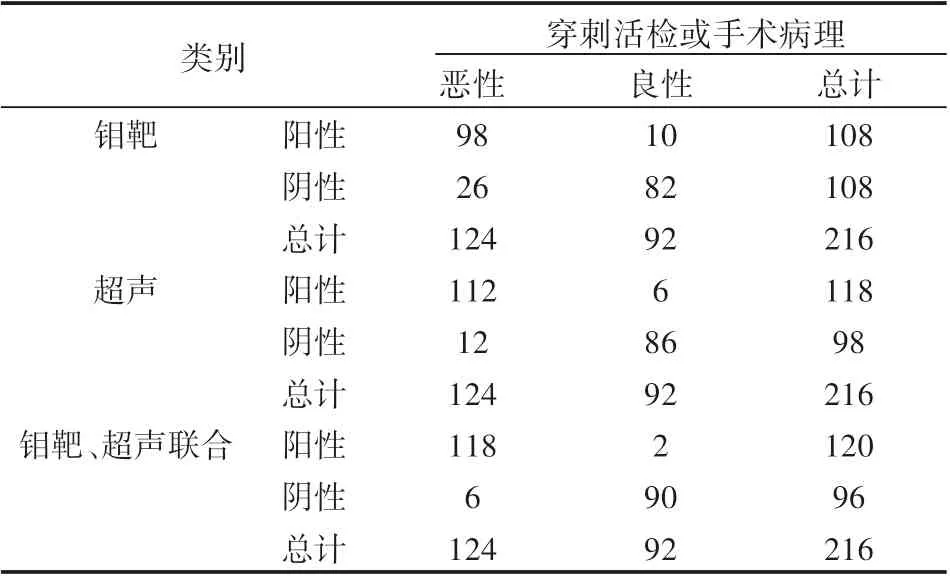
表2 钼靶、超声BI-RADS分类及两者联合对微小乳腺癌的诊断结果 (个)
2.3 钼靶、超声BI-RADS分类比较
124例确诊为微小乳腺癌的患者,在3级诊断中,钼靶的误诊率大于超声,差异有统计学意义(P<0.05)。在4、5级诊断中,超声的诊断敏感性大于钼靶,差异有统计学意义(P<0.05),见表3。

表3 钼靶、超声BI-RADS分类比较 个(%)
2.4 钼靶、超声BI-RADS分类及两者联合对微小乳腺癌的诊断价值
钼靶、超声BI-RADS分类诊断微小乳腺癌的AUC为0.841、0.919;预测敏感度、特异度:钼靶为79.03%、89.13%,超声为90.32%、93.48%。而联合诊断的AUC为0.965,敏感度、特异度为95.16%、97.83%,均高于单项诊断,见表4。

表4 钼靶、超声BI-RADS分类及两者联合对微小乳腺癌的诊断价值
3 讨论
近年来,乳腺癌的发病率在不断的提高,其发生时常伴有乳房胀痛症状,若未及时进行治疗可对女性群体的健康造成严重的威胁。而微小乳腺肿瘤直径较小,缺乏乳腺典型表现,因此易被忽视。随着乳腺的不断生长,肿瘤直径不断增大,易增加肿瘤转移及扩散风险。手术切除、放疗、化疗等对早中期乳腺癌患者的治愈效果较好,而对于乳腺癌晚期患者的预后较差。因此,微小乳腺癌的早期诊断及治疗至关重要。影像学检查是其主要检查方式,钼靶对微小乳腺癌的钙化、结构扭曲等反应较为灵敏;而超声检查具有较高分辨率,可清晰显示乳腺肿块病灶,并通过肿块形态、边界、内部回声、纵横比等的观察有效判定超声BI-RADS级别[4]。因此钼靶及超声BI-RADS分类是目前用于微小乳腺癌诊断的首要方法。
钼靶X线和超声可分别从不同的方面反应病灶的特性,两种检查方式可互补,联合检查可有效提高乳腺癌恶性的检出率[5]。本研究中,经BI-RADS分级发现,BI-RADS超声对微小乳腺癌诊断的准确率高于钼靶,且两者结合准确率更高。另在BI-RADS 3级中,钼靶的误诊率大于超声。在BI-RADS 4、5级中,超声的敏感性大于钼靶,两者比较差异具有统计学意义。分析原因可能在于:(1)高频超声分辨率高,其微小病灶的识别能力不断提升,虽然其对微钙化的敏感度不如钼靶,但高频超声的纵向分辨率强,亦可清晰显示大部分乳腺内部微钙化灶[6]。(2)钼靶对微小乳腺癌的钙化情况虽较为敏感,但其特异性较低,而超声不仅能显示结节,而且对大多数钙化显示较为清晰,因此对乳腺恶性检出率高[7]。而本研究引入BI-RADS分级,从乳腺肿块、边缘、内部回声等多方面出发,对超声检出的低度及高度恶性特征进行分析分类,并以组织病理学检查对可疑恶性特征进行检验,减少了乳腺良、恶性的误诊率。同时BI-RADS分级对乳腺各特征进行规范分级,具有科学依据,降低了超声检查操作者的经验,提高了超声检查的准确性。本研究钼靶、超声BI-RADS分类评估结果显示,预测敏感度、特异度:钼靶为79.03%、89.13%,超声为90.32%、93.48%,而两者联合诊断的AUC为0.965,敏感度、特异度为95.16%、97.83%,均高于单项诊断。
综上所述,钼靶、超声BI-RADS分类联合诊断可有效提高微小乳腺癌诊断的准确率和敏感度,弥补了单项检测的不足之处,具有更高的诊断预测价值,在临床上值得推广。
