煤炭燃烧过程中大气污染物NOX形成与转化研究进展
2021-01-15郭思聪张凯霞刘守军杨颂杜文广张红霞上官炬支国瑞
郭思聪,张凯霞,刘守军,杨颂,杜文广,张红霞,上官炬,支国瑞
(1.太原理工大学 煤科学与技术教育部和山西省重点实验室,山西 太原 030024;2.太原理工大学 化学化工学院,山西 太原 030024;3.太原理工大学 期刊中心,山西 太原 030024;4.中国环境科学研究院,北京 100012)
煤炭作为重要的化石能源,在我国一次能源消费结构中约占60.4%[1]。煤炭直接燃烧在提供能量转化的同时又带来严重的环境问题,煤炭燃烧可产生硫氧化物(SOX)、氮氧化物(NOX)、颗粒物(PM)等。近几年控制NOX的排放引起并得到各级政府和民众的高度关注,2017年NOX的排放量为1 258.83万t,约为SO2排放总量的1.5倍[1]。NOX对大气生态环境破坏主要有:①会形成酸雨;②经光化反应会生成和分解O3;③促进PM2.5形成[2]。2015年环保部、国家发改委、国家能源局联合印发《全面实施燃煤电厂超低排放和节能改造工作方案》,要求NOX的排放值不高于50 mg/m3。因此,在煤炭绿色开发与清洁高效利用中,控制煤炭燃烧中NOX排放就成为重要组成部分之一。煤炭燃烧过程形成的NOX分为热力型、快速型及燃料型,其中燃料型NOX来自煤中氮化合物的燃烧,占NOX总量的90%以上[3],因此减少燃料型NOX的形成是燃烧脱硝的关键。传统控制煤炭燃烧NOX排放方法主要有:燃烧后烟气脱硝和燃烧中脱硝。烟气脱硝在高架源中使用较为普遍,主要使氨、尿素等NOX还原剂在有或无催化剂的条件下,与烟气中的NOX发生反应生成N2和H2O[4]。这些技术在高架源控制NOX排放取得显著成绩,但还存在脱硝效率低、氨逃逸、颗粒物产生等不足[5]。与高架源相比,低矮面源及无组织排放源由于未设置脱硝设施,其造成的环境污染是电厂等高架源的10倍以上[6]。近年来,燃中脱硝技术也得到了很大的发展,由中国科学院过程工程研究所发明的解耦燃烧技术是将燃烧过程分为煤热解和煤焦燃烧两个阶段,热解产生煤气和半焦,将煤气和空气混合燃烧,在半焦的参与下将NOX进行还原[7]。太原理工大学提出[8]:在炭基燃料中添加金属复合助剂,借助中高温干馏进行燃前脱氮与金属助剂的燃中脱硝两条路径达到减少炭基燃料NOX的排放。以上所述的两种燃烧脱硝技术均将燃烧分为煤炭热解和挥发分、半焦燃烧两个阶段来控制NOX的生成。研发控制煤燃烧过程中NOX的形成(燃中原位还原脱硝)对实现民用散煤燃烧NOX达标排放或间接降低NOX浓度来减轻后续烟气脱硝负荷具有重要科学和应用价值。将为煤炭燃烧过程中原位热解减少NOX前驱物和燃烧脱硝的两步协同催化作用[3]科学研究和技术开发提供理论和技术依据。
1 煤炭燃烧过程中NOX的形成和转化
煤炭燃烧过程可分为燃烧初期煤炭低温热解(煤炭初次热解及热解产物挥发分二次热解)和燃烧中后期热解产物煤焦及热解气高温燃烧两个连续阶段。在燃烧过程中煤中氮的迁移途径大致可归为以下四步:①煤中含氮化合物低温热解(干馏)形成的NOX前驱物,即气态挥发分氮化物(HCN、NH3)和固态煤Char-N化物(Char-N);②HCN、NH3高温燃烧均相氧化形成的NOX;③ Char-N高温燃烧多相氧化形成的NOX;④NOX发生均相与非均相的还原反应转化为N2。
1.1 燃煤过程中NOX的形成
煤中的氮化物经高温燃烧形成NOX主要来自两个途径:①燃烧初期煤热解气态产物NH3、HCN的氧化反应,热解释放挥发分阶段有25%~40%的氮迁移到气相中然后燃烧生成NOX[9];②燃烧中后期煤热解固态产物煤焦中氮化物的氧化反应。煤中氮化物在燃烧过程中的迁移路径见图1[10]。

图1 煤中氮化物燃烧迁移路径Fig.1 The migration path of nitrides during the coal burning process
煤低温热解时,煤中的小分子氮化物受热分解为N、NHi、CH、CN等自由基,并主要形成NH3和HCN,经氧化燃烧形成NOX。HCN和NH3在温度350 ℃时开始生成,并分别在450 ℃和670 ℃达到最大值[9]。HCN在均相氧化过程中主要被氧化为NO、N2O、N2;NH3在均相氧化过程中的主要产物是NO和N2。通常来讲HCN的生成量要高于NH3,但在燃烧烟气中,NH3的释放量要略高于HCN[11]。
在煤焦燃烧阶段,稳定存在于焦中的N原子随着C原子的氧化暴露出来,遇到O2被氧化为NO、N2O、NO2。N2O的生成对温度的变化极为敏感,在温度高于900 ℃,N2O的生成量极少,大部分燃料氮直接转化为了NO;在整个燃烧过程中N2O的生成量仅占燃料氮转化的0.1%左右,NO2的生成主要是NO与煤中载氧颗粒发生非均相反应生成的[12]。煤中氮含量对焦炭燃烧NO释放有着明显影响。随着煤中含氮量的增加,NO释放浓度相应增加,但燃料NO生成率却呈下降趋势,原因是含氮量的增加导致NO还原速率比NO生成速率大。当煤中含有较低的挥发分以及较高的碳和氮含量时,焦炭中氮燃烧对NOX排放的贡献度较大;当煤中含有较高的挥发分氮以及较低的碳含量时,挥发分氮燃烧对NOX排放的贡献度较大[13]。
燃烧气氛对NOX的形成影响明显,富O2的存在会使NOX产率增大。从O2的氧化活性来分析:一方面O2的存在加速了焦炭活性位的络合物的脱附,在一定程度上对NO的还原有促进作用;另一方面,相比于NO,焦炭更易与O2反应生成CO2,同时O2的存在使还原NO的成分被氧化,因此整体上看高浓度O2的存在对NO的还原起抑制作用。从挥发分与NO的均相反应分析,氧体积分数的升高能提高碳氢小分子的氧化反应速率,因此O2的存在会降低碳氢小分子与NO的还原反应速率[10]。煤燃烧过程中,凡是与NOX发生还原挥发分均可与O2反应,使还原性气氛减少,因此富O2条件下NOX生成量会增加。
煤炭的燃烧是一个复杂的过程,现关于煤炭燃烧过程中氮迁移路径研究主要是基工业锅炉条件模拟其高温燃烧且研究较为成熟,作为大气污染防治较难管控的民用燃煤,一直以来被忽视。搞清煤炭在民用及露天条件下直接燃烧燃烧过程中煤中氮的迁移规律值得我们思考和研究。
1.2 燃煤过程中NOX的转化
煤燃烧过程中存在着NOX还原转化有两个途径:一是挥发分HCN和NH3燃烧氧化形成NOX发生还原反应生成N2;二是Char-N燃烧氧化形成NOX发生还原反应生成N2。由此,燃烧过程通过促进NOX还原转变成N2的方式就可实现燃煤过程中脱硝。煤燃烧过程中NOX主要还原剂有:焦炭、CO、NH3等。NOX的还原脱硝也与氧含量及燃烧温度等因素有关。在煤燃烧过程中一个低氧区域是低NOX产生的必要条件,高氧浓度抑制了NOX与CO、焦炭的还原反应,而煤粉颗粒附近的氧体积分数极小,抑制了氮的氧化反应,从而降低了燃料氮向NOX的转化率[14]。高温促进了NOX的生成,一方面,高温促进了煤焦的氮位被快速打开;另一方面,高温加快了焦炭的燃烧速率,使NOX在C表面的还原量减少[15]。
1.2.1 焦炭还原NOX关于焦炭还原NOX反应机理在上世纪八九十年代就在反复被研究。首先,Teng等通过苯酚-甲醛树脂为原料,研究了NOX在碳表面的解析作用,并提出了两条NOX在焦炭表面的吸附还原途径:一条是形成碳表面络合物C(NO)的可逆化学吸附途径;另一条是生成N2、碳表面氧化物C(O)和C(O2)的不可逆化学吸附途径。后来,张秀霞等从量子化学的角度论证了反应路径一的正确性[16],计算发现反应途径一所需能量低于反应途径二,NOX在焦炭表面的异相还原主要经由反应途径一进行。目前,普遍认同的NOX在焦炭表面被还原的反应机理为R(1)、R(2)、R(3),其中 R(1)是焦炭还原NO的控制步骤[17]。高温下(—O)和O2在焦炭表面的吸附性较强,与C反应分别生成CO和CO2,一定程度上抑制了N的氧化过程,而促进了NOX的还原过程[18]。同时,高温燃烧形成的NO吸附在煤焦—C表面,可使NO分解为(—N)和(—O)自由基,并被炽热的焦炭吸附形成C(N)、C(O),(—N)最终还原为N2,而C则被氧化为CO。NO在焦炭表面还可被还原为N2O,N2O会在焦炭表面经由氧抽提反应发生异相分解释放出N2[17]。
2C( )+NO→C(O)+C(N)
(1)
C(O)→C( )+CO
(2)
C(N)+NO→C(O)+N2
(3)
NO-焦炭的还原会经历化学反应控制、化学反应与扩散共同控制以及扩散控制3个阶段。张聚伟研究NO-焦炭的反应动力学后,指出NO-焦炭反应在低温区受动力学控制,而在高温区则受扩散控制[19]。温度低于950 ℃时,NO-焦炭反应表观活化能较高,Char-N形成NO和焦炭表面的NO还原反应均进行相对缓慢,总体Char-N向NO转化率较低;温度在950~1 050 ℃时,扩散对燃烧速率起主导作用,焦炭氮被氧化为NO的反应速率迅速加快,且大于NO在焦炭表面的异相还原速率,Char-N向NO转化率明显提高;温度高于1 050 ℃后,NO在焦炭表面的异相还原反应速率超过焦炭氮被氧化的反应速率,NO的生成率随温度的增加而降低[20]焦炭对NO的异相还原作用随着O2浓度的升高而减弱。煤焦与NO的还原反应主要在焦炭的表面和内孔进行,随着氧体积分数的增高,焦炭表面的活性N元素能直接与氧原子结合生成NO,阻碍了NO与焦炭表面的还原反应,使NO含量升高[10]。
焦炭粒径对还原NOX的影响与孔扩散阻力、比表面积及停留时间等综合因素有关。NO还原发生在焦炭的孔隙中,大粒径的焦炭不利于NO的还原,但大粒径的焦炭延长了NO的停留时间,又增加了NO被还原的可能性[21]。在煤炭燃烧过程中,NOX的生成主要来自于燃烧初期挥发性氮化物的氧化燃烧,而煤焦燃烧阶段相对于该过程滞后很多,通过改良燃煤锅炉的工艺条件,增加高浓度NOX与煤焦的有效反应时间,可有效降低NOX的排放。
1.2.2 NH3还原NOXNH3是煤的燃烧过程中主要的还原性挥发分氮;同时NH3具有很强选择性,通过反应R(4)、R(5)将NOX还原生成无污染的N2和H2O[22]。NH3还原NOX由美国Eegelhard公司开发并申请了专利,NH3主要是通过氨自由基NH、NH2与NO的反应而形成N2[23]。温度高于1 000 ℃时,HCN与H2会发生二次气相反应生成NH3,有利于NOX的还原[24]。
4NO+4NH3+O2→4N2+6H2O
(4)
6NO2+8NH3→7N2+12H2O
(5)
在燃烧过程中,水蒸汽可导致NO排放减少。一方面,水蒸气与焦炭产生的H自由基会极大促进NH3的生成,从而直接影响NOX的排放量;另一方面,煤中水含量的增加可降低了还原反应基团(—NH)和氧自由基反应的可能性[25]。
其次,燃烧温度与氧气浓度也会影响NH3还原NOX。高温下主燃区可形成高温强还原性气氛,促进了NOX的还原[26];高氧环境中NH3被氧化为HNO,最终形成NO;贫氧环境中NH3分解为NH2、NNH中间体,将燃烧产生的NO还原为N2[23],同时贫氧还可以有效增加NH3还原NOX的反应温度区间[27]。
可见,燃烧过程中NH3的存在会极大促进NOX的还原,现在阶段燃煤脱硝多为燃后烟气脱硝且主要用于工业锅炉。鉴于NH3的排放伴随煤炭的整个燃烧过程及散煤燃烧无污染控制设施的现状,提高散煤燃烧过程NH3的生成及还原NOX的利用率,可有效降低煤炭直接燃烧NOX的释放。
1.2.3 CO还原NOXCO还原NO的研究,最早由Unland在Pt表面证实[28]。在燃煤过程中,由于炽热的炭与CO2的气化反应使得局部形成大量的CO,并通过反应R(6)-R(9)对NO进行还原[29]。CO还原NO的反应步骤包括:CO、NO的分子吸附、NO的解离、表面活性物种的重组以及产物的脱附,其中激活态Nads和Oads的产生是NO被还原的关键。
阮丹等[30]利用Chemkin软件对CO还原NO反应热力学与动力学模拟分析结果表明,无催化剂时,NO还原温度为1 380 ℃;有催化剂时,NO在250 ℃时就可以被CO在铂表面还原生成N2O和N2,低温下N2的生成为主,高温下N2O的生成为主。当CO浓度过高时,CO会优先占据C( )活性位经R(10)、R(11) NO排放量下降,同时CO浓度的升高还可促进了N2O的还原为N2[22,31]。
NO+·↔NOads+·↔Nads+Oads
(6)

(7)

(8)
(9)
(10)
(11)
在催化还原反应过程中,CO2的存在会影响CO对NO的还原。首先CO2的气化破坏了稳定的(—CN)键,并且使(—CN)键暴露出来,促进了焦—N的脱除[24],其次,高浓度CO2会与焦炭反应生成高浓度的CO,高浓度的CO又可以促进NO的还原反应[15,22]。当CO2在焦炭表面气化形成CO,但若CO周围有O2的存在会阻止CO的解析,使焦炭表面的CO浓度降低,从而抑制NOX的还原[15]。水蒸气的存在可提高了自由基、H2和CO的浓度,促进了NO的还原[22]。
从煤炭的整个燃烧过程来看,在燃烧初期煤炭低温热解及局部氧化燃烧阶段,是NH3和CO高产的阶段;在高温燃烧阶段,煤中挥发性氮化物基本逸出,同时煤炭燃烧较为充分,CO和NH3的生成减少,主要表现为焦炭对NOX的还原。现利用NH3、CO及煤焦对NO的脱除应用也较多,但研究都较为单一,针对燃煤直接燃烧NH3、CO及煤焦对还原NOX的协同作用研究较少。
2 矿物质对NOX的形成和转化的影响
煤中含有大量无机矿物杂质(如Si、Al、Fe、Ca、Mg、Na等),其中碱金属(K、Na)、碱土金属(Ca、Mg)和过渡金属(Fe、Ti)化合物对煤燃烧过程中NO还原、N2O分解、NH3氧化等反应具有明显的催化作用。矿物杂质的催化作用大致归纳为:①煤炭中的某些矿物成分促进了对NO的还原;②不同成分矿物质催化活性不同,且与温度和气氛等因素有关;③催化效果与各化合物的化学形式及含量有密切关系,且多数存在“催化剂饱和”现象;④几种物质组合催化效果要比单一物质明显增强,不同催化剂间存在相互作用;⑤CO、CO2、O2、H2O等气体对矿物质催化效果存在影响。
煤中原有的金属矿物质对燃烧中NOX的催化还原作用影响很大。在煤热解阶段,煤中金属矿物质可促进NH3、HCN、Char-N转化为N2;在煤燃烧阶段,金属矿物质对NOX的催化作用主要表现在两方面:一是分散在焦炭内部,和碳基质相互作用共同促进含氮化合物反应,二是灰分中的金属矿物质单独催化[21]。
2.1 过渡金属化合物
研究表明:金属氧化物,尤其是过渡金属氧化物对CO还原NO有极大的促进作用[32]。常见的过渡金属有Fe、Cr、Cu等,这些金属的氧化物对CO的氧化的活性顺序为:Fe2O3>CuCr2O4>Cu2O>Cr2O3>NiO>Pt>Co3O4>Al2O3(5%SiO2)>MnO>V2O5,其中Fe2O3和Cr2O3对CO还原NO 的选择性较好。Fe基在煤炭燃烧过程中对氮化物的影响,可从热解形成的NOX前驱物HCN和燃烧形成的NOX两方面来讨论。
就热解形成的NOX前驱物HCN来说。Fe2O3能够有效地催化氧化HCN为N2,并通过反应R(12)-R(14)达到对HCN 的无污染脱除,避免了HCN在燃烧过程中的二次氧化[33]。

(12)

(13)

(14)
就燃烧形成的NOX来说,铁基对NOX的还原作用主要通过CO和焦两类还原途径。首先,Iizuka最早发现SiO2负载的Fe2O3是催化CO还原NO的高活性催化剂[34]。Fe与NOX反应后的氧化物为Fe2O3,在CO作用下,Fe的表面呈松散结构,可以保证Fe对NOX的连续还原反应。CO有利于铁的氧化物还原为金属铁,进一步提高了铁直接催化还原NO的效率;而O2能将金属铁氧化为Fe2O3,降低了铁直接催化还原NO的效率;CO2气体的影响相对较小。水蒸气的存在将加速金属铁的氧化,在Fe表面生成一层致密的氧化膜(FeO、Fe3O4),阻止了NO与Fe的接触,使脱硝效率大大降低[35]。其次,铁基可以催化NO—焦还原反应。在600 ℃时Fe3+被还原生成单质铁,高温下Fe金属的原位生成率大幅提高,促进了NO—焦还原反应[36]。
复合金属催化剂的催化活性明显高于单金属催化剂,Na的存在会降低C还原Fe的温度,间接促进NO—焦的还原反应,表现出复合金属的协同催化效应[36]。在负载不同元素(Mn、Cu和Fe)—Ce的二元催化剂中,Mn相和Fe相的添加能够提高催化剂的低温活性;Cu相的添加能够提高催化剂的高温活性[37]。在Fe—Co二元金属催化剂中,Fe3+和Co3+被证明为分别为CO和NO的活性位点[38]。在氧化铁中引入过渡金属元素(Ce、Cu、Co)后,过渡金属元素的引入增加了铁基催化剂的比表面积和吸附能力,同时提高了掺杂催化剂的氧化还原能力[39]。Ce和Ti掺杂会抑制铁氧化物中Fe2O3的结晶,细化其孔径,增大其比表面积和比孔容; 促使催化剂表面活性铁、铈组分分散度增加;铈钛掺杂会增强铁氧化物表面NH3和NO的吸附性能,尤其是铁氧化物表面对NH3的低温吸附,从而提高铁基氧化物低温NH3—SCR脱硝性能,降低NOX的排放[40]。
2.2 碱土金属化合物
常见的而碱土金属有Ca、Mg等。单质Ca仅在2 000 ℃以上的温度下才会生成,因而在煤焦表面对NO起还原作用的钙基是CaO,CaO的前驱物主要有机钙和钙基金属氧化物。
常见有机钙有甲酸钙(CF)、醋酸钙(CA)、醋酸钙镁(CMA)等。有机钙对NOX的作用机理主要表现为三点:首先,有机钙高温煅烧后比表面积和比孔容远大于普通钙基;其次,有机钙含有丰富的有机可燃气体,裂解时会释放大量的CH、H等还原性小基团,促进NOX向N2的转化;最后,Ca对煤焦还原NOX的均相和异相还原反应均具有催化作用[41]。
就热解形成的NOX前驱物HCN来说。CaO和MgO可以将HCN转化为N2[42]。就燃烧过程形成NOX来说。CaO对C 和CO 还原NOX的催化机理为氧传递催化机理,CaO的存在提高了焦炭表面络合物C(O)的浓度促进了CO对NO的还原[43]。其次,CaO能够促进碳的结晶化,CaO分散程度越高,对Char-N向N转化的催化作用越强[44]。
燃烧过程中SO2、CO2、O2对钙剂催化NOx还原存在一定影响。SO2对钙基催化还原NOX有很大的抑制作用,随着SO2浓度的升高,石灰的硫化程度增大,石灰的孔隙堵塞,孔隙率下降,降低了CaO对NOX的催化还原作用[45]。CO2对CaO催化还原NOX有“双温区效应”:一定温度范围内CO2与CaO反应生成CaCO3,抑制了CaO的催化作用;但高温下可以将CaCO3分解为CaO提高了CaO的催化作用[43]。CaO可以与NOX前驱物挥发分HCN在低氧条件下发生反应生成NH3、H2、CO还原性气体,促进NOX的还原;而在氧化环境下则容易生成NO,提高了NOX的生成[46]。

碱土金属一直以来作为固硫剂研究较多,在燃煤脱硝方面研究较少。此外,基于我国蓝天事业,清洁煤逐渐走进千家万户,碱土金属化合物作为重要的添加剂,在研究碱土金属化合物脱硫脱硝效果的基础上,我们还应考虑到碱土金属化合物对燃料燃烧特性的影响。清洁煤多用于冬季农村取暖,燃料的燃烧性能与农户的生活及健康息息相关,因此将我国的基本国情、民情也考虑在实验研究过程中很有必要和意义。
2.3 碱金属化合物
常见的碱金属主要有Na、K等。煤中的Na元素主要以无机钠的形式存在,主要存在于粘土矿物、沸石、岩岩等无机矿物质中。钠基化合物对焦炭还原NO的有显著催化作用,向燃煤中添加钠基化合物,可以降低NOX的排放;钠基化合物还可以减少OH、O的浓度来抑制挥发分氮的氧化,促进NOX的还原,达到减排的效果[47]。姚佳彬等[48]向煤中添加Na2CO3和NaCl进行燃烧实验,结果表明,钠基化合物可以消除燃烧后期NOX的集中排放过程。但燃烧条件下金属钠很难被还原出来,在焦炭表面金属钠含量极少;其次,随着时间的推移,Na2O很可能与CO2在焦炭表面形成了Na2CO3抑制了NO的还原反应[36]。
孙桐等[49]采用Chemkin动力学模拟软件,研究 Na/K 添加剂对SNCR脱硝性能影响,模拟结果表明,不同 Na/K添加剂对 NO还原促进顺序为 NaOH≈Na2CO3> KOH≈K2CO3> KCl > NaCl;Na/K添加剂通过循环路径产生 OH基,进而增加NH2基团的浓度来促进NO的还原,其中碱金属氢氧化物(MOH)对 SNCR 脱硝的促进路径为 NaOH→NaO2→Na→NaO→NaOH,碱金属氯化物(MCl)则主要通过 MCl→M→MCl 削弱 Na/K 添加剂的促进作用。
温正成等[50]首次用量子化学模拟研究了Na/K对煤再燃过程中的NO-焦炭非均相的催化机理(见图2),研究发现:NO-焦炭和NO-Na/K反应分三步进行,添加碱金属化合物能提高NOX还原效率。
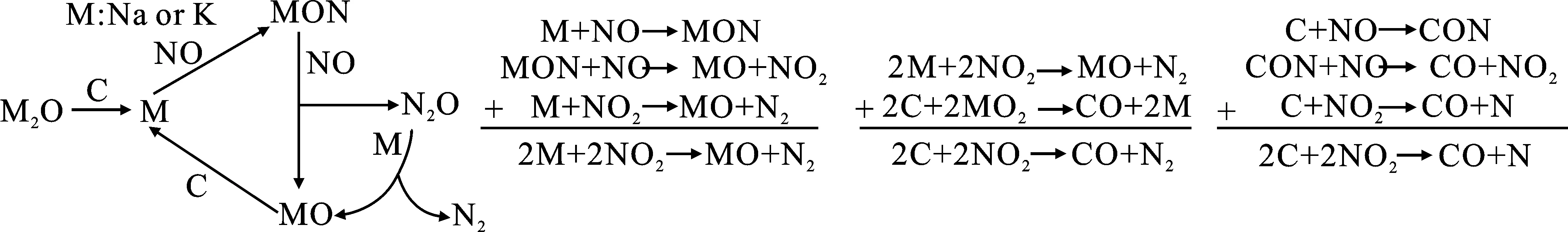
图2 Na/K对煤再燃过程中的NO-char非均相的催化机理Fig.2 Catalytic mechanism of Na/K for NO-char heterogeneous reactions during the coal reburning process
在煤炭中加入金属化合物对煤炭直接燃烧脱硝有很大的促进作用。随着我国环保事业的发展,煤炭作为重要的大气污染源,燃煤脱硝力度也在不断加大,在研究过程中仍存在以下几点不足:①脱硝性能多注重脱硝效率的研究而忽略了脱硝机理研究,以至于在研究过程中不能很好地借鉴前人已有研究成果;②燃煤改性多局限于添加单一金属助剂,对添加生物质、生物质-单一金属化合物、及多生物质-多金属助剂耦合作用研究较少;③在煤炭燃烧脱硝研究的基础上配合炉具的改造也是目前较为欠缺的方向;④学科之间的交流不够密切,在研究及方案决策方案的过程中考虑过于片面,应加强交流合作共同解决国内面临的环境问题。
基于以上的考虑,本文提出一种多因素作用燃煤直接燃烧脱硝思路(见图3),利用不同燃烧阶段、不同还原剂、不同助剂在不同工况下的对NOX的协同还原作用,旨在寻求一种最大化促进煤中氮化物转化为N2的途径。

图3 多因素作用煤直接燃烧脱硝Fig.3 Multiple factors are applied to denitration in direct combustion process of coal
3 结语
综上,煤燃烧过程可细分为煤低温热解与热解产物高温燃烧两个连续阶段,在燃烧过程中煤中的氮化物先热解形成NH3、HCN和Char-N,经燃烧形成NO、N2O、NO2并以NO为主,因此控制NOX的排放为煤燃中脱硝的关键。NOX的形成主要来自挥发分中HCN和NH3的燃烧和Char-N的燃烧两个方面。从燃烧条件看,低氧浓度是NOX还原转化为N2的必要条件;其次,适当提高燃烧温度对NOX的还原转化有一定的促进作用。从燃烧过程看,煤炭燃烧过程中产生的焦炭、NH3以及CO均可将NOX还原为N2。焦炭对NOX的还原作用,主要表现在对NO的还原作用,NO经在焦炭表面吸附解离形成表面碳氮组分C(N),并通过以下反应R(1)-R(3)被还原为N2,增加NOX与焦炭的接触时间可提高NOX的还原率;NH3主要是通过氨自由基NH、NH2与NO的反应而形成N2,适当增加燃煤过程中水蒸气的浓度及提高温度,均可促进NH3的生成,间接促进NOX的还原;经CO、NO分子吸附、NO的解离、表面活性物种的重组以及产物的脱附等过程CO可有效将NO还原为N2。在焦炭、NH3、CO还原NOX反应中,NO的解离是还原脱硝的关键。但焦炭、NH3、CO与NOX的还原反应的发生温度均较高,且反应速率较慢;加入金属助剂可适当降低NOX被还原的活化能,加快反应速率。
过渡金属、碱土金属、碱金属等金属化合物助剂对NOX还原反应具有促进作用。就热解来说,过渡金属和碱土金属氧化物均可有效的将NOX前驱物HCN氧化为N2;就燃烧过程来说,过渡金属、碱金属和碱土金属主要表现为对焦炭、CO还原NOX的催化作用。过渡金属和碱金属可将NO还原为N2,焦炭和CO又可将金属氧化物还原为金属单质,金属助剂被循环利用,达到对NOX还原的催化促进作用;而碱土金属氧化物主要表现为对CO还原NOX的氧传递催化机理,碱土金属氧化物的存在提高了焦炭表面络合物C(O)的浓度,促进了CO对NO的还原。此外,碱金属可以减少焦炭表面OH、O的浓度,为NOX的还原创造低氧环境,促进NOX的还原;碱土金属可以促进HCN生成NH3,在避免HCN直接氧化的前提下,增加了NH3还原NOX的几率;不同金属助剂之间对NOX的还原还存在一定的协同作用。
基于民用散煤燃烧排放现状及现有烟气脱硝技术的缺陷,在前人的研究基础上本研究团队提出新思路,即在原煤中加入生物质及金属化合物助剂后直接燃烧,耦合生物质及金属化合物助剂对热解NOX前驱物转化为N2和燃烧过程中C、CO、NH3对NOX还原为N2的协同还原作用并适当调整燃烧工况,使煤中氮化物最大程度转化为N2,实现散煤直接燃烧达标排放,或间接降低NOX浓度来减轻烟气脱硝负荷。本文研究结果将为上述思路的科学研究及技术开发,最终降低燃煤NOX释放提供理论和技术依据。
