喹啉类生物碱在治疗COVID-19中的应用与问题
2021-01-14徐嘉萌韩继丽王格格陈国宁王佩龙
徐嘉萌,韩继丽,王格格,陈国宁,王佩龙,2,傅 强
(1. 西安交通大学药学院,陕西西安 710061;2. 西安市第八医院,陕西西安 710061)
新型冠状病毒肺炎(coronavirus disease 2019, COVID-19)是一种由β属冠状病毒严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2, SARS-CoV-2)引发的发热性呼吸道疾病[1]。截至2020年4月8日,全球累计COVID-19确诊患者逾140万例,疫情形势严峻。各国科研工作者正在全力研发可用于治疗COVID-19的药物。但由于新药研发存在周期长、资金投入巨大、上市审批手续繁复等客观限制,在已上市药物中筛选具有抗SARS-CoV-2活性的药物可大大节省研发时间并提高临床应用安全性,已成为疫情紧急态势下解决问题的主要策略之一。目前,多种已上市抗病毒药物被用于抗SARS-CoV-2活性筛选,如抗HIV药物利托那韦、抗流感药物法匹拉韦等,皆已投入临床试验并取得了一定的研究进展。喹啉类生物碱氯喹、羟氯喹作为临床应用多年的经典抗疟药,已在早期体外试验中被证明具有抗SARS-CoV-2活性,且与其他候选药物相比,喹啉类生物碱具有更优的临床安全性,有望成为治疗COVID-19的重要药物。本文围绕氯喹与羟氯喹的研究现状及应用中可能存在的问题作一概述,以期为开展喹啉类生物碱治疗COVID-19的临床应用提供支持。
1 喹啉类生物碱药物的主要作用
1.1 药物的结构喹啉类药物是一类结构中含有喹啉环的生物碱,具有抗疟原虫、抗病毒、抗肿瘤等药理活性,代表药物有奎宁、氯喹、羟氯喹等(化学结构式见图1)。其碱性源自结构中的氮原子,可与酸形成稳定的盐,临床常以硫酸盐、磷酸盐等形式口服给药。
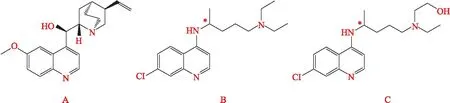
图1 奎宁(A)、氯喹(B)和羟氯喹(C)的化学结构式
喹啉类药物作为临床应用多年的经典抗疟药,在发展过程中历经多次结构优化。1820年,奎宁(quinine)作为具有抗疟作用的活性成分首次被法国科学家PELLETIER和CAVENTOU从金鸡纳树皮中提取出来,成为了第一个有效治疗恶性疟原虫引起的疟疾的药物[3]。19世纪初期,奎宁的分子式与化学结构被阐明,其含有一个喹啉环,是一种天然的生物碱[4]。1934年,德国科学家首次在奎宁的基础结构中引入碱性侧链,合成了抗疟效果更优的氯喹(chloroquine, CQ)。氯喹经过数年的临床前研究后,于1944年开始广泛应用于临床,因其安全、高效且价廉而逐渐取代奎宁成为抗疟首选药。1946年,科学家在氯喹的基础上用羟乙基替代氯喹中的一个乙基合成了新型抗疟药羟氯喹(hydroxyehloroquine, HCQ)。羟氯喹的药理活性与氯喹相似,但在体内吸收更快、分布更广,在胃肠道及眼部的毒性更小[5]。
1.2 抗疟原虫作用疟疾是一种由疟原虫引起的可危及生命的传染病,喹啉类化合物在疟疾临床治疗中起到了至关重要的作用。氯喹与羟氯喹抗疟原虫的机制较为类似,主要作用于疟原虫红内期,通过干扰疟原虫色素形成并影响其裂殖体DNA复制、转录过程,使疟原虫死亡[6]。世界卫生组织在2015年发布的第三版疟疾治疗指南中指出,氯喹对于间日疟原虫、卵形疟原虫和诺氏疟原虫引起的疟疾均有较好的疗效[7]。
1.3 抗病毒作用氯喹具有亲溶酶体特性和弱碱性,主要通过改变内吞体酸碱度值干扰细胞内DNA复制和基因表达来发挥广谱抗病毒作用[8-10]。研究表明,羟氯喹对人类冠状病毒、登革热病毒、HIV病毒等多种病毒具有抑制作用,作用机制有诱导细胞产生活性氧和激活IFN-β、AP-1和NFκB的先天性免疫信号通路[11],影响T细胞和单核细胞中糖蛋白120的翻译后修饰等[12]。
2003年SARS暴发后,有研究发现,氯喹可抑制感染后的Vero E6细胞中SARS-CoV病毒活性,作用机制可能与细胞受体血管紧张素转换酶2(angiotensin converting enzyme 2, ACE2)末端糖基化的损伤导致ACE2与SARS-CoV刺突蛋白之间的结合亲和力降低有关[13]。KEYAERTS等[14]的研究验证了这一点,并进一步确认氯喹体外抑制SARS-CoV的IC50与治疗急性疟疾时的血药浓度较为接近。
1.4 抗SARS-CoV-2作用由于SARS-CoV-2与SARS-CoV同属冠状病毒,且皆作用于S蛋白-ACE2受体,研究人员开始探索SARS-CoV-2是否也可被氯喹抑制。近日有研究表明,氯喹在体外对SARS-CoV-2显示出良好的抑制作用[15],并可通过抑制肿瘤坏死因子-α和白细胞介素-6的释放减少新型冠状病毒感染的中后期的免疫病理性损伤[16]。日前,氯喹在小样本临床研究中已初步显示出了抗SARS-CoV-2的明显效果[2],并被纳入了国家卫生健康委员会发布的《新型冠状病毒肺炎诊疗方案(试行第七版)》[17]。
羟氯喹具有与氯喹相似的抗SARS-CoV-2作用机制与活性,其临床安全性较氯喹更好,也许可以成为治疗COVID-19的更优选择。YAO等[18]使用SARS-CoV-2感染的Vero细胞测试氯喹和羟氯喹的抗病毒活性,实验结果表明,羟基氯喹(EC 50=0.72 μmol/L)比氯喹(EC 50=5.47 μmol/L)能更有效地在体外抑制SARS-CoV-2病毒。近日一项研究也认为,羟氯喹是较氯喹更好的治疗COVID-19药物,其主要原因有三:①羟氯喹在感染前和感染后两个阶段都具有与氯喹类似的抗病毒作用;②羟氯喹可通过降低T细胞CD154的表达来抑制细胞因子风暴,从而减轻COVID-19的严重进展;③羟氯喹比氯喹副作用更少且价廉易得[19]。
2 喹啉类生物碱的药代动力学特征
2.1 氯喹的药代动力学特征
2.1.1吸收 氯喹口服后经肠道快速吸收,通过胃肠道的吸收率为70%~80%。服药后氯喹缓慢释放入血,约2 h达到最高血药浓度,其中与血浆蛋白结合的氯喹约占60%[20]。
2.1.2分布 氯喹在体内广泛分布于肝、脾、肺等内脏组织,血药浓度维持较久,血浆终末消除半衰期长且可变(40~60 d)[21]。
2.1.3代谢 氯喹的代谢转化在肝脏微粒体系统进行,主要经CYP2D6、CYP3A4/5和CYP2C8等细胞色素酶介导,去乙基氯喹为主要代谢产物且仍有抗疟活性,浓度可达氯喹浓度的40%[22]。
2.1.4排泄 氯喹主要经由肾脏排泄,约占总排泄形式的55%,另有约8%的药物随粪便排泄,其他经唾液、汗液等排出[23]。肾排泄中原型药物约占70%,去乙基氯喹约占23%,尿液pH可影响其排泄速度,酸化加快而碱化降低[24]。
2.2 羟氯喹的药代动力学特征
2.2.1吸收 羟氯喹通常以口服片剂的形式服用,口服后可在2~4h内被完全吸收,通过胃肠道的吸收率为70%~80%[25]。
2.2.2分布 羟氯喹的血药浓度在达到峰值后因迅速分配到器官而相对快速下降[26]。其优先与白蛋白、血小板和白细胞结合,其中白蛋白结合比例约占50%;对肝脏、脾脏、皮肤和视网膜色素上皮具有高度亲和力[27]。以每日给药400 mg为例,羟氯喹血浆浓度需4~6个月达到稳态。
2.2.3代谢 羟氯喹的代谢主要在肝脏中进行,通过CYP3A4、CYP2C3等细胞色素酶驱动的脱烷基作用形成主要代谢产物脱乙基羟氯喹[28-29]。羟氯喹具有较长的消除半衰期(40~50 d)和较低的血液清除率(96 mL/min),这是由于其广泛的组织分布导致系统清除减少造成的[30-31]。
2.2.4排泄 羟氯喹的排泄主要发生在肾脏,占40%~50%,其余通过粪便和皮肤排泄[32]。
3 喹啉类生物碱药物的相互作用
3.1 氯喹的药物相互作用氯喹的代谢主要由细胞色素酶CYP2D6、CYP3A4、CYP2C8等亚型介导,故氯喹与上述酶亚型介导药物联用时可能导致血药浓度发生变化以致药物毒性增加[33-34]。可与氯喹发生相互作用的药物及其可能作用机制见表1。
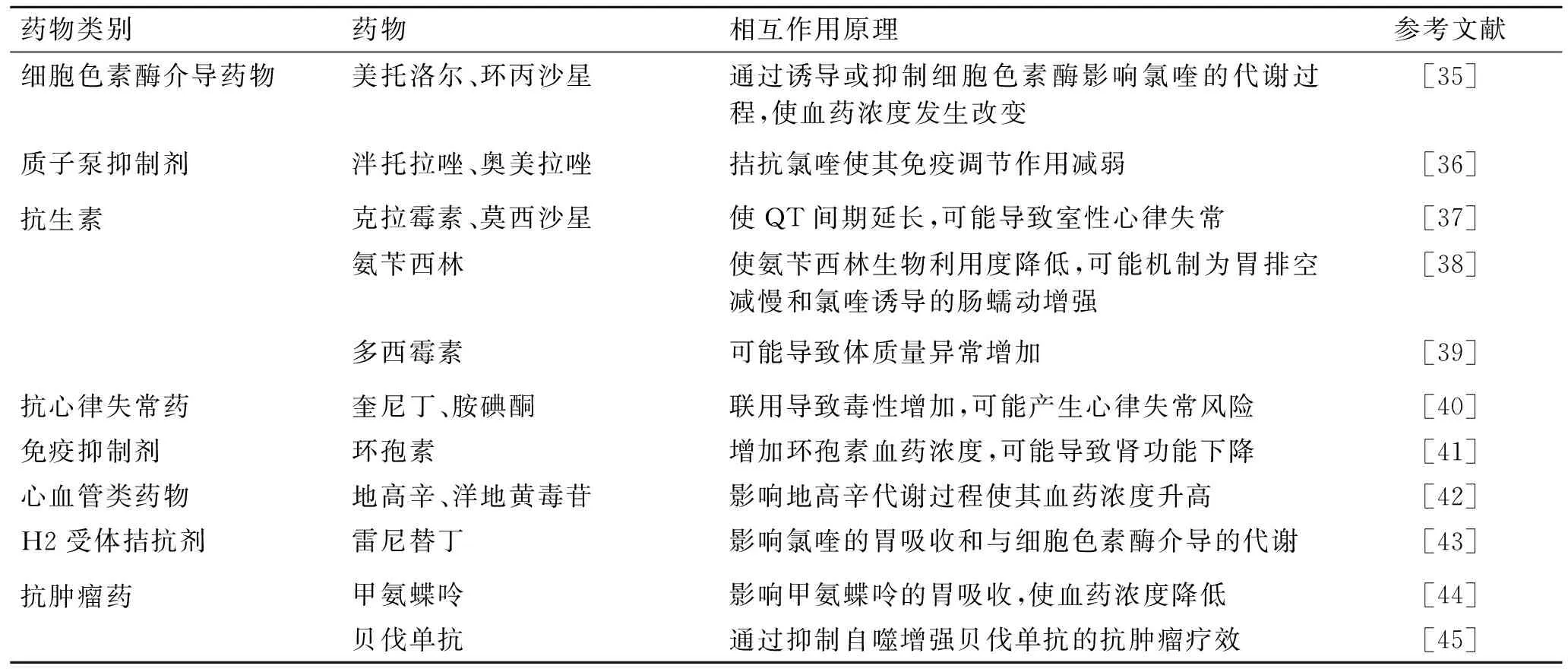
表1 氯喹的药物相互作用Tab.1 Drug interaction of chloroquine
3.2 羟氯喹的药物相互作用羟氯喹的代谢机制与氯喹相似,在肝脏中经CYP2D6、CYP3A4/5和CYP2C8等细胞色素酶介导[46]。可与羟氯喹发生相互作用的药物及其相互作用机制见表2。
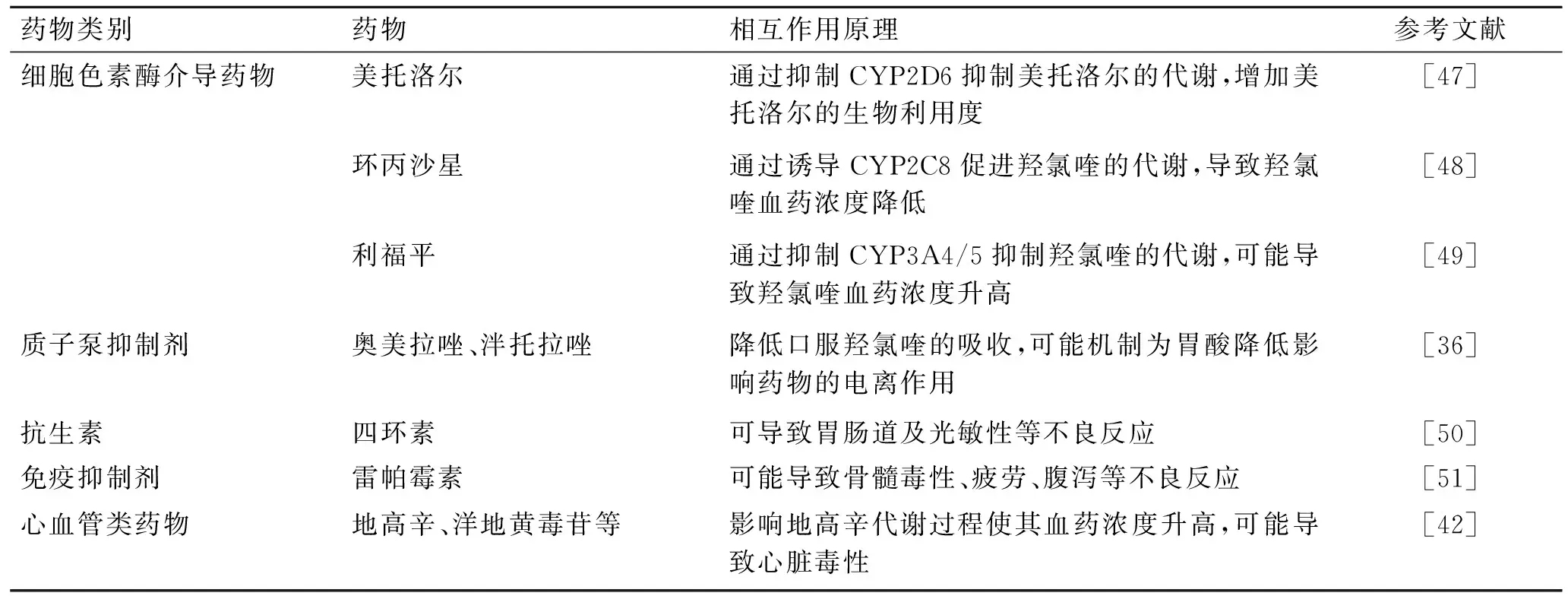
表2 羟氯喹的药物相互作用Tab.2 Drug interaction of hydroxychloroquine
3.3 喹啉类生物碱与新冠肺炎推荐药物的可能相互作用《新型冠状病毒肺炎诊疗方案(试行第七版)》中建议洛匹那韦/利托那韦可用于COVID-19的治疗,但利托那韦为细胞色素酶CYP3A4抑制剂,若与氯喹或羟氯喹联用,可能引起血药浓度升高,进而导致不良反应[17]。此外,诊疗方案推荐药物阿比多尔主要经CYP3A4代谢[52],与氯喹及羟氯喹联用可能引起代谢途径的竞争,从而导致血药浓度升高。
近日一项研究表明,联用阿奇霉素可增强羟氯喹治疗COVID-19的效果[2],而大环内脂类抗生素(如克拉霉素)具有使QT间期延长的副作用,与氯喹或羟氯喹联用可能导致室性心律失常[37]。阿奇霉素作为大环内酯类抗生素,与喹啉类生物碱联用时应进行严格的临床安全性试验,谨防药物相互作用导致的不良反应。
4 喹啉类生物碱药物的临床安全性
4.1 氯喹的临床安全性氯喹可致眼部、胃肠道、神经系统等不良反应,长期使用可能引起神经肌病和视网膜不可逆病变。氯喹可在血浆半衰期较长的深层隔室中累积,在肾脏或肝脏功能不全及高剂量下毒性增强[53]。氯喹与视网膜色素上皮中的黑色素有较强的结合,可导致黄斑中央凹外侧的黄斑锥受损,长期使用可能引起不可逆的感光细胞丢失和视网膜色素上皮萎缩[54]。分布在眼部的氯喹半衰期较长,即使在停药后2个月,其浓度也仅略有下降,应定期进行视网膜检查及密切注意药物剂量[55]。氯喹也较易与皮肤中的黑色素结合,出现色素沉着过度和光动力反应。此外,氯喹对妊娠期妇女有潜在的胎儿损失风险,如听力损伤、视网膜出血、流产等[56],也有少量氯喹可经乳汁排出,且氯喹对婴儿的安全性缺少临床证据,因此,妊娠期、哺乳期妇女应尽量避免服用氯喹。
4.2 羟氯喹的临床安全性羟氯喹的不良反应主要有头晕恶心、呕吐腹泻等,较之氯喹胃肠道及眼部不良反应发生率较低,程度较轻且通常可逆,可能原因是羟基限制了羟氯喹穿过血视网膜屏障的能力[57]。羟氯喹引起的视网膜毒性主要表现为中央凹区光感受器内段/外段连接和中央凹保留丢失,光谱域光学相干断层扫描显示视网膜外层早期变薄[58]。羟氯喹导致的视网膜病变不良反应发生风险尚无药物能有效消除,如果能充分认识到羟氯喹的毒性并在视网膜色素上皮受损之前采取措施,产生的不良反应将大大降低[59]。因此,一旦在羟氯喹的应用过程中识别出可能的视网膜病变迹象,应及时与患者沟通并决定是否停止用药,以控制眼毒性发生的风险[60]。
5 喹啉类生物碱与COVID-19候选药物的临床试验进展
截至2020年5月30日,已有25项氯喹或羟氯喹治疗COVID-19临床研究项目于“中国临床试验注册中心”平台注册[61]。在早期的COVID-19临床研究中,喹啉类生物碱的临床有效性存在争议,如2项分别在法国和中国上海开展的临床试验显示出了羟氯喹治疗COVID-19的不同结果[2,62],这一差异产生的原因可能是样本数量过小导致偏倚(法国36人,上海30人),同时也揭示了非随机、非双盲临床试验的局限之处。在一项近日发表的多中心前瞻性观察研究中,共197例患者完成了氯喹治疗,其中176例患者被列为历史对照,研究结果显示氯喹组患者病毒抑制的速度明显快于非氯喹组,且未观察到严重的不良反应事件,表明氯喹可以作为治疗COVID-19的有效药物[63]。
然而,其他几种备受关注的COVID-19候选药物临床进展不尽人意。近日有多项临床研究表明,洛匹那韦/利托那韦用于COVID-19治疗在改善临床症状、降低病毒载量等方面并无获益[64-65],且存在较高的不良反应发生率[66]。已上市抗流感药物法匹拉韦虽已显示出较洛匹那韦/利托那韦更短的SARS-CoV-2清除的时间[67],然而高尿酸血症和QT间期延长等严重不良反应使其临床应用存在安全隐患[68]。瑞德西韦作为早期在体外试验中已初步显示出抗SARS-CoV-2活性的未上市药物[69],在一项随机、双盲、安慰剂对照的多中心试验(n=237)中显示与临床获益无关[70],且有研究表明瑞德西韦的不良反应发生较为普遍,其导致的严重不良反应事件高转氨血症和急性肾损伤的发生率分别高达42.8%和22.8%[71]。
喹啉类药物在临床研究中展示出了更优的安全性,其引起的不良反应较上述3种药物少。磷酸氯喹治疗的不良反应发生率显著低于洛匹那韦/利托那韦联合治疗[66,72],且短期小剂量服用未见眼部和听力损害[65]。总体而言,喹啉类药物用于治疗COVID-19的耐受性良好,通过严格遵循药物的标准给药剂量并加强患者监测,可以避免严重不良反应的发生[73]。相比较其他3种目前投入临床研究的COVID-19候选药物,喹啉类药物具有更优的临床安全性和价廉易得的优势,更有望成为治疗COVID-19的理想药物。
6 喹啉类生物碱应用中的问题
6.1 临床治疗方案尚待优化氯喹与羟氯喹虽在体外试验与初步的临床试验中显示出了治疗COVID-19的良好效果,但其临床用药的具体治疗方案尚待进一步完善。《新型冠状病毒肺炎诊疗方案(试行第七版)》明确指出[17],磷酸氯喹的推荐治疗方案为每次500 mg,每日2次。既往临床试验表明,磷酸氯喹每日500 mg持续1周,此后每周500 mg共计12周的给药方案,可引起头晕恶心、视物模糊等不良反应,且发生1例可能与氯喹相关的肝炎严重不良反应事件[74]。有研究显示,高剂量、长期用药是羟氯喹毒性作用的主要风险因素[75],每日超过5.0 mg/kg体质量的剂量将使发生视网膜病变的概率增加5.7倍[76];而每日以800~1 000 mg接受羟氯喹的患者则在1~2年内有高达25%~40%视网膜发生病变和产生损伤迹象[77-78]。
上述报道提示,尽管喹啉类生物碱氯喹、羟氯喹皆为临床应用多年的经典药物且目前临床研究已取得一定进展,但面对研究尚不充分、临床试验证据不足的新型疾病,仍应保持谨慎的态度。在得到确切可信的临床数据前,应进行严格的随机、双盲大样本临床试验以确定最佳治疗方案,使喹啉类生物碱的安全有效性在COVID-19的治疗中得以保障。
6.2 光学对映体问题氯喹与羟氯喹均为手性药物,存在光学对映体。目前喹啉类生物碱在临床中的常用制剂形式主要为硫酸氯喹片与硫酸羟氯喹片,但药物采用外消旋混合物的形式,并未进行手性拆分。手性药物对映异构体的体内过程可能具有立体选择性和不同的作用机制,典型药物如沙利度胺[79]。有研究表明,氯喹和羟氯喹的对映体消除速率皆存在差异,可能存在立体选择性药代动力学效应[80-81]。虽然截至目前尚未见氯喹与羟氯喹光学异构体不同药理作用或不良反应的报道,但出于药物安全性考虑,其光学异构体的药物活性、药代动力学和毒性等性质是否存在差异是一个值得研究的问题。
氯喹和羟氯喹的异构体拆分方法主要有毛细管电泳法(CE)、高效液相色谱法(HPLC)等,其中毛细管电泳法因其操作简便、试剂用量少、分离效果好等优点,成为目前氯喹和羟氯喹对映体拆分的首选方法。
6.2.1毛细管电泳法(表3) MULLER等[82]采用毛细管电泳法结合激光诱导荧光检测方法 (CE-LIF) 测定血浆中的氯喹,以羟丙基-γ-环糊精(HP-γ-CD)为手性选择剂,可以10 min内实现基线分离。DICKOW等[83]采用羟丙基-β-环糊精(HP-β-CD) 和硫酸盐-β-环糊精(S-β-CD)为混合手性选择剂的毛细管电泳方法,可在125~2 000 ng/mL范围内对羟氯喹进行手性测定。ANDERSON等[84]采用S-β-CD、HP-γ-CD为手性选择剂、三羟甲基氨基甲烷缓冲液为电解质进行人尿液中羟氯喹及其代谢物的手性测定,该方法选择性强、灵敏度高,允许羟氯喹立体异构体在10~1 000 ng/mL范围内进行手性测定。DING等[85]以聚甲基丙烯酸缩水甘油酯-二甲基丙烯酸乙烯酯(GMA-co-EDMA)为载体,沸石咪唑酸酯-8(ZIF-8)为骨架,胃蛋白酶作为手性选择剂,制备得到胃蛋白酶-ZIF-8-聚(GMA-co-EDMA)柱对羟基氯喹(羟氯喹)成功将羟氯喹对映体分离。MA等[86]以聚甲基丙烯酸缩水甘油酯-co-二甲基丙烯酸乙烯酯 [Poly(GMA-co-EDMA)]为载体与纳米金(AuNP)结合,以胃蛋白酶作为手性选择剂制得胃蛋白酶-AuNP-聚(GMA-co-EDMA)柱,实验结果显示,氯喹与羟氯喹分辨率较以往报道均有明显提高。

表3 毛细管电泳法分离氯喹和羟氯喹Tab.3 Separation of chloroquine and hydroxychloroquine by CE
6.2.2高效液相色谱法(表4) CARDOSO等[87]使用HPLC-UV法对氯喹对映体进行分离,采用Chirobiotic V色谱柱和Chiralpak-ID多糖手性色谱柱获得了较好的分离效果。STALCUP等[88]采用肝素作为HPLC的固定相手性配体对氯喹进行分离,实验结果表明(-)型氯喹与肝素的结合力较强,后被从色谱柱上洗脱从而达到分离的目的。MORAES等[89]采用两种多糖手性色谱柱对羟氯喹进行分离,一种是基于纤维素的3, 5-二甲基苯氨基甲酸酯衍生物(Chiralcel OD-H),另一种是基于直链淀粉衍生物(Chiralpak AD-RH),皆可在50~1 000 mL范围内对羟氯喹实现手性测定,且操作简便,选择性强。

表4 高效液相色谱法分离氯喹和羟氯喹Tab.4 Separation of chloroquine and hydroxychloroquine by HPLC
7 结 论
近来,随着喹啉类生物碱临床研究的不断深入,已有研究结果表明氯喹、羟氯喹具有良好的治疗COVID-19前景。作为临床应用数十年的经典抗疟药,氯喹与羟氯喹药代动力学、药物相互作用及不良反应等性质经过长期的研究与验证,相比其他可能具有抗SARS-CoV-2活性的未批准药物,喹啉类药物具有临床安全性好、价廉易得等优势。然而,作为治疗COVID-19的候选药物,喹啉类生物碱的研究尚处初期阶段,在实际的临床应用中可能存在一些问题:①抗SARS-CoV-2作用机制尚未研究透彻;②现行治疗剂量与毒性剂量之间的界限狭窄,可能导致不良反应的发生;③手性对映体在治疗中可能的药理作用、药代动力学等性质差异尚不明确。尽管喹啉类药物已在体外试验中被证实具有良好的抗SARS-CoV-2活性,并在初步的临床研究中显示出了优于其他候选药物的有效性和安全性,但目前其临床试验证据尚不充分,仍应保持谨慎的态度进行严格的随机、双盲大样本临床试验。未来在获得喹啉类药物治疗COVID-19的高质量临床数据基础上,应对轻度、中度和重度患者采取有针对性的治疗方案,并充分考虑需服用心血管、降血糖等药物的患者同时服用喹啉类药物的临床用药安全性。此外,因羟氯喹相比氯喹不良反应的发生率更低,应开展二者之间的临床比较试验,以期为喹啉类生物碱治疗COVID-19的临床应用提供参考。
