番木瓜干旱胁迫相关CpDHN1基因的克隆与分析
2021-01-13郭静远邹智孔华贺萍萍郭安平
郭静远 邹智 孔华 贺萍萍 郭安平


摘 要:番木瓜(Carica papaya L.)隶属于番木瓜科番木瓜属,是一种营养价值高的热带果树,广泛种植于热带和亚热带地区。作为全年结果的典型热带作物,番木瓜易受寒害、旱害等非生物胁迫的影响。然而,目前有关番木瓜的抗逆研究主要集中于导致绝产的病毒病,鲜见针对非生物胁迫的报道。脱水素又名第二类胚胎发育晚期丰富蛋白,属于亲水性高、富含甘氨酸、复杂度低的非结构蛋白,因其与生物的抗逆性密切相关而受到广泛关注。为解决番木瓜生产在地域上的局限性,并进一步提高其品质和产量,积极筛选和鉴定参与非生物胁迫响应的关键基因具有重要的理论意义和应用价值。本研究基于转录组获得的CpDHN1转录本序列,以‘台农二号’番木瓜组培苗叶片为材料,提取总RNA进行反转录,结合RT-PCR技术克隆了该基因636 bp的全长编码区序列,在此基础上对其进行序列、表达特性以及原核表达分析。结果显示,CpDHN1编码211个氨基酸,其理论分子量为24.09 kDa,等电点为5.05,总平均疏水指数为–1.584,不稳定系数为66.51,属于不稳定、高度亲水的细胞核定位蛋白。CpDHN1蛋白富含谷氨酸、赖氨酸和丝氨酸,含有3个保守区域,即2个K片段和1个S片段,符合脱水素蛋白的基本结构特征,属于SKn型脱水素。生物信息学分析表明CpDHN1无跨膜螺旋,其二级结构中以α-螺旋结构占主导。表达分析显示,该基因在根、叶片和韧皮部树液中均有表达,且其表达水平受干旱胁迫调控。同源分析表明,CpDHN1与拟南芥AtLEA4序列相似性最高,为46.8%,而与番木瓜中已报导的另一个脱水素CpDHN的相似性仅为19.4%。研究还构建了CpDHN1的原核表达载体,根据SDS-PAGE结果,CpDHN1在40 kDa处有条中强度的诱导条带,而在55 kDa处有条高亮的诱导条带,可能与其无规结构有关。这些结果为进一步的功能分析与应用奠定了坚实的基础。
关键词:番木瓜;胚胎发育晚期丰富蛋白;脱水素;干旱胁迫;原核表达
中图分類号:S667.9 文献标识码:A
Abstract: Papaya (Carica papaya L.), which belongs to the Carica genus within the Caricaceae family, is a popular tropical fruit with high nutritional value that are widely cultivated in tropical and subtropical areas. As a typical tropical crop that fruits through the whole year, papaya is vulnerable to abiotic stresses such as cold and drought. Presently, there are few reports on stress resistance of papaya, and main studies focus on the virus disease which leads to the extinction of papaya production. Dehydrin, also known as type two late embryogenesis abundant protein, is a class of natural non-structural proteins with high hydrophilicity, rich in glycine, and low complexity. It has attracted extensive attention because it is highly related to the ability of plants to resist abiotic stresses. In order to solve the regional limitation of papaya cultivatation and further improve the fruit quality and yield, it is of importance to screen and characterize key genes involved in abiotic stress response. Based on a de novo assembled transcript, a 636 bp open reading frame of a gene that was denoted as CpDHN1 was isolated from the leaf tissue of cultivar ‘Tainong No. 2’ using RT-PCR. Bioinformatic analysis showed that CpDHN1 putatively encodes 211 amino acids, which was predicted to target the nuclear and have a theoretical molecular weight (Mw) of 24.09 kDa, an isolectric point (pI) of 5.05, a GRAVY value of –1.584, and an instability index of 66.51, implying its unstable, hydrophilic, and nuclear-targeted characteristics. CpDHN1 is rich in glutamate, lysine and serine, and it can be categorized as the SKn-type dehydrin with two conserved K-segments and one S-segment. CpDHN1 doesn’t contain any transmembrane helix and its secondary structure is mainly composed of α-helixes. Homology analysis showed that CpDHN1 shares the highest sequence similarity with AtLEA4 (i.e. 46.8%), while the sequence similarity with another reported dehydrin (i.e. CpDHN) is just 19.4%. Expression analysis revealed that CpDHN1 was expressed in all tested tissues, i.e. root, leaf, and sap, and the transcript level was significantly regulated by drought stress. Moreover, its prokaryotic expression vector was also successfully constructed, and SDS-PAGE showed that CpDHN1 could efficiently accumulate in Escherichia coli. It accumulated a small amount at the theoretical molecular weight of 40 kDa, but a large amount at 55 kDa, supporting that CpDHN1 is an intrinsically unstructured protein. These results lay a solid foundation for further functional analysis and utilization of this special gene in papaya and other species.
Keywords: papaya; late embryogenesis abundant; dehydratin; drought stress; prokaryotic expression
DOI: 10.3969/j.issn.1000-2561.2021.12.015
番木瓜(Carica papaya L.)隶属于双子叶植物纲番木瓜科番木瓜属,是一种广泛种植于热带和亚热带地区的特色果树。番木瓜果实营养丰富、肉质甜美,受到越来越多人的青睐。然而,作为典型的热带作物,番木瓜极易遭受寒害、旱害等非生物胁迫的影响[1]。寒害是番木瓜生长和生产上的一个严重问题,番木瓜是的最适生长温度为21 ℃~33 ℃,生长主要集中在温度较高的初夏到初秋时期,在这一时期番木瓜植株的株高、茎围、叶、根、花和果实等的生长迅速增加,每周平均长出2.5片新叶,而到了寒冷的冬天,番木瓜的生长速率减慢,株高、茎围和根系的生长几乎不再增加,叶的平均寿命在这个时期最短[2]。番木瓜植物被认为是相对抗旱的物种,它能通过干燥延迟机制来响应干旱胁迫[3]。在干旱胁迫下体内大量累积的K+、Na+、Cl−以及脯氨酸也有助于番木瓜的渗透调节[4]。但是,由于番木瓜叶面积大、根系分布浅且又是全年结果,在生产中特别是在坡地栽培条件下易发生干旱而影响植株生长和果实品质与产量。在我国,番木瓜主要分布于华南地区如海南、广东、广西和福建,此外,在云南和四川也有少量种植。这些地方,在不同程度上受到低溫和干旱胁迫的影响,影响番木瓜的品质及产量。如2008年冬季番木瓜种植地广西南宁受阴冷型灾害天气影响,连续33 d平均温度为7.2 ℃,导致番木瓜幼苗严重受害[5]。因此,开展番木瓜逆境生物学研究及相关分子育种具有重要理论意义和应用价值。
脱水素(dehydrin, DHN),又名第二类胚胎发育晚期丰富蛋白(late embryogenesis abundant, LEA),最早发现于20世纪80年代[6]。因其与植物抵御非生物胁迫的能力高度相关而受到广泛关注,是目前研究较多的一类LEA蛋白[7]。DHN是一种小分子蛋白,一般由82~575个氨基酸构成,分子量为9~200 kDa,富含甘氨酸和赖氨酸,缺乏半胱氨酸和色氨酸,具有高度的亲水性[8]。DHN包含3类高度保守的基序,即K、S和Y片段。根据这3类基序的存在与分布顺序,脱水素可以分为YnSK2、Kn、SKn、KnS和Y2Kn等5种类型[9]。研究表明,DHN基因与生物的抗逆性密切相关,当植物遭受低温、干旱和盐害等逆境条件胁迫时,DHN在细胞中表达上调[10]。过量表达DHN类基因可以提高拟南芥、水稻、烟草、草莓、酵母和大肠杆菌等的抗寒、抗旱或耐盐能力[11-14]。
研究组前期报道了一个番木瓜脱水素基因CpDHN,该基因编码93个氨基酸,属于KS型脱水素;该基因的表达在根和叶片中均受干旱胁迫显著诱导[15]。本实验研究另一个不同类型的番木瓜脱水素基因CpDHN1的序列特征、表达特性及原核表达情况。
1 材料与方法
1.1 材料
本研究的植物材料为‘台农二号’番木瓜组培苗。番木瓜的基因组数据下载于Phytozome v12(https://phytozome.jgi.doe.gov/pz/portal.html),转录组数据下载于NCBI SRA数据库(https://www. ncbi. nlm.nih.gov/sra/)。
植物总RNA取试剂盒TransZolTM Plant购自北京全式金生物技术有限公司,反转录试剂盒Takara PrimeScript™ RT reagent Kit with gDNA Eraser 购自宝日医生物技术(北京)有限公司,质粒提取试剂盒Plasmid DNAMini KitⅠ购自Omega Bio-Tek公司。胶回收试剂盒Gel Extraction Kit购自Omega Bio-Tek公司,高保真酶Takara PrimerSTAR MaxDNA Polymerase购自宝日医生物技术(北京)有限公司,限制性内切酶均购自美国New England Biolabs(NEB)公司,重组克隆试剂盒ClonExpress II One Step Cloning Kit(C112-02)购自诺唯赞公司,其余试剂均为国产分析纯。各对引物由生工生物工程(上海)股份有限公司合成。
1.2 方法
1.2.1 CpDHN1基因克隆 以提取番木瓜总RNA反转录得到的cDNA为模板,以研究组从头组装的转录组获得CpDHN1的转录本序列设计该基因5'和3' UTR引物对(CpDHN1F:5'-ATTGAT CTTCGTTCGGAGTTT-3'和CpDHN1R:5'-ATC CCACAAGGAAGGAAACAG-3'),以及在开放读码框(ORF)的两侧设计包含可以跟pET-32a(+)载体进行同源重组同源臂的引物对(CpDHN1HF:5'-ACCGACGACGACGACAAGATGGCTGAACACCACGAGAGC-3'和CpDHN1HR:5'-GCAGCCG GATCTCAGTGGTTAATCTGACGTCTCTTTCTT-3'),参照文献[15]进行基因的克隆、测序并构建pET-32a(+)-CpDHN1原核表达载体。
1.2.2 CpDHN1基因序列分析 对CpDHN1基因的ORF进行分析并翻译成蛋白质,对CpDHN1编码蛋白的理化性质、亲水性/疏水性、进行分析预测、跨膜结构以及二级结构进行分析预测,将CpDHN1蛋白与已知的部分脱水素进行多序列比对并绘制进化树。
1.2.3 CpDHN1基因的表达特性分析 参照文献[16],利用转录组数据(SAMN09096786)分析基因在根、叶片和韧皮部树液中的表达模式及其对干旱胁迫的响应模式,植株为3月龄的种子苗,以正常浇水的作为对照,断水10 d和20 d分别定义为轻度和重度干旱胁迫,每个处理设置2个生物学重复。
1.2.4 CpDHN1基因在大肠杆菌BL21中的表达 将重组质粒pET-32a(+)-CpDHN1和对照质粒pET-32a(+)分别转化大肠杆菌菌株BL21,分别命名为BL-CpDHN1和BL-pET32a。挑取菌落PCR正确的单克隆于LB液体培养基中培养过夜,分别吸取100 µL过夜培养的菌液于10 mL含有相应抗生素的LB液体培养基中,于37 ℃、250 r/min摇床培养1~2 h,至OD600为0.6,加入IPTG至终浓度为0.8 mmol/L,于37 ℃、250 r/min摇床诱导培养4 h,细胞裂解后离心,取上清进行SDS- PAGE分析。
2 结果与分析
2.1 CpDHN1基因克隆
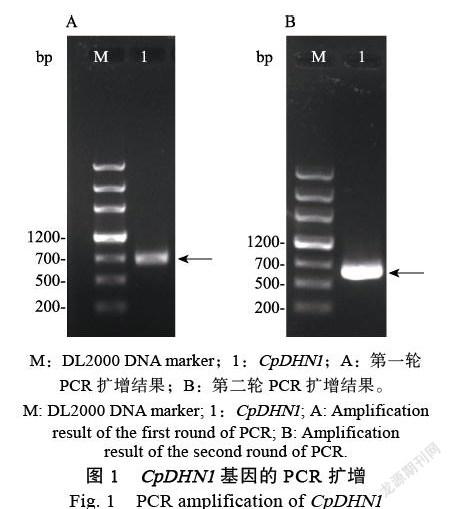
以CpDHN1F/R为引物、番木瓜叶片反转录的cDNA作为模板进行PCR扩增,成功扩增到1条约700 bp的特异条带(图1)。然后,以第一轮PCR产物作为模板、以CpDHN1HF/R作为引物进行第二轮PCR,成功扩增到1条约600 bp的清亮条带(图1),与预期片段大小相符。目标片段切胶回收后采用同源重组的方法克隆到pET-32a(+),筛选单克隆进行测序分析。
2.2 序列分析
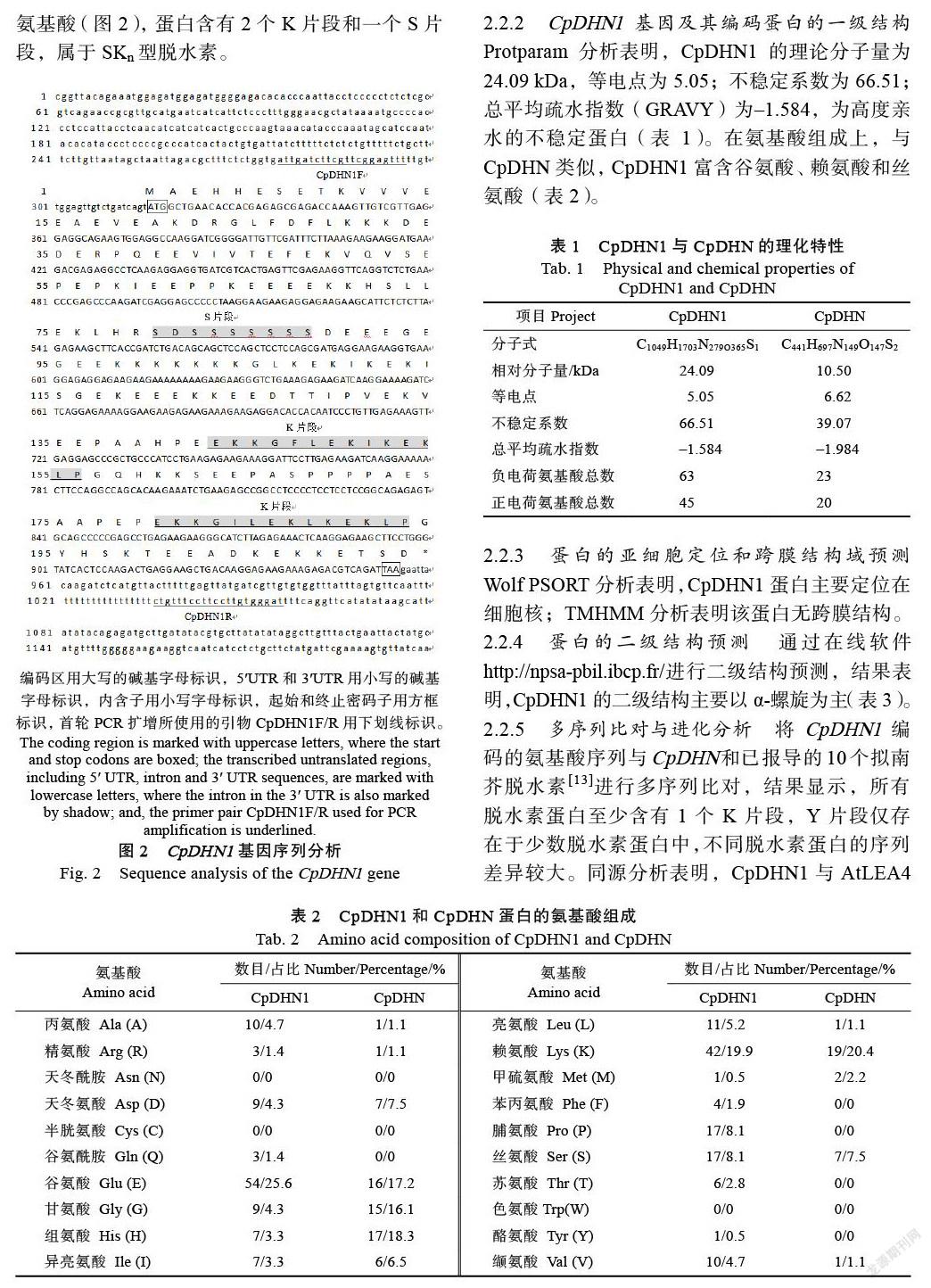
2.2.1 CpDHN1基因的序列分析 测序结果表明,研究分离到的cDNA与基因和转录本的对应区域完全一致,ORF为636 bp,预测编码211个氨基酸(图2),蛋白含有2个K片段和一个S片段,属于SKn型脱水素。
2.2.2 CpDHN1基因及其编码蛋白的一级结构 Protparam分析表明,CpDHN1的理论分子量为24.09 kDa,等电点为5.05;不稳定系数为66.51;总平均疏水指数(GRAVY)为–1.584,为高度亲水的不稳定蛋白(表1)。在氨基酸组成上,与CpDHN类似,CpDHN1富含谷氨酸、赖氨酸和丝氨酸(表2)。
2.2.3 蛋白的亚细胞定位和跨膜结构域预测 Wolf PSORT分析表明,CpDHN1蛋白主要定位在细胞核;TMHMM分析表明该蛋白无跨膜结构。
2.2.4 蛋白的二级结构预测 通过在线软件http://npsa-pbil.ibcp.fr/进行二级结构预测,结果表明,CpDHN1的二级结构主要以α-螺旋为主(表3)。
2.2.5 多序列比对与进化分析 将CpDHN1编码的氨基酸序列与CpDHN和已报导的10个拟南芥脱水素[13]进行多序列比对,结果显示,所有脱水素蛋白至少含有1个K片段,Y片段仅存在于少数脱水素蛋白中,不同脱水素蛋白的序列差异较大。同源分析表明,CpDHN1与AtLEA4(AT1G20440.1)序列相似性最高,为46.8%,与AtLEA45(AT4G39130.1)最低,为17.2%,而与CpDHN的序列相似性为19.4%(图3)。进一步的进化分析表明CpDHN1与拟南芥中同属于SKn型脱水素的AtLEA4、AtLEA5、AtLE10和AtLEA44聚为一类,CpDHN与拟南芥中同属于KnS型脱水素的AtLEA8聚为一类,这表明CpDHN1与CpDHN的亲缘关系较远(图4)。
2.3 CpDHN1基因的表达特性分析
表达分析显示,CpDHN1在根、叶片和韧皮部树液中均有表达,韧皮部树液中的表达丰度最高。随着干旱胁迫处理时间从10 d延长至20 d,该基因在根和韧皮部树液的表达水平均随处理时间的延长而逐步降低,而在叶片中的表达水平均随处理时间的延长而逐步上升(图5)。
2.4 CpDHN在原核细胞中的表达
为探讨CpDHN能否在原核细胞中进行高效表达,研究将重组质粒pET-32a(+)-CpDHN1和对照质粒pET-32a(+)分别转化大肠杆菌BL21,取1%过夜培养的菌液37 ℃、200 r/min培养至OD值为0.6后,用0.8 mmol/L IPTG诱导4 h,取裂解上清进行SDS-PAGE分析。结果显示,在对照BL-pET32a细胞的上清中检测到1条约20 kDa的特异性条带,此结果与pET-32a(+)载体中TrxA- intein融合蛋白的理论分子量为20.4 kDa相符,而CpDHN1在理论分子量40 kDa处观察到有少量蛋白被诱导,但在55 kDa处大量蛋白诱导表达(图6),暗示CpDHN1为固有无结构蛋白质(intrinsically unstructural protein, IUP),在SDS- PAGE实验中,IUPs与SDS结合较少,它们的表观分子量通常是真实分子量的1.2~1.8倍[17]。在拟南芥、玉米、大豆的LEA蛋白中,存在相似的报道[18]。
3 讨论
番木瓜作为热带及亚热带地区广泛栽培的重要经济果树,其研究主要集中于导致番木瓜绝产的病毒病,而鲜见非生物胁迫研究报道。脱水素属于典型的逆境诱导型基因,在干旱、低温、高盐等非生物逆境胁迫下其产物能维持植物细胞正常代谢以及细胞膜结构稳定性,具有重要的保护功能[19]。
本研究报道了一个新的番木瓜脱水素基因CpDHN1,该基因的编码区内无内含子,预测编码211个氨基酸。虽然其与先前报道的CpDHN的序列相似性仅为19.4%,但2个蛋白在序列特征和理化性质上任具有一定的相似性:分子量小,具有高度的亲水性,富含甘氨酸和赖氨酸,缺乏半胱氨酸和色氨酸,均含有2类高度保守的基序,即位于C末端的通常由15个高度保守的氨基酸残基(EKKGIMDKIKEKLPG)组成的K片段和主要由丝氨酸残基组成S片段。这两类基序与脱水素蛋白的功能密切相关,K片段存在于所有脱水蛋白中,含有丰富的赖氨酸,能形成脫水素的重要功能结构—双亲性的α-螺旋[20],通过疏水性作用与蛋白的变性位点相结合,防止蛋白变性,同时通过亲水性作用排斥变性蛋白,从而使变性蛋白自行恢复;S片段后常跟随有能与蛋白磷酸激酶结合的EDD或DDE位点,有研究表明S片段的磷酸化有助于脱水素在信号肽的引导下进入细胞核,并且还能增加蛋白的钙结合能力[21-23]。根据K片段和S片段基序的分布顺序,CpDHN属于KnS型脱水素,而CpDHN1属于SKn型脱水素[24]。脱水素的结构与其性质之间存在紧密的联系。KnS是一类酸性蛋白质,多含有1~3个K片段和1个S片段,主要由低温和干旱诱导;SKn是一类酸性蛋白质,多包含1个S片段和2~3个K片段,它们主要由低温诱导[25]。
脫水素提高植物抗逆能主要表现为对生物膜和蛋白质结构的稳定作用,从而降低逆境对植物细胞的伤害。其作用的分子机理目前尚不清楚,可能存在如下几种机制:与细胞膜结合,维持膜的稳定性和完整性;通过螯合作用起到保护细胞膜的作用,通过与水分子、糖类等结合,作为脱水保护剂,捕获更多的水分到细胞内,螯合各种金属离子、活性氧等,清除活性氧自由基,保护细胞免受胁迫伤害;具有维持或提高生物酶活性的功能;清除植物细胞中的活性氧自由基,从而降低低温、干旱等逆境导致的活性氧自由基增加而造成细胞膜系统的损伤[24]。
为进一步揭示CpDHN1的生物学功能,研究还构建了CpDHN1的原核表达载体。SDS-PAGE分析证实其蛋白可在大肠杆菌中高水平积累,但在40 kDa和55 kDa处存在2条特异性的谱带,这表明CpDHN1可能为固有无结构蛋白质。这类蛋白在生理条件下缺乏刚性折叠结构,结构松散,肽链呈无规卷曲构象,但却具有明确功能的蛋白质。在SDS-PAGE实验中,IUP与SDS结合较少,它们的表观分子量通常是真实分子量的1.2~1.8倍[16],与本研究结果相符。研究报道,拟南芥LEA基因ERD10、LEA1-Em6、LEA3-76和LEA4-D113的蛋白分子量(48、16、23、19 kDa)均大于其理论分子量(29.5、9.9、18.1、16 kDa),且将ERD10和LEA4-D113基因在大肠杆菌中过表达后,导致大肠杆菌的生长受到抑制,这种抑制作用依赖于蛋白质的离散区域[17]。至于CpDHN1在非生物胁迫中的分子机理及可能的功能还有待深入研究。
参考文献
[1] Beniwal V S, Sarina, Laura J. Drought and salt tolerance screening of papaya (Carica papaya L.) cultivars using in vitro techniques[J]. Acta Horticulturae, 2010, (851): 209- 212.
[2] Allan, P. Carica papaya response under cool subtropical growth conditions[J]. Acta Horticulturae, 2002, 575(575): 757-763.
[3] Jalel M, Ana R S, Manuel T. Responses of papaya seedlings (Carica papaya L.) to water stress and re-hydration: growth, photosynthesis and mineral nutrient imbalance[J]. Plant & soil, 2006, 281(1-2): 137-146.
[4] Jalel M, Vicent A, Aurelio G. Hormonal changes in papaya seedlings subjected to progressive water stress and re-watering[J]. Plant Growth Regulation, 2007, 53(1): 43-51.
[5] 钟思强, 黄党源, 刘任业, 等. 2008年香蕉、番木瓜寒害状况及灾后恢复[J]. 广西农业职业技术学院学报, 2009, 2(1): 1-4.
[6] Bray E A. Molecular responses to water deficit[J]. Plant Physiology, 1993, 103(4): 1035-1040.
[7] Kosová K, Vítámvás P, Prášil I T. The role of dehydrins in plant response to cold[J]. Biologia Plantarum, 2007, 51(4): 601-617.
[8] Kim E C, Lee H S, Choi D. Sequence variability and expression pattern of the dehydrin gene family in Populus alba × P. tremula var. glandulosa[J]. Plant Omics, 2012, 5(2): 122- 127.
[9] Close T J. Dehydrins: emergence of a biochemical role of a family of plant dehydration proteins[J]. Physiologia Planta-rum, 1996, 97(4): 795-803.
[10] Hara M, Fujinaga M, Kuboi T. Radical scavenging activity and oxidative modification of citrus dehydrin[J]. Plant Phy-siology and Biochemistry, 2004, 42(7-8): 657-662.
[11] Puhakainen T, Hess M W, Pirjo M, et al. Overexpression of multiple dehydrin genes enhances tolerance to freezing stress in Arabidopsis[J]. Plant Molecular Biology, 2004, 54(5): 743-753.
[12] Houde M, Dallaire S, Dong D, et al.. Overexpression of the acidic dehydrin WCOR410 improves freezing tolerance in transgenic strawberry leaves[J]. Plant Biotechnology Journal, 2010, 2(5): 381-387.
[13] Kaye C. Characterization of a gene for spinach CAP160 and expression of two spinach cold-acclimation proteins in to-bacco[J]. Plant Physiology, 1998, 116(4): 1367-1377.
[14] Park S Y, Noh K J, Yoo J H, et al. Rapid upregulation of Dehyrin3 and Dehydrin4 in response to dehydration is a characteristic of drought-tolerant genotypes in barley[J]. Journal of Plant Biology, 2006, 49(6): 455-462.
[15] 郭静远, 邹 智, 孔 华, 等. 番木瓜干旱胁迫相关CpDHN基因的克隆与原核表达[J]. 热带作物学报, 2020, 41(12): 2406-2412.
[16] Zou Z, Gong J, An F, et al.. Genome-wide identification of rubber tree (Hevea brasiliensis Muell. Arg.) aquaporin genes and their response to ethephon stimulation in the laticifer, a rubber-producing tissue[J]. BMC Genomics, 2015, 16: 1001.
[17] Tompa P. Intrinsically unstructured proteins[J]. Trends in Biochemical sciences, 2002, 27(10):527-533.
[18] Campos F, Zamudio F, Covarrubias A A. Two different late embryogenesis abundant proteins from Arabidopsis thaliana contain specific domains that inhibit Escherichia coli growth[J]. Biochemical & Biophysical Research Communications, 2006, 342(2): 406-413.
[19] 马 慧, 孙 檬, 安亭亭, 等. 脱水素的分布、结构和功能[J]. 分子植物育种, 2015, 13(7): 1668-1672.
[20] Baker J, Dennsteele C V, Dure L. Sequence and characteri-zation of 6 LEA proteins and their genes from cotton[J]. Plant Molecular Biology, 1988, 11(3): 277-291.
[21] Alsheikh M K, Heyen B J, Randall S K. Ion binding proper-ties of the dehydrin ERD14 are dependent upon phosphorylation[J]. Journal of Biological Chemistry, 2003, 278(42): 40882-40889.
[22] Riera M, Figueras M, Lopez C,et al.. Protein kinase CK2 modulates developmental functions of the abscisic acid res-ponsive protein Rab17 from maize[J]. Proceedings of the National Academy of Sciences of the United States of America, 2004, 101(26): 9879-9884.
[23] Jensen A B, Goday A, Mercè Figueras. Phosphorylation mediates the nucLEAr targeting of the maize Rab17 pro-tein[J]. Plant Journal, 1998, 13(5): 691-697.
[24] 孫 歆, 雷 韬, 袁 澍, 等. 脱水素研究进展[J]. 武汉植物学研究, 2005, (3): 299-304.
[25] Richard S, Marie-Josée Morency, Drevet C. Isolation and characterization of a dehydrin gene from white spruce in-duced upon wounding, drought and cold stresses[J]. Plant Molecular Biology, 2000, 43(1): 1-10.
责任编辑:沈德发
