仿真技术辅助于聚烯烃反应教学的实验案例
2021-01-12于淑媛张亚曼赵云杰李童谱陈晓钰张成根
于淑媛,张亚曼,赵云杰,李童谱,陈晓钰,任 萍,张成根
(廊坊师范学院,河北 廊坊 065000)
0 引言
对于化学专业的学生来讲,完成实验教学环节是学生熟悉、巩固和掌握理论知识的重要手段。通过对实验的预习、完成实验的过程以及对数据结果的处理,可以更好地理解知识,锻炼动手能力。但是有一些实验项目在实验室完成操作环节存在很大的难度,如:聚烯烃的催化反应,该反应机理是高分子化学课程中的重要内容,是教学重点也是难点,聚合时烯类单体首先在过渡金属引发剂活性中心上进行配位、活化,随后单体分子相继插入进行链增长的过程。完成此类实验反应需要无水、无氧、高真空的条件,操作时有一定的危险性,不适宜实验室开设。
为了解决该问题,采用计算机仿真模拟技术[1-2],使学生在安全的环境下,使用仿真模拟技术完成该实验。笔者从2017 年开始使用高斯软件开设聚烯烃反应机理仿真模拟化学实验,并在教学中使用,效果良好。学生在进行该模拟实验的过程中可以直观清晰地学习理论知识,更好地理解聚烯烃反应机理,同时掌握计算机仿真模拟高斯(Gaussian)[3]软件的使用。
1 实验目的
(1)使学生了解烯烃聚合Cossee机理[4],认识金属催化剂介导的烯烃配位聚合机理,体会计算化学在化学研究中的重要性。
(2)使学生加深对课堂知识的理解程度,掌握如何从众多计算结果中选择、记录、整理以及分析数据,培养学生创新能力和应用型技能。
2 实验原理
聚烯烃具有密度小、耐腐蚀性、常温下良好的抗冲击性、可重复利用等特点,在材料、包装、电子、汽车以及医疗等方面有广泛应用[5-6]。烯烃聚合反应及其反应机理的研究对聚烯烃的应用发展具有重要的推动作用。本文通过模拟催化烯烃聚合反应机理,加深学生对聚烯烃反应机理的理解。
3 仿真模拟方法
本实验使用计算软件Gaussian09 和GaussView进行研究,采用密度泛函方法(DFT)[7]研究在不同类型催化剂催化下乙烯插入步骤以及其插入原理的异同。在B3LYP/LANL2DZ[7]水平上优化了反应中的驻点,包括反应物、产物、中间体和过渡态等的构型。
4 结果与讨论
4.1 二氯型催化剂的构型
选择了一种茂金属催化剂Me2Si(Cp)2TiCl2(ACl2)和一种非茂金属催化剂{ƞ2-1-[C(H) =N(2,6-diflfluorophenyl)]-2-O-3-tBu-C6H3}2TiCl2(BCl2),两种催化剂均以金属钛Ti为中心原子,他们在乙烯聚合反应中均表现出高催化活性的特点。本次实验主要研究学习聚烯烃反应机理,比较乙烯在这两种催化剂聚合的插入步骤以及插入原理。
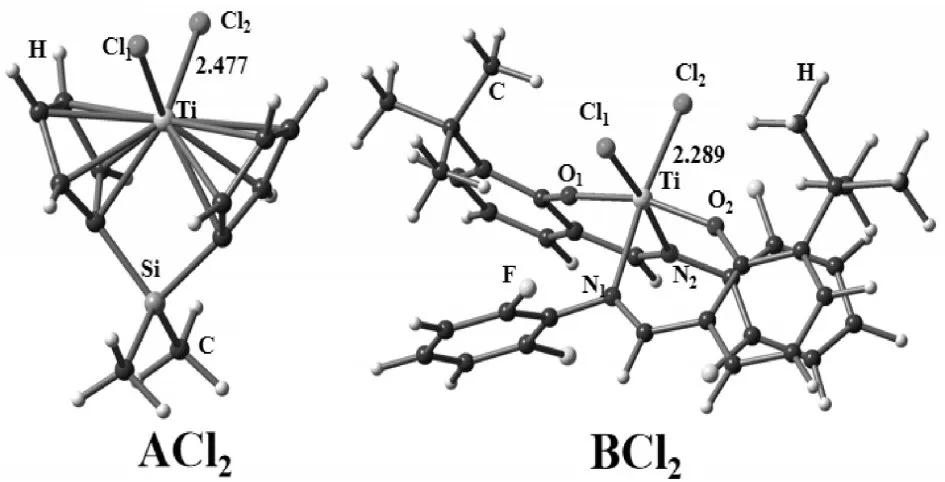
图1 二氯型催化剂ACl2和BCl2的优化构型,键长单位Å
图1中的二氯型催化剂,需要由诸如甲基铝氧烷之类的助催化剂激活,生成具有催化活性的阳离子催化剂物种来进行催化。活性催化剂是带正电性的,带有烷基或增长的高分子链。为了简单起见,下面文中用甲基来表示烷基,将阳离子活性中心指定为AMe+和BMe+,并将它们称为催化剂。因此,研究的反应实际上是乙烯插入AMe+和BMe+的C-Ti键。
4.2 乙烯在茂金属类催化剂中的插入
AMe+是典型的茂金属类,C2H4在AMe+的C-M键中的插入遵循Cossee 机理。乙烯在AMe+中的插入反应首先形成AMe+和C2H4之间的配合物AMe+_C2H4,再经过过渡态AMe+_TS,最后到达产物AMe+_PR。图2 给出了乙烯插入AMe+的能量分布,图3 给出了沿插入路径的驻点(阳离子催化剂,配合物,过渡态,产物)的优化结构。如图2 能量曲线所示,乙烯首先与AMe+的Ti 中心配位,形成比反应物能量低13.0kcal/mol 的AMe+_C2H4,说明它比反应物更稳定。如图3 所示,在AMe+_C2H4形成后,与乙烯插入到AMe+形成过渡态AMe+_TS。由图2 可知,在能量方面,过渡态AMe+_TS 比AMe++C2H4低8.8kcal/mol;同时与配合物AMe+_C2H4的能量相比,插入位垒为4.2 kcal/mol。产物AMe+_PR 的能量比反应物(AMe++C2H4)低26.0 kcal/mol。由以上结果可知插入过渡态较低(4.2 kcal/mol),放热较多(26.0 kcal/mol),所以ACl2对乙烯聚合反应具有较好的促进作用。
4.3 乙烯在非茂金属类催化剂中的插入
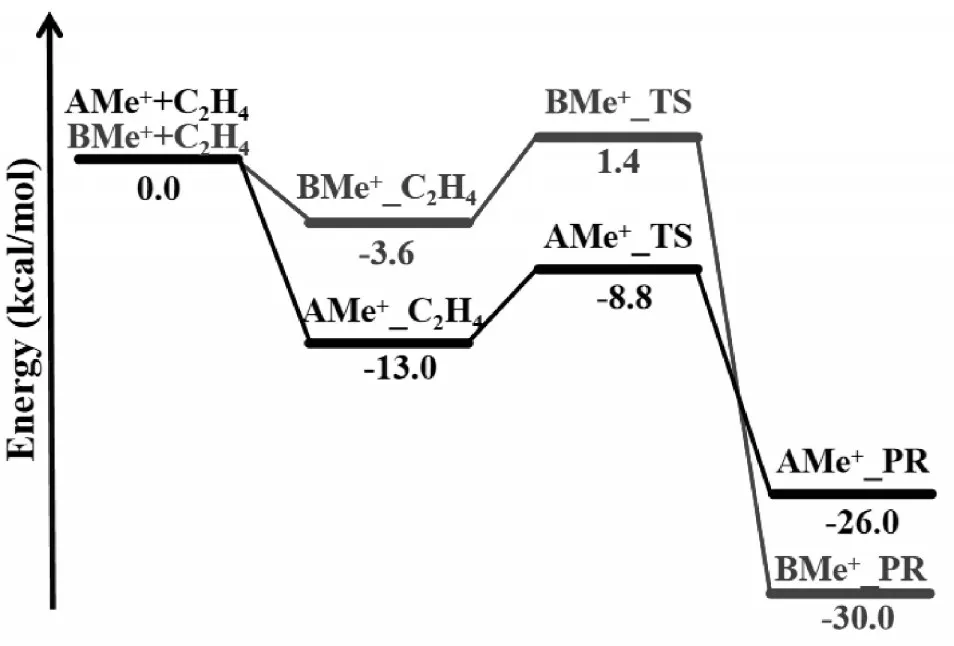
图2 乙烯插入AMe+和BMe+反应的能量曲线(kcal/mol)
乙烯插入非茂金属类(BMe+)的机理与插入茂金属类AMe+的机理相似,但能量不同。图2 比较了乙烯插入到BMe+和插入AMe+的能量分布。虽然在过渡态BMe+_TS 之前存在一个能量最小值(BMe+_C2H4),但与茂金属催化剂AMe+_C2H4中的-13.0 kcal/mol 相比较,最小值仅比反应物低-3.6 kcal/mol。如图3 所示,在BMe+_C2H4形成后,BMe+进行插入形成过渡态BMe+_TS。与对应反应物(BMe++C2H4)相比,过渡态BMe+_TS 的能量为1.4 kcal/mol,而茂金属催化剂AMe+_TS 的能量低得多,为-8.8 kcal/mol。结果分析表明:茂金属催化剂产生的活性阳离子催化剂更易于被乙烯攻击配位,从而形成稳定的配位络合物;与之相反,由于非茂金属催化剂产生的活性阳离子催化剂具有更多的空间位阻,形成配位络合物。非茂金属催化剂形成产物BMe+_PR 时的放热量为-30.0 kcal/mol。能量结果同样表明,BCl2对乙烯聚合也有促进作用。
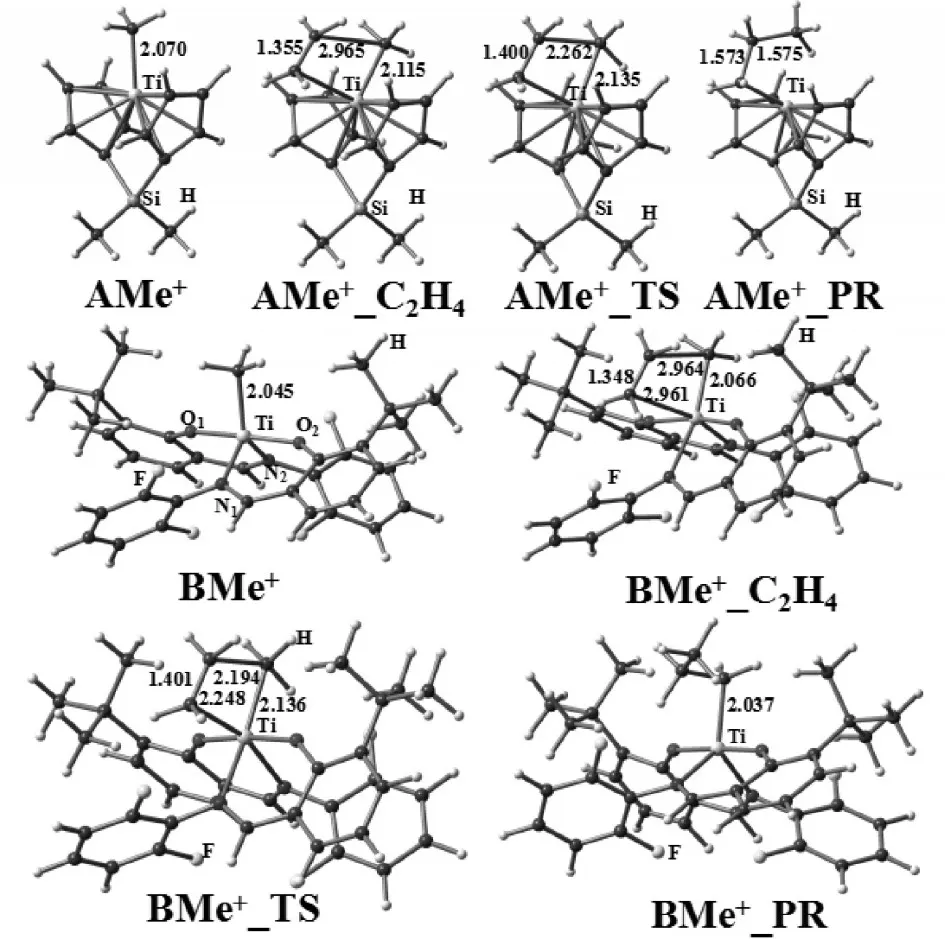
图3 反应过程中主要的优化构型,键长单位Å
4.4 结论
本仿真实验模拟了聚烯烃反应机理,分别计算了乙烯在不同类型催化剂中的插入能量。C2H4在AMe+中的插入形成稳定的配合物,而在BMe+中的插入仅形成弱的配合物。乙烯C2H4在这两种催化剂的插入步骤相同,插入原理也都遵循Cossee机理。
5 结语
该仿真模拟实验不仅弥补了真实实验难以实施的不足,而且起到了帮助学生深刻理解课堂教学内容的作用,充分发挥了学生的积极性和创造性。经过该仿真模拟实验的开展与实践,学生能了解到高分子化学的前沿知识,对于以后培养应用型人才也有一定的益处。
