磁共振3D TOF-MRA和ZTE-MRA在脑血管成像的对比
2021-01-11宋宇晁迎九徐运军
宋宇,晁迎九,徐运军
1.安徽医科大学附属省立医院影像科,安徽合肥230001;2.中国科学技术大学附属第一医院神经外科,安徽合肥230036
前言
脑血管疾病是指脑血管阻塞或脑循环障碍,导致缺血性或出血性脑卒中的各种疾病,包括缺血或出血性脑血管病、动脉粥样硬化性疾病、高血压脑病、颅内动脉瘤等,在当前人群中发病率很高,约5%~10%[1-2]。颅内动脉瘤是高发的脑血管疾病之一,易破裂出血,存在极高的风险,目前临床常用的治疗手段包括支架辅助弹簧圈栓塞、动脉瘤夹闭术等[3]。颈内动脉虹吸部由于存在多个生理性弯曲,血管走行迂曲,是血管狭窄与动脉瘤的好发部位[4-5]。
数字减影血管造影(Digital Subtraction Angiography, DSA)是目前评价脑血管的金标准,但由于是导管血管造影,存在一定的神经系统并发症、对比剂过敏、X 线辐射等风险[6]。磁共振血管成像(Magnetic Resonance Angiography, MRA)无需注射对比剂,具有非创伤性、无辐射等优势,逐渐成为临床常规评估脑血管病变的手段之一。然而传统的三维时间飞跃法MRA(3D Time-of-Flight MRA,3D TOF-MRA)在一些情况下可能会造成血管内部分信号丢失,如血液流速较慢、因血管走行迂曲造成的湍流、血管栓塞术后的磁化率伪影等[7]。ZTE-MRA 成像将零回波时间技术(Zero Echo Time, ZTE)与伪连续动脉自旋标记技术(Pseudocontinuous Arterial Spin Labeling, PCASL)相融合,有效地避免血流速度、血流方向及磁化率伪影等的干扰[8]。本研究将ZTEMRA 成像与传统3D TOF-MRA 成像进行对比,探究ZTE-MRA 在脑血管成像上的应用,比较两种MRA成像技术在脑血管的成像质量。
1 材料与方法
1.1 一般资料
收集2019年3月至2020年1月于安徽医科大学附属省立医院放射科行3D TOF-MRA 及ZTE-MRA成像的患者31例,其中,男13例,女18例,年龄23~72岁;其中颅内动脉瘤5例,颅内动脉瘤介入栓塞术后4例,右侧大脑中动脉狭窄闭塞1 例,颅内血管畸形1例,其余患者脑血管未见明显异常。
1.2 MRI检查设备及扫描方法
采用美国GE Discovery MR750W 3.0T MR 扫描仪,8 通道头线圈。3D TOF-MRA 扫描参数:TR/TE 19/3.4,FOV 220 mm×220 mm,矩阵416×416,扫描层厚1.4 mm,翻转角20°,扫描时间为6 min 49 s。ZTEMRA 扫描参数:TR/TE 862.45/0.016,FOV 200 mm×200 mm,矩阵166×166,扫描层厚1.2 mm,翻转角3°,扫描时间为6 min 51 s。
1.3 图像处理
将所有数据传送至GE ADW 4.6 工作站,使用固有最大密度投影(MIP)、多平面重建(MPR)软件对原始图像进行后处理。
1.4 影像评估方法
1.4.1 主观评价分别由两名具有神经影像诊断工作经验的放射科医师,分别对3D TOF-MRA 及ZTEMRA成像的图像进行血管可视化及饱和伪影两方面的质量评分,首先对两名医师的评分结果进行Kappa一致性检验,后以两名医师商讨达成一致的评分作为最终评分。我们采用四分制[9]的评分标准进行主观评估,评分内容包括血管可视化及饱和伪影两方面,具体评分标准如下,①血管可视化:无法诊断或不可见,1 分;结构可见、有明显模糊或伪影、不能明确诊断,2 分;尚可诊断、轻微的模糊或伪影,3 分;可明确诊断、血管边界清晰,4分。②饱和伪影:重度信号丢失、无法诊断,1 分;中度信号丢失、诊断准确性降低,2 分;轻度信号丢失、不影响诊断,3 分;无明显饱和伪影,4分。
1.4.2 客观评价由两名医师在3D TOF-MRA 及ZTE-MRA 序列的原始图像上,使用专用工作站测量图像的信噪比(SNR)、对比噪声比(CNR)、对比度(C)。我们采用改良的SNR、CNR 及C 的计算方式[10],将感兴趣区(ROI,大小0.05~0.10 cm2)分别放置在颈内动脉虹吸部、动脉瘤瘤体、动脉瘤介入术后栓塞段,避开血管及脑脊液,以邻近均匀的脑组织作为背景组织(2.5 cm2)。取两名医师在各部位测量值的平均值作为最终值。按如下公式计算SNR、CNR、C:

其中,SIROI是指感兴趣区的信号强度,SITissue是指邻近脑组织的信号强度,SDTissue是指邻近脑组织(背景组织)信号强度的标准差。
1.5 统计学分析
采用SPSS 26.0软件对影像评估结果进行统计学分析。采用Kappa 检验评估两名放射科医生对图像质量评分的一致性。Kappa 值评判一致性强度的标准:<0.2 时为一致性较差,0.21~0.40 时为一致性一般,0.41~0.60时为一致性中等,0.61~0.80为一致性较强,0.81~1.00 为一致性很强。采用Wilcoxon 符号秩检验比较两种MRA 成像技术的质量评分,并采用配对样本t检验评价两组客观半定量资料的SNR、CNR及C。P<0.05为差异有统计学意义。
2 结果
2.1 图像质量主观评价
两名医师对两种MRA 技术的血管可视化及饱和伪影质量评分的Kappa 值如下:ZTE-MRA 分别为0.682、0.635,3D TOF-MRA 分别为0.705、0.785,均具有较强的一致性(Kappa>0.6),两名医师对两种MRA技术的质量评分中,血管可视化的评分差异无统计学意义(P>0.05),但在饱和伪影评分方面,ZTEMRA技术质量评分显著优于3DTOF-MRA技术(P<0.05),见表1。
表1 两种MRA技术主观评分比较结果(± s)Tab.1 Comparison of subjective scores between two MRA techniques(Mean±SD)
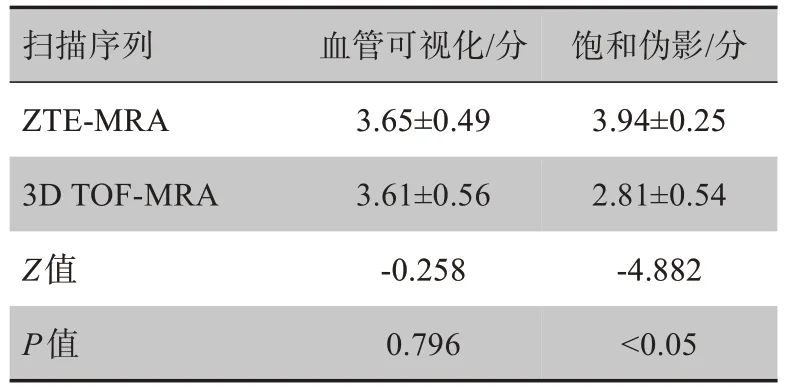
表1 两种MRA技术主观评分比较结果(± s)Tab.1 Comparison of subjective scores between two MRA techniques(Mean±SD)
扫描序列血管可视化/分饱和伪影/分ZTE-MRA 3D TOF-MRA Z值P值3.65±0.49 3.61±0.56-0.258 0.796 3.94±0.25 2.81±0.54-4.882<0.05
2.2 图像质量客观评价
ZTE-MRA 技术在颈内动脉虹吸部成像、动脉瘤瘤体处成像的SNR、CNR 及C 均高于3D TOF-MRA技术,在动脉瘤介入术后栓塞段成像的CNR 及C 均高于3D TOF-MRA 技术,且两者差异均具有统计学意义(P均<0.05),见表2。
3 讨论
根据世界卫生组织(WHO)发布的最新数据,脑血管疾病已经成为全球最大杀手之一,造成的死亡人数仅次于缺血性心脏病。早期、准确诊断脑血管疾病,具有重要的临床意义。颅内动脉瘤是较为常见的脑血管疾病,且易破裂出血,早期准确检出小动脉瘤能有效地降低破裂风险[11]。颈内动脉虹吸部是海绵窦段、膝段及前床突上段的合称,该部分血管走行迂曲,血流动力学复杂,好发动脉狭窄闭塞及动脉瘤等病变[4,12]。
表2 两种MRA技术图像客观评价指标对比(± s)Tab.2 Comparison of objective evaluation indexes between two MRA techniques(Mean±SD)
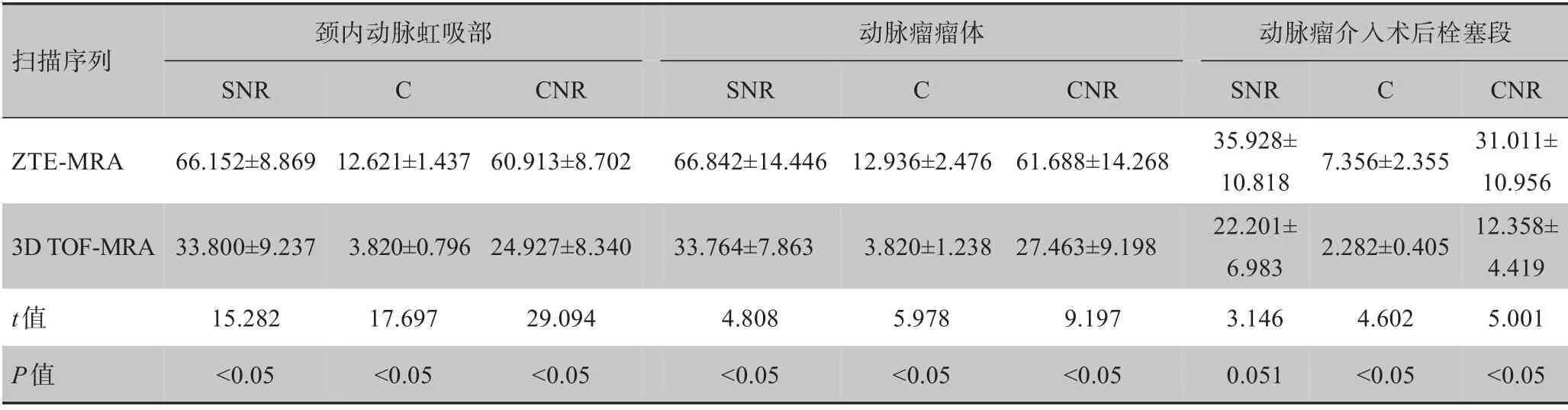
表2 两种MRA技术图像客观评价指标对比(± s)Tab.2 Comparison of objective evaluation indexes between two MRA techniques(Mean±SD)
SNR:信噪比;CNR:对比噪声比;C:对比度
扫描序列颈内动脉虹吸部SNR CNR 31.011±10.956 12.358±4.419 5.001<0.05 C CNR动脉瘤瘤体SNR C CNR C ZTE-MRA 66.152±8.869 12.621±1.437 60.913±8.702 66.842±14.446 12.936±2.476 61.688±14.268 7.356±2.355 3D TOF-MRA 33.800±9.237 3.820±0.796 24.927±8.340 33.764±7.863 3.820±1.238 27.463±9.198 2.282±0.405 t值P值15.282<0.05 17.697<0.05 29.094<0.05 4.808<0.05 5.978<0.05 9.197<0.05动脉瘤介入术后栓塞段SNR 35.928±10.818 22.201±6.983 3.146 0.051 4.602<0.05
临床工作中常用DSA、CT 血管造影(CT Angiography, CTA)和对比增强MRA(Contrast-Enhanced MRA, CE-MRA)等进行脑血管病变的评估,DSA 普遍被认为是金标准,CTA 及CE-MRA 也是常用手段,但上述方法均有一定的风险性,作为有创性检查,除存在创伤性的风险外,小部分对含钆或碘对比剂过敏者或有肾功能衰竭的患者无法进行相关检查。
TOF-MRA 成像无辐射、无创、无需对比剂,避免了穿刺、对比剂带来的不适和潜在的不良反应风险,成为脑血管成像的优势选择[13]。3D TOF-MRA 基于GRE 梯度回波序列中扰相T1WI序列,采用短TR 的重复射频激励脉冲,反复激发血管周围的背景,使静止的背景组织中的质子饱和,从而实现背景抑制,而当新鲜的血液流入成像容积时,未经上述射频激励脉冲饱和,血管显示出高信号,因而血管与背景组织形成了鲜明的高低信号对比[7]。3D TOF-MRA 成像的原理是假设血流的方向与成像层面相垂直,且血流处于平流的状态,因此对成像容积内血流方向、速度及血流状态的变化敏感度高。当血流速度降低时,在成像容积内停留时间较长,被射频脉冲反复激发,信号也随之减低。在血管狭窄、分叉等部位,血液由层流变成湍流状态,信号相位发散导致信号减低甚至丢失,从而夸大狭窄程度[14]。颈内动脉虹吸部血管走行曲折,血流方向变化多端,复杂的血流状态扰乱了磁场的均匀性,质子失相位而导致信号强度下降,因此在颈内动脉虹吸部成像时血管信号不均(图1)。
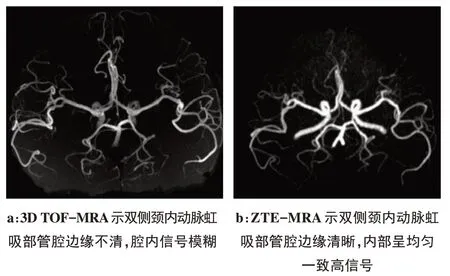
图1 颈内动脉虹吸部Fig.1 The siphon of the internal carotid artery
ZTE-MRA 结合了PCASL 动脉自旋标记技术与ZTE技术,是一种全新的MRA成像技术,又称静音血管成像技术Silent MRA。PCASL 动脉自旋标记成像以动脉血中的水质子为内源性标记物,无需外源性对比剂,通过减去标记前后扫描的图像而获得灌注图像,只包含标记的血流信号,对血流方向没有限制,有效地避开了TOF MRA 的慢血流饱和抑制效应,提高了慢血流的显像效果,对于严重狭窄、微动脉瘤和侧支血管的精准显像具有深远意义[15];且PCASL 通过对标记时间的控制,对动脉选择性成像,避免了静脉污染,背景抑制效果明显[16]。由于ZTEMRA 对磁场的不均匀性及血流状态的改变不敏感,可以在颈内动脉虹吸部狭窄或动脉瘤等血管病变中获得更均匀的血流信号[17]。
ZTE 技术的采集过程先将投影梯度设置为所需的方向和振幅,然后施加硬脉冲的射频激励,射频结束后立刻开始信号编码,从而达到零回波时间的效果。为了缩短总扫描时间,ZTE技术通常在磁化稳定状态下以较短的脉冲重复时间(TR)和较小的翻转角操作。ZTE 技术采用全新的微动式连续梯度编码技术,在连续射频激励之间仅对梯度幅度进行细微调整,实现最小的梯度变化,显著降低了扫描产生的噪声,同时改善了涡流效应。目前,ZTE 技术已经在脑血管、骨肌、腹部等部位的成像上得到了初步的研究及应用,证实了ZTE 成像在多个系统中的应用潜能[15-16,18-20]。
本次研究中,我们发现ZTE-MRA 技术在颈内动脉虹吸部成像效果较3D TOF-MRA 有着明显的优势,在3D TOF-MRA 序列上部分病例在血管弯曲段,尤其是在颈内动脉虹吸部,成像的血管边缘模糊、不连续,内部信号欠均匀,可见部分信号缺失(图1a);而在ZTE-MRA 序列所有病例的颈内动脉虹吸段均呈现均匀的高信号,且边缘清晰光整(图1b);但3D TOF-MRA 在其余血管平直部位的血管边缘显示更为清晰锐利,且对血管远端末梢小分支的显示比ZTE-MRA 更清晰,尤其是在血流速度较快的年轻人的脑血管;同时ZTE-MRA 成像的背景存在一定的颗粒感。此外,我们收集的5例颈内动脉虹吸部动脉瘤的成像中,较3D TOF-MRA,ZTE-MRA 成像显示的瘤体更清晰,内部信号也更均匀(图2a~2b)。同时,在4例动脉瘤介入术后栓塞段后病人的影像中,ZTEMRA 较3D TOF-MRA 显示的磁化率伪影更少(图3a~3c),从而更清晰准确地显示载瘤血管结构和评估栓塞治疗效果,这与之前Shang等[16]研究结果一致。
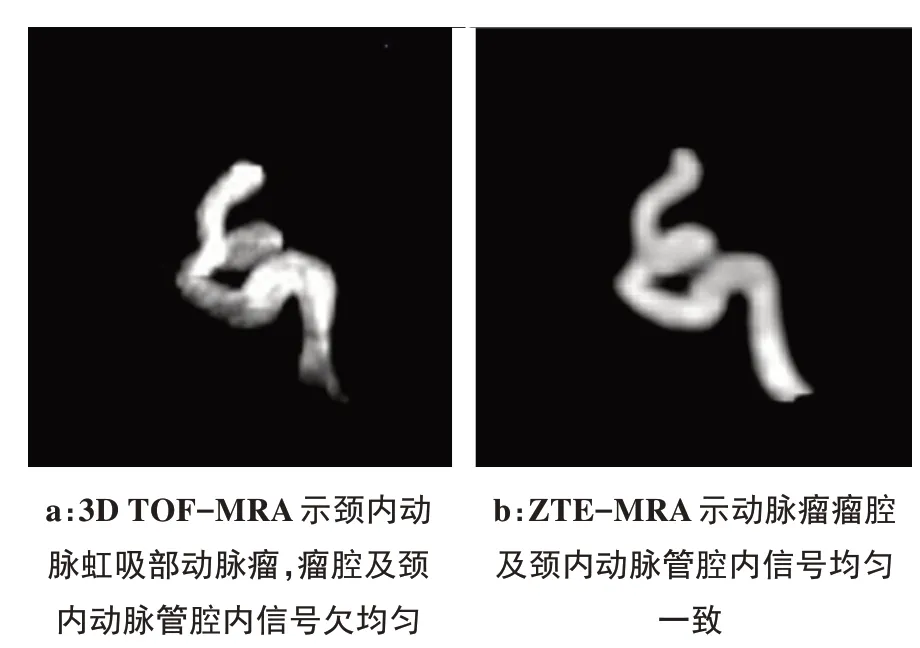
图2 颈内动脉瘤Fig.2 Carotidal aneurysms
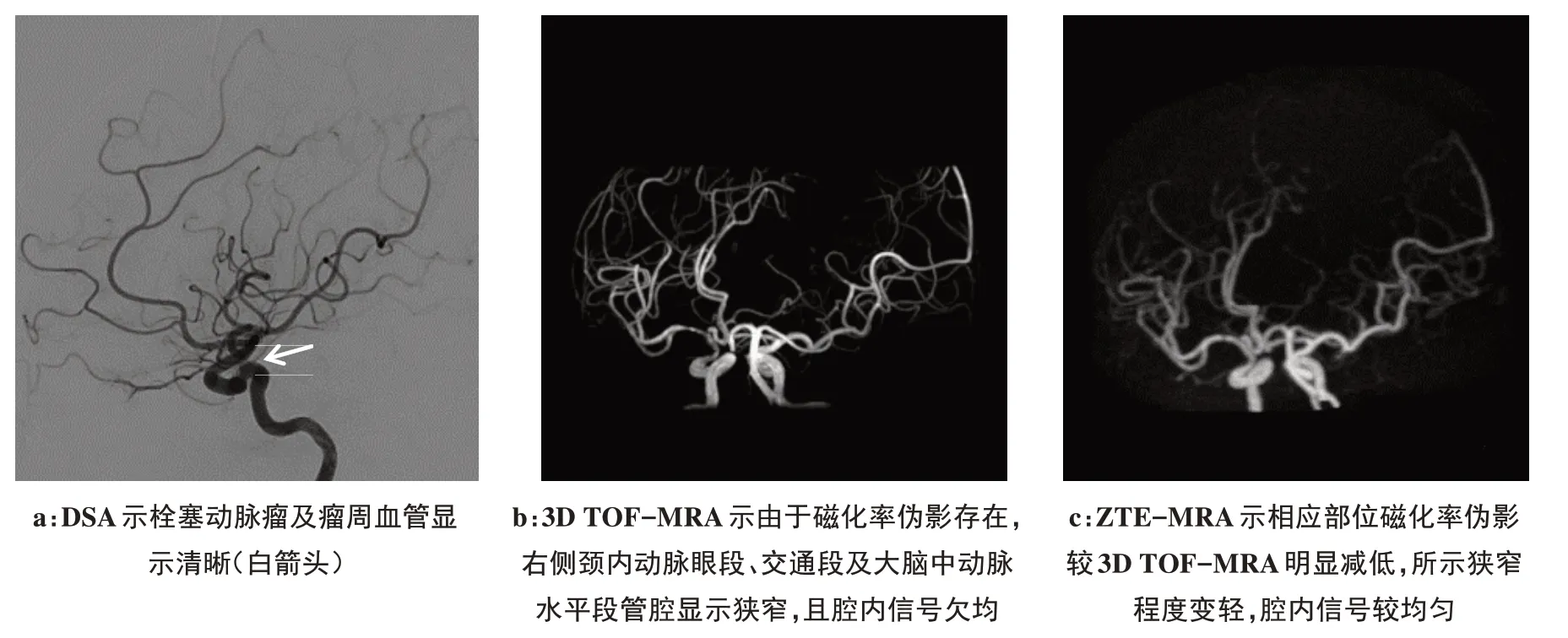
图3 动脉瘤介入术后Fig.3 Aneurysm after transcatheter arterial coil embolization
本次研究的不足之处:(1)样本量较少,且疾病类型较少,需后期进一步增加疾病类型及病例数量;(2)参与血管质量评估的医师较少,且无法做到盲法评估,因两种成像技术的影像特点较为明显,极易分辨。