不同氨(铵)对CuO-La2O3/SiO2催化剂结构与性能的影响*
2021-01-11刘慧敏王美慧于戈文
刘慧敏 王美慧 于戈文 丁 健,2
(1.内蒙古自治区煤化工与煤炭综合利用重点实验室,内蒙古科技大学化学化工学院,014010内蒙古包头;2.内蒙古煤炭绿色开采与绿色利用协同创新中心,014010 内蒙古包头)
0 引 言
我国煤炭资源种类多种多样,储量大,分布广。为充分实现煤资源的价值,有效减少石油资源的缺口,满足我国日益增长的市场需求,必须注重对煤炭资源的科学合理利用。煤化工产业即煤制油[1]、煤制烯烃[2]、煤制乙二醇(EG)[3]、煤制天然气[4]、煤制甲醇[5]和煤制乙醇[6]等技术逐渐成熟,其产品的环保性能和经济效益突出。EG是一种重要的石油化工原料,广泛用于生产聚酯纤维、防冻剂、润滑剂和涂料等[3],因此煤制EG技术受到广泛重视。草酸二甲酯(DMO)选择性加氢制EG是煤制EG路线中关键步骤之一。DMO加氢制EG的工艺中由于均相加氢需在高压下进行,且产品分离回收困难,研究者更倾向于采用以铜基催化剂为主的非均相气相加氢法[7-8]。Cu/SiO2催化剂由于具有较好的加氢选择性并且无环境污染问题,成为研究的焦点[9-10]。但Cu/SiO2催化剂依然存在分散度低、高温易烧结和产物选择性低等问题,严重阻碍了其在草酸酯加氢中的应用[11]。浸渍法制备催化剂操作简单,但所制备的Cu/SiO2催化剂中因活性组分Cu与载体的作用力弱,导致Cu粒子大量聚集,分散度不高,使得催化剂的活性及稳定性降低[12-15]。目前,研究者对于制备Cu/SiO2催化剂的方法也做了一些改进。REN et al[16]研究了稀土元素(Ce,Y和La)改性的Cu/SiO2催化剂,发现加入助剂LaOx,减小了催化剂的粒径,增加了铜物种的分散度,改变了铜物种的表面化学状态,使得催化剂加氢具有良好的活性和稳定性。倪萍[17]研究制备了不同Cu负载量的Cu/SiO2催化剂,发现Cu的分散度与负载量成反比,Cu负载量为20%时,催化性能最佳。LOOI et al[18]制备负载在SiO2上高度分散的Cu催化剂时,发现在制备过程中添加柠檬酸可以提高铜物种的分散度,达到调节催化剂微观结构的效果。刘宾宾等[19]研究了铜负载量相同但在沉淀过程中加入不同无机钠盐的Cu/SiO2催化剂,发现加入无机钠盐能使催化剂孔径增大,促进反应物与其内部的活性位进行催化反应,提高催化剂的活性。但关于在制备过程中以不同氨(铵)源调节溶液的酸碱环境或络合过程来改变铜硅催化剂微观结构和催化性能的研究却较鲜见。本实验采用等体积浸渍法,以四甲基氢氧化铵、氨水和甘氨酸作为氨(铵)源,探讨通过不同氨(铵)源调节制备环境对所得CuO-La2O3/SiO2催化剂微观结构和催化性能的影响。
1 实验部分
1.1 实验试剂
所有试剂均为分析级,可直接使用。硝酸铜、硝酸镧、甘氨酸、氨水(25%(质量分数,下同))和四甲基氢氧化铵水溶液(25%)均购于国药集团试剂有限公司。二氧化硅(平均孔径为12 nm、孔容为0.78 cm3/g、比表面积为260 m2/g)购于上海肴弋合金材料有限公司。H2,N2O,Ar,He,NH3和CO2的纯度均大于99.99%。
1.2 催化剂制备
采用等体积浸渍法制备CuO-La2O3/SiO2催化剂,铜负载量为20%,La掺杂量为1%。为探讨氨源调节pH值对所制备CuO-La2O3/SiO2催化剂结构和活性的影响,采用四甲基氢氧化铵、氨水和甘氨酸调节溶液的pH值,或仅以金属硝酸盐水溶液进行浸渍过程。所得样品分别记为CuLaSi-Te,CuLaSi-Am,CuLaSi-Gl和CuLaSi-No。现以CuLaSi-Am的制备为例,具体步骤如下:在室温下将硝酸铜和硝酸镧充分溶解于去离子水中,与配置好的氨水络合并测其pH值,之后将该络合溶液缓慢滴加到SiO2上,边滴加边用玻璃棒搅拌,直到底物实现饱和吸附,所得饱和浸渍SiO2于120 ℃干燥2 h,之后反复进行此浸渍和干燥过程,直到金属盐溶液全部浸渍于SiO2表面。最后将所得样品于空气中、550 ℃下焙烧4 h可得最终催化剂。其他催化剂的制备过程与此类似。
1.3 催化剂的表征
使用DX-2700型X射线衍射仪(德国,Bruker公司)测试催化剂的晶体结构信息,所用辐射源为CuK α(波长为0.154 05 nm),运行条件为40 kV和30 mA。仪器在5°~85°的2θ范围内采集衍射峰,扫描速度为2 (°)/min。使用JEM-2100F型透射电子显微镜(日本,日立公司)对催化剂形貌进行测试,加速电压为200 kV。
在液氮条件下使用Mcromeritics ASAP 2460型物理吸附仪(美国,Mcromeritics公司)得到N2-吸附/脱附等温曲线。测量前先将样品在200 ℃条件下真空脱气24 h。通过使用Brunauer-emmett-teller(BET)计算得出比表面积(SBET,m2/g),使用Barrett-joyner-halenda(BJH)孔隙分析方法,推导孔容(Vpore,cm3/g)和平均孔径(dpore,nm)。
以N2O滴定法测定所得催化剂的Cu分散度(DCu,%)、Cu表面积(SCu,m2/g(catalyst))和Cu晶粒大小(dCu,nm)[20],计算公式如下:
(1)
(2)
(3)
式中:X为第一个程序升温还原(TPR)的耗氢量;Y为第二个TPR的耗氢量,耗氢量用峰面积计算;NA为阿伏伽德罗常数为6.022×1023;MCu为铜的摩尔质量,63.5 g/mol;1.4×1019为表面铜原子的相对密度。
催化剂的还原性和表面酸度/碱度分别通过VDsorb-91i型化学吸附仪(西安沃德仪器有限公司)进行H2程序升温还原(H2-TPR)和NH3/CO2程序升温解吸(NH3-TPD/CO2-TPD)测量来确定。对于H2-TPR实验,将20 mg样品放入石英管中,通入10%H2/Ar(流速15 mL/min)混合气。待基线走稳后,以10 ℃/min的升温速率加热至800 ℃,通过热导检测器(TCD)在线监测氢气的消耗量。对于CO2-TPD实验,将150 mg样品放入石英管中,为清除吸附在样品表面的水分和其他杂质,在300 ℃下以He气(18 mL/min)吹扫1 h。将温度降至室温后,通入CO2使样品获得饱和吸附。经He吹扫除去催化剂表面物理吸附的CO2并等到检测信号线走稳后,以15 ℃/min的速率将温度升至550 ℃,连续监测流出物,通过TCD监测解吸的CO2。催化剂的NH3-TPD实验过程与上述CO2-TPD过程相似。
1.4 催化活性实验
在YZuBPR-G2-L1-B型不锈钢固定床反应器(上海岩征仪器有限公司)中进行催化活性研究。反应器是一个内径为9.8 mm、长度为290 mm的等温固定床,恒温区高度约为40 mm。先将催化剂与惰性石英砂混合,以减轻局部热点的形成、使整个催化剂床层温度保持均匀。其次,在250 ℃、常压下对催化剂进行原位还原,H2流量为30 mL/min、还原时间为6 h。待反应器冷却到室温后,以2 ℃/min的速度加热到反应温度,同时将压力提高到反应压力。将含有15%DMO(纯度>99%)的甲醇由双柱塞泵(北京卫星制造厂)进料,并在190 ℃下由预热器汽化。将蒸汽与H2混合、并由BROOKS质量流量计控制以实现对液时空速(VLHS)的调节。用两台GC-950型在线气相色谱仪(上海海欣公司)定期分析气体产物。对永久性气体(CO,CO2和H2等),气相色谱仪配备TCD检测器和氧化铝填充柱。对烃类气体,气相色谱仪配备FID检测器和碳分子筛填充柱。冷阱中收集的未反应的DMO和可凝产物,使用配有19091n-213型毛细管柱(美国,安捷伦公司,0.25 mm×30 m)和FID检测器的Shimadzu GC14A分析;使用具有TCD检测器和填充柱(TDX-101)的气相色谱仪(上海海欣公司)测定水的含量。各项评价指标由下式计算:
(4)
(5)
(6)
(7)

在对所得催化剂进行活性测定前,空白实验表明,床层内未装填催化剂、只装填石英砂或未负载Cu和La物种且以氨水处理的载体时,在相同的反应条件下并未观察到任何DMO加氢反应的发生。
2 结果与讨论
2.1 结构表征
2.1.1 织构表征分析
表1所示为焙烧后CuO-La2O3/SiO2催化剂的织构参数。由表1可以看出,不同氨(铵)源制备的催化剂中,随着溶液pH值升高,催化剂的Cu分散度和Cu暴露表面积逐渐增大。其中,CuLaSi-Te在四个催化剂中显示了最大的DCu和SCu,且其比表面积SBET也最大。

表1 CuO-La2O3/SiO2催化剂的织构参数Table 1 Texture parameters of CuO-La2O3/SiO2 catalyst
2.1.2 XRD分析
图1所示为焙烧后CuO-La2O3/SiO2催化剂的XRD谱。由图1可以看出,所有催化剂都表现出具有黑铜矿结构的结晶CuO相(PDF#48-1548)。尤为明显的是,随着溶液pH值的升高,所得催化剂中CuO的衍射峰强度越来越低,CuO粒径越来越小。显然,CuLaSi-Te中的CuO分散更均匀,但其在2θ=26.9°处出现了一个明显的衍射峰,表明了载体由无定型向石英的转变。这很可能是由于四甲基氢氧化铵为强有机碱,其与SiO2作用使得载体发生了晶化。物理混合物CuLaSi-No有很强的CuO衍射尖峰,说明催化剂中的Cu物种呈大颗粒状,分散性较差,可能导致催化剂的活性相对较低[21]。此外,没有迹象表明存在任何结晶氧化镧相,这意味着La物种以无定形氧化物存在于催化剂中或其尺寸超过了XRD技术的检测能力(<3 nm)[22],说明了La的添加量较小且分布均匀。综上所述,添加氨(铵)源调节催化剂制备环境,可以改变活性组分Cu在催化剂中的分散性及粒径。

图1 焙烧后CuO-La2O3/SiO2催化剂的XRD谱Fig.1 XRD spectra of calcined CuO-La2O3/SiO2 catalysts
2.1.3 TEM分析
图2所示为CuLaSi-Am和CuLaSi-Te催化剂还原前后与反应后的TEM照片。由图2可以看出,不同氨(铵)类含氮化合物对催化剂的微观结构有一定的影响。还原前的CuLaSi-Am(见图2a)表面颗粒团聚较多,导致CuO粒度较大,而还原前的CuLaSi-Te(见图2d)表面颗粒疏松分散且粒度均匀,这些与由XRD谱分析的结论相似。但比较还原后和反应后的CuLaSi-Am催化剂(分别见图2b和图2c),发现CuLaSi-Am催化剂经过焙烧后,仍然保留了大多数较小的Cu颗粒;然而CuLaSi-Te催化剂在还原后(见图2e)颗粒发生严重团聚,使活性位大量减少。CuLaSi-Te催化剂在经过了72 h的连续反应后(见图2f),颗粒烧结严重、甚至出现大量块状烧结材料。上述结果的出现原因可能在于,强有机铵虽可以改善活性组分的分散性,但会使载体在还原过程中发生晶化,改变了金属-载体的作用,容易使催化剂在反应时出现严重的烧结现象。
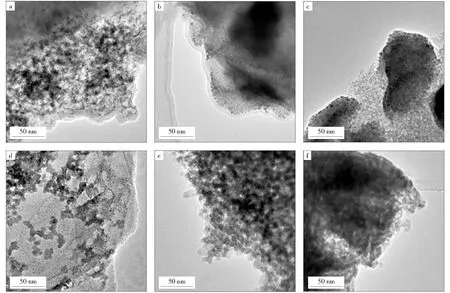
图2 CuO-La2O3/SiO2催化剂的TEM照片Fig.2 TEM photos of CuO-La2O3/SiO2 catalysta,b,c—CuLaSi-Am;d,e,f—CuLaSi-Te a,d—Before reduction;b,e—After reduction;c,f—After reaction
2.1.4 H2-TPR分析
图3所示为焙烧后的CuO-La2O3/SiO2催化剂的H2-TPR谱。通常CuO还原峰温度的高低可反映CuO的尺寸和分散性,即低温还原峰是表面高分散的氧化铜粒子或微小氧化铜簇还原为金属铜,高温还原峰是较大氧化铜颗粒的还原,也就是说还原峰温度越低,物种的粒度越小,CuO分散度越高,CuO越容易还原[23-25]。由图3可以看出,CuLaSi-Am最先出现还原峰并且峰面积最大,说明其还原温度最低、粒径最小且还原度最大。这归因于,添加氨水使得铜氨络合离子的形成更加有利于Cu物种的分散,因此所得催化剂中铜颗粒尺寸较小,且较易被H2还原使表面活性位点增多。然而奇怪的是CuLaSi-Te虽然分散度较高,且在XRD测试中显示了最小的CuO粒径,但在H2-TPR测试中还原温度较高,还原峰面积减少且出现明显的双峰。究其原因为强有机铵的加入,使得载体在催化剂制备过程中发生晶化,其与CuO之间发生很强的作用,增大了CuO的还原难度;另一方面,载体晶化也导致聚集态的CuO团簇的出现,使还原温度增大。相比来说,添加甘氨酸且溶液pH呈酸性所制备的CuLaSi-Gl的还原温度最高,说明甘氨酸的添加未能促进络合过程而改善Cu物种的分布,因此CuO颗粒尺寸较大,Cu活性位较少。

图3 熔烧后CuO-La2O3/SiO2催化剂的H2-TPR谱Fig.3 H2-TPR spectra of calcined CuO-La2O3/SiO2 catalyst
2.1.5 NH3-TPD和CO2-TPD分析
图4所示为焙烧后的CuO-La2O3/SiO2催化剂的NH3-TPD谱和CO2-TPD谱。NH3与催化剂表面作用越强,催化剂的固体酸性越强,且固体酸性位数量越多,脱附峰面积就越大[26]。由图4a可以看出,CuLaSi-No展现了大量的表面酸中心。与此类似,CuLaSi-Te的峰面积也相对较大,酸性位较多。这可能是由于催化剂制备过程中缩聚产物形态和性质发生变化,使得所得催化剂表面酸性增强[27]。相比来说,CuLaSi-Am的脱附峰面积最小,酸性位较少。一般来说,CO2的脱附峰面积越大,所对应的温度越高,说明催化剂的表面碱性位越多,固体碱性越强。由图4b可以看出,CuLaSi-No同时具有三种碱中心(即弱碱中心、中强碱中心和强碱中心)且数量巨大。对于添加氨(铵)源后制备的CuLaSi-Gl,CuLaSi-Am和CuLaSi-Te,脱附峰温度明显降低且峰面积减少,说明上述三种碱中心的强度和数量都减小。根据NH3-TPD和CO2-TPD的表征结果可知,CuLaSi-Am的表面酸性位和碱性位最少。综上所述,氨(铵)源的加入对催化剂制备环境的调节可以改变催化剂表面的酸/碱性中心分布,从而影响催化剂在反应中对乙二醇的选择性。
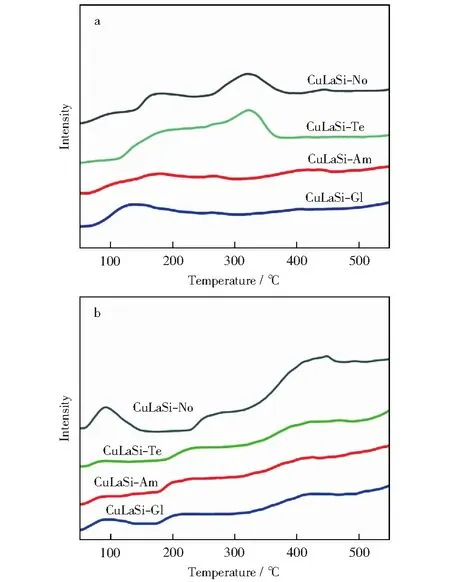
图4 CuO-La2O3/SiO2催化剂的NH3-TPD谱和CO2-TPD谱Fig.4 NH3-TPD and CO2-TPD spectra of calcined CuO-La2O3/SiO2 catalysta—NH3-TPD;b—CO2-TPD
2.2 活性测试
图5所示为在p=2.4 MPa,t=220 ℃,n(H2)/n(DMO)=60,VLHS=1.0 h-1条件下,CuO-La2O3/SiO2催化剂在DMO气相加氢中的催化性能。DMO气相加氢包含几个连续的反应,DMO加氢生成乙醇酸甲酯(MG),MG加氢生成EG,EG进一步加氢脱水生成乙醇。由图5可知,添加不同氨(铵)源调节溶液pH值对所制备CuO-La2O3/SiO2催化剂的DMO转化率和EG选择性有显著影响。在相同反应条件下,CuLaSi-Am的DMO初始转化率约为98%,EG选择性则高达约97%,同时MG选择性低于2%。虽然连续反应200 h后DMO转化率降至95%,但EG选择性维持在98%以上。此外,EG的空时产率保持在0.48 g(EG)/(g(catalyst)·h)以上。而其他几个催化剂的活性和稳定性却远低于此。如CuLaSi-Gl虽然具有较高的DMO转化率,但MG的出现也不可忽略,导致其对EG选择性低于50%。而CuLaSi-No的活性和稳定性则进一步降低。对于铜催化加氢反应来说,铜分散性往往被认为是影响催化活性的重要因素。但具有最高Cu分散度的CuLaSi-Te却在反应中表现出了极差的催化活性和稳定性,如DMO转化率从反应初的71%(连续反应8 h)迅速降低至13%(连续反应48 h),而此时EG的空时产率仅为0.04 g(EG)/(g(catalyst)·h)。
大量研究发现Cu基催化剂的催化活性与铜的分散度成正比,所以铜活性位是草酸酯加氢的高效位点[28-30]。N2O测定结果(见表1)表明氨(铵)源的引入调节催化剂制备环境可以改变所得催化剂的Cu分散度和暴露表面积。而图1和图2也证实了这一结论。虽然碱性条件下制备的CuLaSi-Am和CuLaSi-Te催化剂的Cu分散度均较大,但加入强有机碱四甲基氢氧化铵后,载体发生了晶化,影响了铜和载体间的作用,导致催化剂的还原性能降低且在还原氛围下极易发生热烧结,出现大量团聚,最终使反应所需活性位数量大为减少。CuLaSi-Am却在反应中显示出了较高的活性和稳定性。除具有较高的分散度之外,H2-TPR也证实了CuLaSi-Am具有较大的还原度。NH3-TPD和CO2-TPD的结果也表明,该催化剂表面较少的酸/碱性位的数量,可以抑制EG进一步加氢生成乙醇,或抑制其他副产品的形成,使得该催化剂有更高的EG选择性。因此,相较于无络合过程制备催化剂,加入具有络合能力的氨水形成铜氨络合离子,可以提高所得催化剂的DMO加氢性能和EG产率,同时改善催化剂的稳定性,但过强的有机铵(如四甲基氢氧化铵)却适得其反。

图5 CuO-La2O3/SiO2催化剂在DMO气相加氢中的催化性能Fig.5 Catalytic performance of CuO-La2O3/SiO2 catalyst in gas phase hydrogenation of DMO△—CuLaSi-Am;▽—CuLaSi-Gl;□—CuLaSi-No;◇—CuLaSi-Te
3 结 论
1) 不同氨(铵)类含氮化合物会改变催化剂制备环境(如络合过程的发生),使所得催化剂中Cu的分散性和暴露表面积显著改变,进而影响其DMO加氢制EG的催化性能。
2) 综合XRD,TEM和H2-TPR等分析来看,强有机铵(四甲基氢氧化铵)的加入并与载体作用会使载体发生晶化,使催化剂还原性变差、大量Cu粒子在反应条件下烧结,减少了Cu活性位的数量,最终导致DMO加氢性能降低。
3) 由于络合过程促进了Cu物种的分散,以氨水制备的CuLaSi-Am具有较高Cu暴露表面积和较低的固体酸碱性,其在DMO加氢制EG反应中具有优异的活性和稳定性,如在DMO转化率约为95%时表现出较高的EG选择性(约98%),且催化剂保持稳定运行超过200 h。
