健胃消食片对不同性别大鼠的长期毒性研究
2021-01-06万建华詹扬杨妮胡旭李颖萌刘文君
万建华詹扬杨妮胡旭李颖萌刘文君
江中牌健胃消食片所选用的药材包含太子参、陈皮、山药、麦芽(炒)、山楂,具有健胃消食的作用。其上市前的成年大鼠安评实验方案如下:低、中、高(1.65、3.30、4.95g/kg)3个剂量分别给药2个月,给药期间记录体重变化,给药结束分别检测谷丙转氨酶活性、酚红排泄率、红细胞数量、白细胞数量,并对肝脏、脾脏、肾脏和胃进行病理分析。由于该产品上市近30年,当时的安评实验检测指标现在来看不够全面[1,2],同时很多患者服用健胃消食片的剂量和周期超过药品说明书的规定,因此有必要补充一个更高剂量更长周期的毒性研究试验,为临床安全用药提供更充分的数据支撑。
1 材料与方法
1.1 药物与试剂江中牌健胃消食片(江中药业股份有限公司生产,0.8g/片,生药含量约0.7g/片,生药含量比例为87.5%,批号:19051026),临用前使用纯化水配制成70%的溶液。
1.2 主要仪器BC-2800vet 全自动血液细胞分析仪(迈瑞医疗);Chemray 240 血生化仪(深圳雷杜生命科技);C3510 全自动凝血分析仪(迈瑞医疗)。Epoch 酶标检测仪(BioTeK),Eclipse Ci 病理显微镜(Nikon 公司);RM2126 石蜡切片机(Leica 公司);石蜡包埋机。
1.3 动物SPF级大鼠80 只,雌雄各半,体重180~220g,购自江西中医药大学,许可证号SCXK(赣)2018-0003。大鼠均饲养于江西中医药大学实验动物中心的SPF级动物房内,分笼饲养,每笼大鼠不超过5 只,自由摄食饮水,室温控制在20℃~25℃,相对湿度维持在40%~70%,每天光照12h,黑暗处理12h,每小时通风≥15次。
1.4 剂量设计江中健胃消食片成人临床用药剂量约为0.1g·kg-1·d-1,根据体重将大鼠随机分为高剂量组和对照组,高剂量组给药剂量约为10g/kg,为临床剂量的100 倍。
1.5 分组和给药将大鼠按体重随机分为对照组和高剂量组(10g/kg),每组40 只,雌雄各半,高剂量组大鼠给予健胃消食片水溶液(70%的浓度)灌胃,对照组给予等量纯水,给药体积均为15ml/kg,每日1次,每天进行1次一般临床观察并定期测定体重和摄食量。连续给药13 周和26 周后分别剖杀1/4和1/2 的大鼠,经过4 周的恢复期后再剖杀1/4 的大鼠,分别进行血液学、血生化、凝血功能检测;解剖时称量主要脏器的湿重并对脏器组织进行病理学检查。
1.6 观察与记录指标生长发育指标:体重、摄食量、一般临床特征。血液学指标:白细胞数目(WBC)、淋巴细胞数目(Lypmh#)、平均红细胞体积(MCV)、平均红细胞血红蛋白含量(MCH)、血小板压积(PCT)。血生化指标:总胆红素(TBIL)、谷氨酰转肽酶(r-GT)、总胆汁酸(TBA)、高密度脂蛋白胆固醇(HDL-C)。凝血功能指标:凝血酶原时间(PT)、活化部分凝血活酶时间(APTT)、纤维蛋白原(FIB)。不同部位的脏器湿重和脏器系数:心脏、肝脏、脾脏、肺、肾、大脑、肾上腺、胸腺、睾丸、附睾、子宫、卵巢;组织病理学检查部位:心脏、肝脏、脾脏、胃、肾、大脑、皮肤、十二指肠。
1.7 统计学分析采用SPSS 20.0 统计软件进行统计分析,两组计量资料用±s表示,比较采用t检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 健胃消食片对SD 大鼠一般状况、体质量、摄食量的影响给药期间各组大鼠的自主活动、饮水、摄食及二便均正常,精神状态良好;毛色有光泽,口、鼻、眼未出现异常分泌物,皮肤也未出现过敏现象。各组成年大鼠在给药后体重均保持稳定增长。从给药第1 周至恢复期结束,给药组雄性大鼠的体重低于对照组(P<0.05 或P<0.01);从给药第5 周至恢复期结束,给药组雌性大鼠的体重低于对照组(P<0.05 或P<0.01),见图1、2。
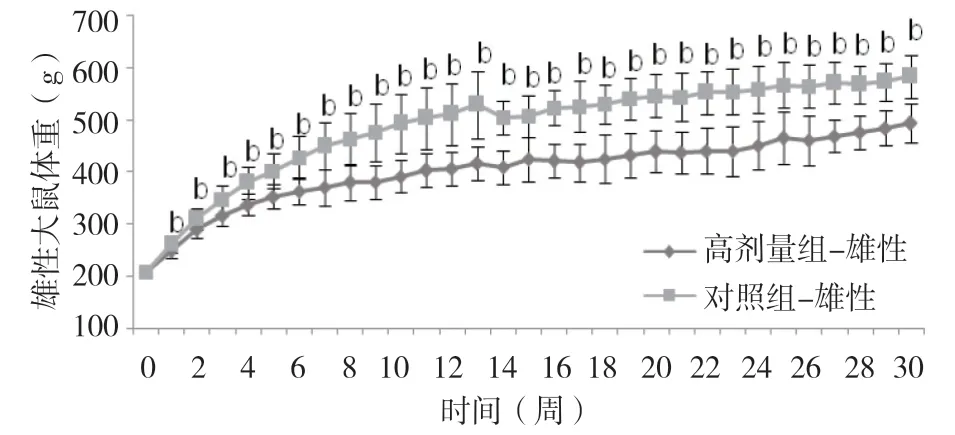
图1 雄性SD 大鼠体重变化
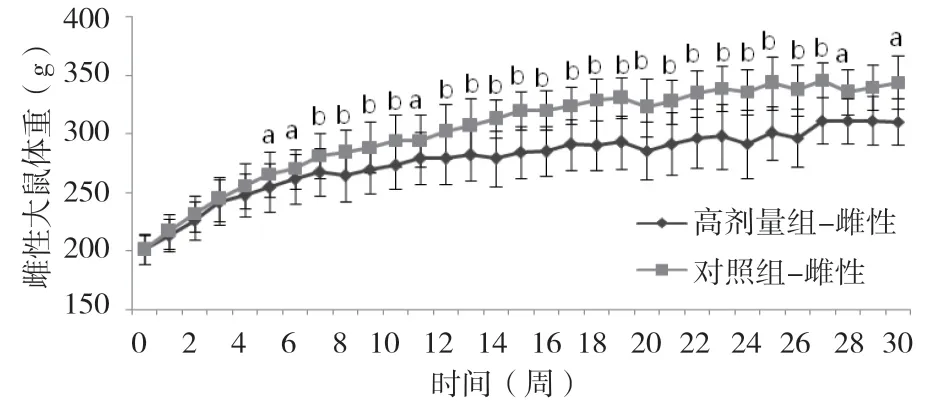
图2 雌性SD 大鼠体重变化
2.2 健胃消食片对SD大鼠血液学指标的影响与对照组相比,在给药中期,高剂量组雄性和雌性大鼠血常规指标差异无统计学意义(P>0.05);给药末期,高剂量组雄性大鼠WBC和Lymph#降低(P<0.05),MCV和MCH 升高(P<0.05);雌性大鼠PCT 升高(P<0.05)。恢复期结束时,指标均恢复至正常水平,结果见表1、2。
2.3 健胃消食片对SD大鼠血生化及凝血功能的影响与对照组相比,在给药中期,高剂量组雄性和雌性大鼠血生化和凝血指标无明显差异(P>0.05);给药末期,高剂量组雄性大鼠TBA、HDL-C和APTT 降低(P<0.05);雌性大鼠TBIL、r-GT和FIB降低(P<0.05),APTT 升高(P<0.01);恢复期结束,雌性大鼠TBIL 降低(P<0.01),其它指标均恢复至正常水平,见表3、4。
2.4 健胃消食片对SD大鼠脏器湿重和脏器系数的影响与对照组相比,在给药中期,高剂量组雄性大鼠肝脏、大脑、肾脏、胸腺和附睾的湿重降低(P<0.05),大脑和睾丸的脏器系数升高(P<0.05);雌性大鼠心脏、脾脏、胸腺的脏器系数升高(P<0.05 或P<0.01)。给药末期,高剂量组雄性大鼠肝脏、脾脏、胸腺的湿重降低(P<0.05 或P<0.01),心脏、大脑、肾脏、肺、睾丸和附睾的脏器系数升高(P<0.05 或P<0.01);雌性大鼠心脏和肾脏的脏器系数升高。恢复期结束,高剂量组雄性大鼠心脏和肾脏的脏器湿重降低(P<0.05或P<0.01),大脑的脏器系数升高(P<0.05);雌性大鼠胸腺的湿重降低,大脑、肾脏和卵巢的脏器系数升高(P<0.05 或P<0.01),见表5、6。
表1 各组雄鼠不同时间点血常规比较(±s)
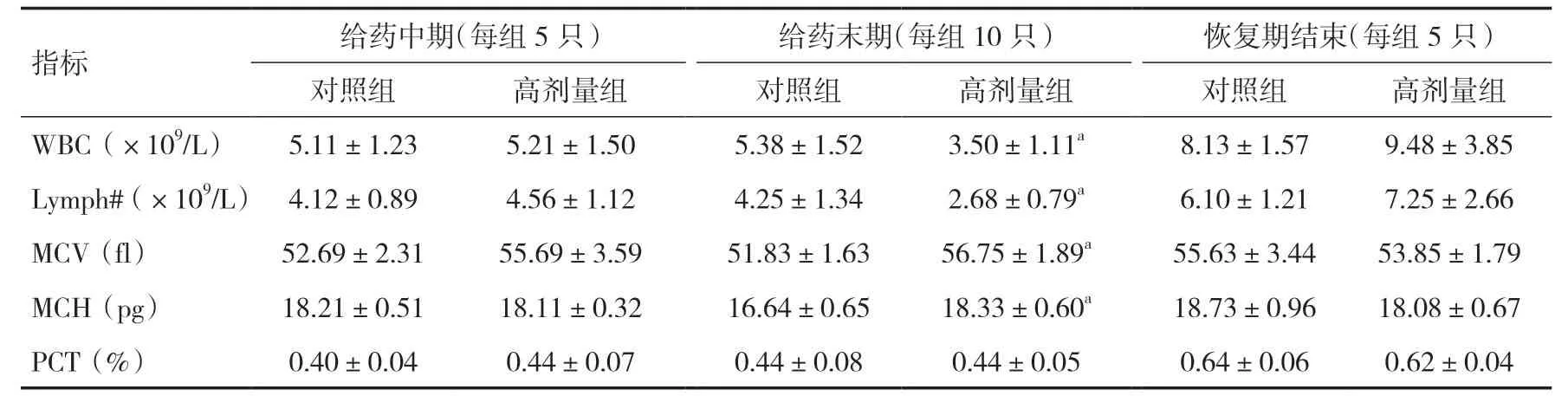
表1 各组雄鼠不同时间点血常规比较(±s)
注:与对照组相比,aP<0.05
指标 给药中期(每组5 只) 给药末期(每组10 只) 恢复期结束(每组5 只)对照组 高剂量组 对照组 高剂量组 对照组 高剂量组WBC(×109/L) 5.11±1.23 5.21±1.50 5.38±1.52 3.50±1.11a 8.13±1.57 9.48±3.85 Lymph#(×109/L) 4.12±0.89 4.56±1.12 4.25±1.34 2.68±0.79a 6.10±1.21 7.25±2.66 MCV(fl) 52.69±2.31 55.69±3.59 51.83±1.63 56.75±1.89a 55.63±3.44 53.85±1.79 MCH(pg) 18.21±0.51 18.11±0.32 16.64±0.65 18.33±0.60a 18.73±0.96 18.08±0.67 PCT(%) 0.40±0.04 0.44±0.07 0.44±0.08 0.44±0.05 0.64±0.06 0.62±0.04
表2 各组雌鼠不同时间点血常规比较(±s)

表2 各组雌鼠不同时间点血常规比较(±s)
注:与对照组相比,aP<0.05
指标 给药中期(每组5 只) 给药末期(每组10 只) 恢复期结束(每组5 只)对照组 高剂量组 对照组 高剂量组 对照组 高剂量组WBC(×109/L) 4.15±1.21 4.35±0.69 3.69±1.16 4.05±0.76 5.48±1.14 6.03±1.31 Lymph#(×109/L) 3.21±0.51 3.11±0.42 3.00±0.96 3.18±0.55 4.33±0.70 4.83±0.85 MCV(fl) 54.23±2.11 57.10±4.20 58.04±1.72 54.2±2.30 57.53±3.35 58.53±2.40 MCH(pg) 17.89±0.22 17.66±1.20 18.74±0.53 17.38±0.66 19.58±1.47 19.95±0.84 PCT(%) 0.41±0.04 0.39±0.05 0.40±0.06 0.42±0.06a 0.60±0.07 0.59±0.05
表3 各组雄鼠不同时间点血生化与凝血功能比较(±s)
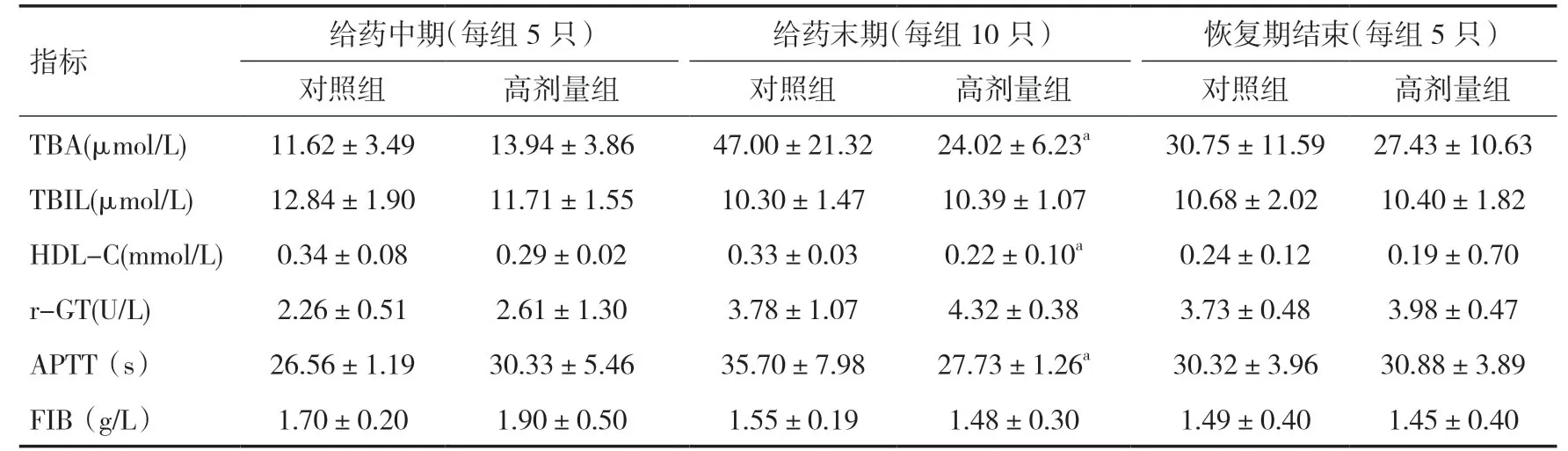
表3 各组雄鼠不同时间点血生化与凝血功能比较(±s)
注:与对照组相比,aP<0.05
指标 给药中期(每组5 只) 给药末期(每组10 只) 恢复期结束(每组5 只)对照组 高剂量组 对照组 高剂量组 对照组 高剂量组TBA(μmol/L) 11.62±3.49 13.94±3.86 47.00±21.32 24.02±6.23a 30.75±11.59 27.43±10.63 TBIL(μmol/L) 12.84±1.90 11.71±1.55 10.30±1.47 10.39±1.07 10.68±2.02 10.40±1.82 HDL-C(mmol/L) 0.34±0.08 0.29±0.02 0.33±0.03 0.22±0.10a 0.24±0.12 0.19±0.70 r-GT(U/L) 2.26±0.51 2.61±1.30 3.78±1.07 4.32±0.38 3.73±0.48 3.98±0.47 APTT(s) 26.56±1.19 30.33±5.46 35.70±7.98 27.73±1.26a 30.32±3.96 30.88±3.89 FIB(g/L) 1.70±0.20 1.90±0.50 1.55±0.19 1.48±0.30 1.49±0.40 1.45±0.40
表4 各组雌鼠不同时间点血生化与凝血功能比较(±s)
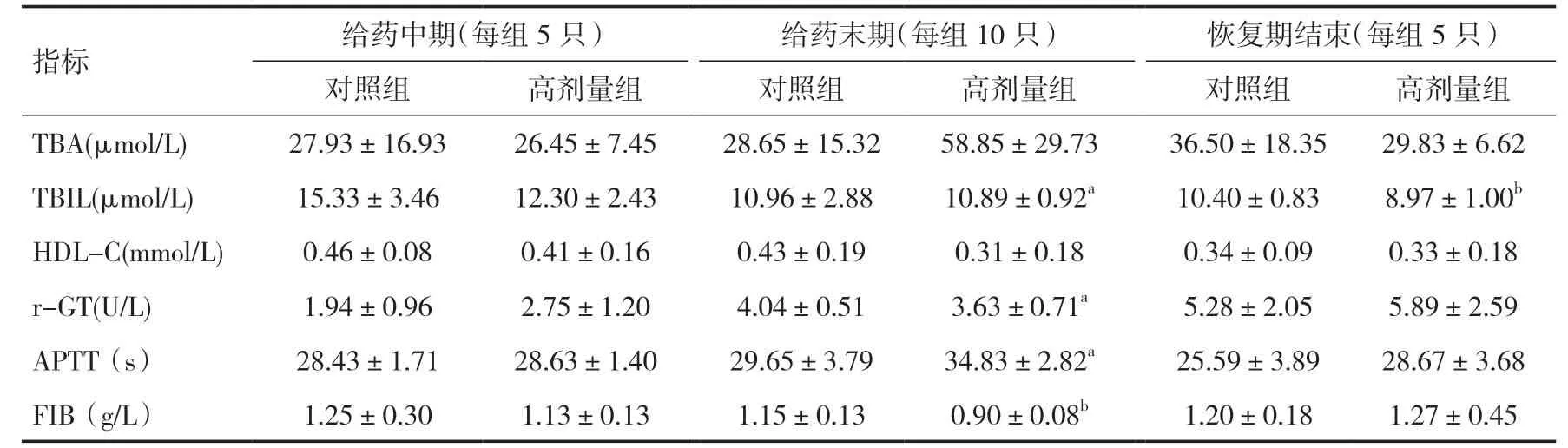
表4 各组雌鼠不同时间点血生化与凝血功能比较(±s)
注:与对照组相比,aP<0.05,bP<0.01
指标 给药中期(每组5 只) 给药末期(每组10 只) 恢复期结束(每组5 只)对照组 高剂量组 对照组 高剂量组 对照组 高剂量组TBA(μmol/L) 27.93±16.93 26.45±7.45 28.65±15.32 58.85±29.73 36.50±18.35 29.83±6.62 TBIL(μmol/L) 15.33±3.46 12.30±2.43 10.96±2.88 10.89±0.92a 10.40±0.83 8.97±1.00b HDL-C(mmol/L) 0.46±0.08 0.41±0.16 0.43±0.19 0.31±0.18 0.34±0.09 0.33±0.18 r-GT(U/L) 1.94±0.96 2.75±1.20 4.04±0.51 3.63±0.71a 5.28±2.05 5.89±2.59 APTT(s) 28.43±1.71 28.63±1.40 29.65±3.79 34.83±2.82a 25.59±3.89 28.67±3.68 FIB(g/L) 1.25±0.30 1.13±0.13 1.15±0.13 0.90±0.08b 1.20±0.18 1.27±0.45
表5 各组雄鼠不同时间点脏器重量和系数比较(±s)
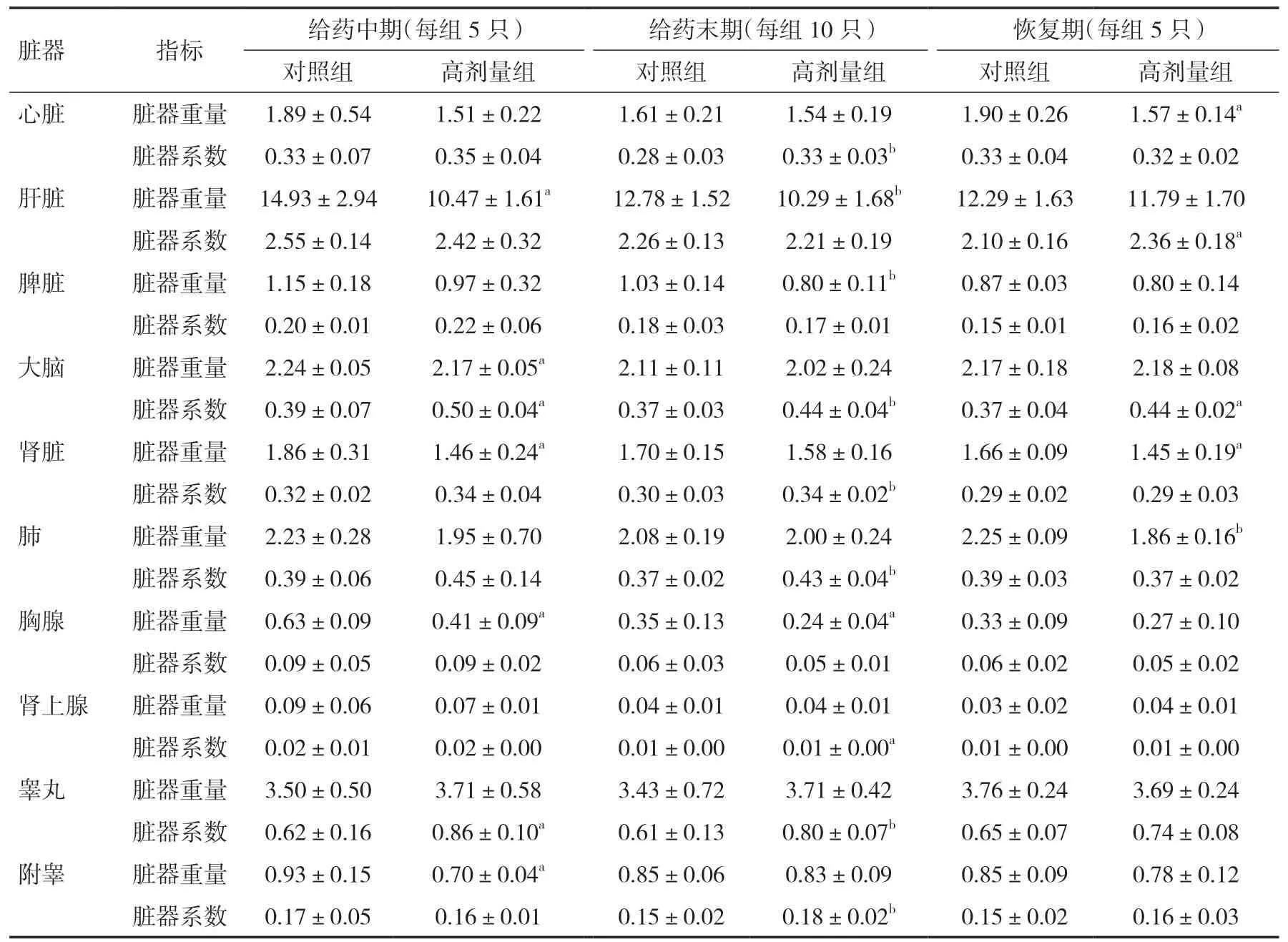
表5 各组雄鼠不同时间点脏器重量和系数比较(±s)
注:与对照组相比,aP<0.05,bP<0.01
脏器 指标 给药中期(每组5 只) 给药末期(每组10 只) 恢复期(每组5 只)对照组 高剂量组 对照组 高剂量组 对照组 高剂量组心脏 脏器重量 1.89±0.54 1.51±0.22 1.61±0.21 1.54±0.19 1.90±0.26 1.57±0.14a脏器系数 0.33±0.07 0.35±0.04 0.28±0.03 0.33±0.03b 0.33±0.04 0.32±0.02肝脏 脏器重量 14.93±2.94 10.47±1.61a 12.78±1.52 10.29±1.68b 12.29±1.63 11.79±1.70脏器系数 2.55±0.14 2.42±0.32 2.26±0.13 2.21±0.19 2.10±0.16 2.36±0.18a脾脏 脏器重量 1.15±0.18 0.97±0.32 1.03±0.14 0.80±0.11b 0.87±0.03 0.80±0.14脏器系数 0.20±0.01 0.22±0.06 0.18±0.03 0.17±0.01 0.15±0.01 0.16±0.02大脑 脏器重量 2.24±0.05 2.17±0.05a 2.11±0.11 2.02±0.24 2.17±0.18 2.18±0.08脏器系数 0.39±0.07 0.50±0.04a 0.37±0.03 0.44±0.04b 0.37±0.04 0.44±0.02a肾脏 脏器重量 1.86±0.31 1.46±0.24a 1.70±0.15 1.58±0.16 1.66±0.09 1.45±0.19a脏器系数 0.32±0.02 0.34±0.04 0.30±0.03 0.34±0.02b 0.29±0.02 0.29±0.03肺 脏器重量 2.23±0.28 1.95±0.70 2.08±0.19 2.00±0.24 2.25±0.09 1.86±0.16b脏器系数 0.39±0.06 0.45±0.14 0.37±0.02 0.43±0.04b 0.39±0.03 0.37±0.02胸腺 脏器重量 0.63±0.09 0.41±0.09a 0.35±0.13 0.24±0.04a 0.33±0.09 0.27±0.10脏器系数 0.09±0.05 0.09±0.02 0.06±0.03 0.05±0.01 0.06±0.02 0.05±0.02肾上腺 脏器重量 0.09±0.06 0.07±0.01 0.04±0.01 0.04±0.01 0.03±0.02 0.04±0.01脏器系数 0.02±0.01 0.02±0.00 0.01±0.00 0.01±0.00a 0.01±0.00 0.01±0.00睾丸 脏器重量 3.50±0.50 3.71±0.58 3.43±0.72 3.71±0.42 3.76±0.24 3.69±0.24脏器系数 0.62±0.16 0.86±0.10a 0.61±0.13 0.80±0.07b 0.65±0.07 0.74±0.08附睾 脏器重量 0.93±0.15 0.70±0.04a 0.85±0.06 0.83±0.09 0.85±0.09 0.78±0.12脏器系数 0.17±0.05 0.16±0.01 0.15±0.02 0.18±0.02b 0.15±0.02 0.16±0.03
表6 各组雌鼠不同时间点脏器重量和系数比较(±s)
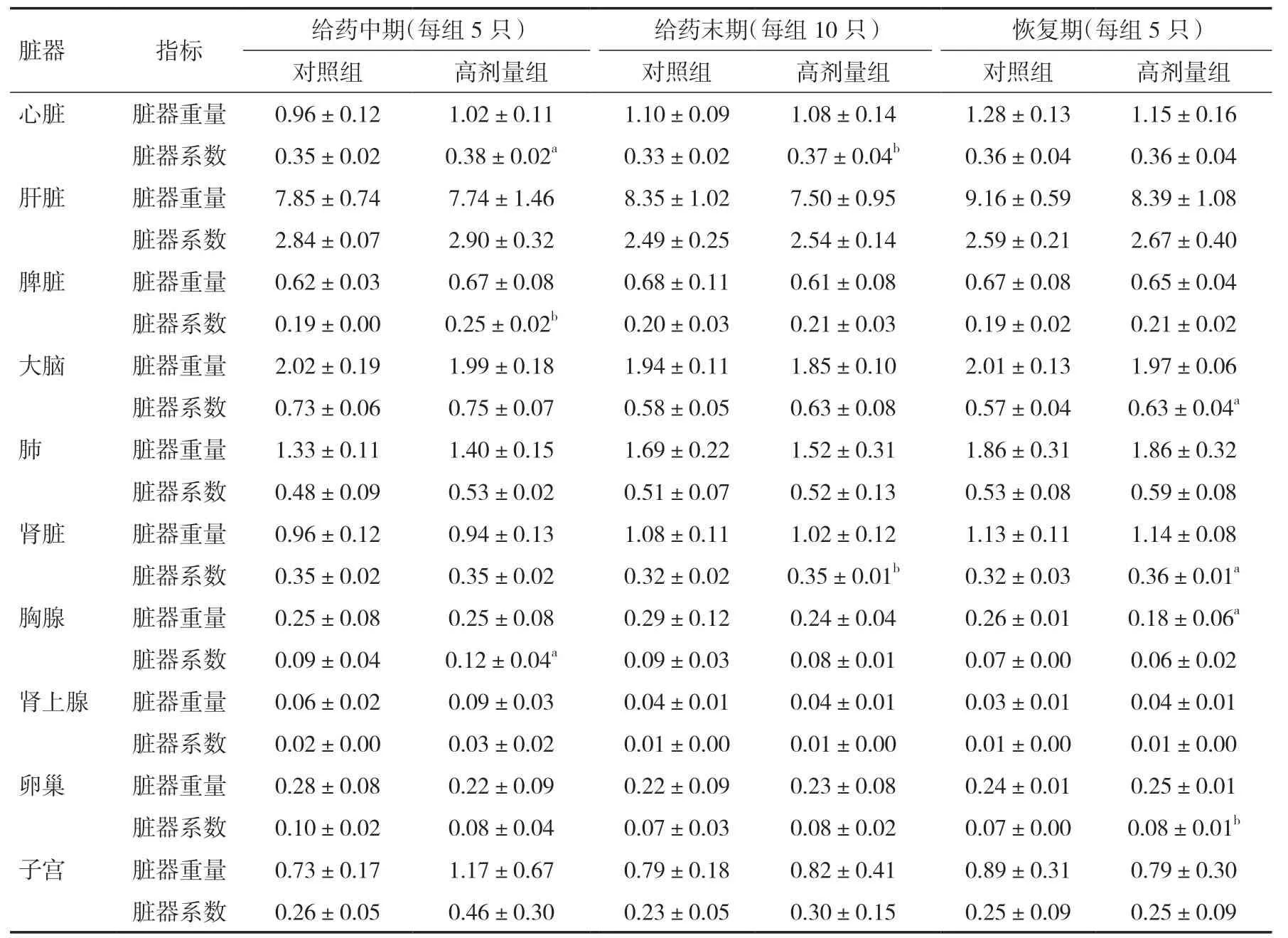
表6 各组雌鼠不同时间点脏器重量和系数比较(±s)
注:与对照组相比,aP<0.05,bP<0.01
脏器 指标 给药中期(每组5 只) 给药末期(每组10 只) 恢复期(每组5 只)对照组 高剂量组 对照组 高剂量组 对照组 高剂量组心脏 脏器重量 0.96±0.12 1.02±0.11 1.10±0.09 1.08±0.14 1.28±0.13 1.15±0.16脏器系数 0.35±0.02 0.38±0.02a 0.33±0.02 0.37±0.04b 0.36±0.04 0.36±0.04肝脏 脏器重量 7.85±0.74 7.74±1.46 8.35±1.02 7.50±0.95 9.16±0.59 8.39±1.08脏器系数 2.84±0.07 2.90±0.32 2.49±0.25 2.54±0.14 2.59±0.21 2.67±0.40脾脏 脏器重量 0.62±0.03 0.67±0.08 0.68±0.11 0.61±0.08 0.67±0.08 0.65±0.04脏器系数 0.19±0.00 0.25±0.02b 0.20±0.03 0.21±0.03 0.19±0.02 0.21±0.02大脑 脏器重量 2.02±0.19 1.99±0.18 1.94±0.11 1.85±0.10 2.01±0.13 1.97±0.06脏器系数 0.73±0.06 0.75±0.07 0.58±0.05 0.63±0.08 0.57±0.04 0.63±0.04a肺 脏器重量 1.33±0.11 1.40±0.15 1.69±0.22 1.52±0.31 1.86±0.31 1.86±0.32脏器系数 0.48±0.09 0.53±0.02 0.51±0.07 0.52±0.13 0.53±0.08 0.59±0.08肾脏 脏器重量 0.96±0.12 0.94±0.13 1.08±0.11 1.02±0.12 1.13±0.11 1.14±0.08脏器系数 0.35±0.02 0.35±0.02 0.32±0.02 0.35±0.01b 0.32±0.03 0.36±0.01a胸腺 脏器重量 0.25±0.08 0.25±0.08 0.29±0.12 0.24±0.04 0.26±0.01 0.18±0.06a脏器系数 0.09±0.04 0.12±0.04a 0.09±0.03 0.08±0.01 0.07±0.00 0.06±0.02肾上腺 脏器重量 0.06±0.02 0.09±0.03 0.04±0.01 0.04±0.01 0.03±0.01 0.04±0.01脏器系数 0.02±0.00 0.03±0.02 0.01±0.00 0.01±0.00 0.01±0.00 0.01±0.00卵巢 脏器重量 0.28±0.08 0.22±0.09 0.22±0.09 0.23±0.08 0.24±0.01 0.25±0.01脏器系数 0.10±0.02 0.08±0.04 0.07±0.03 0.08±0.02 0.07±0.00 0.08±0.01b子宫 脏器重量 0.73±0.17 1.17±0.67 0.79±0.18 0.82±0.41 0.89±0.31 0.79±0.30脏器系数 0.26±0.05 0.46±0.30 0.23±0.05 0.30±0.15 0.25±0.09 0.25±0.09
2.5 健胃消食片对SD大鼠脏器组织病理的影响在给药中期、给药末期和恢复期结束时分别剖杀大鼠,对其主要脏器进行病理分析发现,高剂量组和对照组胃和十二指肠均出现了轻微上皮细胞脱落,脾脏局部可见脾小结扩张,肝脏胆管轻度增生等,上述病变表现的程度均较轻微,在各时期出现病变大鼠的数量和病变程度也未见明显差异。
3 讨论
研究结果显示,从给药开始,高剂量组大鼠体重增长相对于对照组明显减缓,认为长期高剂量服用健胃消食片可延缓实验大鼠的体重增长。
给药中期,高剂量组和对照组的血常规、血生化和凝血功能相比较,均无异常波动;给药末期,高剂量组的血常规、血生化和凝血功能中的少数指标出现了轻微波动;恢复期结束,高剂量组所有血常规、凝血功能及生化指标绝大多数恢复正常。这提示长期高剂量服用健胃消食片可对大鼠血常规、血生化和凝血功能产生影响,但幅度较轻微,且大多未偏离文献报道的同龄大鼠数值范围[3~7],同时这种影响在停药后大多可逆,不构成永久性机体损伤。
同时在整个实验的不同时期发现大鼠多个脏器的湿重和脏器系数出现异常波动[8,9],但呈现一个共同的规律,即高剂量组相对于对照组脏器湿重降低,脏器系数升高。已有研究表明一些影响动物食欲或消化吸收的药物可导致实验动物体重增长明显减缓,同时脏器湿重增加也会减缓,但体重增长减缓的幅度要比脏器湿重减缓的幅度大许多,这时相关的脏器系数统计学检验会出现不能准确反映检验者目的的显著性差异[10,11]。结合本次实验高剂量组大鼠体重增长明显减缓,因此推断这次实验脏器湿重降低和脏器系数升高多是由此导致的。而且主要脏器的病理分析显示,高剂量组大鼠主要脏器的病理检查未发现异常,多为自发性病变[12~15],基本可判定脏器湿重和脏器系数的异常波动无毒性意义。
综上,10g/kg 高剂量健胃消食片灌胃26 周对幼龄期SD 大鼠的肝功能指标和凝血指标具有轻微影响,但无明显毒性反应;同时未对脏器产生实质性的损伤。故认为健胃消食片的无毒性反应剂量(no observed adverse effect level, NOAEL)不低于10g/kg,相当于临床成人剂量的100 倍。
