LDH/Fe3O4@Cu2O复合材料对盐酸四环素的光催化性能研究
2020-12-29王小凤谭乐乐陈金毅
陈 冉,王小凤,2,3,谭乐乐,肖 妮,陈金毅,2,3*
(1.武汉工程大学化学与环境工程学院,武汉 430205; 2.绿色化工过程教育部重点实验室,武汉 430205;3.湖北省化工环境污染控制工程技术研究中心,武汉 430205)
盐酸四环素(TC)作为典型的抗生素,被广泛用来医疗、农业和畜牧业等领域[1-4].含有抗生素废水的不当处理会污染地下水、地表水,增加水生动物死亡率和人类癌症风险,这引起了全世界的极大关注.传统降解TC的方法主要有物理吸附法(如活性炭,壳聚糖,沸石和膨润土作为吸附剂),化学法,生物法等,但这些方法只是污染物相的转移,不能彻底降解污染物且处理成本高、效率低[5-8].因此,寻求一种经济适用的处理方法具有一定的研究意义.
近年来,半导体光催化剂被广泛用于降解污染物、除藻、产氢、固氮和CO2还原等领域[9,10].Cu2O是一种禁带宽度窄(1.8~2.2 eV)的P型半导体光催化材料,能够在可见光下被激发,从而达到降解有机污染物的目的[11-13].但是单一Cu2O用于光催化试验时,会出现材料团聚、光腐蚀和容易氧化变黑等现象[12,14].为了提高Cu2O的稳定性和光催化效果,本实验采用液相还原法制备了LDH/Fe3O4@Cu2O复合材料,进行光催化实验降解TC,研究了投加量、光照强度和pH值对光催化效果的影响,通过自由基抑制实验分析了LDH/Fe3O4@Cu2O复合材料光催化降解TC过程中起主要作用的自由基.
1 材料与方法
1.1 试剂与仪器
实验试剂主要有乙酸铜(AR,国药集团化学试剂有限公司)、氢氧化钠(AR,国药集团化学试剂有限公司)、抗坏血酸(AR,国药集团化学试剂有限公司)、氨水(AR,西陇化工股份有限公司)、无水乙醇(AR,郑州派尼化学试剂厂)、叔丁醇(AR,阿拉丁工业公司)、对苯醌(AR,阿拉丁工业公司)、硝酸银(AR,西陇化工股份有限公司),盐酸四环素(biosharp赛国生物科技有限公司).实验用水为去离子水.
实验过程中使用的主要仪器有HH-S5油浴锅(金坛市亿能实验仪器厂)、真空干燥箱(上海精宏实验设备有限公司)、超静音可调气泵(广东海利集团有限公司)、磁力搅拌器(上海珂淮仪器有限公司)、TU-1901紫外可见光分光光度计(北京普析通用仪器有限责任公司)、中教金源光催化反应器等.
1.2 材料的制备与表征
根据文献[15],采用共沉淀法制备LDH/Fe3O4复合材料,在水滑石的前驱体中,加入Fe3O4洗涤烘干,可得LDH/Fe3O4复合材料.在制备Cu2O的过程中,加入一定量的LDH/Fe3O4复合材料,离心分离,水洗醇洗各三次,真空干燥,即可得到LDH/Fe3O4@Cu2O复合材料.
采用日本岛津公司的XR-3A型X线衍射仪(XRD)分析材料的晶体结构.
1.3 实验方法
实验在北京中教金源科技有限公司的光催化反应器中进行,光源为LAX500长弧Xe灯模拟可见光光源,光源外部通冷凝水冷却光源产生的热量.
光催化降解TC实验:取50 mg·L-1TC溶液200 mL,调节pH值后,加入一定量的催化剂,暗吸附60 min达到吸附解析平衡,再以500 W Xe灯作为光源进行光催化降解实验,每隔20 min取样测吸光度,TC浓度由标准曲线计算所得,降解率Re(%)的计算公式如下:
式中:Re为TC的降解率(%);Ct为t时刻的瞬时浓度(mg·L-1);C0为初始浓度(mg·L-1).
2 结果与讨论
2.1 LDH/Fe3O4@Cu2O晶体结构分析
利用XRD对复合材料的晶体结构进行分析,结果如图1所示,复合材料出现位于2θ值为29.76°,36.6°,42.51°,61.57°和73.7°处的5个衍射峰,分别对应Cu2O的(110)、(111)、(200)、(220)和(300)晶面,同时在11.52°和22.3°处出现衍射峰,对比LDH/Fe3O4的XRD,表明材料复合成功.
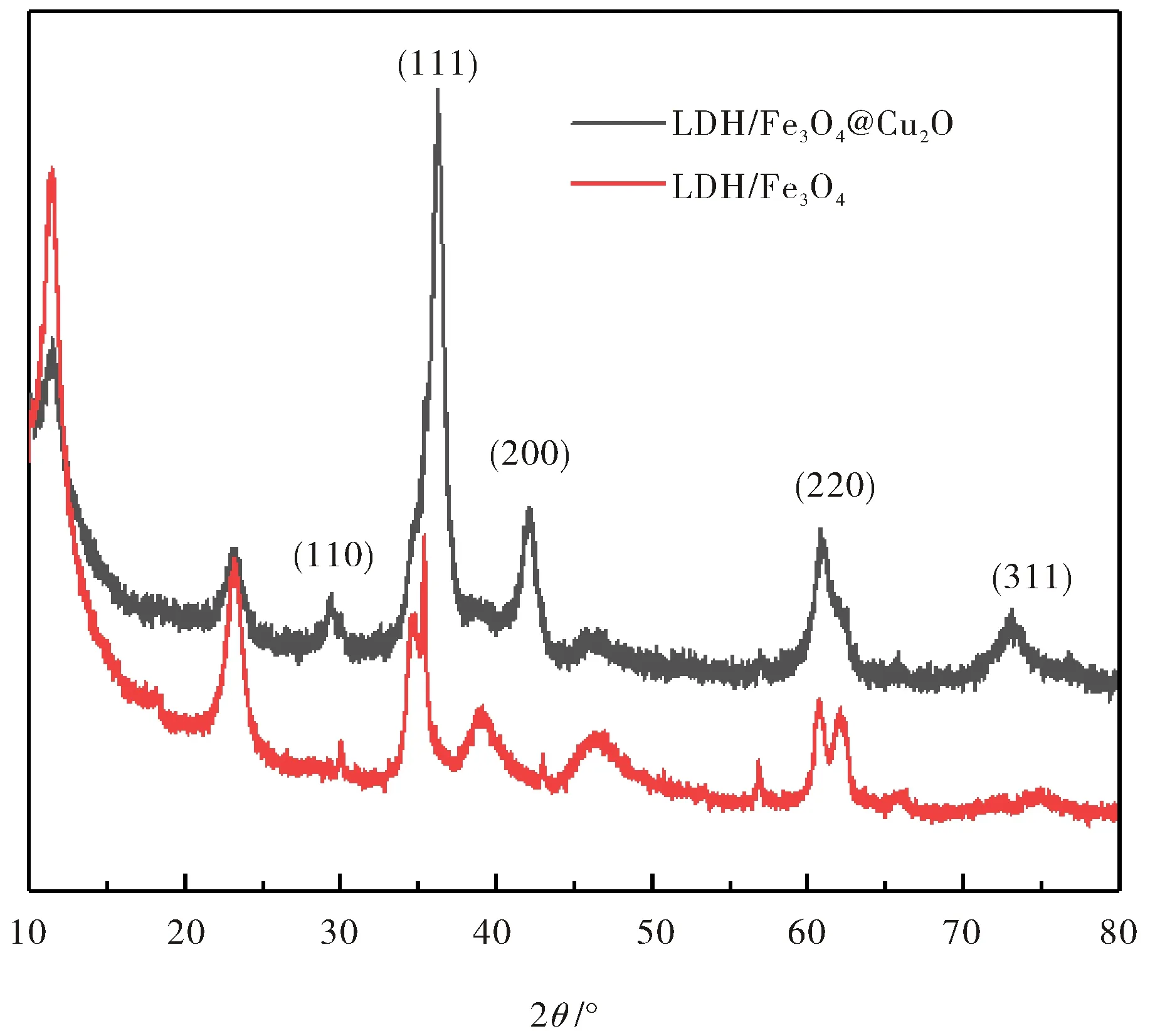
图1 LDH/Fe3O4和LDH/Fe3O4@Cu2O的XRD图Fig.1 XRD patternsofLDH/Fe3O4 and LDH/Fe3O4@Cu2O
2.2 光催化活性测试
为探究复合材料的光催化性能,在相同条件下,进行实验对比了光催化性能,如图2所示,Cu2O、LDH/Fe3O4@Cu2O对TC的去除率分别为75.57%、94.19%,且LDH/Fe3O4@Cu2O光反应40 min对TC去除率可达93.96%.复合后的材料,降低了对TC的吸附性能,提高了光催化性能,这是因为材料复合后,主要的铁位点形成Fe(II),促进反应过程中产生自由基.
2.2.1 催化剂投加量对降解TC的影响 实验考察了复合材料的投加量对光催化性能的影响,由图3可知,仅在光照条件下,TC的光解效率很低,随着催化剂投加量的增大,光催化速率得到明显提高.这是因为反应溶液中光催化剂的相对质量浓度较高,一方面TC被催化剂表面吸附,另一方面,催化剂的适当增加提供了较多的活性位点.光催化反应60 min时,0.1 g·L-1和0.25 g·L-1可以达到相同的光催化效果,但继续光催化时,0.25 g·L-1的催化活性没有继续升高,可能是光催化过程中有一部分催化剂团聚,影响光的辐射面积,使得催化剂的表面活性位点减少所致,因此,在进行光催化时,保证催化效果的前提下,应选择一个适当的投加量(0.1 g·L-1),降低成本.

图3 不同投加量对LDH/Fe3O4@Cu2O 降解盐酸四环素的影响Fig.3 Effects of different dosage to LDH/Fe3O4@Cu2O on degradation of tetracycline hydrochloride
2.2.2 光照强度对降解TC的影响 光催化剂在可见光或者紫外光下激发产生电子-空穴对,从而产生自由基,实现对污染物的降解.实验考察了光照强度对LDH/Fe3O4@Cu2O复合材料光催化效果的影响.由图4可知,通过调节电流强度改变Xe灯输出功率(0 W、300 W、500 W),随着光照强度的增加,光催化降解速率和效果得到明显提升,这主要是因为强光下,光催化剂被激发产生更多的自由基.
2.2.3 pH值对降解TC的影响 在不同pH条件下进行光催化降解实验,TC初始pH对光催化降解性能的影响如图所示.由图可以看出,在不同pH值下,复合材料对TC的吸附性能不同,因为TC具有三个电离常数值(pKa),导致TC溶液中非解离离子在催化剂表面竞争吸附的能力有所差距.光催化阶段,当初始pH 10时,降解速率最快,光照40 min去除率达到89.74%,而初始pH为4、6、8时,光照40 min去除率分别为79.82%、74.7%、81.65%,继续光照20分钟,均能达到92%以上的去除效果,但是继续升高pH至12,光催化效果显著下降.由此看来,中性条件下LDH/Fe3O4@Cu2O复合材料对TC的降解速率优于酸性和碱性,这可能是由于中性条件下催化剂表面产生大量自由基,提高了光催化的性能.

图4 不同光照强度对LDH/Fe3O4@Cu2O 降解盐酸四环素的影响Fig.4 Effects of different lightin tensity to LDH/Fe3O4@Cu2O on degradation of tetracycline hydrochloride

图5 不同pH值对LDH/Fe3O4@Cu2O 降解盐酸四环素的影响Fig.5 Effect of different pH to LDH/Fe3O4@Cu2O on degradation of tetracycline hydrochloride


图6 共存离子对LDH/Fe3O4@Cu2O 降解盐酸四环素的影响Fig.6 Effect of coexisting ions to LDH/Fe3O4@Cu2O on degradation of tetracycline hydrochloride
2.3 降解机理
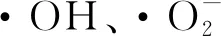

图7 不同活性基团在LDH/Fe3O4@Cu2O 降解盐酸四环素过程中的作用Fig.7 Role of different active groups in photocatalytic degradation of tetracycline hydrochloride by LDH/Fe3O4@Cu2O
3 结论

