电化学氧化法处理高氯盐氨氮废水
2020-12-28胡元娟廖春华郑晓凤马千里宋少华
胡元娟 廖春华 郑晓凤 马千里 宋少华
(深圳市深投环保科技有限公司 广东深圳 518049)
0 引言
氨氮是引起水体富营养化的主要原因,氨氮废水广泛来源于电镀线路板行业、冶炼行业、石化行业等各行业,其处理技术一直是研究热点与难点。目前市场上成熟应用的各类方法均存在各自的优缺点和适用范围[1-2],吹脱法、离子交换法和脱气膜法存在氨氮解吸液或吸收液需要进行二次处理[3-4];化学沉淀法存在污泥无出路产生二次污染问题;折点加氯法需要外加大量药剂,且存在药剂失效问题[5];生物法不适用于高盐氨氮废水的处理[6]。电化学氧化法作为一种环境友好型技术,在有机物和氨氮的去除方面均受到广泛的关注,如用于垃圾渗滤液、畜禽废水、冶炼废水的处理均取得很好的效果[7-10]。电化学氧化法尤其适用于含高氯盐氨氮废水的处理,它可直接利用废水中氯离子作为媒介产生氧化剂,进而间接氧化氨氮,具有对氨氮浓度适用范围广、处理效率高、氧化彻底、操作简单等优点[10-13]。现有相关研究主要侧重于电化学法去除氨氮效果的研究,对影响因素的全面考察,以及对能耗成本和总氮去除效果关注较少。
本文以模拟高氯盐氨氮废水为对象,研究了电流密度、极板间距、废水pH值、pH控制方式、氯离子浓度及氨氮初始浓度对电化学氧化氨氮效率的影响,同时对比了电化学氧化与漂水氧化的效果,获得了能耗成本及总氮去除效果基础数据,为该技术的工程化应用提供了参考。
1 实验原理
电化学法去除氨氮主要是通过氨氮在阳极直接氧化或间接氧化作用[10-13]。
(1)氨直接被氧化为氮气脱除

(1)
(2)氨氮的间接氧化
在阳极表面,溶液中的Cl-被氧化成Cl2,Cl2与水反应进而生成次氯酸,从而将水中的氨氮氧化使之得以去除。其反应过程式(2)~式(5):

(2)

(3)
(4)

(5)
2 实验材料与方法
实验采用电源为输出电流0~10 A,输出电压0~15 V的直流稳流电源。采用IrO2-RuO2-TiO2/Ti电极板为阳极,Ti板做阴极,阳极阴极的极板面积比例为1∶1,电极尺寸为10 cm×7.5 cm。反应器有效容积为1 L,实验水流利用磁力泵直接进行外循环。
用NH4Cl和NaCl配制模拟废水,实验废水用量为1 L,利用NaOH调节废水pH值。进行单因素实验,考察电流密度、极板间距、pH值、pH控制方式、Cl-浓度及初始氨氮浓度对电解氧化法去除氨氮和总氮的影响。氨氮分析采用离子选择电极法,总氮分析采用碱性过硫酸钾消解紫外分光光度法,pH值用雷磁pH计测定。
3 实验结果与分析
3.1 电流密度的影响
保持Cl-质量浓度8 g/L,氨氮质量浓度为500 mg/L,废水初始pH值为7.5,极板间距7 cm,分别控制电流密度为20、27、33、40 mA/cm2开始电解,每隔1 h取样测定溶液氨氮浓度,考察电流密度对电解氧化去除氨氮的影响,实验结果如图1。

图1 电流密度对电解氧化去除氨氮的影响
从图1可以看出,电流密度越大,氨氮浓度降低速率越快,完全降解相同浓度的氨氮所需时间也越短。在电流密度为20、27、33、40 mA/cm2的条件下,电解时间为4 h时溶液中氨氮质量浓度从约500 mg/L分别降至239.8、107.2、0.5、0 mg/L。当电流密度达到33 mA/cm2后,继续增大电流密度也并未减小氨氮完全降解时间,因为部分电量被电解水消耗使阳极产生氧气,阻止氯离子与电极表面接触,反而降低电流效率。另外,增大电流密度将会额外增加能耗。因此从氨氮去除速率与能耗两个方面来选择合适的电流密度为33 mA/cm2。
3.2 极板间距的影响
保持Cl-质量浓度8 g/L,氨氮质量浓度为500 mg/L,废水初始pH值为7.5,电流密度为33 mA/cm2开始电解,每隔1 h取样测定溶液氨氮浓度。分别改变极板间距为7、3、2、1 cm进行电解,考察极板间距对电解氧化去除氨氮的影响,实验结果见图2所示,能耗与极板间距的关系见图3。

图2 极板间距对电解氧化去除氨氮的影响

图3 极板间距与能耗的关系(能耗以kg氮计)
从图2可以看出,极板间距为7 cm时的氨氮降解速率明显大于间距为5 cm、3 cm和1 cm的情况,氨氮完全氧化的时间前者为4 h,后者则均为5 h。
导致这种情况的原因可能是随着极板间距的减小,阳极产生的Cl2、阴极产生的H2迁移扩散距离大大变短,使得Cl2还来不及溶于水即被H2带出导致单位时间生成的有效氯HClO减少。也可能是因为由于扩散距离的变短使得阴极生成的OH-迅速迁移至阳极被氧化生成氧气,OH-与Cl-的竞争反应使得析氯效率下降,从而导致氨氮氧化速率下降。
从图3可以看出,随着极板间距的增大,氨氮完全电解氧化的能耗也随着增加,极板间距7 cm时的能耗是1 cm时能耗的2倍。这是由于极板间距增大,极板间的电阻增大,电压增高,能耗随之增大。
因此从氨氮完全氧化时间及能耗两个方面综合考虑选择合适的极板间距为1 cm。
3.3 pH值的影响3.3.1 初始pH值的影响
保持废水氨氮质量浓度 500 mg/L,Cl-质量浓度8 g/L,电流密度为33 mA/cm2,极板间距1 cm,改变模拟废水初始pH值分别为7.5、8.5、9.0、9.5、10.0、10.5、11.0,考察废水初始pH值对电解氧化去除氨氮的影响,实验结果如图4所示,能耗与pH值的关系如图5所示。氨氮氧化过程pH值的变化情况如图6所示。
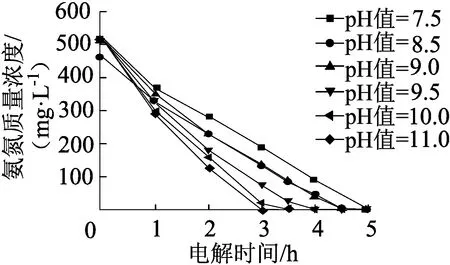
图4 废水初始pH值对电解氧化去除氨氮的影响

图5 pH值与能耗的关系(能耗以kg氮计)

图6 电解过程pH值的变化
从图4和图5可以看出,pH值对氨氮氧化速率有明显影响。随着溶液初始pH值的升高,氨氮氧化速率加快,氨氮完全电解氧化时间也减少。在pH值为7.5、8.5、9.0、9.5、10.0、11.0的条件下,溶液中氨氮质量浓度从约500 mg/L下降至0 mg/L所需时间分别为5、4.5、4.5、4、3.5、3 h。由于电解氧化时间的减少,pH值由7.5升至11.1时,1 kg氨氮完全氧化能耗也相应地由125 kW·h下降至75 kW·h。
产生上述结果的原因可以由图6进行阐述。初始pH值为7.5~9.0时,氨氮氧化以间接氧化为主,溶液pH值随着电解时间的延长而逐渐下降,这是因为在电解过程中产生的HClO在氧化氨氮的过程中生成了H+,发生如方程(3)~(5)所示的反应,H+来不及在阴极被还原而在溶液中积累,导致体系pH值下降,不仅直接抑制氨氮氧化反应,而且使得阳极析出的Cl2溶解度变低容易逸出,导致体系活性氯浓度降低,也会进一步影响氨氮的氧化速率。随着初始pH值的增加(pH值>9),溶液pH值下降变缓慢,阳极产生的氯气在溶液中的溶解度增加,产生的活性氯浓度也升高,加快了氨氮的氧化。另外当氨氮溶液呈碱性时,氨氮的去除还依靠如反应(1)所示的在电极表面的直接氧化作用,同时也不能排除在碱性条件下,有一部分NH3被电解中产生的气体带出得以去除,故而获得比中酸性条件下更好的效果。当溶液中氨氮被氧化完全时,体系仅发生阳极产氯阴极电解氢产生OH-从而pH值呈上升趋势,基本上可通过pH值的上升点来作为氨氮完全氧化的依据。
3.3.2 稳定过程pH值范围的影响
在高pH值条件下(pH值>9),废水中氨氮大部分以NH3形式存在,而电解过程阳极产生Cl2,阴极产生H2,整个过程是一个气液混合状态,氨氮可能在吹脱的作用下部分以NH3形式逸出,导致二次污染。另外,不控制pH值时,在电解过程中pH值随着电解时间的延长逐渐降低,影响氯气的溶解和HClO的生成,从而影响氨氮的降解。为了使氨氮的氧化能够达到更好的效果,实验考察了在相同碱投加量的条件下(nOH-∶nN=1∶1,pH值=11),一次加碱即直接调初始pH值与分批加碱控制恒定pH值对电解氧化去除氨氮的影响,实验结果见图7所示。

图7 恒定过程pH值与调节初始pH值对电解氧化氨氮的影响
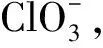
(6)
另外,分析了恒定过程pH值为7~8与初始pH值为11的条件下,电解3 h后溶液中总氮的质量浓度分别为13.3 mg/L和22.3 mg/L,由此可见,控制恒定pH值可使氨氮氧化更彻底。
综上所述,确定合适的pH值调节方式为控制恒定过程pH值为6~9。
3.4 氯离子浓度的影响
保持废水氨氮质量浓度 500 mg/L左右,电流密度为33 mA/cm2,极板间距1 cm,控制恒定pH值为6~9,改变废水Cl-质量浓度分别为4、8、10、12、16 g/L,考察氯离子浓度对电解氧化去除氨氮的影响,实验结果如图8所示。同时分析Cl-浓度与能耗关系如图9所示。

图8 氯离子浓度对电解氧化去除氨氮的影响

图9 氯离子浓度与能耗的关系
从图8和图9可以看出,随着氯离子浓度的增加,氨氮完全氧化所需时间逐渐减少,能耗也相应地降低,当Cl-质量浓度为4、8、10 g/L时氨氮完全氧化所需时间分别为4 h、3 h和2.5 h,1 kg氨氮完全氧化的能耗分别为120、75、56.3 kW·h,这说明增加氯离子有利氨氮的去除和能耗的降低。但是当氯离子质量浓度>10 g/L时,对提高氨氮的氧化速率和降低能耗的贡献不大,且过量的氯离子还会造成盐分污染。综上所述,Cl-质量浓度选择10 g/L较为合适。
3.5 氨氮浓度的影响
保持废水Cl-质量浓度10 g/L,电流密度为33 mA/cm2,极板间距1 cm,控制恒定pH值为6~8,改变废水氨氮质量浓度分别为300、500、1 000 mg/L考察氨氮浓度对电解氧化去除氨氮的影响,实验结果如图10所示。
从图10可以看出,在电流密度、Cl-浓度、pH值一定的条件下,氨氮浓度随着电解时间的变化曲线基本平行,单位时间内氨氮浓度变化趋势基本一致,这说明氨氮的氧化速率与氨氮浓度无关,只是初始氨氮浓度越高,完全电解氧化所需时间越长。

图10 初始氨氮浓度对电解氧化去除氨氮的影响
3.6 电解氧化与NaClO氧化的简单对比
保持废水Cl-质量浓度10 g/L,氨氮质量浓度500 mg/L左右,取100 mL模拟废水分别按不同比例20、40、60 L/t加入质量分数10%的NaClO溶液进行磁力搅拌反应,控制过程pH值在6~7,反应时间2.5 h。实验结果如图11所示。

图11 次氯酸钠氧化法去除氨氮
从图11可以看出,质量分数为10%的NaClO投加量为40 L/t时,氨氮质量浓度从440.5 mg/L下降至4.5 mg/L。NaClO单价以700元/t计,计算出药剂消耗成本为28元/t即1 kg氨氮完全氧化的成本64元。对比相同条件下,电解氧化法去除1 kg氨氮所需能耗为53.8 kW·h,电费以1元/(kW·h)计,则电解氧化法去除1 kg氨氮所需能耗为53.8元,再加上电解氧化法去除1 kg氨氮过程所需要投加的NaOH(nOH-∶nN=1∶1)药剂成本为8.6元,如此合计电解氧化法去除1 kg氨氮所需能耗为62.4元。由此可见,电解氧化法去除氨氮成本略低于次氯酸钠氧化法,但优势不明显。需进一步对电解氧化法在如何降低能耗成本方面进行深入研究。
4 结论
(1)电流密度、极板间距、pH值和Cl-浓度是影响电解氧化去除氨氮效果的关键因素。较高的电流密度、较宽的极板间距、高Cl-浓度和较高的初始pH值,有利于显著提高氨氮去除速率,但碱性环境将导致总氮去除率下降,宜控制反应过程在中性偏碱条件,间距越大能耗越高。电解优化条件为:电流密度33 mA/cm2,极板间距1 cm,控制过程恒定pH值为6~9,Cl-质量浓度为10 g/L,电解时间2.5 h,在此条件下,废水氨氮质量浓度从500 mg/L下降至0.2 mg/L,去除率为99.9%,此时出水总氮质量浓度为12 mg/L,总氮去除率97%。
(2)在最佳工艺参数条件下,电解氧化法去除1 kg氨氮所需能耗为62.4元,相同情况下,次氯酸钠药剂成本为64元。电解氧化法去除氨氮成本略低于次氯酸钠氧化法,但优势不明显。需进一步对电解氧化法在如何降低能耗成本方面进行深入研究。
(3)该法在稳定持续处理大量中低浓度氨氮废水时较其它方法有更多的物流成本、工艺控制优势,值得深入研究。
