利用OCTA观察糖尿病性黄斑水肿抗VEGF治疗后黄斑区血流变化 ①
2020-12-18刘晓辉崔鲲龙
秦 程,刘晓辉 , 崔鲲龙
(桂林医学院第二附属医院眼科,广西 桂林 541199)
由糖尿病引起的黄斑中心两个视盘直径范围内的视网膜增厚和硬性渗出沉积称之为糖尿病黄斑水肿(diabetic macular edema,DME),主要表现为视物模糊,严重者可致失明[1],是常见的致盲眼病之一。玻璃体腔注射抗血管内皮细胞生长因子(vascular endothelial growth factor,VEGF)抗体、视网膜光凝、糖皮质激素玻璃体腔注射等是DME的有效治疗方法[2-3]。大部分抗VEGF药物能够明显抑制新生血管和减轻黄斑水肿,使患者获得较好的视力,抗VEGF药物已成为DME的一线治疗药物。以往对DME患者视网膜血管的检查主要依靠荧光素眼底血管造影(fundus fluorescein angiography,FFA),但是因其操作有创、静脉使用造影剂存在过敏、甚至是过敏性休克等严重并发症的发生,在临床应用中有一定的局限性。光学相干断层扫描血管成像(optical coherence tomography angiography,OCTA)作为一种新兴的安全无创、快速、高分辨率的眼底血管成像技术,不仅能定性分析视网膜血管形态特征,更能定量的测量眼底血管及血流灌注情况,同时还能对病变深度进行评估。
观察DME患者抗VEGF治疗的疗效及治疗后黄斑区微循环改变情况,利用光相干断层扫描(OCT)、OCTA对最佳矫正视力(best corrected visual acuity,BCVA)、黄斑区血流密度(vessel density,VD)、黄斑中心凹视网膜厚度(central macular retinal thickness,CMT)进行定量分析,利用OCTA观察DME图像特征,阐明OCTA的临床应用价值。
1 资料与方法
1.1 一般资料
收集2019年1~12月在本院就诊并确诊为重度非增殖型糖尿病视网膜病变(NPDR)的患者,同时合并有黄斑水肿,共30例49只眼。男16例(27只眼),女14例(22只眼),年龄35~70岁,平均(57.9±12.8)岁。本项目在医院伦理委员会批准许可下进行,所有研究对象均签署知情同意书。
1.2 入选标准
纳入标准:①经FFA、OCT检查诊断为DME并且需要抗VEGF治疗的患者。②患眼最佳矫正视力均>0.1,屈光不正<±6 D。③Goldmann压平式眼压测量<21 mmHg。④血糖≤11.0 mmol/L,血压<140/90 mmHg。⑤依从性好、坚持随访者。⑥OCTA影像扫描质量值≥4。
排除标准:①因中心性浆液性脉络膜视网膜病变、视网膜静脉阻塞、葡萄膜炎等引起黄斑厚度改变的疾病。②既往接受过眼部治疗者。③屈光间质混浊影响检查者。④全身或局部使用含有影响血流的药物,凝血异常者。⑤对造影剂(荧光素钠)过敏者。⑥OCTA影像扫描质量值<4。⑦有全身心脑血管疾病、年老体衰不适合检查、手术者。
DME诊断标准按照ETDRS推荐“临床有意义的黄斑水肿诊断标准(clinically significant macular edema,CSME)”[4],应具备以下情况≥1项:①视网膜增厚位于距黄斑中心凹500 μm范围或以内区域。②眼底见硬性渗出及邻近视网膜水肿增厚区距黄斑中心凹500 μm以内。③至少有一个视盘直径范围的视网膜水肿增厚,且有部分病变发生于距黄斑中心凹一个视盘直径的范围内。根据OCT形态学将DME分为3型[5]:视网膜弥漫性增厚(diffuse retinal thickening,DRT)型、黄斑囊样水肿(cystoid macular edema,CME)型和浆液性视网膜脱离(serous retinal detachment,SRD)型。
1.3 检查方法
所有入组者均行最佳矫正视力、眼压、裂隙灯显微镜、眼底照相、OCT、OCTA检查,由专门负责检查的同一医师完成受试者的所有检查,2名资深眼底病专家阅片。OCTA检测利用德国海德堡的spectralis OCT,扫描范围是黄斑区3 mm×3 mm部位,受试者被检查眼需注视前方目镜蓝色光线直到检查结束,尽量避免眼部和头部的移动,通过系统自带软件完成图像结果获得视网膜脉络膜分层血流图像,对黄斑区视网膜浅层血流图像进行分析。入组者受检眼测量指标为:BCVA、VD、CMT。利用OCT、OCTA对数据进行定量分析。
1.4 抗VEGF治疗
由同一医师在眼科手术室按无菌手术操作规范完成所有患者玻璃体腔注射。根据患者意愿选择抗VEGF药物(康柏西普注射液和雷珠单抗注射液)。
1.5 统计学方法
2 结果
2.1 不同类型DME的OCTA及OCT图像特征
弥漫增厚型DME:OCT主要表现为神经上皮层间不同程度增厚,其间可伴有点状高反射信号;OCTA主要表现为黄斑拱环结构的破坏、黄斑区血流密度下降、部分无灌注区的出现。黄斑囊样水肿型DME:OCT主要表现为神经上皮层间大小不等的囊腔样增厚;OCTA主要表现为黄斑中心凹无灌注面积增大、黄斑区血流密度下降、静脉迂曲扩张、大量微血管瘤等。浆液性视网膜脱离型DME:OCT主要表现为神经上皮层的脱离,伴视网膜下液,也可伴神经上皮层间囊腔样水肿;OCTA表现类似黄斑囊样水肿型DME。详见图1。
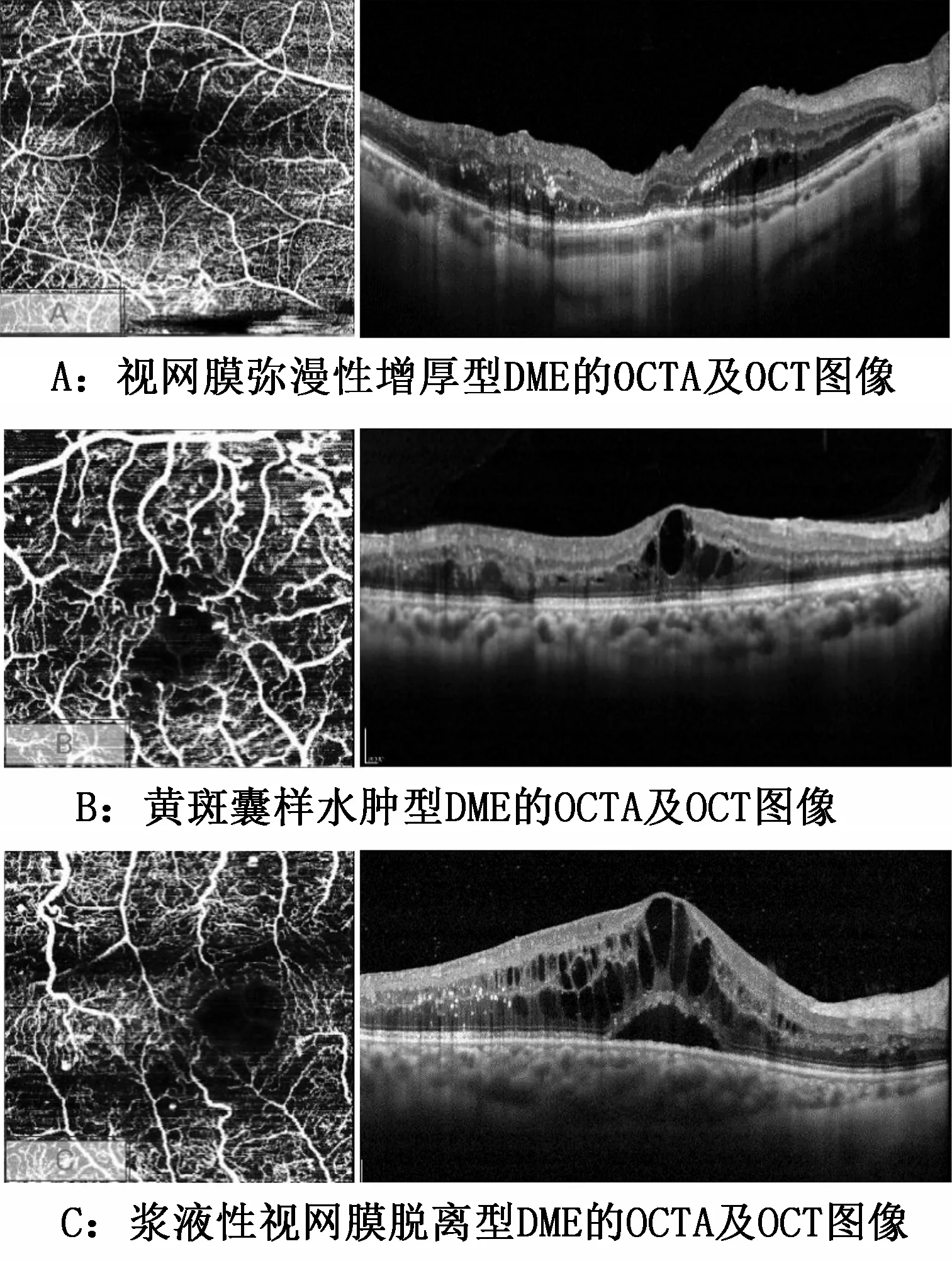
图1 不同类型DME的OCTA及OCT生成的黄斑区图像
2.2 DME抗VEGF治疗前后BCVA、CMT及黄斑区血流密度比较
DME患者抗VEGF治疗后BCVA改善明显,治疗前后差异有统计学意义(P<0.05);治疗前后黄斑区血流密度变化不明显,差异无统计学意义(P>0.05);治疗前后黄斑水肿减轻、CMT变薄,差异有统计学意义(P<0.05)。但是,BCVA、CMT以及黄斑区血流密度治疗后1周与治疗后1个月相比较,改善不明显,差异没有统计学意义(P>0.05)。详见表1。
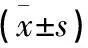
表1 DME患者BCVA、CMT及黄斑区血流密度比较
3 讨论
近年来,DME的发病率逐年上升,相关调查研究显示我国DME发病率高达35.6%,已成为20~74岁年龄段致盲的主要原因之一,严重影响了患者的视功能和生活质量[6]。研究发现DME患眼玻璃体内VEGF水平明显升高,且高于血管内水平[7]。目前公认的DME发病的主要机制是VEGF通过增加血管通透性引起血-视网膜屏障破坏,视网膜微血管渗漏,致黄斑区内层视网膜液体积聚[8]。多项研究证实,抗VEGF治疗DME效果显著,文章研究也发现DME患者经抗VEGF治疗后BCVA、CMT较治疗前变化显著,黄斑区血流密度变化不大,没有统计学意义。上述结果与以往研究结论一致。
本研究旨在探讨OCTA在观察DME抗VEGF治疗前后黄斑区血流变化中的应用价值,证实了玻璃体腔注射抗VEGF药物可明显改善黄斑水肿,使视力提高。进一步证实了BCVA、VD、CMT可作为评估抗VEGF治疗疗效的敏感指标。本研究收集的DME病例大部分为浆液脱离型DME,因黄斑区血流密度明显下降、黄斑中心凹无灌注区面积扩大等原因,使得黄斑区明显缺血,抗VEGF治疗后视网膜下液吸收、神经上皮层复位、层间水肿消退,但是与以往研究相比较抗VEGF治疗后BCVA提高不是特别理想,估计与上述原因有关。OCTA在定量分析DME患者黄斑区血流密度在抗VEGF治疗前后变化不明显,说明抗VEGF不会加重黄斑区缺血情况,眼内注射治疗安全有效;同时OCTA可清晰呈现黄斑区微循环改变情况,如黄斑中心凹无灌注面积、黄斑区血流密度、无灌注区等改变情况,同时可明显呈现静脉迂曲扩张、大量微血管瘤等特征性改变。本研究中,OCT在定量评估CMT方面优势显现,因此可以根据具体临床问题联合应用OCTA及OCT,可起到事半功倍的效果。
抗VEGF治疗DME的效果是肯定的。利用OCTA观察视网膜黄斑区血流变化情况,可以清晰观察拱环结构的改变、血流密度的下降(抗VEGF治疗前后血流密度变化无统计学意义)、无灌注区面积的扩大,以及可以清晰地观察到微血管瘤。大部分学者通过研究证实抗VEGF治疗并没有加重DME患者视网膜毛细血管的闭塞。Falavarjani等[9]观察13眼DME和5眼视网膜中央静脉阻塞引起的黄斑水肿,在眼内单次注射抗VEGF后,应用OCTA观察浅层视网膜层、深层视网膜层及内层视网膜层的中心凹血管密度,发现治疗前后中心凹和旁中心凹视网膜毛细血管密度变化不明显。这些结论也与DME患者抗VEGF治疗后未引起 FAZ 面积及无灌注区面积明显变化一致[10]。综上所述,OCTA技术在观察糖尿病病变患者黄斑区血流变化中具有图像清晰、获得数据可进行定量分析等突出优势。BCVA、VD、CMT可作为评估抗VEGF治疗疗效的敏感指标。
本研究不足:①未按照DME的分类分析抗VEGF治疗的疗效。②抗VEGF药物未分类分析疗效。③样本量小,随访时间短。④抗VEGF药物作用时间较短,如不配合激光等治疗,DME可能会反复发作,未来需要利用OCTA观察进一步联合激光治疗的远期疗效。
