胆道发育不良患儿的临床病理特点及其预后影响因素分析
2020-12-17吴宙光王斌程珍张文杰叶泳钦郑佳辰
吴宙光,王斌,程珍,张文杰,叶泳钦,郑佳辰
深圳市儿童医院普外科,广东深圳 518026
胆道发育不良(biliary dysplasia,BD)是一种由肝内外胆管发育异常引起的胆汁淤积性疾病,常伴随进行性肝内小胆管损坏,从而导致胆汁入十二指肠减少和肝内胆汁淤积,病理学表现为肝内胆管数与汇管区胆管数比例明显下降[1-2]。胆汁淤积性疾病的发生主要与代谢性疾病、病毒感染、中毒、胆管发育异常、胆汁分泌功能下降、基因异常等有关[1,3-4]。 婴幼儿胆道发育不良若不能得到有效治疗,常会导致胆汁淤积和胆道闭塞,发生肝纤维化和肝硬化,甚至肝衰竭[1,3,5]。在药物治疗的基础上,常需行胆囊造瘘及胆道冲洗引流等外科手术治疗,发生肝衰竭时甚至需行肝移植治疗[1,3,5-6]。目前关于BD患儿临床病理特点及其预后影响因素的研究较少。本研究旨在探讨BD患儿的临床病理特点及其预后不良的影响因素,以期为指导BD的精准个性化治疗提供依据。
1 资料与方法
1.1 研究对象 选取2014年1月-2019年1月深圳市儿童医院普外科收治的BD患儿32例,收集患儿的一般资料(包括年龄、性别、出生体重、母亲生产方式、出现黄疸时间、尿液颜色、大便颜色、肝脾大情况、腹水情况、伴随疾病情况、肝肾功能、手术日龄、胆道造影情况、用药情况),以及术中胆道造影和术后肝组织病理学资料。纳入标准:符合BD诊断标准[肝活检示肝小叶间胆管缺乏,即胆管数与汇管区比例<0.5,胆管造影示肝外胆管显影纤细(≤2 mm),肝内胆管显影细微且不清晰,肠道有造影剂渗入,临床表现为进行性加重的梗阻性黄疸]。排除标准:胆道造影显示为其他原因引起的胆汁淤积性肝病、胆道闭锁或诊断不明。本研究通过深圳市儿童医院伦理委员会批准。
1.2 治疗方法 所有患儿均进行药物(保肝药、肝酶诱导剂、利胆药)治疗及蓝光照射治疗,药物治疗无明显好转且大便颜色浅、肝功能持续性损害的患儿进行外科手术治疗(胆囊造瘘、胆道冲洗),术后予以抗生素、保肝药、利胆药、激素、丙种球蛋白等治疗,所有患儿手术顺利,无明显并发症发生。
1.3 肝组织病理学观察 术后采用肝穿刺针取少量肝右叶前缘组织,用10%多聚甲醛固定后于4 ℃冰箱保存。所有患儿肝穿刺术后无明显出血情况。
1.3.1 HE染色 肝组织切片后行HE染色,倒置显微镜下观察胆汁淤积、胆栓形成、炎性细胞浸润、肝纤维化、肝细胞变性等情况。
1.3.2 免疫组化染色 肝组织切片后行免疫组化染色,先在枸橼酸盐缓冲液中修复抗原10~15 min,P B S 洗涤后,在1 0%山羊血清中封闭,加入一抗[EMA(ab70475,英国Abcam公司,稀释倍数1:1000)、CK19(ab7754,英国Abcam公司,稀释倍数1:1000)]4 ℃孵育过夜,孵育二抗(HRP标记山羊抗小鼠二抗ZB-2305,北京中杉金桥生物技术有限公司,稀释倍数1:5000),DAB显影10 min,苏木素/ 伊红(HE)复染,漂洗、封片,显微镜下观察。高倍镜下采用病理图像分析系统对组织病理结果进行判定,组织中出现棕黄色或棕褐色为相应的上皮膜抗原(EMA)、细胞角蛋白19(CK19)表达阳性。在表达阳性的部位各取5~10个不同视野,采用IPP图像分析系统测定EMA和CK19蛋白的平均光密度值(AOD)。AOD为阳性细胞的光密度值与阳性细胞总面积的比值。
1.4 观察指标 术后随访至2020年4月,观察患儿肝功能[主要包括谷丙转氨酶(ALT)、谷草转氨酶(AST)、总胆红素(TBIL)、直接胆红素(DBIL)、碱性磷酸酶(ALP)、γ-谷氨酰转移酶(γ-GT)等指标]、黄染情况、营养状况、身高、体重、肝纤维化程度等预后情况。根据预后情况分为预后良好组与预后不良组,其中预后良好指术后6个月内迅速退黄(TBIL≤20 μmol/L),患儿营养状况、生长发育良好;预后不良指术后6个月内未退黄(TBIL>20 μmol/L),患儿营养状况、生长发育不良,伴有并发症甚至死亡。
1.5 统计学处理 采用SPSS 19.0软件进行统计分析。计数资料以频数(%)表示,组间比较采用χ2检验;正态分布的计量资料以±s表示,非正态分布的计量资料以中位数表示,组间比较采用t检验或秩和检验。采用logistic回归分析BD患儿预后不良的影响因素。P<0.05为差异有统计学意义。
2 结 果
2.1 BD患儿临床病理特点分析 32例BD患儿中男19例,女13例,多为剖宫产足月儿(68.8%,22/32);出生体重0.85~6.20(2.68±1.06) kg,处于正常范围;出现黄疸时间(31.5±7.2) d;主要伴有尿色深(62.5%,20/32)、大便颜色浅黄(90.6%,29/32)、肝脾大(59.4%,19/32)及轻度腹水(40.6%,13/32)等症状;常伴有先天性心脏病(25.0%,8/32)等疾病;病毒感染以巨细胞病毒(56.3%,18/32)为主(表1)。
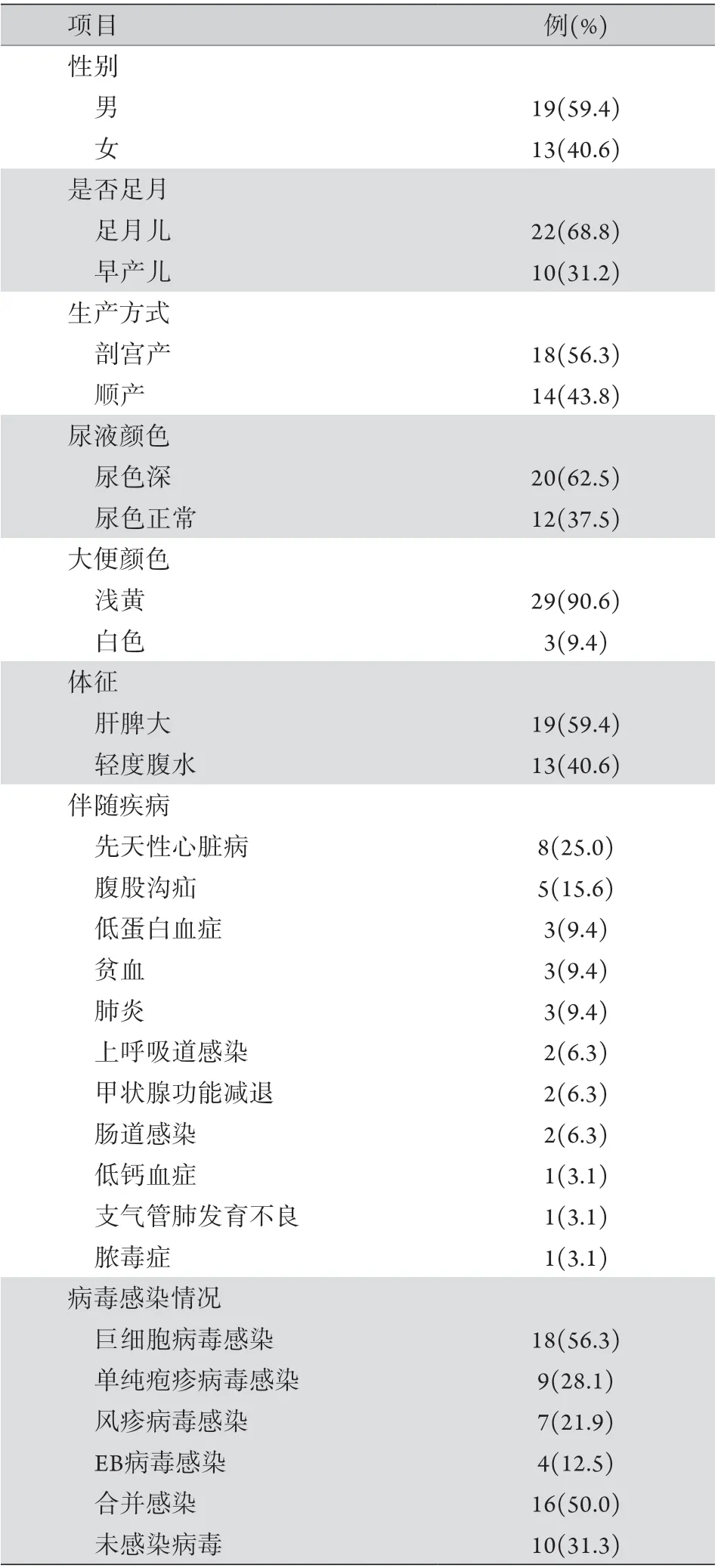
表1 BD患儿临床病理特点(n=32)Tab.1 Clinicopathological features of children with BD (n=32)
2.2 BD患儿胆道造影及肝组织病理学特点分析 胆道造影结果显示,所有BD患儿胆囊及胆管显影,肝内胆管纤细,其中11例为肝外胆管纤细,6例为胆囊发育不良。BD患儿手术日龄为30~125(82.5±36.2) d,肝组织病理学表现为胆汁淤积、胆栓形成、肝小叶间胆管及汇管区胆管减少或消失、炎性细胞浸润、肝细胞变性、点状坏死、不同程度肝纤维化、肝内胆管增生,并伴有EMA、CK19阳性表达(图1)。其中炎性细胞浸润25例,肝细胞变性16例(水样变性9例,空泡样改变6例,纤维样变1例),点状坏死11例,肝纤维化10例(Ⅰ级7例,Ⅱ级3例)。有5例患儿进行了基因检测,其中2例为JAG1基因突变的Alagille综合征患儿,余3例基因检测阴性。
2.3 BD患儿随访情况及预后不良影响因素分析 术后随访14~74个月,中位随访时间50个月,其中20例预后良好(6个月内退黄,无明显并发症发生),12例预后不良(10例6个月未退黄,5例出现术后肝功能损害等并发症,3例术后皮肤瘙痒伴发育迟缓,2例贫血,2例死亡),所有患儿均未进行肝移植治疗。以手术日龄、性别、出生体重、母亲生产方式、出现黄疸时间、尿液颜色、大便颜色、肝脾大、腹水情况、伴随疾病情况、肝肾功能指标、病理学检测结果为自变量,是否发生预后不良为因变量进行单因素logistic分析显示,与预后良好组比较,预后不良组手术日龄,肝脾大、腹水、肝细胞变性、肝纤维化比例,TBIL水平以及EMA、CK19的表达水平明显升高,差异有统计学意义(P<0.05,表2);将P<0.1的因素纳入多因素logistic回归分析,结果显示,手术日龄、肝纤维化、TBIL及EMA、CK19的表达为BD患儿预后不良的影响因素(P<0.05,表3)。
3 讨 论
BD是肝内或肝外胆道发育不良引起的进行性胆汁淤积性疾病,常被误诊为胆道闭塞。研究发现,BD是形成胆道闭锁的一个中间阶段,而胆管纤细可能会造成肝脏胆汁淤积,引起肝纤维化和肝硬化,甚至肝衰竭[1,3,7]。BD可分为综合型和非综合型两类,其中综合型小叶间胆管缺乏又名Alagille综合征,临床表现为心脏杂音、特殊面容、慢性胆汁淤积、角膜后胚胎环及蝴蝶椎骨等[1,8];非综合型小叶间胆管缺乏主要表现为无胆汁性粪便、黄疸,部分患儿可伴有先天性发育畸形,其发生主要与先天发育不良、胆道损伤后造成的胆道萎缩有关,病因多与染色体异常、代谢遗传相关[1,5]。
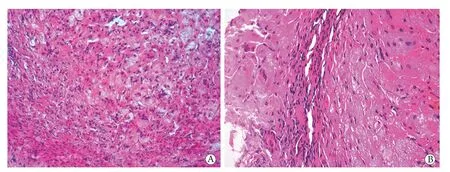
图1 BD患儿肝组织病理学特点Fig.1 Histopathological features of liver biopsy in children with BD

表2 BD患儿预后不良影响因素的单因素logistic回归分析Tab.2 Univariate logistic regression analysis of the adverse factors affecting prognosis in children with BD
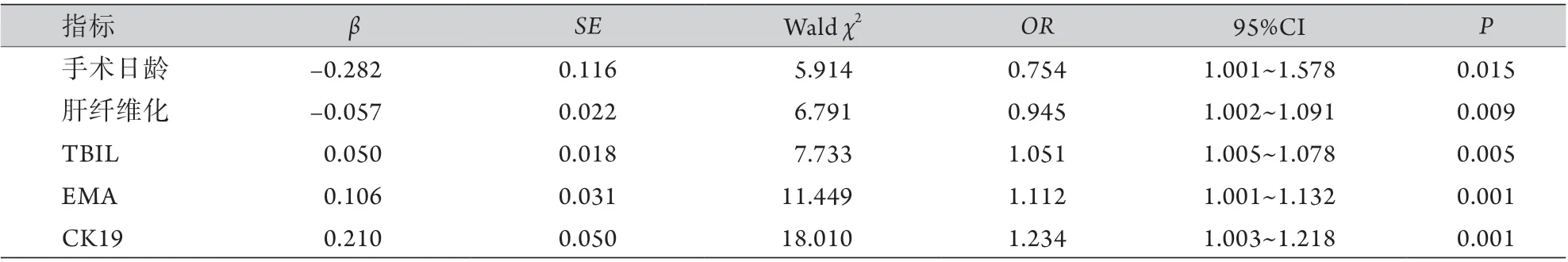
表3 BD患儿预后不良影响因素的多因素logistic回归分析Tab.3 Multivariate logistic regression analysis of the adverse factors affecting prognosis in children with BD
本研究分析32例BD患儿的临床病理特点发现,男性患儿多于女性,多为剖宫产足月儿,出生体重正常,出现黄疸时间(31.5±7.2) d,伴有尿色深、大便颜色浅、肝脾大及轻度腹水等症状,常伴有先天性心脏病等疾病,且巨细胞病毒感染多见,这与既往研究结果较为一致[1,3,6-7],表明BD是一种进行性胆汁淤积性疾病,可出现梗阻性胆汁淤积,同时伴随多系统的损害,与病毒感染或免疫介导的损伤以及疾病的发生发展有关[3]。
BD患儿胆道造影可见肝内及肝外胆管纤细,胆囊发育不良,符合胆道系统的解剖学和病变特点。胆道纤细和胆囊发育不良易引起胆汁淤积。对于BD患儿常规行Kasai手术的效果并不显著,术后可能出现感染、吻合口漏等风险,而采用胆道造瘘和引流手术配合利胆等药物治疗,可明显减轻胆汁淤积性肝损害,尽可能减轻肝纤维化的程度以预防肝硬化的发生[1,9-10]。本研究中BD患儿手术月龄主要为2~4个月,表明早期手术治疗能有效减轻肝脏进行性损害的程度。本研究肝活检病理学观察发现,BD患儿肝小叶间胆管及汇管区胆管减少或消失、胆汁淤积、胆栓形成、炎性细胞浸润、肝细胞变性、点状坏死、不同程度肝纤维化、肝内胆管增生,表明胆管缺乏会造成胆管系统处于高浓度胆汁酸中,反应性地造成胆管细胞和肝细胞变性损伤,触发炎性细胞浸润,导致肝纤维化的发生[5]。既往研究发现,大龄BD患儿(≥180 d)可出现进行性小叶间胆管数量减少或消失,肝内胆管增生和不同程度的胆汁淤积,且大龄组患儿较小龄组患儿肝纤维程度加重,表明小叶间胆管数量进行性减少可刺激肝内胆管增生等损伤修复反应[5]。本研究尚未对肝内胆管增生程度进行分析比较,今后需扩大样本进一步探讨。肝组织EMA、CK19免疫组化染色可提示肝内胆管减少或缺如的程度,与肝脏损伤程度相关[5,11]。此外,BD发病可能与基因变异相关,本研究通过基因检测发现2例与JAG1基因突变相关的Alagille综合征患儿,是综合型胆道发育不良的基因诊断,此类患儿的病变多累及肝内外胆管,渐进性出现胆道闭锁,最终发展为肝纤维化[12-13]。此外,有研究发现,部分BD患儿与NOTCH2基因突变有关[14-15],但本研究并未检测到,今后需扩大样本量进一步研究。
本研究在预后分析中发现,手术日龄、肝纤维化、TBIL及EMA、CK19表达是BD患儿预后不良的影响因素。分析其原因如下:BD是一种进展性肝脏损害性疾病,手术日龄增加、胆汁淤积程度加重、TBIL表达量增加均会持续加重肝纤维化程度甚至引起肝硬化,与预后不良相关;而预后不良患儿常常出现胆汁淤积、皮肤瘙痒、营养状况缺乏和生长发育受限等,这可能主要与肝脏损害引起肝酶、维生素等合成及分泌障碍有关[16],而肝组织中EMA、CK19的表达量可反映肝损伤程度,其表达量增加多提示预后不良[5,11]。
综上所述,BD患儿存在典型的临床病理特点和胆道影像学特征,而手术日龄、肝纤维化、TBIL及EMA、CK19的表达是其预后不良的影响因素。今后仍需扩大样本进一步研究证实,以期为BD的诊断和治疗提供依据。
