金属有机骨架-碳点纳米电化学发光体用于尿酸的灵敏检测
2020-12-14赵莉丹
赵莉丹,刘 伟,卓 颖
(西南大学化学化工学院,重庆400715)
0 前言
尿酸(Uric Acid,UA)具有清除氧自由基、维持机体免疫功能、对抗氧化应激的作用,人体血液中UA含量异常会导致肾结石、痛风性关节炎和心血管疾病[1]。因此,人体中UA的含量监测对人体的身体健康至关重要。电化学发光(Electrochemiluminescence,ECL)是指发光体在电极表面经历电化学反应过程,生成激发态物质,其以光辐射的形式回到基态的一种现象。电化学发光生物传感器结合ECL技术和生物识别策略,具有灵敏度高、线性响应范围广、背景干扰低[2]等特点,在现代化学分析、药物分析、环境监测、生物分析等方面蓬勃发展。
碳点(Carbon dots,CDs)作为一种新型的纳米材料,因其具有的小尺寸、低细胞毒性、生物相容性好等特点[3]而受到越来越多的关注。然而,由于CDs的界面固载效率低,使得构建以CDs为发光体的固态ECL生物传感器仍具挑战[4]。据文献报道,在CDs溶液中加入1.0%壳聚糖(Chitosan,CS)溶液,形成的CDs-CS复合膜能有效提高CDs在玻碳电极上的固载效率,增强了CDs的ECL响应信号[5]。沸石咪唑酯骨架结构材料ZIF-8(Zeolitic Imidazole Framework-8)是被研究最多的MOF之一,其由锌离子和2-甲基咪唑(Hmlm)配体组成,在pH高于7的水相中具有很高的稳定性[6]。有研究报道了利用富含纤维素的玉米芯残基作为支架,原位锚定制备Ag NPs修饰的ZIF-8纳米复合材料,通过“茶包”策略制备了具有强的吸附催化性能和抗菌活性的多功能生物吸附剂Ag NPs@ZIF-8[7]。基于此,该工作以ZIF-8作为CDs的载体,通过原位生长包埋法制备了金属有机骨架ZIF-8固载的CDs复合纳米材料,并以此作为发光体构建了电化学发光生物传感器,用于UA的高灵敏检测。
首先,采用溶剂热法,以鲁米诺(Luminol)和二硫代二苯甲酸(DTSA)为原料,合成了硫原子掺杂的碳点(CDs)。然后,在含有CDs的溶液中合成金属有机骨架ZIF-8,使得大量CDs在ZIF-8生长成型的过程中负载于ZIF-8框架上,合成了具有强ECL信号的CDs@ZIF-8复合纳米材料。基于UA能够有效猝灭CDs@ZIF-8/溶解氧ECL体系的响应信号,构建了一个“ON-OFF”型的ECL生物传感器,并研究了其对UA检测的线性响应范围、选择性和稳定性。
1 实验部分
1.1 实验仪器与试剂(表1、表2)

表1 研究使用的实验仪器Tab.1 The list of apparatus used in this study

表2 研究使用的试剂Tab.2 The list of reagants used in this study
采用标准三电极体系检测ECL信号,用铂丝电极为对电极、Ag/AgCl电极(含饱和KCl溶液)为参比电极,玻碳电极(GCE,Φ=4 mm)为工作电极。
1.2 CDs的合成
首先,称量0.0266 g Luminol和0.0460 g DTSA溶于10 mL冰乙酸中,对此混合溶液进行2 h的超声处理,直至溶液分散均匀。然后将此混合溶液转移到高压反应釜(聚四氟乙烯)中,并将其置于烘箱中(180℃)反应10 h。待溶液冷却至室温后,将此溶液进行离心处理(11000 r/min,10 min),多次离心直至完全去除棕黄色沉淀物。取离心后的棕色溶液进行透析(3500 Da,24 h),透析后的CDs溶液置于4℃冰箱中保存。
1.3 CDs@ZIF-8的合成
根据已报道的方法,首先合成ZIF-8[8],用分析天平称取0.2000 g的2-甲基咪唑和0.0880 g Zn(NO3)2·6H2O溶于5 mL上述制得的溶液,搅拌12 h(500 r/min),并于室温下静置24 h。静置完成后离心(8000 r/min,10 min)分离,随后用去离子水多次离心洗涤沉淀(8000 r/min,10 min),最后60℃真空干燥8 h,得到白色的纳米复合材料CDs@ZIF-8共0.0609 g。将此粉末平均分为5份,每份0.0122 g,依次分散在含1至5 mL去离子水中,获得质量浓度依次为12.20 mg/mL、6.10 mg/mL、4.07 mg/mL、3.05 mg/mL、2.44 mg/mL的CDs@ZIF-8溶液,超声均匀后于4℃冰箱中保存。
1.4 传感器的制备和检测过程
首先,对玻碳电极(GCE)进行抛光打磨,用蒸馏水、乙醇交替超声清洗。滴加3μL上述质量浓度为4.07 mg/mL的CDs@ZIF-8溶液在打磨干净的电极上,于37℃烘箱中烘15 min,得到UA生物传感器(CDs@ZIF-8/GCE)。ECL的检测底液为2 mL含有不同UA浓度的PBS(0.1 mol/L,pH7.4),运用MPI-E型电化学发光分析仪进行ECL信号的测定。设置扫描电压为-0.6V~0.7V,光电倍增管(PMT)高压设置为800 V,放大级数为3,灵敏度为1×10-4,扫描速率为0.3 V/s。图1为UA电化学发光生物传感器的制备过程及响应机制示意图。

图1 UA电化学发光生物传感器的制备过程及响应机制示意图Fig.1 Schematic diagram of preparation and response mechanism of the ECL biosensor
2 结果与讨论
2.1 材料的TEM表征
通过透射电子显微镜(TEM)对CDs和ZIF-8的形貌进行表征。如图2(A)所示,CDs呈现良好的单分散性,且没有明显的聚集。图2(B)可以观察到球形CDs的粒径较为均一,其粒径平均约为3.75 nm;图2(B)插图展示了CDs的晶格条纹间距为0.24 nm。ZIF-8的形貌表征如图2(C)所示,可以看到ZIF-8呈现良好的十二面体结构,且粒径大小比较均一,与文献报道一致[9]。

图2 (A)、(B)CDs和(C)ZIF-8的TEM表征图Fig.2 TEM images of(A)、(B)CDs and(C)ZIF-8
2.2 材料的光学性质
CDs@ZIF-8的UV-vis吸收光谱如图3所示,在208 nm、251 nm、297 nm、340 nm处均有吸收峰,其中208 nm的极强吸收峰和251 nm的肩峰来源于CDs中sp2C=C双键的π-π*跃迁;297 nm和340 nm的吸收峰主要源自于CDs表面态酰肼基团的n-π*跃迁,这与文献报道一致[10]。

图3 CDs@ZIF-8的紫外可见光谱图Fig.3 The Ultraviolet Visible spectrum of CDs@ZIF-8
复合材料CDs@ZIF-8的荧光光谱如图4(A),可以发现当CDs@ZIF-8在363 nm的激发下,CDs@ZIF-8的最强荧光发射峰位于421 nm。通过图4(B)可知,CDs@ZIF-8的ECL发射峰位于424 nm,与荧光发射峰波长基本一致[11]。
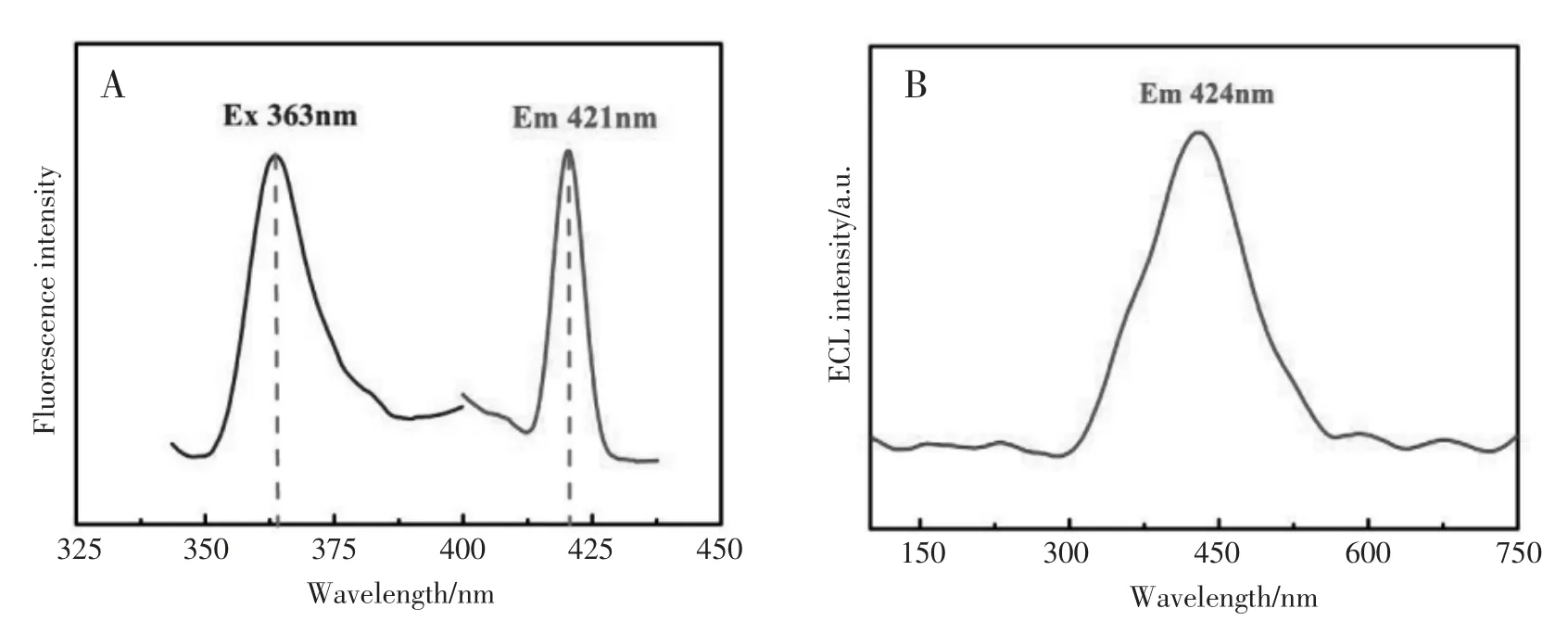
图4 CDs@ZIF-8的(A)荧光光谱图(B)ECL光谱图Fig.4 (A)Ultraviolet Visible and(B)Fluorescence spectrum of CDs@ZIF-8
2.3 分析条件的优化
为了对传感器的最佳分析条件进行优化,探究了不同的扫描电压以及不同浓度的CDs@ZIF-8溶液对ECL信号的影响。滴加3μL质量浓度为4.07 mg/mL的CDs@ZIF-8溶液于电极上,在37℃烘箱中烘15 min后,选择不同的电压范围进行ECL信号的测定。如图5(A)所示,可以看出在-0.6 V~0.7 V时材料具有较强的ECL信号和较好的峰形,因此,将-0.6 V~0.7 V确定为材料的最佳扫描电压。
此外,还对CDs@ZIF-8浓度进行了优化。如图5(B)所示,CDs@ZIF-8溶液为质量浓度4.07 mg/mL时的ECL响应信号最强,当材料的质量浓度为6.10 mg/mL和12.20 mg/mL时,此时的CDs@ZIF-8溶液浓度较高,推测纳米复合材料容易发生团聚,导致此浓度下的材料颗粒尺寸较大,因此ECL信号显著下降。当浓度低于4.07 mg/mL时,即质量浓度为3.05 mg/mL、2.44 mg/mL时,ECL信号随材料浓度降低而降低,故选择CDs@ZIF-8质量浓度为4.07 mg/mL为最佳实验条件。
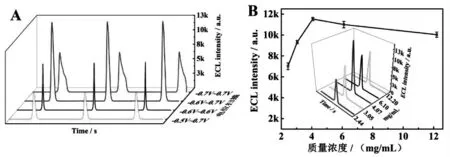
图5 CDs@ZIF-8的扫描电压(A)和浓度(B)的优化Fig.5 Optimization of scanning voltage(A)and the centration(B)of CDs@ZIF-8
2.4 传感器对UA的ECL响应
如图6(A)所示,实验表明,随UA浓度的增加CDs@ZIF-8修饰电极的ECL信号逐渐降低。并且,如图6(B),ECL信号的变化值(△I)与UA浓度的对数值在5.0×10-9mol/L至1.0×10-4mol/L浓度内呈线性关系,利用Origin软件拟合出△I与lg cUA的关系为:△I=1587.2 lg cUA+4115.2,R=0.9971。根据3σ规则[12],计算出该传感器的检测限为5.4 nmol/L。

图6 (A)传感器对不同浓度UA的ECL响应曲线(底液为0.1 mol/L PBS,pH7.4),从a到f UA的浓度分别为5.0×10-9 mol/L,5.0×10-8 mol/L,5.0×10-7 mol/L,5.0×10-6 mol/L,5.0×10-5 mol/L,1.0×10-4 mol/L.(B)ECL信号的变化值(△I为ECL信号与空白信号的差值)与UA浓度的对数值的线性关系Fig.6 (A)ECL response curves of the sensor to different concentrations of Uric Acid(base solution is 0.1 mol/L PBS,pH7.4)from(a)to(f):(5.0×10-9 mol/L,5.0×10-8 mol/L,5.0×10-7 mol/L,5.0×10-6 mol/L,5.0×10-5 mol/L,1.0×10-4 mol/L)respectively and(B)The linear relationship between the change value of ECL signal(△I is the difference between ECL signal and blank signal)and the log value of Uric Acid concentration
2.5 ECL生物传感器的选择性和稳定性
为了进一步验证所制备的生物传感器对UA的响应是否具有特异性,选择了几种可能对UA的检测产生干扰的物质:尿素(Urea)、葡萄糖(Glu)、精氨酸(Arg)和L-组氨酸(L-His)。如图7(A)所示,当干扰物质的浓度为目标物UA浓度的10倍时(干扰物质的浓度1000μmol/L,UA浓度100μmol/L),传感器测定UA时的ECL信号变化值明显大于测定干扰物质时的ECL信号变化值,并且加入干扰物质时的ECL信号与空白的ECL信号较为接近,说明该传感器能够用于对UA特异性检测。另一方面,连续测定了传感器在50 nmol/L UA底液中的ECL信号,如图7(B)所示,可见测定的ECL信号具有良好的稳定性。计算得出相对标准偏差(RSD)低至0.57%,证明此传感器稳定性良好。
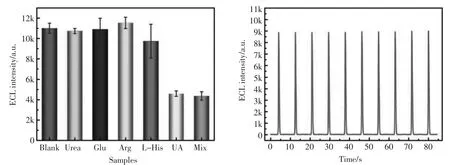
图7 ECL生物传感器的(A)选择性和(B)稳定性Fig.7 (A)Selectivity and(B)Stability of the ECL biosensor
表3是该工作和UA的其他检测法的对比,说明ECL分析法检测UA具有更宽的线性范围。

表3 该工作与其他相关工作的对比Tab.3 The comparsion between this work and others
3 结论
综上所述,该工作以鲁米诺(Luminol)和二硫
代二苯甲酸(DTSA)为原料,通过溶剂热法合成了硫原子掺杂的CDs。然后通过原位生长包埋法使得大量CDs在ZIF-8生长成型的过程中负载在ZIF-8的框架上,合成了具有强ECL信号的CDs@ZIF-8复合材料。实验结果表明,UA能够有效猝灭CDs@ZIF-8/溶解氧体系的ECL信号,相较于传统的荧光法、比色法、分光法检测生物小分子,该实验的电化学发光生物传感器能够实现对UA的高灵敏、高特异性检测,对人体UA含量的检测具有重要的意义。
